老年局部晚期乳腺癌新辅助化疗的疗效分析
2013-07-02马传栋严伟国丁涵之
马传栋 严伟国 丁涵之 全 红 韩 晶*
(上海市东方医院乳腺外科,同济大学附属东方医院,上海 200120)
老年局部晚期乳腺癌新辅助化疗的疗效分析
马传栋 严伟国 丁涵之 全 红 韩 晶*
(上海市东方医院乳腺外科,同济大学附属东方医院,上海 200120)
目的 老年乳腺癌患者具有伴随疾病多,化疗耐受性相对较差等特点,本研究旨在分析新辅助化疗在老年局部晚期乳腺癌中的疗效。方法 收集2004年1月至2011年12月经细胞学或组织学证实的老年局部晚期乳腺癌29例。全部患者接受术前2~6个周期的新辅助化疗。化疗方案分别为:CMF(环磷酰胺,甲氨蝶呤,氟尿嘧啶),CEF(环磷酰胺,表柔比星,氟尿嘧啶),TE(多西他赛,表柔比星)。化疗后按照实体瘤疗效评价标准(RECIST 1.1)评价近期疗效。不良反应按照WHO抗肿瘤药物毒性反应分级标准分为0~Ⅳ级。采用电话和信件的方式进行随访。结果 29例患者中,CR 2例(6.9%),PR 19例(65.5%),SD 6例(20.7%),PD 2例(6.9%),总有效率(CR+PR)为72.4%(21/29)。本组中无严重心脏毒性反应,无副反应导致的死亡事件发生。术后随访12至84个月,随访率为93.1%。3年总生存率为51.3%。结论 新辅助化疗在某些老年局部晚期乳腺癌患者中可能是安全而有效的。
局部晚期乳腺癌;老年;新辅助化疗
随着人类寿命的延长和乳腺癌发病率的增高,老年乳腺癌患者越来越多。在美国,近50%的乳腺癌患者为65岁以上的女性,但是这些患者经常没有接受到标准的治疗,导致老年乳腺癌患者的复发和病死率较高[1]。新辅助化疗能够降低肿瘤分期,使患者获得手术机会或者增加保乳的概率,同时可以观察化疗的敏感性。新辅助化疗已成为局部晚期乳腺癌治疗中不可或缺的组成部分,但是老年局部晚期乳腺癌的新辅助化疗报道不多,本文回顾性分析老年局部晚期乳腺癌患者新辅助化疗的疗效。
1 资料与方法
1.1 临床资料
2004年1月至2011年12月我院共收治29例接受新辅助化疗的老年乳腺癌患者,均为女性,年龄为65~78岁(平均68.5岁)。所有患者均经细胞学或组织学诊断为恶性肿瘤。自发病至就诊的时间间隔为1~6个月。肿块最小者约2cm,最大者约10cm;左侧14例,右侧15例;其中ā皮肤破溃者2例,炎性乳腺癌2例,皮肤红肿、橘皮征3例,腋窝淋巴结肿大首发2例,乳房、腋窝淋巴结、锁骨上淋巴结同时存在肿瘤2例。根据AJCC乳腺癌TNM分期(第六版)标准,ⅡB期3例,ⅢA期14例,ⅢB期10例,ⅢC期2例。29例中有12例合并其他慢性疾病,10例合并高血压,1例同时合并陈旧性脑梗死,2例合并冠心病。化疗前有HER2和ER、PR结果者8例,HER2阳性者(++~+++)4例;ER和/或PR阳性者5例。
1.2 治疗方案
1.2.1 化学治疗
化疗方案分别为CMF(环磷酰胺 500mg/m2静脉滴注,第1天,第8天;甲氨蝶呤40mg/m2静脉滴注,第1天,第8天;氟尿嘧啶500mg/m2静脉滴注,第1天,第8天;每28天重复)9例; CEF(环磷酰胺500mg/m2静脉滴注,第1天;表柔比星75mg/m2静脉滴注,第1天;氟尿嘧啶500mg/m2静脉滴注,第1天,第8天;每21天重复)13例;TE(多西他赛75mg/m2静脉滴注,第1天;表柔比星60 mg/m2静脉滴注,第1天;每21天重复)7例。
1.2.2 外科治疗
化疗后除1例行扩大根治术外,其余均行改良根治术。
1.2.3 术后辅助治疗
根据术后病理结果采用原方案化疗者25例,更换方案化疗方案者4例。术后接受辅助放疗者9例。术后口服他莫昔芬者(10mg, 2次/日)7例,口服第三代芳香化酶抑制剂(来曲唑,阿那曲唑,依西美坦)者15例。术后无1例接受曲妥珠单抗辅助治疗者。
1.3 疗效评价
按照实体瘤疗效评价标准(RECIST 1.1),通过临床体检和(或)超声判定化疗后反应情况。以原发灶反应为准,分为完全缓解(CR)、部分缓解(PR)、稳定(SD)及进展(PD)。总有效率=(CR+PR)例数/总例数×100%。不良反应按照WHO抗肿瘤药物毒性反应分级标准分为0~Ⅳ级。
1.4 免疫组织化学判断标准
雌、孕激素受体(ER, PR)以细胞核内出现棕黄色颗粒为阳性染色,分为阴性、弱阳性、阳性。HER2判断标准采用美国临床肿瘤协会/美国病理学家学院2007年提出的评分系统[2],分为0,1+,2+,3+。
1.5 随访
采用电话和信件方式进行随访。随访内容包括复发时间,复发部位,死亡原因等。随访起点时间为手术结束时,截止时间为出现死亡或者失访。
1.6 统计学处理
采用SPSS 17.0 统计软件建立数据库,计量资料比较采用卡方检验,以P<0.05为差别有统计学意义。生存时间以Kaplan-Meier法计算并绘制生存曲线。
2 结 果
2.1 新辅助化疗的完成情况
29例患者中,完成2个周期新辅助化疗者7例(24.1%),完成3个周期者13例(44.8%),完成4个周期者6例(20.7%),完成6个周期者3例(10.3%)。
2.2 近期疗效
全组患者中,CR 2例(6.9%),PR 19例(65.5%),SD 6例(20.7%),PD 2例(6.9%),总有效率(CR +PR)为72.4%(21/29)。各分期缓解率之间无统计学差异(表1)。
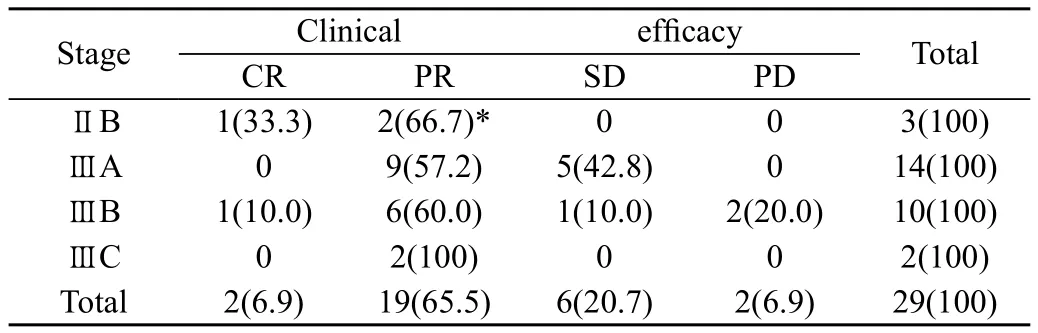
表1 老年乳腺癌患者新辅助化疗的疗效
2.3 不良反应
全组患者均未发生严重毒副反应。全组患者均发生不同程度的骨髓抑制,其中3度骨髓抑制19例(65.5%),给予粒细胞集落刺激因子支持治疗后均好转。25例(86.2%)患者发生了不同程度的胃肠道反应,对症治疗休息后缓解。全组无严重心、肺、肝、肾副反应发生。
2.4 新辅助化疗前后HER2受体和雌孕激素受体变化情况
术后免疫组织化学HER2阳性 (++~+++)者 6例;ER和/或PR阳性者22例;HER2、ER、PR均阴性者5例;术前与术后均有HER2、ER、PR报告者7例,其中2例ER由化疗前阳性转为术后阴性,2例ER由化疗前弱阳性转为术后阴性,1例ER和PR由化疗前阳性转为术后弱阳性;1例HER2化疗前(+)转为术后(+++)。化疗后腋窝淋巴结转移0个6例,1~3个8例,4个以上15例。
2.5 随访及远期疗效
全组患者中,2例失访,原因为无法取得联系;随访率为93.1%(27/29)。随访时间为12至84个月,中位时间48个月。3年总生存率为51.7%(图1)。不同分期的生存率比较见图2。
3 讨 论

图1 总生存期(Kaplan-Meier 法)

图2 不同分期的生存期比较(Kaplan-Meier 法)
老年乳腺癌的生物学特点为激素受体阳性比例较高,国内外文献报道ER、PR多为70%~80%;肿瘤细胞分化较好,组织学分级较低,HER2过表达和肿瘤脉管侵犯较少见等。因此,内分泌治疗在老年乳腺癌治疗中一直占有重要地位。如果合并严重的内科疾病,手术存在很大的风险性,可能导致严重并发症甚至死亡,并且患者的激素受体为阳性,内分泌治疗经常被考虑作为老年乳腺癌的初始治疗方式[3-4]。另外,欧美进行的大规模随机临床试验中65岁以上老年病例往往相对较少,而有幸参加临床试验的那部分老年患者往往比较健康,故不具有代表性,缺乏有力的证据来指导临床实践。老年期乳腺癌就诊时经常合并其他系统慢性疾病,期望寿命较短,化疗耐受力较差,因此老年期乳腺癌术后是否行辅助化疗一直存在争议[5-6]。由于上述种种原因,导致老年乳腺癌新辅助化疗的研究较少。
新辅助化疗已成为局部晚期乳腺癌的标准治疗方式。新辅助化疗的价值在于,可以使不能手术的患者达到可以手术;为保乳手术创造机会;了解肿瘤对化疗药物的敏感性。局部晚期乳腺癌新辅助化疗有效率为60%~90%,绝大多数病例可以达到降期的效果。乳腺癌新辅助化疗的方案目前没有统一的标准,一般认为,所有用于术后辅助化疗的方案均可用于新辅助治疗。含蒽环类的化疗方案是乳腺癌辅助化疗的基石,但是蒽环类具有心脏毒性[7]。年龄是蒽环类相关的充血性心力衰竭的主要危险因素,65岁以上的老年患者多柔比星的累积剂量达到400mg/m2时发生充血性心力衰竭的危险性更高[8]。本组主要为含蒽环类的方案,术前均未行心脏彩超或同位素扫描检查心脏功能,但心电图检查未见明显异常,围手术期没有发生充血性心力衰竭和其他严重并发症。本组新辅助化疗通常为3~4个周期,本组65%的患者完成3~4个周期新辅助化疗,其中3例顺利完成6个周期化疗。本组中约40%的患者同时合并其他脏器慢性疾病,均能够完成2个周期以上的化疗,说明老年乳腺癌患者对新辅助化疗还是具有一定的耐受力[9]。本组的近期总有效率为72%,表明老年乳腺癌的新辅助化疗是有效的。文献多报道,新辅助化疗后ER或PR由化疗前阴性转为化疗后阳性。有趣的是,本组中7例均有化疗前和术后病理免疫组化结果,其中4例ER或PR由化疗前阳性转为术后阴性,无1例由阴性转为化疗后阳性。
本组病例中生存时间最短者为术后10个月,最长者为7年4个月。本组病例病期较晚,ⅢB和ⅢC期患者比例较高,包括2例锁骨上转移患者,经积极治疗后1例仍健在。Brancato[10]等报道7例ⅢB期老年乳腺癌经新辅助化疗后,1例生存4年以上,2例3年后死亡,1例2年后死亡,1例4年后死亡,2例死于其他原因。本组的生存情况与上述结果相似。
本研究是回顾性研究,且样本量较少,可能存在选择偏倚,不能获得老年乳腺癌患者接受化疗后毒副反应以及耐受性的准确资料。但是,从本研究中仍可以看出老年乳腺癌,尤其是局部晚期患者,新辅助化疗应该得到充分地应用,以增加手术的机会和提高生存率。因此,对于身体比较健康、估计预期寿命较长的老年局部晚期乳腺癌患者,在制定综合治疗方案时,是否采用新辅助化疗值得进一步研究。
[1] Bellury L,Pett M,Ellington L,et al.The effect of aging and cancer on the symptom experience and physical function of elderly breast cancer survivors[J].Cancer,2012,118(24):6171-6178.
[2] Wolff A,Hammond M,Schwartz J,et al.American Society of ClinicalOncology/College of American Pathologists guideline recommendations for human epidermal growth factor receptor 2 testing in breast cancer[J].J Clin Oncol,2007,25(1):118-145.
[3] 陈伟财,何劲松,王敏,等.老年乳腺癌患者新辅助内分泌治疗的临床应用[J].中国癌症杂志,2011,21(5):359-362.
[4] Barnadas A,Gil M,Gonzalez S,et al.Exemestane as primary treatment of oestrogen receptor-positive breast cancer in postmenopausal women:a phase Ⅱ trail[J].Br J Cancer,2009,1000(3): 442-449.
[5] Leung M,Shapira I,Bradley T,et al.Adjuvant chemotherapy for early breast cancer in the elderly[J].Curr Treat Options Oncol, 2009,10(3):144-158.
[6] 马祥敏,崔文静,张矫,等.老年人乳腺癌综合治疗研究进展[J].中华老年医学杂志,2012,31(5):442-444.
[7] Shi Y,Moon M,Dawood S,et al.Mechanisms and management of doxorubicin cardiotoxicity[J].Herz,2011,36(4):296-305.
[8] Appel J,Jensen B,Nielsen D,et al.Systolic versus diastolic function variables during epirubicin treatment for breast cancer[J].Int J Cardiovasc Imaging,2010,26(2):217-223.
[9] 吕晶,陈征,张青松.老年进展期乳腺癌患者应用CEF新辅助化疗的疗效观察[J].中华乳腺病杂志(电子版),2008,2(6):647-652.
[10] Brancato G,Gandolfo L,Privitera A,et al.Locally advanced breast cancer in the elderly:A major challenge requiring effective and appropriate treatment[J].Tumori,2002,88(6):467-469.
The Efficacy Analysis of Neoadjuvant Chemotherapy in the Elderly Patients with Locally Advanced Breast Cancer
MA Chuan-dong, YAN Wei-guo, DING Han-zhi, QUAN Hong, HAN Jing
(Department of Breast Surgery, Shanghai East Hospital, Affiliated East Hospital of Tongji University , Shanghai 200120, China)
Objective There are more comorbidity in elderly patients with breast cancer who are poorly tolerable to chemotherapy. The goal of this study is to analyze the clinical efficacy of neoadjuvant chemotherapy in the elderly patients with locally advanced breast cancer (LABC). Methods From January 2004 to December 2011, 29 patients with LABC diagnosed by cytological or histological pathology were treated with neoadjuvant chemotherapy operatively. The patients were treated for 2-6 cycles of different regimens, including CMF(CTX, MTX, 5-Fu); CEF(CTX, EPI, 5-Fu); TE(Doc, EPI). Chemotherapy response was evaluated by RECIST 1.1 and the toxicity was estimated by WHO evaluation standard. The way of follow-up was telephone or letter. Results 29 patients, there was CR in 2 cases (6.9%), PR in 19 cases (65.5%), SD in 6 cases (20.7%), PD in 2 cases (6.9%); and the overall response rate (CR +PR) was 72.4% There were no severe cardiotoxicity and chemotherapy related death. The duration of follow-up was from 12 months to 84 months, and the rate of follow-up was 93.1%. The overall survival rate of three years was 51.3%. Conclusion Neoadjuvant chemotherapy in some elderly patients with LABC may be safe and effective.
Locally advanced breast cancer; Elderly; Neoadjuvant chemotherapy
R737.9
B
1671-8194(2013)25-0005-03
*通讯作者:E-mail:kristall1341@foxmail.com
