大脑前动脉区域梗死的临床特征及其预后影响因素研究
2013-06-22陈晓丽陈为安鲍剑虹王汉旻
陈晓丽,陈为安,鲍剑虹,王汉旻
大脑前动脉 (ACA)区域梗死占卒中患者的1.1%~3.0%[1-2],但有关其临床特征及预后影响因素的研究报道较少。Kang等[3]于2008年详细阐述了韩国ACA区域梗死患者的临床表现、病因及发病机制,但其样本量仅为100例;我国目前关于ACA区域梗死的大型研究较为少见。本研究通过回顾性分析我院收治的86例ACA区域梗死患者的临床资料,分析患者的临床特征,评估责任病灶及血管病变情况,随访患者神经功能缺损情况并探讨其预后影响因素。
1 对象与方法
1.1 研究对象 2009年4月—2012年4月在我院住院并经磁共振弥散加权序列 (DWI)检查证实为ACA区域梗死患者共86例,排除同时合并其他血管区域梗死患者及蛛网膜下腔出血继发血管痉挛患者等。
1.2 检查方法 所有患者入院后接受血常规、血生化、尿常规等实验室检查;完善胸部CT、12导联心电图、经胸心脏超声、颈部血管超声、经颅多普勒超声 (TCD)、颅脑磁共振成像 (MRI),颅脑及颈部磁共振血管成像 (MRA)等影像学检查,部分患者行经食管心脏超声、脑血管造影检查;详细询问患者既往史、个人史。
1.3 病因分型 采用国际通用分型:(1)大动脉粥样硬化,分为颈内动脉病变 (ICA)和内源性ACA动脉粥样硬化病变;(2)心源性梗死;(3)其他原因;(4)不明原因。ACA病变血管分为5部分:A1段 (水平段)、A2段 (上升段)、A3段(膝段)、A4段 (胼周段)、A5段 (终段);ACA主干病变包括皮层支病变和深穿支病变,其中皮层支支配区域包括胼胝体嘴部、膝部、体部、压部、扣带回、额极、额上回内侧面、运动辅助区、旁中央小叶、楔叶,深穿支主要支配内囊前支和尾状核头的下部[4]。
1.4 预后评估 按照脑卒中患者临床神经功能缺损程度评分(NDS评分)标准 (1995)[5],评估患者发病90 d时预后情况,从意识水平、凝视功能、面瘫、语言、上肢功能、步行能力等8个方面进行评估,共分为4级:(1)显著进步:NDS评分改善程度≥50%;(2)进步:NDS评分改善程度介于25%~49%;(3)无改善:NDS评分改善程度<25%;(4)死亡。显著进步及进步患者归为预后良好组,无改善及死亡患者归为预后不良组。
1.5 统计学方法 采用Access建立数据库,SPSS 11.5软件包进行统计学分析,计数资料以例数或百分数表示,采用χ2检验;ACA区域梗死患者预后的影响因素分析采用多因素Logistic回归分析。以P<0.05为差异有统计学意义。
2 结果
2.1 一般情况及颅脑MRI 本组86例患者中男45例,女41例;年龄28~92岁,平均 (69.1±11.5)岁;既往史:高血压74例、糖尿病32例、吸烟32例、饮酒18例、心房纤颤17例、卒中11例。头颅MRI:左侧病灶53例、右侧病灶29例、双侧病灶4例;累及胼胝体62例 (72.1%),其中累及膝部29例、体部23例、压部7例、嘴部3例;累及额极32例(37.2%)、累及扣带回22例 (25.6%)、累及辅助运动区19例 (22.1%)、累及基底核13例 (15.1%)。
2.2 临床表现 运动障碍80例 (93.0%):偏瘫54例 (下肢瘫痪为重42例)、单下肢瘫22例、双下肢瘫4例,严重运动障碍22例 (MRC肌力分级 <Ⅲ级);尿失禁34例(39.5%);感觉障碍:精神淡漠22例、强握反射22例、偏身感觉障碍19例、失语12例、认知功能损害12例、单下肢感觉障碍10例。
2.3 病因及发病机制 大动脉粥样硬化63例 (73.3%):内源性ACA动脉粥样硬化病变53例、ICA 10例;心源性梗死11例 (12.8%):心房纤颤9例、卵圆孔未闭2例;混合机制8例 (9.3%);抗心磷脂抗体综合征1例 (1.1%);不明原因3例 (3.5%)。
53例内源性ACA动脉粥样硬化病变患者中,A1段病变12例、A2段病变 (见图1)24例、A3段病变17例,以A2段病变最多 (χ2=6.586,P=0.037);局部血栓形成11例、分支动脉闭塞17例、动脉-动脉栓塞12例,分支动脉闭塞合并动脉-动脉栓塞13例。ICA发病机制主要为低灌注合并动脉-动脉栓塞。
2.4 胼胝体累及 累及胼胝体62例患者中内源性ACA动脉粥样硬化病变48例、心源性梗死6例、ICA 4例、抗心磷脂抗体综合征1例、不明原因3例。
2.5 预后影响因素 根据评估结果将患者分为预后良好组73例,预后不良组13例。预后不良组中2例患者死亡(2.3%),均为心源性梗死,1例由卵圆孔未闭引起ACA主干闭塞 (见图2),另1例为心房纤颤引起脑梗死伴出血转化;其余11例患者均为大动脉粥样硬化。以患者的性别、年龄、高血压史、糖尿病史、心房纤颤史、吸烟史、饮酒史、辅助运动区病变、基线NDS评分作为自变量 (赋值见表1),预后情况作为因变量进行多因素Logistic回归分析,结果显示,辅助运动区病变、基线NDS评分增高对回归方程的影响有统计学意义 (P<0.05,见表2)。
3 讨论
虽然ACA区域梗死发病率较低,但因其临床表现多样,临床工作中容易误诊漏诊,而成功预防卒中很大程度上取决于其病因及发病机制。目前,我国关于ACA区域梗死临床特征的研究报道均为小样本研究,而关于其预后影响因素的研究报道则更少。

表1 变量赋值表Table 1 Variable assignment table

表2 ACA区域脑梗死患者预后影响因素的Logistic回归分析Table 2 Logistic regression analysis of factors influencing the prognosis of patients with ischemic stroke in the territory of the anterior cerebral artery
本研究结果显示,ACA区域梗死患者的临床表现中运动障碍占93.0%,是最常见的临床表现,与国内外文献报道相似[2,6-7]。运动症状中以偏瘫及下肢瘫为主,考虑与病灶累及辅助运动区或旁中央小叶有关,该区运动纤维主要支配下肢运动功能。其他临床表现为尿失禁、精神淡漠、强握反射等。目前尚未发现肯定的尿失禁解剖生理基础;精神淡漠考虑与胼胝体、优势半球前额叶内侧、扣带回受累有关[3,8]。临床上遇到以下肢瘫痪为重并伴尿失禁、精神淡漠的患者要高度怀疑ACA区域梗死可能,应行颅脑MRI以进一步证实。
本组患者的主要病因为大动脉粥样硬化,占73.3%,远高于 Arboix等[1]报道的 29%,但与 Kang等[3]、Bogousslavsky等[9]报道的结果相似。心源性梗死较为少见,仅占12.8%,低于 Arboix等[1]和 Kumral等[2]报道的27% ~45%。究其原因有以下两个方面:(1)大脑中动脉为颈内动脉主干,其血液供应范围大,故心源性梗死以大脑中动脉血液供应区域为主,因此ACA区域梗死患者心源性梗死所占比例较小,符合脑血液供应病理生理;(2)可能与研究对象人群差异有关,西方人群ACA区域梗死以心源性梗死为主[1-2,5-6],东南亚地区人群ACA区域梗死以大动脉粥样硬化为主。因此,在寻找病因时一定要进行血管影像学检查。本组大动脉粥样硬化患者中10例为ICA,53例为内源性ACA动脉粥样硬化病变,且主要累及A2、A3段,以A2段最多,与Kang等[3]报道结果一致。目前,动脉粥样硬化易发生在A2段的原因及机制尚不明确,可能与前交通动脉的存在使A1段动脉硬化常表现为无症状性有关。
影像学表现方面,ACA区域梗死累及部位依次为胼胝体(72.1%)、额极 (37.2%)、扣带回 (25.6%)、辅助运动区(22%)、基底核 (15.1%),而累及胼胝体患者主要累及膝部和体部,累及压部和嘴部较少。既往研究认为,胼胝体血供丰富[10],不易出现缺血事件,分析其原因可能是随着MRI的广泛应用,胼胝体缺血越来越多地被发现并报道。本组62例累及胼胝体患者中48例为内源性ACA动脉粥样硬化病变,其原因可能为脑血管动脉粥样硬化导致血流动力学改变。
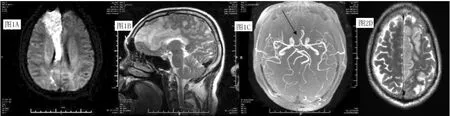
图1 ACA区域脑梗死患者A2段闭塞Figure 1 Example of stroke caused by right A2 segment occlusion
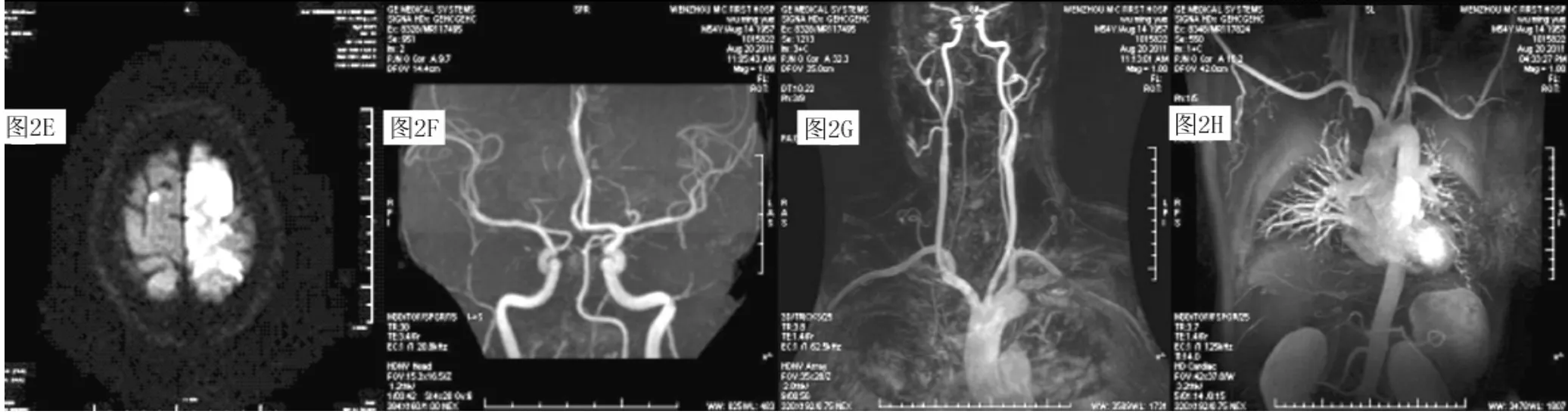
图2 卵圆孔未闭导致ACA主干闭塞患者影像学检查结果Figure 2 Example of stroke caused by paradoxical embolism through patent foramen ovale
本研究结果显示,ACA区域梗死患者病死率为2.3%,与Kumral等[2]报道的0 ~7.8% 基本一致,但低于 Arboix等[1]报道的大脑中动脉区域梗死患者病死率 (17.3%)。本组13例预后不良患者中11例为大动脉粥样硬化;2例死亡患者均为心源性梗死,其中1例由卵圆孔未闭引起ACA主干闭塞,与双侧ACA共干变异有关,另1例为心房纤颤引起脑梗死伴出血转化。相对于大脑中动脉,ACA区域梗死预后较好,可能与大脑中动脉支配区域发生致命性大面积梗死几率更高,而双侧ACA系统存在丰富的侧支循环、血供丰富有关。多因素Logistic回归分析结果显示,辅助运动区病变、基线NDS评分增高是ACA区域梗死患者预后不良的危险因素。
总之,运动障碍是ACA区域梗死的主要临床表现,内源性ACA动脉粥样硬化病变是主要病因,胼胝体最易受累,当患者出现单下肢瘫或以下肢为主的偏瘫,尤其伴尿失禁、精神淡漠时,要高度警惕ACA区域梗死,应及时行脑实质及脑血管检查;辅助运动区病变、基线NDS评分增高是患者预后不良的危险因素。但本研究样本量较小,且未针对患者语言、记忆、执行、情绪等高级功能进行深入研究,可能会影响预后因素的分析结果。
1 Arboix A,García-Eroles L,Sellarés N,et al.Infarction in the territory of the anterior cerebral artery:clinical study of 51 patients[J].BMC Neurol,2009(9):30.
2 Kumral E,Bayulkem G,Evyapan D,et al.Spectrum of anterior cerebral artery territory infarction:clinical and MRI findings[J] .Eur J Neurol,2002,9(6):615-624.
3 Kang SY,Kim JS.Anterior cerebral artery infarction:stroke mechanism and clinical-imaging study in 100 patients [J] .Neurology,2008,70(24 Pt 2):2386-2393.
4 Brust JCM,Sawada T,Kazui S.Anterior cerebral artery[M] //Bogousslavsky J,Caplan LR,eds.Stroke Syndromes.New York:Cambridge University Press,2001:439-450.
5 全国第四届脑血管病学术会议.脑卒中患者临床神经功能缺损评分标准 (1995) [J].中华神经科杂志,1996,29(6):381-383.
6 Kazui S,Sawada T,Naritomi H,et al.Angiographic evaluation of brain infarction limited to the anterior cerebral artery territory [J].Stroke,1993,24(4):549-553.
7 陈红兵,王莹,杨智云,等.大脑前动脉供血区梗死患者的临床分析[J].中国脑血管病杂志,2011,8(8):412-417.
8 吕宪民,李欣,刘静,等.胼胝体压部病变四例病因分析[J].中国全科医学,2011,14(4):1234.
9 Bogousslavsky J,Regli F.Anterior cerebral infarction in the Lausanne Stroke Registry.Clinical and etiological patterns [J] .Arch Neurol,1990,47(2):144-150.
10 Kuzma BB,Goodman JM.Corpus callosum infarction [J].Surg Neurol,1999,52(6):210-212.
