胃肠胰神经内分泌肿瘤病理诊断的规范和进展
2013-06-09
复旦大学附属肿瘤医院病理科,复旦大学上海医学院肿瘤学系,上海 200032
胃肠胰神经内分泌肿瘤病理诊断的规范和进展
盛伟琪
复旦大学附属肿瘤医院病理科,复旦大学上海医学院肿瘤学系,上海 200032

盛伟琪,副主任医师,硕士生导师,1992年至今就职于复旦大学附属肿瘤医院病理科;1999-2001年在日本产业医科大学第一病理作为访问学者进行肿瘤分子和遗传学研究的学习和工作。从事肿瘤外科病理的诊断和研究工作,尤其是胃肠道肿瘤和恶性淋巴瘤的诊断、鉴别诊断及其相关研究。曾在J Pathol, Am J Clin Pathol, Cancer Genet Cytogenet, Appl Immunohistochem Mol Morphol等杂志发表多篇论文,负责上海市科委、复旦大学医学院等多项科研项目。。
神经内分泌肿瘤(neuroendocrine neoplasm,NEN)是一组起源于肽能神经元和神经内分泌细胞的异质性肿瘤。2010年第4版《世界卫生组织(World Health Organization,WHO)消化系统肿瘤分类》对NEN的命名、分类和分级进行修订和统一,纠正以往NEN诊断名称使用的混乱、规范NEN的病理分类和分级,增加NEN诊断的互认性,为NEN的临床治疗、预后判断提供必要的病理学信息。病理医师在常规病理诊断报告时应当按照一定的步骤要求,结合免疫组织化学染色结果进行准确的诊断、分类和分级,并提供临床分期必需的病理参数。近年来,有关NEN的临床和基础研究结果,使学者们对2010年第四版《WHO消化系统肿瘤分类》的部分内容和分级标准有了新的认识,提出了新观点,一些数据有待于进一步的大样本探讨证实。
胃肠胰神经内分泌肿瘤;病理诊断;免疫组化
[Key words]Gastroenteropancreatic neuroendocrine neoplasm; Pathological diagnosis; Immunohistochemistry
神经内分泌细胞广泛分布于人体多处器官和组织,包括胃肠道、胰腺、胆管、肝、支气管、肺、甲状腺、甲状旁腺、肾上腺髓质、副神经节等。起源于肽能神经元和神经内分泌细胞的神经内分泌肿瘤(neuroendocrine neoplasm,NEN)可发生在全身许多器官和组织。它是一组异质性显著的肿瘤,显示从惰性、低度恶性到显著恶性、高侵袭性和转移性的一系列生物学行为。胃肠道和胰腺分别分布着12种和4种神经内分泌细胞,是NEN最常发生的部位,约占所有NEN的55%~70%。胃肠道和胰腺的发病率约5.25/10万,是胃肠道第二类常见肿瘤[1]。
在以往较长一段时间内,NEN的命名、分类混乱、不统一,诊断和治疗缺乏规范,使NEN的早期诊断率低,延误治疗,导致确诊时往往已出现转移,病死率居高不下。2010年第4版《世界卫生组织(World Health Organization, WHO)消化系统肿瘤分类》对NEN的命名、分类和分级进行修订[2],2011年4月“中国胃肠胰神经内分泌肿瘤病理学诊断共识”[3]发表,成为统一我国NEN病理诊断名称、分类和分级,规范NEN病理诊断报告的指导性意见。现就消化道NEN的病理诊断规范及最近研究进展介绍如下。
1 命名
1907年,德国医师Oberndorfer[4]发现了一种形态较为单一、侵袭性低下的上皮样肿瘤,认为是一种类似于癌的良性肿瘤,命名为类癌(carcinoid)。1914年Gosset和Masson证明了类癌是神经内分泌肿瘤的本质,1929年Oberndorfer本人撰文修改原有观点,承认这种肿瘤是恶性并可以发生转移,但“类癌”在病理和临床医师中已广为流传,以至于长期以来一直用于NEN的诊断[5]。此后,随着具有内分泌功能的胃肠道亲银细胞、嗜银细胞以及肺透明细胞的发现,逐渐形成弥漫性神经内分泌系统的概念。进一步的研究发现,弥漫性神经内分泌系统的细胞都具有摄取胺前体和脱羟基(amine precursor uptake and decarboxylation,APUD)的功能,故把这些细胞统称为APUD细胞,形成的肿瘤称为APUD瘤[6]。无论是“类癌”或“APUD瘤”都不能反映NEN的起源、分泌激素的特性,更不能正确提示肿瘤的生物学行为,应当弃用。
2010年第4版《WHO消化系统肿瘤分类》将所有源自神经内分泌细胞的肿瘤称为“neuroendocrine neoplasm,NEN”,中文译名为“神经内分泌肿瘤”。根据不同分化程度,NEN分为高分化神经内分泌肿瘤和低分化神经内分泌肿瘤,前者英文名为“neuroendocrine tumor,NET”,中文译名为“神经内分泌瘤”,后者英文名为“neuroendocrine carcinoma,NEC”,中文译名为“神经内分泌癌”。所有神经内分泌肿瘤都有转移潜能,均为恶性[2]。除了“类癌综合征”,建议在常规诊断时不再使用“类癌”这一名称。“类癌综合征”约发生于10%的NEN患者,因肿瘤产生5-羟色胺及其代谢产物所致,患者出现面部潮红、出汗、腹泻、哮喘、水肿和右心内膜纤维化等症状。
2 分类和分级
WHO、欧洲神经内分泌肿瘤学会(ENETS)等都分别发表过NEN的分类和分期系统,但在命名、肿瘤分级和分期标准等方面存在不同。2010年第4版《WHO消化系统肿瘤分类》摒弃了2000年第3版分类兼顾分级、分期的复杂体系,采纳了ENETS补充分类方法[7-8],将病理分级和临床分期分开,形成了较为容易掌握的新分类和分级系统(表1)。
分级根据肿瘤细胞的增殖活性,增殖活性的级别采用核分裂象和(或)Ki-67指数两项指标(表2)。大多数情况下,核分裂象和Ki-67指数呈正相关,少数情况下可能不一致,此时采用分级更高的结果[2]。无论采用哪项指标,都应当在病理报告中记录具体数值。核分裂象计数时应计数分裂象活跃的区域,至少计数50个高倍视野,并根据所使用的显微镜物镜视野直径进行换算。表2所列的核分裂象数是以物镜视野直径0.5 mm,单个视野面积0.196 mm2计数的数值[2]。

表 1 2010年第4版《世界卫生组织消化系统肿瘤分类》神经内分泌肿瘤分类Fig. 1 WHO Classification of Tumors of the Digestive System, Fourth Edition

表 2 胃肠胰神经内分泌肿瘤的分级标准Fig. 2 The standard of the classification of astroenteropancreatic neuroendocrine neoplasm
Ki-67指数的计数方法有多种,使用目测估计百分比的粗略方法最不可靠。显微镜下“眼睛注视法”(eyeballing method)是大多数有经验的病理医师采用的方法,但它存在一定的主观性和欠准确性。自动图像分析系统通过自动化软件分析获得Ki-67指数,但是软件系统本身不能识别肿瘤细胞和非肿瘤细胞,需要由有诊断经验的医师操作,否则得到的结果甚至不如人工计数方法准确[9]。Bagci等[10]发现采用将显微镜下选取的图像传输到电脑屏幕或打印成照片,再在图像上通过画圈的方法人工计数得到的Ki-67指数最准确。
Ki-67在肿瘤细胞中的阳性表达存在异质性[11],在计数时应当挑选表达最强的区域至少计数500个肿瘤细胞。切片厚度、免疫组织化学染色质量、显色强弱等因素都会影响Ki-67指数的准确性。
根据图纸说明并结合相关标准规范要求,在建筑模型中创建构造柱、圈梁、门过梁、反坎和门槛等二次结构构件,并生成材料明细表精确提取单层材料运输量,对构件进行平面标识,输出二维和三维深化图,指导现场施工(见图 5)。
3 免疫组织化学检测指标
免疫组织化学染色是NEN诊断和鉴别诊断不可替代的方法,不仅能够帮助确定肿瘤细胞具有神经内分泌细胞分化,而且能够确定NEN分泌的特定的多肽激素和生物活性胺。免疫组织化学检测的指标可以分为“必须检测项目”和“可选检测项目”。
3.1 必须检测项目
3.1.1 突触素和嗜铬粒素A
突触素(synaptophysin,Syn)是由X染色体上SYP基因编码的相对分子质量为38×103的一种突触囊泡糖蛋白,存在于人体所有神经内分泌细胞。绝大多数NEN瘤细胞弥漫表达Syn。由于所有神经元细胞都参与Syn的呈递,因此神经元细胞和部分神经细胞也表达Syn阳性,此外部分非NEN瘤细胞(如胰腺实性假乳头状肿瘤)也可以显示阳性。
嗜铬粒素A(chromogranin A,CgA)位于神经元和神经内分泌细胞的分泌囊泡内,不是所有神经内分泌细胞均含此类分泌囊泡,不同神经内分泌细胞所含囊泡数量也不同。因此,CgA在不同部位、不同分化的NEN中的表达有所不同。例如发生在直肠和阑尾的NEN以及十二指肠的生长抑素瘤一般不表达CgA,肺小细胞癌常弱表达或不表达CgA[12]。
由于Syn和CgA在NEN瘤细胞表达的特点不同,联合检测将有助于确定肿瘤是否具有神经内分泌细胞性质。其他神经内分泌标志物如CD56、PGP9.5、NSE等,因标志物本身或检测用抗体的特异性不高,不能作为NEN独立的诊断依据。
3.1.2 Ki-67
NEN分级依靠肿瘤细胞的增殖活性,免疫组织化学方法检测Ki-67指数是诊断NEN必不可少的步骤,Ki-67染色的常用抗体为MIB-1、Ki-67指数的阳性定位于细胞核,在计数时不仅避免计数非肿瘤细胞,也不应计数显示细胞膜阳性的肿瘤细胞。Ki-67指数的计数方法和相关要点如前所述。
3.2.1 多肽激素和生物活性胺
部分NEN瘤细胞可以产生多肽激素或生物活性胺,如胃泌素、生长抑素、5-羟色胺、胰高血糖素、血管活性肠肽等,在细胞水平或血液中能检测到,但至少一半的病例不出现临床症状,即为无功能性NEN[13]。功能性NEN的诊断必须结合临床表现、血清学检查,而不能仅仅依靠免疫组织化学染色结果。无功能性的NEN和相应有临床症状的功能性NEN在生物学行为方面没有显著区别[13]。
免疫组织化学检测特定多肽激素和生物活性按可以用于:①在细胞水平证实引起临床症状的激素或生物活性胺的种类;②为转移性NEN提供原发灶的线索,如表达胃泌素首先考虑胰腺和十二指肠;③特殊类型细胞或肿瘤的诊断和鉴别诊断,如节细胞副神经节瘤。
3.2.2 其他标志物
大多数NEN瘤细胞表面存在生长抑素受体(somatostatin receptor,SSTR),尤其是SSTR2。尽管目前没有依据表明SSTR的表达与生长抑素类似物(如奥曲肽)的治疗效果相关,但SSTR的检测可以用于NEN的诊断和鉴别诊断。Papotti等[14]研究结果提示,SSTR的表达与NEN分化程度相关。
尾型同源盒转录因子2(caudal related homeodomain transcription 2,CDX2)和转录终止因子1(transcription termination factor -1,TTF1)分别作为胃肠胰和肺肿瘤的标志物,可以用于转移性NEN寻找原发灶的辅助诊断[15]。
4 病理诊断要点和规范
NEN的诊断步骤见图1。组织病理学形态是诊断NEN的基础,NEN具有独特的显微镜下表现。分化良好的NET具有典型的组织病理学形态特点。光镜下,典型的NET瘤细胞排列成实性巢状、缎带状、小梁状或腺管样。肿瘤细胞形态均匀一致,细胞质中等量或丰富,核圆形或卵圆形,大小形态规则,染色质呈略粗的颗粒状,核仁一般不明显。在瘤细胞巢周围有丰富的小血管和不等量的纤维间质围绕。
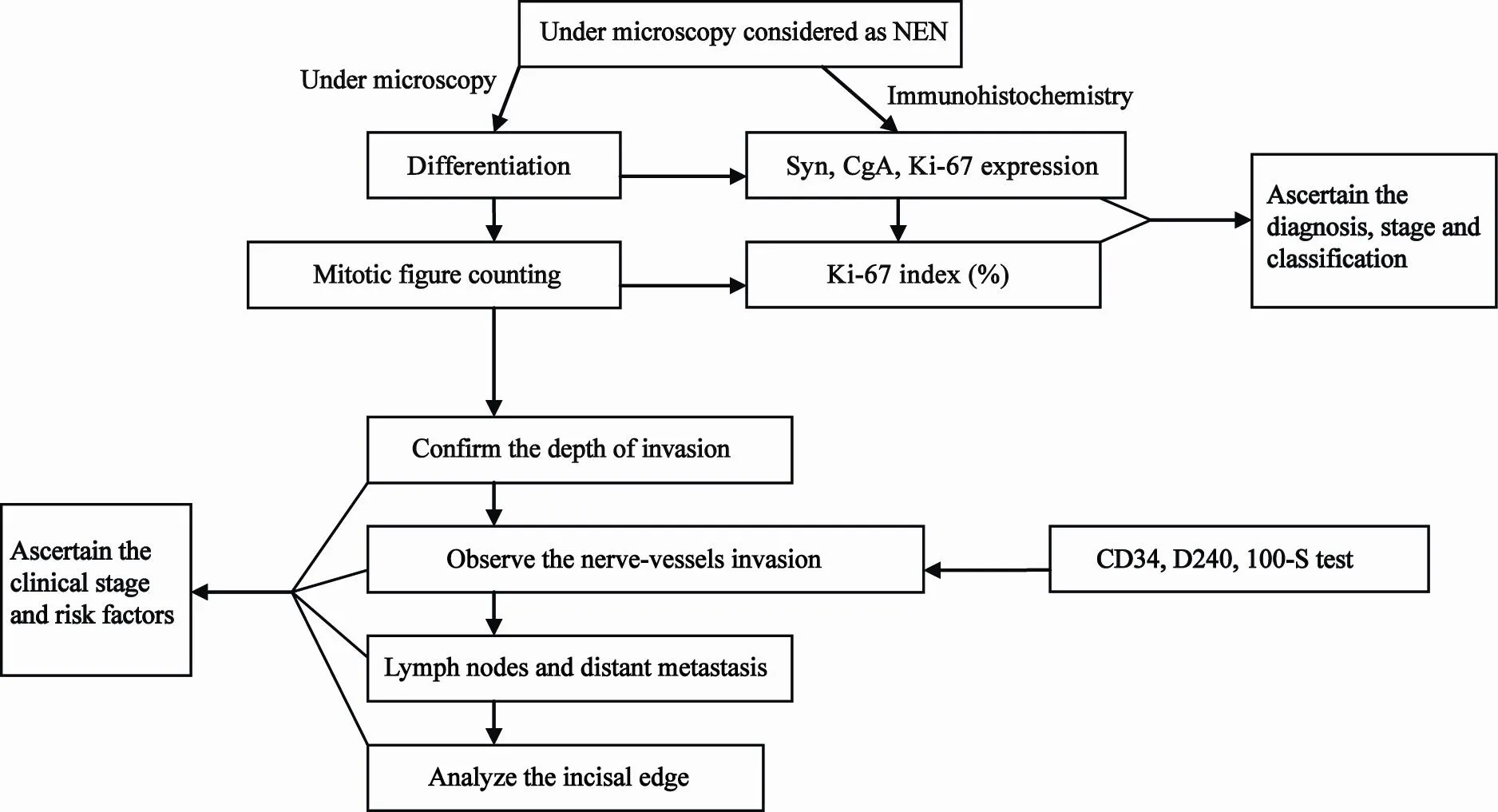
图 1 神经内分泌肿瘤病理诊断步骤简图Fig. 1 The step of the diagnosis of neuroendocrine tumor
典型的分化差的NEC包括小细胞癌和大细胞癌,形态表现与发生在肺的相应病变类似,核分裂象易见,常伴坏死。小细胞癌的瘤细胞小,似淋巴细胞,细胞质稀少,呈弥漫分布或巢团状排列;大细胞癌的瘤细胞大,往往是小细胞的3倍,染色质颗粒状,呈器官样、菊心团状排列或弥漫分布
由于2010年第4版《WHO消化系统肿瘤分类》NEN分类将病理分级和临床分期分开,而不同部位的临床分期存在差异。因此,NEN的病理诊断报告中必须包含临床分期所需要的各种必要信息(表3)。

表 3 神经内分泌肿瘤病理报告的内容Fig. 3 The content of the report of neuroendocrine tumor
5 最近研究进展
5.1 分类和分级
2010年第4版《WHO消化系统肿瘤分类》定义NET是高分化肿瘤,为低度或中度恶性,而G3属于高度恶性肿瘤,因此建议不宜采用NET G3分类。但最近法国的一项多中心研究[16]分析了778例胃肠、胰腺NEN,结果显示,除外小细胞癌后,G3肿瘤中有20%病例组织形态学分化良好,但Ki-67指数介于25%~60%,按照2010年第4版《WHO消化系统肿瘤分类》标准无法归类。Adsay等[17]研究结果提示,Ki-67指数为25%~30%的G3分级的NEN与Ki-67指数超过50%的小细胞NEC和大细胞NEC相比,两者的预后有明显差别。Yachida等[18]通过比较9例胰腺小细胞NEC、10例大细胞NEC和11例分化好的NET之间临床病理特点和基因表达差异,结果显示,NET和NEC是两种具有不同分子机制的不同肿瘤,在治疗上可能需要区别对待。目前,临床上对于组织形态学分化良好,但分级达到G3(Ki-67指数一般不超过60%)的这部分无法归类的NEN病例应当采用何种治疗方法尚无定论[16]。
5.2 胰腺NEN分级的临界值
2010年第4版《WHO消化系统肿瘤分类》NEN分类将Ki-67阳性指数2%和20%作为G1、G2和G3分级的临界值,但最近的部分研究结果提出了不同意见。Scarpa等[19]分析了274例胰腺NEN,将5%和20%作为临界值,分级才能成为预后相关的独立因素。Panzuto等[20]对202例晚期胰腺NEN的研究结果同样发现,如果以2%作为G1和G2的临界值,在预测疾病进展上差异无统计学意义(P=0.074),如果以5%作为临界值,则分级在预测疾病进展上差异有统计学意义(P=0.006)。以上研究提示,至少在胰腺,作为NEN G1和G2的分级指标,Ki-67指数临界值的设定有待进一步、大样本的深入研究。
[1] YAO J C, HASSAN M, PHAN A, et al. One hundred years after ‘carcinoid’: epidemiology of and prognostic factors for neuroendocrine tumors in 35,825 cases in the United States[J]. J Clin Oncol, 2008, 26(18): 3063-3072.
[2] HAMILTON S R, BOSMAN F T, BOFFETTA P, et al. Carcinoma of the colon and rectum. In: WHO Classification of Tumours of the Digestive System[M]. BOSMAN F T, CARNEIRO F, HRUBAN R H, et al, eds. Lyon: IARC Press, 2010.
[3] 中国胃肠胰神经内分泌肿瘤病理专家组. 中国胃肠胰神经内分泌肿瘤病理学诊断共识意见[J]. 中华病理学杂志, 2011, 40(4): 257-262.
[4] OBERNDORFER S. Karzinoide tumoren des dunndarms[J]. Frankf Z Pathol, 1907, 1: 426-432.
[5] KLIMSTRA D S, MODLIN I R, COPPOLA D, et al. The pathologic classification of neuroendocrine tumors: a review ofnomenclature, grading, and staging systems[J]. Pancreas, 2010, 39(6): 707-712.
[6] PEARSE A G. The cytochemistry and ultrastructure of polypeptide hormone-producing cells of the APUD series and the embryologic, physiologic and pathologic implications of the concept[J]. J Histochem Cytochem, 1969, 17(5): 303-313.
[7] RINDI G, KLOPPEL G, ALHMAN H, et al. TNM staging of foregut (neuro)endocrine tumors: a consensus proposal including a grading system[J]. Virchows Arch, 2006, 449(4): 395-401.
[8] RINDI G, KLOPPEL G, COUVELARD A, et al. TNM staging of midgut and hindgut (neuro) endocrine tumors: a consensus proposal including a grading system[J]. Virchows Arch, 2007, 451(4): 757-762.
[9] TANG L H, GONEN M, HEDVAT C, et al. Objective quantification of the Ki-67 proliferative index in neuroendocrine tumors of the gastroenteropancreatic system: a comparison of digital image analysis with manual methods[J]. Am J Surg Pathol, 2012, 36(12): 1761-1770.
[10] BAGCI P, OHIKE N, DURSUN N, et al. Comparative analysis of different counting methodologies for Ki-67 in pancreatic neuroendocrine tumors[J]. Mod Pathol, 2012, 25: 441A.
[11] YANG Z, TANG L H, KLIMSTRA D S. Effect of tumor heterogeneity on the assessment of Ki-67 labeling index in well-differentiated neuroendocrine tumors metastatic to the liver: implications for prognostic stratification[J]. Am J Surg Pathol, 2011, 35(6): 853-860.
[12] KLIMSTRA D S, MODLIN I R, ADSAY N V, et al. Pathology reporting of neuroendocrine tumors: application of the Delphic consensus process to the development of a minimum pathology data set[J]. Am J Surg Pathol, 2010, 34(3): 300-313.
[13] MODLIN I M, OBERG K, CHUNG D C, et al. Gastroenteropancreatic neuroendocrine tumours[J]. Lancet Oncol, 2008, 9(1): 61-72.
[14] PAPOTTI M, BONGIOVANNI M, VOLANTE M, et al. Expression of somatostatin receptor types 1-5 in 81 cases of gastrointestinal and pancreatic endocrine tumors. A correlative immunohistochemical and reverse-transcriptase polymerase chain reaction analysis[J]. Virchows Arch, 2002, 440(5): 461-475.
[15] SAQI A, ALEXIS D, REMOTTI F, et al. Usefulness of CDX2 and TTF-1 in differentiating gastrointestinal from pulmonary carcinoids[J]. Am J Clin Pathol, 2005, 123(3): 394-404.
[16] SCOAZEC J Y, COUVELARD A, MONGES G, et al. Welldifferentiated grade 3 digestive neuroendocrine tumors: myth or realty? The PRONET study group[J]. J Clin Oncol, 2012, 30(suppl): abstr 4129.
[17] ADSAY V. Ki-67 labeling index in neuroendocrine tumors of the gastrointestinal and pancreatobiliary tract: to count or not to count is not the question, but rather how to count[J]. Am J Surg Pathol, 2012, 36(12): 1743-1746.
[18] YACHIDA S, VAKIANI E, WHITE C M, et al. Small cell and large cell neuroendocrine carcinomas of the pancreas are genetically similar and distinct from well-differentiated pancreatic neuroendocrine tumors[J]. Am J Surg Pathol, 2012, 36(2): 173-184.
[19] SCARPA A, MANTOVANI W, CAPELLI P, et al. Pancreatic endocrine tumors: improved TNM staging and histopathological grading permit a clinically efficient prognostic stratification of patients[J]. Mod Pathol, 2010, 23(6): 824-833.
[20] PANZUTO F, BONINSEGNA L, FAZIO N, et al. Metastatic and locally advanced pancreatic neuroendocrine carcinomas: analysis of factors associated with disease progression[J]. J Clin Oncol, 2011, 29(17): 2372-2377.
附录:
Advances and pathological diagnostic standard of gastroenteropancreatic neuroendocrine neoplasms
SHENG Wei-qi (Department of Pathology, Fudan University Shanghai Cancer Center, Department of Oncology, Shanghai Medical College, Fudan University, Shanghai 200032, China)
SHENG Wei-qi E-mail: shengweiqi2006@yahoo.com.cn
Neuroendocrine neoplasm (NEN)is a group of heterogeneous tumors originated from the peptidergic neurons and neuroendocrine cells. A revised system of classification, nomenclature and grading of NEN was proposed by the fourth edition of “World Health Organization classification of tumours of the digestive system”in 2010. It apparently contributes to unify the method of classification, put an end of the confusion in nomenclature, standardize the grading system and predict the outcomes more accurately. With the combination of the results by immunohistochemical studies, pathologists should be in accordance with the requirements to make a diagnosis of NEN with accurate classification, grading and the pathological parameters essential to staging. Recently, new advances in NEN study put forward a new view in the classification and grading system that will lead to the updates of the diagnostic system after further studies on a large scale of samples.

表 1 2010年第4版《世界卫生组织消化道肿瘤分类》神经内分泌肿瘤分类
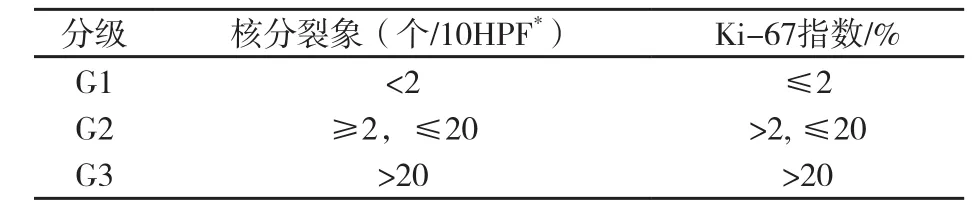
表 2 胃肠胰神经内分泌肿瘤的分级标准

表 3 神经内分泌肿瘤病理报告的内容
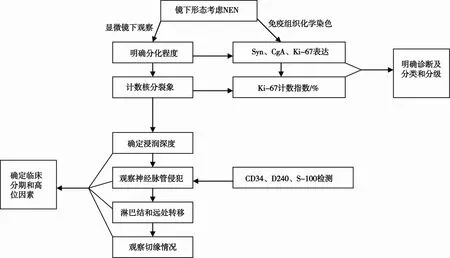
图 1 神经内分泌肿瘤病理诊断步骤简图
10.3969/j.issn.1007-3969.2013.06.001
R739.63
:A
:1007-3639(2013)06-0401-07
2013-05-10)
盛伟琪 E-mail:shengweiqi2006@yahoo.com.cn
