前列腺特异抗原3慢病毒表达载体的构建与包装
2013-06-09刘晓军王娜姚旭东曹达龙
刘晓军王娜姚旭东曹达龙
1.复旦大学附属肿瘤医院泌尿外科,复旦大学上海医学院肿瘤学系,上海 200032;
2.复旦大学附属肿瘤医院肿瘤研究所,复旦大学上海医学院肿瘤学系,上海200032
前列腺特异抗原3慢病毒表达载体的构建与包装
刘晓军1王娜2姚旭东1曹达龙1
1.复旦大学附属肿瘤医院泌尿外科,复旦大学上海医学院肿瘤学系,上海 200032;
2.复旦大学附属肿瘤医院肿瘤研究所,复旦大学上海医学院肿瘤学系,上海200032
背景与目的:前列腺癌抗原3(prostate cancer antigen 3,PCA3)作为一种长链非编码RNA(lncRNA)已被证实在前列腺癌中高度特异性表达,暗示其可能在前列腺癌中发挥重要作用,为深入研究,我们将完整的PCA3基因转入真核表达载体,并构建慢病毒包装系统。方法:从前列腺癌细胞株LNCaP细胞中提取总RNA,运用重叠延伸方法扩增到PCA3基因,测序正确后定向接入真核表达载体pCDH-CMV-MCS-EF1-copGFP,酶切鉴定并测序正确后进行慢病毒包装和滴度测定。结果:经PCR鉴定及测序,PCA3表达质粒序列与Gene Bank序列进行Blast比对分析,同源性为99.8%,PCA3慢病毒滴度测定为2×108。结论:PCA3成功插入真核表达载体并完成了慢病毒包装,为深入研究PCA3基因在前列腺细胞中的作用奠定了基础,进而为探索前列腺癌的治疗提供了新的途径。
前列腺癌;前列腺癌抗原3;真核表达载体;慢病毒
前列腺癌基因3(prostate cancer gene 3,PCA3)是1999年被发现的一种长链非编码RNA[1]。由于PCA3在前列腺癌中的表达具有特异性,它也被用于前列腺癌的早期诊断。已有研究发现,干扰PCA3在前列腺癌细胞株LNCap中的表达后可影响其增殖[2-3],但PCA3的过表达对前列腺癌细胞是否有作用还尚未研究。本文通过PCR扩增PCA3,然后克隆到真核表达载体pCDH-CMV-MCS-EF1-copGFP中,目的是构建重组质粒,用于后续研究PCA3在前列腺癌的增殖和侵袭中的作用。
1 材料和方法
1.1 材料
前列腺癌LnCap细胞株、DU145细胞株、PC3细胞株、TRIzol试剂由本实验室保存;大肠杆菌DH5α、慢病毒载体质粒pCDH-CMV-MCSEF1-copGFP、慢病毒包装系统、病毒生产细胞系293T细胞由胡维国教授惠赠。寡核苷酸引物由上海生工公司合成,逆转录试剂盒、高保真PCR试剂盒、限制性内切酶BamHⅠ、NotⅠ、凝胶纯化回收试剂盒均购自日本Takara公司,质粒小抽试剂盒购自Tiangen公司,其他试剂均为国产或进口分析纯试剂。
1.2 方法
1.2.1 引物设计与合成
根据GenBank的人PCA3基因的序列(序列号:NR_015342.1)设计合成引物,因PCA3含3 735 bp,较难扩增,而且为了保证序列的准确性,本研究设计了3对引物,扩増出3个片段命名为P1、P2、P3,其长度分别为1 263、1 245、1 368 bp,各片段间互相重叠,重叠片段为79及60 bp,便于以后的搭接。引物序列:第1片段P1上游引物F1:5’-ATAGGATCCAGAAGAA ATAGCAAGTGCCGAGAA-3’,下游引物R1:5’-ATAGCGGCCTTTACGTTCTGGGA TACATGT-3’;第2片段P2上游引物F2:5’-GACTAAGTCCTTTATCCCTCCCC-3’,下游引物R2: 5’-GGACTATCCATGAACAC AAAGAGGG-3’;第3片段P3上游引物F3:5’GC TCAGGTGCTTTCACTAATGTCTC-3’,下游引物R3:5’-CGCGGATCCCTTTACGTTCTGGGA TACATGTGCAG-3’,F1、R3引物两端分别加上NotⅠ、BamHⅠ酶切位点。
1.2.2 RNA提取及PCR扩增
采用TRIzol法从PCA3高表达的前列腺癌细胞株LnCap中提取总RNA。取4 μL的RNA用逆转录试剂盒逆转录成cDNA,然后取1 μL用高保真酶扩增PCA3。反应体系20 μL:5×buffer 4 μL,dNTP 2 μL,F1/R1(或F2/R2或F3/R3):0.5/0.5 μL,cDNA:1 μL,HS DNA聚合酶:0.2 μL,ddH2O:11.8 μL扩増出3个片段。PCR扩增条件:94 ℃ 3 min, 98 ℃ 10 s,60 ℃15 s,72 ℃ 1.5 min,72 ℃ 10 min,30个循环。扩增后以1%的琼脂糖凝胶电泳,回收目的片段。然后送测序,测序结果与GenBank中PCA3序列对比,发现序列基本吻合。重叠延伸反应体系20 μL:5×buffer 4 μL,dNTP 2 μL,F2/R2:0.5/0.25 μL及F3/R3:0.25/0.5 μL,模板P2、P3各1 μL,HS DNA聚合酶:0.2 μL,ddH2O:10.3 μL。PCR扩增条件:94 ℃ 3 min,98 ℃10 s,60 ℃ 15 s,72 ℃ 2.5 min,72 ℃ 10 min,30个循环。扩增后1%的琼脂糖凝胶电泳后,回收目的片段。将连接好的后2个片段与第1个片段连接,反应体系20 μL:5×buffer 4 μL,dNTP 2 μL,F1/R3:0.5/0.5 μL,模板P1、P2-P3各1 μL,HS DNA聚合酶:0.2 μL,ddH2O:10.8 μL。PCR扩增条件:94 ℃ 3 min, 98 ℃10 s,60 ℃ 15 s,72 ℃ 4 min,72 ℃ 10 min,30个循环。扩增后1%的琼脂糖凝胶电泳后,回收目的片段并送测序。
1.2.3 重组质粒的构建和鉴定
用NotⅠ、BamHⅠ分别双酶切pCDH-CMVMCS-EF1-copGFP、PCR胶回收产物PCA3分子过夜,然后琼脂糖凝胶电泳检测,切胶后回收酶切片段。将回收的质粒及目的片段以1∶3(摩尔比)进行连接,连接体系10 μL,16 ℃过夜。连接后转化大肠杆菌DH5α并培养,涂布于含氨苄青霉素的LB选择平板,37 ℃培养箱过夜。挑取白色克隆菌落,使用载体多克隆位点两端的引物(F1、R3)进行PCR扩增。PCR扩增条件:94 ℃ 3 min,98 ℃ 10 s,60 ℃ 15 s,72 ℃4 min,72 ℃ 10 min,30个循环,检测载体多克隆位点是否有插入目的基因片段。检测为阳性菌落培养后用小抽试剂盒提质粒,以提取的质粒为模板进行PCR,同时将质粒进行NotⅠ、BamHⅠ双酶切,1%凝胶电泳鉴定,将酶切后和PCR的产物送Invitrogen公司测序,测序引物为3对引物。
1.2.4 慢病毒包装及病毒滴度测定
慢病毒包装:用DMEM培养基培养293T细胞,感染前1天接种到6孔板中,使融合度达到70%~80%。取出2个干净的1.5 mL EP管,各加入500 μL Opti-MEM培养液,将慢病毒包装系统中两种质粒按一定比例与慢病毒载体混合加入其中1个EP管,另外1个EP管加入LipofectamineTM2000,3种质粒的质量与LipofectamineTM2000体积比为1∶1(含空载质粒的病毒的包装同上相同)。混合均匀后静置5 min,然后将2管混合,静置30 min。后将此复合物加入无血清培养液的293T细胞中,培养6 h后弃上清液,加入含10%胎牛血清的培养基继续培养。24 h后荧光显微镜观察,48 h后收取上清液,72 h后再收集1次,于4 ℃条件下12 000×g离心20 min,然后使用0.22 μm滤器过滤,分装于1.5 mL EP管中,冻存于-80 ℃备用。采用逐孔稀释滴度测定法将纯化过的病毒液倍比稀释后感染293T细胞,48 h荧光显微镜观察荧光;用完全培养基按照10倍稀释,最后得到稀释病毒上清的体积均为100 μL。72 h后荧光显微镜下观察。
1.2.5 前列腺癌细胞的培养及感染
RPMI-1640培养基培养前列腺癌细胞DU145及PC3细胞株,细胞消化后按1×105/mL铺在6孔板中,融合度达到70%~80%。吸除培养液,换新鲜培养液,加入30 μL的浓缩病毒,混匀后放入恒温箱。24 h后更换普通培养液,72 h后荧光显微镜观察细胞感染效率。
1.2.6 RT-PCR检测PCA3 mRNA的表达
用TRIzol法提取慢病毒感染DU145及PC3细胞的总RNA,经反转录试剂盒合成cDNA。PCA3RT-PCR检测前引物为:5’-AGAAGAAATAGC AAGTGCCGAGAAG-3’,后引物为:5’-GTGTGGCCTCAGATGGTAAAGTC-3’,β-actin作为内参,使用TaKaRa的RT-PCR试剂盒进行实时荧光定量PCR。
1.3 统计学处理
采用SPSS 11.0统计学软件进行分析,计量资料以x±s 表示,样本均数比较采用单因素方差分析(One-way ANOVA),P<0.05为差异有统计学意义。
2 结 果
2.1 目的基因PCA3 PCR扩增产物电泳结果
从LnCaP细胞中提取的总RNA反转录成cDNA,以此为模板分别扩增P1、P2、P3,然后P2、P3搭接,后再与P1进行重叠延伸反应扩出全长。扩增产物在1%琼脂糖凝胶中进行电泳,显示在3 700 bp处有扩增条带,片段大小与预期相符,表明目的基因克隆成功(图1)。
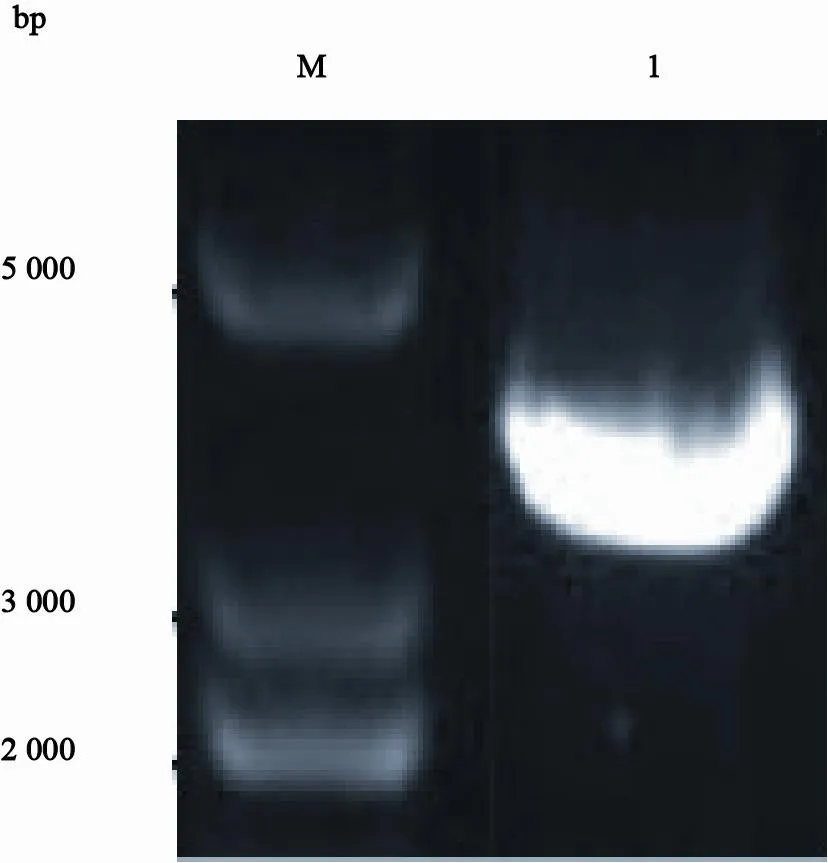
图 1 PCA3重叠延伸PCR扩增产物琼脂糖凝胶电泳图Fig. 1 Agarose gel electrophoresis results of PCR products of PCA3
2.2 慢病毒载体pCDH-CMV-MCS-EF1-copGFP-PCA3测序及双酶切鉴定
将扩出的PCA3片段回收后,插入载体中,然后将重组质粒转化大肠杆菌DH5α,进行菌液PCR,1%琼脂糖凝胶电泳,可见大小约3 735 bp的1条清晰的目的条带,与预计片段相符合(图2)。将质粒载体送测序,测序结果显示表达克隆中插入的目的基因序列与GenBank中PCA3基因的序列(序列号:NR_015342.1)基本相符,大小为3 735 bp,表明慢病毒载体pCDHCMV-MCS-EF1-copGFP-PCA3构建成功。从此阳性克隆株中提取重组质粒,经NotⅠ、BamHⅠ双酶切后可见2个片段,即约7 500 bp的慢病毒载体pCDH-CMV-MCS-EF1-copGFP片段与3 735 bp的目的基因片段,说明重组质粒大小及插入方向正确,重组载体构建成功(图3)。
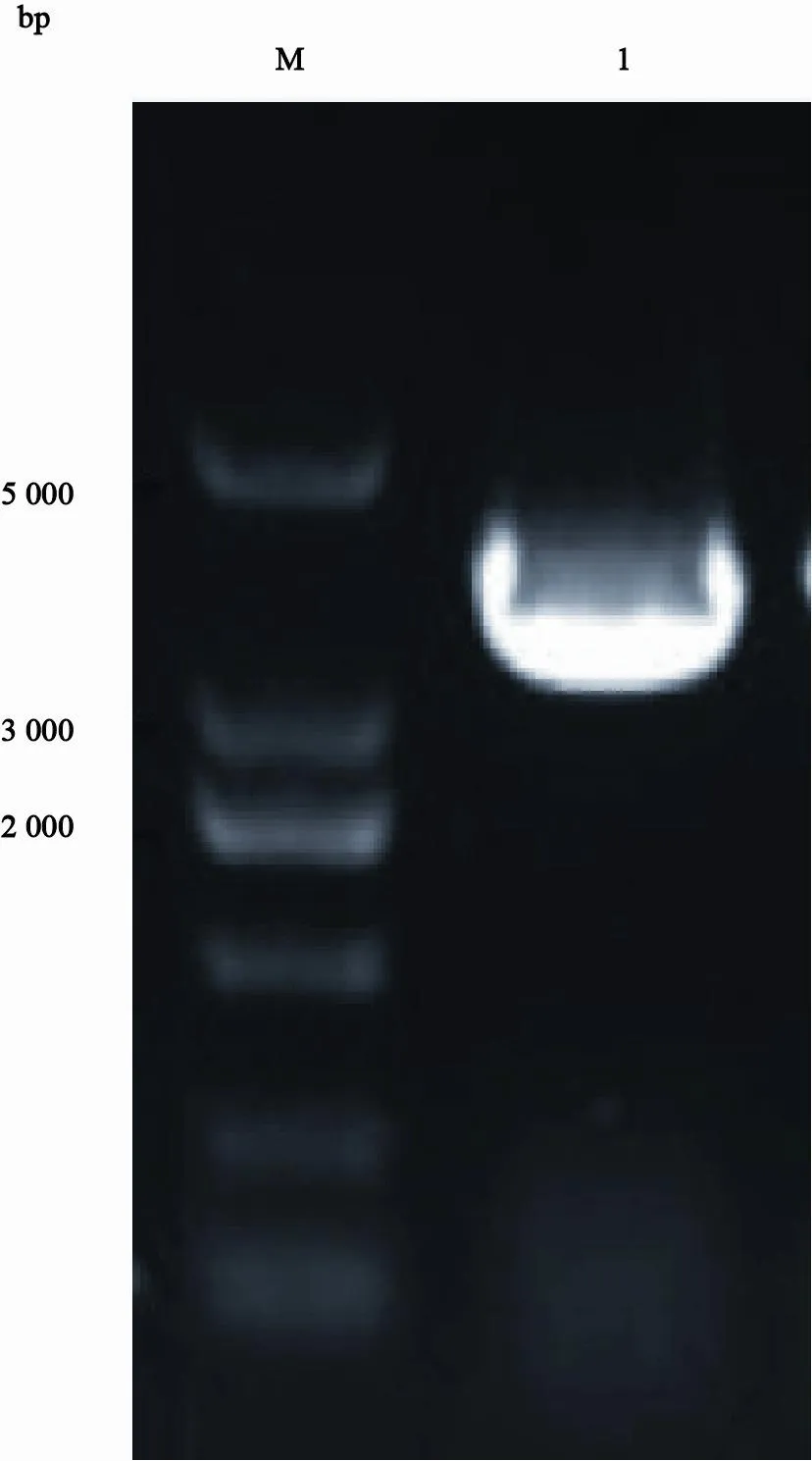
图 2 目的基因PCA3重组克隆PCR鉴定结果Fig. 2 PCR identification results of recombinant lentivirus-PCA3
2.3 慢病毒感染前列腺癌细胞后荧光表达
经过病毒滴度测定,将空载体慢病毒或PCA3过表达慢病毒分别感染前列腺癌细胞株DU145及PC3细胞,细胞感染72 h后,使用荧光显微镜观察,可观察到绿色荧光,感染效率达90%以上(图4)。
2.4 RT-PCR检测慢病毒感染前列腺癌细胞株后PCA3 mRNA的表达
病毒感染细胞株96h后收取两组细胞的RNA,利用反转录试剂盒反转录成cDNA,后进行real-time PCR检测PCA3 mRNA的表达,相对于空载体感染组,PCA3过表达慢病毒组的PCA3 mRNA表达水平上升(P<0.05),表明PCA3过表达成功(图5)。

图 3 pCDH-CMV-MCS-EF1-copGFP-PCA3双酶切鉴定图Fig. 3 Double digestion identification results of pCDH-CMVMCS-EF1-copGFP-PCA3
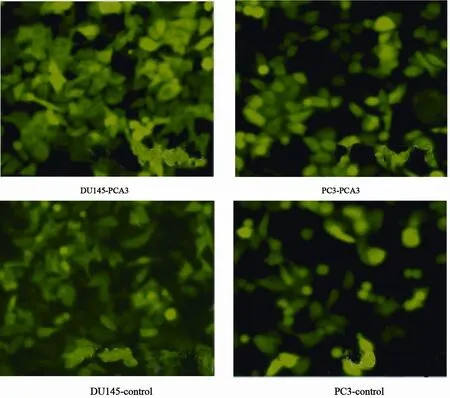
图 4 荧光显微镜观察慢病毒对前列腺癌细胞株的感染效率Fig. 4 GFP expression in lentivirus infected prostate cancer cells

图 5 RT-PCR 检测过表达PCA3基因后前列腺癌细胞株PCA3 mRNA结果Fig. 5 Overexpression of PCA3 mRNA in prostate cancer cells with real time-PCR
3 讨 论
前列腺癌基因3(PCA3)由Bussemakers等[1]于1999年应用差异显示分析比较前列腺癌组织和正常前列腺组织的mRNA表达谱时发现的。它位于第9号染色体上(9q21-22),是一种长链非编码RNA(lncRNA)。报道称多种类型的ncRNA通过对染色质进行修饰、DNA的甲基化、RNA剪接与编辑、转录及转录后基因的沉默、增强基因表达等各种途径参与基因调节[4-5]。在许多生物体内人们还发现了类mRNA样的长ncRNAs,对于它们的功能的研究是较为热门的领域,而PCA3在前列腺癌中的作用尤为备受关注。
Bussemakers等[1]在56个前列腺癌切除样本中发现,有95%的样本其PCA3在癌性组织相对于临近的非癌性组织来说是过度表达的。使用RNA印迹分析来自同一对象的正常前列腺组织和良性前列腺增生(BPH)组织发现其几乎不表达PCA3。用敏感的实时定量反转录聚合酶链反应(qRT-PCR)分析正常前列腺组织和BPH组织中的PCA3显示也仅有较低水平的表达,然而在前列腺癌组织中PCA3表达水平较非恶性组织平均上调近60倍。此外,在其他组织和肿瘤中未发现PCA3[1,6]。初步的研究显示,PCA3在前列腺癌中过表达,对于发现前列腺癌是一个潜在的标志物。然而对于PCA3的功能研究鲜有报道,本课题组曾经以前列腺癌细胞株LNCaP为研究对象,采用针对PCA3的特异干扰RNA转染前列腺癌细胞。结果发现,PCA3 siRNA转染48 h后能显著抑制LNCaP细胞中PCA3的表达水平;运用CCK-8试剂盒检测发现,细胞增殖能力在PCA3 siRNA干扰组显著低于阴性对照组,即在前列腺癌中细胞增殖是PCA3的调控效应之一;克隆形成实验显示,干扰PCA3的表达能够显著减弱LNCaP细胞的克隆形成[2]。为了进一步研究PCA3在前列腺癌细胞株中的作用,我们构建了PCA3过表达病毒载体pCDH-CMV-MCS-EF1-copGFP-PCA3,为后期研究PCA3的功能及其与前列腺癌细胞的作用奠定了实验基础。
目前基因转染途径很多,而慢病毒是较为有效的一种,它具有毒力低、感染效率高、容纳外源性基因片段大等特点。PCA3因分子片段较大,为3 735 bp,我们选择慢病毒使其能将目的基因整合到靶细胞染色体中,并得以长期稳定的表达该基因,因此是目前较为理想的基因治疗载体系统[7]。
综上所述,通过对重组体的酶切鉴定及测序,结果表明成功构建了含有PCA3基因的慢病毒载体,为进一步深入研究PCA3基因在前列腺中的作用机制,进而为探索安全、高效的治疗途径奠定了重要基础。
[1] BUSSEMAKERS M J, VAN BOKHOVEN A, VERHAEGH G W, et al. DD3: a new prostate-specific gene, highly overexpressed in prostate cancer [J]. Cancer Res, 1999, 59(23): 5975-5979.
[2] 曹达龙, 叶定伟, 姚旭东, 等. 前列腺癌特异抗原3对前列腺癌LNCaP细胞增殖的影响 [J].中国癌症杂志, 2012, 22(2): 135-138.
[3] FERREIRA L B, PALUMBO A, DE MELLO K D, et al. PCA3 noncoding RNA is involved in the control of prostate-cancer cell survival and modulates androgen receptor signaling [J]. BMC Cancer, 2012, 12: 507.
[4] SZELL M, BATA-CSORGO Z, KEMENY L. The enigmatic world of mRNA like ncRNAs: their role in human evolution and in human diseases [J]. Semin Cancer Biol, 2008, 18(2): 141-148.
[5] TURNER A M, MORRIS K V. Controlling transcription with noncoding RNAs in mammalian cells [J]. Biotechniques, 2010, 48(6): ix-xvi.
[6] DE KOK J B, VERHAEGH G W, ROELOFS R W, et al. DD3 (PCA3), A very sensitive and specific marker to detect prostate tumors [J]. Cancer Res, 2002(62): 2695-2698.
[7] SAKUMA T, BARRY M A, IKEDA Y. Lentiviral vectors: basic to translational [J]. Biochem J, 2012, 443(3): 603-618.
Construction of eukaryotic expression vector and package of lentivirus vector encoding prostate cancer antigen 3
LIU Xiao-jun1, WANG Na2, YAO Xu-dong1, CAO Da-long1(1.Department of Urology, Fudan University Shanghai Cancer Center, Department of Oncology, Shanghai Medical College Fudan University, Shanghai 200032, China; 2.Department of Cancer Institute, Fudan University Shanghai Cancer Center, Department of Oncology, Shanghai Medical College Fudan University, Shanghai 200032, China)
YAO Xu-dong E-mail: yaoxudong67@sina.com
Background and purpose: The increased of specific expression of prostate cancer antigen 3 (PCA3), as one of long non-coding RNA, has been observed in prostate cancer, indicating that PCA3 may contribute to the development of prostate cancer. To further study its roles in prostate cancer, we construct a lentivirus expression vector carrying the whole PCA3. Methods: PCA3 was amplified from prostate cancer cell line LNCaP by reverse transcriptase polymerase chain reaction (RT-PCR). After the sequence was proved to be correct, we recombined the pCDH-CMV-MCS-EF1-copGFP-PCA3. After transformation into E.coli cells, the candidate clones were identified by PCR amplifying, restricting enzyme digestion analysis and DNA sequencing, and the viral titer was determined. Results: Through the Blast analysis software, we compared the results of PCA3 sequence amplified by PCR with GeneBank sequence, finding that the homology is 99.8%. The lentivirus vector was constructed successfully, and the virus in the supernatant reached a titer of 2*108. Conclusion: The successful construction of the lentivirus vector encoding PCA3 not only lays the foundation for the further research into the effect of PCA3 gene on the prostate cancer but also provides a new therapy for advanced prostate cancer.
Prostate cancer; Prostate cancer antigen 3; Eukaryotic expression vector; Lentivirus
10.3969/j.issn.1007-3969.2013.11.001
R737.25
:A
:1007-3639(2013)11-0857-06
2013-06-13
2013-10-09)
国家自然科学基金(No:81272836);上海市科学技术委员会上海市自然科学基金(No:11ZR1407400);上海市科学技术委员会上海市医学引导类项目(No:114119a4200)。
姚旭东 E-mail:yaoxudong67@sina.com
