胃癌伴神经内分泌分化的临床病理及预后分析
2013-06-07
复旦大学附属肿瘤医院胃及软组织外科,复旦大学上海医学院肿瘤学系,上海200032
胃癌伴神经内分泌分化的临床病理及预后分析
于红梅 刘晓文 龙子雯 张力文 周梦龙 王亚农
复旦大学附属肿瘤医院胃及软组织外科,复旦大学上海医学院肿瘤学系,上海200032
背景与目的:胃是人体重要的具有神经内分泌功能的器官之一,部分胃癌在发生、发展过程中伴随着神经内分泌细胞分化(neuroendocrine cell differentiation,NED)现象,NED对胃癌患者预后的影响还存在争议。本研究旨在探讨胃癌伴NED的临床病理特点、治疗及预后。方法:回顾性分析复旦大学附属肿瘤医院胃及软组织外科2001年3月—2009年7月收治的17例胃癌伴NED患者和具有相同分期的34例不伴NED胃癌患者的临床资料,比较两组患者的临床病理特征和预后差异。结果:肿瘤的发生部位和分化程度与胃癌是否伴有NED具有明显相关性。伴NED的胃癌患者的1年和3年生存率明显低于不伴NED的胃癌患者的1年和3年生存率(71% vs 79%,38% vs 47%,χ2=4.212,P=0.040)。多因素分析结果显示,患者年龄、浸润深度及远处转移是独立的预后因素。结论:免疫组织化学染色对伴NED胃癌的确诊具有重要价值,伴有NED可能是胃癌预后不良的重要因素之一。
胃癌;神经内分泌细胞分化;病理学;预后
胃癌伴神经内分泌细胞分化(neuroendocrine cell differentiation,NED)是指分化的神经内分泌细胞以单个细胞或者细胞巢的形式散在分布于胃癌细胞之间,为胃癌组织的一种伴随成分[1],文献报道其发病率占18.7%~53%[2]。近年来,国内外对胃癌伴NED的研究正在不断深入,而对胃癌预后的正确估计将有助于指导临床进行积极、有效的个体化治疗。本研究回顾分析复旦大学附属肿瘤医院胃及软组织外科9年间收治的17例胃癌伴NED患者和34例具有相同分期的不伴NED的胃癌患者的临床和病理资料,结合随访结果,探讨胃癌伴NED与预后的关系。
1 资料和方法
1.1 一般资料
在2001年3月—2009年7月复旦大学附属肿瘤医院胃及软组织外科共收治胃癌伴NED患者17例,其中男性13例,女性4例,年龄22~77岁,同时抽取同时期内具有相同分期的不伴NED的胃腺癌患者34例。
1.2 诊断标准
确诊主要依靠苏木精-伊红染色下的形态特点和免疫组织化学特异的神经内分泌标志物,包括突触素(synaptophysin,Syn)、嗜铬粒素A(Chromogranin A,CgA)和神经元特异性烯醇化酶(neuron-specific enolase,NSE),3个标志物中有任何1个标志物的表达即为免疫组化神经内分泌标志物阳性。在光镜下发现神经内分泌细胞在癌组织中以单个细胞或细胞巢形式分散存在,且所占比例<30%,即可判断伴NED。
1.3 随访
随访结果通过定期门诊复查的随访资料及电话联系方式获得,截止时间为2012年8月15日,无失访病例,两组随访率均为100%。
1.4 统计学处理
数据处理应用SPSS 19.0软件,百分率比较用χ2检验,生存时间为胃癌手术之日至最后1次随访或死亡时间,并对其进行log-rank检验,作出Kaplan-Meier生存曲线。运用Cox比例风险模型评估伴或不伴NED及各种临床病理因素对胃癌患者预后的影响。P<0.05为差异有统计学意义。
2 结 果
2.1 临床特点
17例胃癌伴NED患者中,发病部位多见于胃体(8例),其次为贲门(6例)、胃窦(3例);所有患者均接受外科手术治疗,其中12例患者进行了根治切除,5例姑息切除。两组患者临床症状相似,主要症状为上腹部不适、吞咽困难、腹痛、腹胀,其他症状包括恶心、黑便和消瘦等,患者均无类癌综合征表现。在这两组患者中,肿瘤的发生部位(P=0.014)和分化程度(P=0.048)与胃癌是否伴有NED具有明显相关性,差异有统计学意义(P<0.05,表1)。
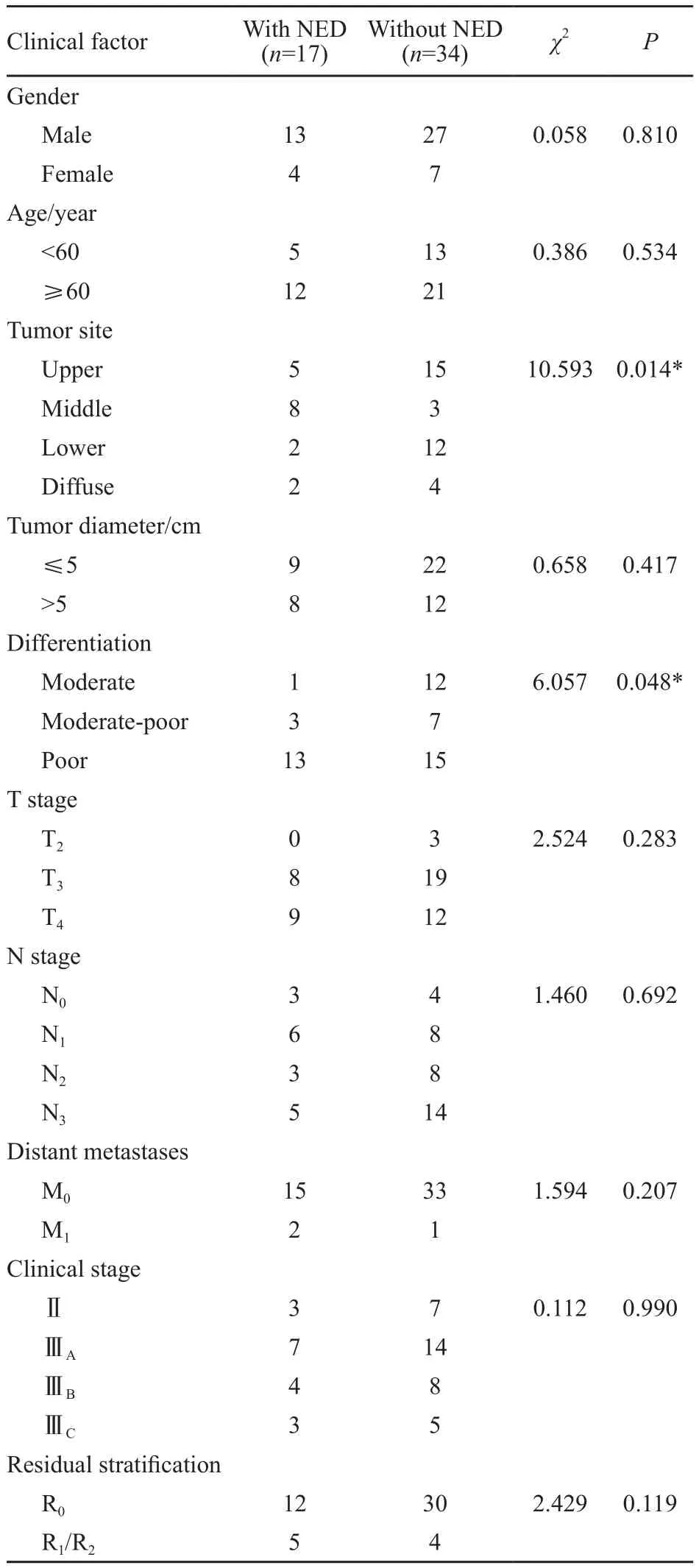
表 1 胃癌伴或不伴NED与临床病理特征的关系Tab. 1 Relationships between gastric cancer with or without NED and its clinicopathological variables
2.2 HE及免疫组化结果
伴NED的胃癌在镜下可见神经内分泌细胞数量多少不等;细胞及细胞核大小不一,极性紊乱;胞质稀少,排列成巢状。免疫组化染色14例Syn阳性,6例CgA阳性,10例NSE阳性(图1)。
2.3 生存分析
中位随访时间27个月(7~109个月),伴NED的胃癌患者术后1年生存率为71%,3年生存率为38%,中位生存期为17个月;不伴NED的胃癌患者术后1年生存率为79%,3年生存率为47%,中位生存期为33.6个月,差异有统计学意义(χ2=4.212,P=0.040),伴NED的胃癌患者术后生存期明显短于不伴NED患者。多因素分析结果显示,患者年龄、浸润深度及远处转移均为胃癌预后的独立影响因素(P<0.05),伴或不伴NED不是影响胃癌预后的独立因素(表2,图2)。

图 1 胃癌伴NED与不伴NED的HE和免疫组织化学染色Fig. 1 HE and immunohistochemical staining for gastric cancer with NED and without NED

表 2 运用COX比例风险模型评估胃癌预后的独立影响因素Tab. 2 Assessment of independent factors influencing prognosis of gastric cancer patients in COX proportional hazard model

图 2 胃癌伴NED与不伴NED患者的Kaplan-Meier生存曲线Fig. 2 Kaplan-Meier survival curves of gastric cancer patients with and without NED
3 讨 论
近年来,胃癌伴NED的现象不断引起学者们的关注。欧洲神经内分泌肿瘤学会和北美神经内分泌肿瘤学会分别于2009年和2010年发布了胃肠胰神经内分泌肿瘤的诊断标准[3-4],2010年第4版WHO消化系统肿瘤分类也对神经内分泌肿瘤的命名和分类作了修订[5],将胃肠胰神经内分泌肿瘤分为神经内分泌瘤(neuroendocrine tumor)、神经内分泌癌(neuroendocrine carcinoma)和混合性腺神经内分泌癌(mixed adenoneuroendocrine carcinoma)。胃神经内分泌瘤属于高分化肿瘤,预后良好;胃神经内分泌癌具有恶性生物学行为,预后不良[6];把神经内分泌细胞达到30%定义为混合性腺神经内分泌癌,而用免疫组织化学证实腺癌中有散在的神经内分泌细胞不被纳入神经内分泌肿瘤之列,被称为腺癌伴神经内分泌分化,并将其归为腺癌一类。
胃癌伴NED在光镜下难以判断,免疫组织化学技术目前已成为最重要的诊断方法。在众多的神经内分泌标志物中,中国胃肠胰神经内分泌肿瘤病理专家组[1]提出,必须检测的项目有Syn、CgA以及核分裂象数和(或)Ki-67。本组病例全部采用免疫组织化学方法,检测Syn、CgA及NSE来判断神经内分泌分化,其中14例Syn阳性,6例CgA阳性,10例NSE阳性。值得注意的是,国内外学者在对胃癌伴NED进行研究时,所采用的神经内分泌标志物组合项目数不尽相同,而且在免疫组化阳性判断标准上也缺乏统一性,使得诊断的准确性和各家研究结果的可比性受到不同程度的影响。我们认为对HE染色疑似伴NED的胃癌患者需要联合检测Syn、CgA以及NSE才更可靠。
胃癌伴NED的治疗原则采取以手术治疗为主的综合治疗方法。手术范围取决于原发肿瘤的病理类型、大小、部位、浸润深度、淋巴结是否受累以及是否存在远处转移,术中要仔细探查是否存在多发灶或并存其他肿瘤,手术方式与一般腺癌无异。本研究中伴NED的17例胃癌患者全部接受手术治疗,其中12例进行了根治切除,5例姑息切除。由于神经内分泌细胞能产生促肿瘤恶性程度增加的因子,其化疗效果不如一般腺癌。生长抑素类似物在治疗神经内分泌肿瘤中显示出很好的效果,它不仅可以减轻功能性神经内分泌肿瘤分泌多肽类激素所引起的症状,还可以通过阻断细胞周期G1期,从而达到控制肿瘤生长的作用,能使1/3神经内分泌肿瘤患者的病情由进展转为稳定[7]。
目前多数学者认为肿瘤伴发的神经内分泌细胞是肿瘤发展过程中干细胞多向分化的结果,细胞分化障碍时肿瘤细胞获得较强的增殖优势,肿瘤很快进入相对晚期[8]。本研究也发现,在伴NED的胃癌患者中超过一半已达到T4期,手术时晚期病人占大多数,且更易发生远处转移。然而,胃癌伴NED患者的术后生存情况,各文献报道不同。Naritomi等[9]研究发现胃癌伴NED的患者术后生存时间较短,预后差。何松等[10]也得出了相似的结论。但Radi等[11]认为,伴NED的胃癌反而比一般腺癌预后好。此外,还有学者解释胃腺癌中神经内分泌分化虽然可能不是独立的提示肿瘤预后的因素,但可以在一定程度上影响肿瘤的分级和分期[12]。本研究中伴有NED的胃癌患者总体预后不佳,3年生存率仅为38%,与汪慧访等[13]报道的相符,伴有NED组术后生存时间明显短于无NED组,差异有统计学意义(χ2=4.212,P=0.040)。多因素分析结果显示,患者年龄、浸润深度及远处转移均为胃癌预后的独立影响因素(P<0.05),但是伴或不伴NED不是影响胃癌预后的独立因素。因此,本研究认为,胃癌伴NED可能在胃癌进展过程中起着促进作用,是否伴NED可以作为辅助判断胃癌预后的一项指标,在临床上应对这一部分特殊病例采取积极而有效的治疗措施。
综上所述,免疫组织化学染色对伴NED胃癌的确诊具有重要价值,伴有NED可能是胃癌预后不良的重要因素之一,判断是否伴有NED,对于临床医师进行预后评估及辅助治疗的选择有一定价值。然而,神经内分泌细胞与胃癌恶性程度的关系以及术后个体化治疗方案的拟定,将有待于进一步研究。
[1] 中国胃肠胰神经内分泌肿瘤病理专家组. 中国胃肠胰神经内分泌肿瘤病理学诊断共识[J]. 中华病理学杂志, 2011, 40(4): 257-262.
[2] QVIGSTAD G, SANDVIK A K, BRENNA E, et al. Detection of chromogranin A in human gastric adenocarcinomas using a sensitive immunohistochemical technique [J]. Histochem J, 2000, 32(9): 551-556.
[3] KLOEPPEL G, COUVELARD A, PERREN A, et al. ENETS Consensus Guidelines for the Standards of Care in Neuroendocrine Tumors: towards a standardized approach to the diagnosis of gastroenteropancreatic neuroendocrine tumors and their prognostic stratification [J]. Neuroendocrinology, 2009, 90(2): 162-166.
[4] KLIMSTRA D S, MODLIN I R, ADSAY N V, et al. Pathology reporting of neuroendocrine tumors: application of the Delphic consensus process to the development of a minimum pathology data set [J]. Am J Surg Pathol, 2010, 34(3): 300-313.
[5] BOSMAN F T, CARNEIRO F, HRUBAN R H, et al. WHO classification of tumours of the digestive system [M]. Geneva: World Health Organization, 2010: 1-314.
[6] LA ROSA S, INZANI F, VANOLI, et al. Histologic characterization and improved prognostic evaluation of 209 gastric neuroendocrine neoplasms [J]. Hum Pathol, 2011, 42(10): 1373-1384.
[7] AMOLD R, SIMON B, WIED M. Treatment of neuroendocrine GEP tumors with somatostatin analogues: a review [J]. Digestion, 2000, 62(1): 84-91.
[8] FURLAN D, CERUTTI, UCCELLA S, et al. Different molecular profiles characterize well-differentiated endocrine tumors and poorly differentiated endocrine carcinomas of the gastroenteropancreatic tract [J]. Clin Cancer Res, 2004, 10(3): 947-957.
[9] NARITOMI K, FUTAMI K, ARIMA S, er al. Malignant potential regarding mucin phenotypes and endocrine cell differentiation in gastric adenocarinoma [J]. Anticancer Res, 2003, 23(6): 4411-4422.
[10] 何松, 严桥, 陈旭东, 等. 胃癌细胞中神经内分泌分化与术后生存关系的研究 [J]. 中国肿瘤临床, 2007, 3(22):1283-1286.
[11] RADI M J, FENOGLIO-PREISER C M, BARTOW S A, et al. Gastric carcinoma in the young: a clinicopathological and immunohistochemical study [J]. Am J Gastroenterol, 1986, 81(9): 741-756.
[12] MARCU M, PADU E, SAJIN M. Neuroendocrine transdifferentiation of prostate carcinoma cells and its prognostic significance [J]. Rom J Morphol Embryol, 2010, 51(1): 7-12.
[13] 汪慧访, 武爱文, 袁鹏, 等. 具有神经内分泌特征胃癌的诊治及预后分析 [J]. 中华胃肠外科杂志, 2011, 14(2): 96-99.
Analysis of clinicopathological features and prognosis of gastric cancer with neuroendocrine cell differentiation
YU Hong-mei, LIU Xiao-wen, LONG Zi-wen, ZHANG Li-wen, ZHOU Meng-long, WANG Ya-nong (Department of Gastric Cancer and Soft Tissue Sarcoma, Fudan University Shanghai Cancer Center; Department of Oncology, Shanghai Medical College, Fudan University, Shanghai 200032, China)
WANG Ya-nong E-mail: wangyn1111@hotmail.com
Background and purpose:Stomach plays an important role in neuroendocrine function, therefore some cases of gastric cancer couple with neuroendocrine cell differentiation (NED). The prognostic significance of NED in gastric cancer patients is still in controversy. The aim of this study was to investigate the clinicopathological features, treatment, and prognosis of gastric cancer with NED. Methods:From Mar. 2001 to Jul. 2009, 17 gastric cancer patients with NED and 34 without NED having the same stage
gastrectomy in Fudan University Shanghai Cancer Center. Clinicopathological features and prognosis of the 2 groups were compared. Results:Tumor location and differentiation were significantly related with NED. The 1 and 3 years survival rates were significantly lower in gastric cancer patients with NED than in those without NED (71% vs 79%, 38% vs 47%, χ2=4.212, P=0.040). The Cox proportional hazard model was used in multivariate analysis. Conclusion:Immunohistochemistry is important to the diagnosis. With NED may be one of the important factors for the poor prognosis of gastric cancer patients.
Gastric cancer; Neuroendocrine cell differentiation; Pathology; Prognosis
R735.2
:A
:1007-3639(2013)01-0042-05
2012-09-03
2012-11-22)
王亚农 E-mail:wangyn1111@hotmail.com
DOI: 10.3969/j.issn.1007-3969.2013.01.007
