电感耦合等离子体质谱测定硫的方法研究及应用进展
2013-05-28黄志丁杨晓进
黄志丁,王 军,逯 海,杨晓进
(1.北京化工大学化学工程学院,北京 100029;2.中国计量科学研究院,北京 100013)
硫元素广泛存在于自然界中,与人类生活密切相关。硫元素有-2、0、+4、+6等多种化合价,对应的S2-、S、SO32-、S2O32-和SO42-是几种常见的含硫形态。硫含有18种同位素,其中32S、33S、34S、36S属于稳定同位素。硫元素是矿石、蛋白质、化石燃料等物质的重要组成元素,因此,硫的测定在地球化学、蛋白质组学、环境科学等领域受到了广泛关注。例如,在地球化学中,可通过对硫及其同位素分布的研究,考察特定时期的地球活动[1];在蛋白质组学中,硫是蛋氨酸(人体必需氨基酸之一)的组成元素,并被认为是最适合用于蛋白质定量分析的内标元素[2];在环境科学中,硫不仅是影响气候变化的重要元素[3],还是环境污染的主要来源之一。为了控制和降低硫造成的环境污染,国内外关于汽油和柴油燃料中硫限量标准越来越低,因而对硫(特别是微痕量硫)的准确分析测定提出了更高的要求。目前已有多种分析方法被用于各种基体样品中硫的测量,如分光光度法[4]、离子色谱法[5]、X-射线荧光光谱法[6]等。
20世纪80年代发展起来的电感耦合等离子体质谱法(ICP-MS)[7],因具有图谱简单,检出限低,线性动态范围宽,灵敏度高,样品处理简单,分析速度快,可进行多元素分析,可与高效液相色谱、离子色谱、气相色谱等分离技术联用等优点[8-9],已成为一种广泛使用的、有利的元素和元素形态分析技术。近年来,ICP-MS用于硫元素总量、形态和同位素等方面的分析研究受到越来越多的关注,并且在地质学、蛋白质组学、环境科学等领域中也得到了广泛和深入的应用。
本工作着重阐述ICP-MS用于硫测定时所存在技术问题的研究进展,总结ICP-MS测定硫的方法在地质学、蛋白质组学、环境科学、食品科学、计量学等领域中的应用,并展望了ICP-MS测定硫的方法研究和应用。
1 ICP-MS测定硫的方法研究进展
1.1 ICP-MS测定硫的干扰及其消除
虽然ICP-MS在硫的测量中具有独特的优势,但由于ICP-MS测定易受到多种复合离子的干扰以及样品基体的影响,如何克服或消除各种干扰已成为研究人员关注的焦点。
1.1.1 质谱干扰及其消除 ICP-MS测定硫的质谱干扰主要包括同量异位素、多原子分子离子和双电荷离子干扰等。其中,多原子分子离子是ICP-MS测定硫的最主要干扰因素,它们主要是由样品基体及酸或溶剂中引入的H、O、N和样品本底元素等在等离子体中发生离子分子反应而形成。ICP-MS测定硫时潜在的多原子分子离子干扰列于表1。
在ICP-MS测定中,采用碰撞/反应池技术(CC/DRC)或提高质谱仪的分辨率可有效地消除多原子分子离子的干扰。碰撞/反应池技术又分为两种模式:一是加入碰撞气体,通过电荷转移效应消除多原子分子离子对S+的干扰。Mason等[10]用 He/H2/Xe混合气体作为碰撞气取得了良好的效果,示于图1;另一种是加入O2作为反应气,将S+氧化为SO+,从而避开了O2+的干扰[11]。当测定蛋白质、药物等含有大量有机物基体中的硫时,可能还会受到碳的干扰。如 Wolf等[12]采用 HPLC-ICP-CC-MS测定氯氮平中的硫时,加入O2后测定质量数为48和50处信号时受到了ArC+的干扰。

表1 ICP-MS测定硫中潜在的多原子分子离子干扰Table 1 Possible polyatomic interferences in sulfur analysis by ICP-MS
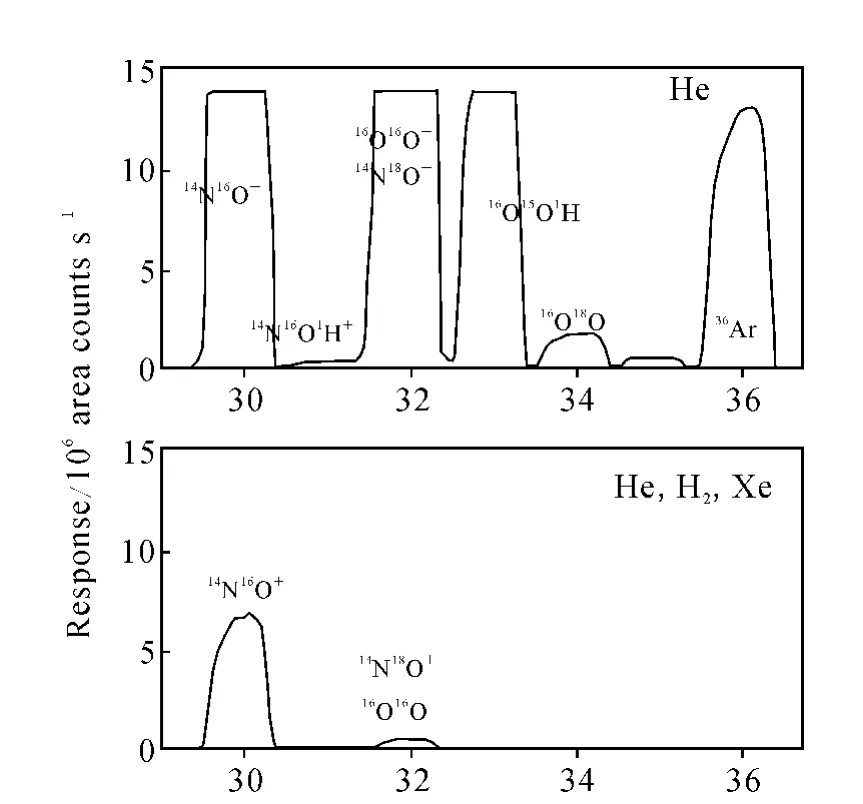
图1 加入碰撞气体后m/z 30~36处的信号Fig.1 Addition of collision gases on response from m/z 30to m/z 36
消除ICP-MS测定硫时质谱干扰的另一种重要方式是使用高分辨率电感耦合等离子体质谱(HR-ICP-MS)[13-14]。从表1可以看出,理论上当分辨率达到844~1 800时,即可将干扰谱线与硫的谱线有效地分开,解决部分多原子分子离子干扰的问题。但是,该技术的缺点是提高分辨率会导致待测元素灵敏度损失。
1.1.2 非质谱干扰及其消除 ICP-MS测定过程中,各式各样的化学或物理效应将不同程度地影响目标元素测定的准确性,由此产生的测定干扰即为非质谱干扰。关于ICP-MS测定硫中消除非质谱干扰的研究已有报道,其中最有效的方法是采用必要的样品前处理技术,如通过离子交换分离、共沉淀分离,使样品基体中的干扰成分与被测物分离,同时还能降低溶液总盐度,富集被测物。Menegaário等[15]把带有阴离子交换柱AG1-X8的进样系统与ICP-MS雾化器连接,用于水稻中硫同位素34S/32S的测定,使硫的测量灵敏度增加至原来的3.71倍,硫含量为17 mg/L的溶液中34S/32S的 RSD<1%(n=5)。Craddock等[16]将含硫矿物用 HNO3/HCl混合酸消解后,使用AG50-X8阳离子交换柱分离样品中的Fe、Ca、Cu、Zn等元素,硫的回收率达到(98±4)%。
1.2 硫形态分析测定
硫有多种不同的价态,常见的无机硫存在形态主要有S2-、S、S2O32-、SO32-、SO42-等,硫的形态分析在制药、石油勘探、化工过程、环境污染源的确定等方面发挥着重要作用。但ICP-MS等离子体源的高温(6 000~10 000K)会破坏物质的化学结构而不能直接进行形态分析[17],因此,需要将ICP-MS与相应的分离技术联用,以实现对不同形态或不同种类含硫化合物的准确测定。目前,硫形态的分析主要采用气相色谱(GC)、高效液相色谱(HPLC)、离子色谱(IC)等色谱分离技术与ICP-MS联用,将在ICP-MS应用部分给出详细介绍。
研究发现在ICP-MS测定中,部分元素的不同形态或价态的灵敏度有较大差异[18],形态的差异给硫含量的准确测定也带来了难以确定的影响。黄志丁等[19]研究了ICP-MS测定硫时不同形态硫的影响,结果表明,在2%HNO3溶剂介质中,S2-、SO32-中硫的ICP-MS测量灵敏度(标准曲线的斜率)分别约为SO42-的6倍和4倍,S2O32-的灵敏度与SO42-基本一致,示于图2。
对于S2-,H2S的离解常数明显低于H2S2O3和 H2SO4;对于SO32-,溶液中存在着化学平衡(公式(1),(2),(3))。因此,S2-、SO32-在HNO3介质中存在着气态的 H2S和SO2,使得ICP-MS测定的雾化效率和离子化效率显著提高,从而导致测量灵敏度的提高。
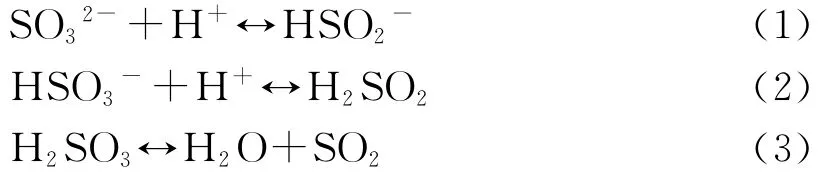
Divjak等[20]将IC-ICP-MS 用 于 水 溶 液 中S2-、SO32-、SO42-、S2O32-的测定研究,结果表明,以60mmol/L NaOH溶液作为淋洗液可将S2-、SO32-、SO42-、S2O32-有 效 分 离,S2-、SO32-、SO42-、S2O32-的检出限分别为35、200、130、270mg/L。

图2 S2- 、S2O32- 、SO32- 、SO42-标准曲线对比Fig.2 Calibration curves in S2- ,S2O32- ,SO32- and SO42-solution
2 ICP-MS测定硫的应用研究进展
目前ICP-MS测定硫的方法和技术主要应用在地质学、蛋白质组学、环境科学、食品科学、计量标准研究等领域。
2.1 地质学
硫是大多数矿床中的成矿元素之一,测定矿石中的硫含量对矿床的开发或形成条件的研究具有重要意义。范立民等[21]探讨了陕北侏罗纪煤田榆神矿区低硫煤中的硫含量特征及其成因,发现煤中硫含量与成煤物质、沉积环境、沼泽的覆水程度等有关,该研究对低硫煤矿区的开发具有指导意义。Makishima等[22]将地质材料酸解后,用Br2把样品中的硫氧化为硫酸根,再用同位素稀释(ID)技术与 HR-ICP-MS相结合,测定了硅酸盐样品中痕量硫,32S和34S的检出限分别为0.07μg/g和0.3μg/g。
近年来,样品前处理简单的激光剥蚀(LA)技术与ICP-MS联用在地学研究中倍受青睐。Guillong等[23]通过测定美国NIST标准物质样品,系 统 地 研 究 了 LA-Q-ICP-MS 和 LA-SFICP-MS测定流体包裹体中硫含量的准确性,两种方法的测定误差分别为小于7%和小于5%,均能满足地质样品中硫含量测定的要求。Seo等[24]还采用 LA-SF-ICP-MS考察了铜-金矿床形成过程中流体包裹体的硫含量,发现大量的硫(相对于金和铜)是铜-金矿床形成的重要元素。Seo等[25]研究发现激光剥蚀过程中的硫污染会导致该方法的检出限偏高,通过反复清洗激光池体可在一定程度上降低硫的本底干扰。
同位素技术是地质学研究中的重要手段,硫同位素组成的分析测定是ICP-MS方法的另一重要应用领域。国际纯粹与应用化学联合会(IUPAC)在2002年发表的技术报告[26]中指出,自然界中硫同位素变化较大,δ(34S)值在-55‰~+135‰之间。Cai等[27]通过考察黄铁矿中的δ(34S)值,研究了鄂尔多斯东胜铀矿中与石油相关矿石的形成过程,该铀矿中δ(34S)值为-34‰~+17‰,表明了黄铁矿中的硫主要来源于硫酸盐还原菌的还原作用。此外,研究发现该矿中铀的总量与δ(34S)值的大小之间并无直接关联性。Thomas等[28]通过采用 MC-ICP-MS测定矿石中硫同位素组成,研究了层控矿床和脉型矿床之间的关系,以及硫在不同类型矿床成矿中的作用和矿石沉积机理。Aebersold等[29]使用ICP-MS考察了海底热液中铁和硫同位素分馏及其机理,并对海底热液矿床的成矿机制进行了分析。
2.2 蛋白质组学
蛋白质定量分析是蛋白质组学研究中的重要内容之一。然而由于蛋白质表达的动态范围大、种类繁多、目标分析物含量低、蛋白质翻译后修饰改变了目标蛋白质的化学性质等原因[30],使得蛋白质的准确定量面临着艰巨挑战。此外,就分析技术而言,普遍使用的电喷雾电离质谱(ESI-MS)和基质辅助激光解吸质谱(MALDIMS)技术,由于受到质谱信号与蛋白质含量不呈线性的限制[31],难以实现蛋白质的准确定量分析。
近年来,ICP-MS技术越来越多的被应用于蛋白质的定量分析研究。由于绝大多数蛋白质中含有硫,且较为稳定,因此通过测定硫含量来实现蛋白质的定量测量受到广泛关注。HPLC分离技术与ICP-MS联用是蛋白质中硫含量测定的常用方法[32-34]。Giner等[35]使用 HPLC 与ICP-MS联用技术,采用等度淋洗的方式将样品中的硫酸盐、半胱氨酸、谷胱甘肽、蛋氨酸有效分离,实现了含硫生物样品的定量分析。Yeh等[36]采用毛细管电泳(CE)ICP-MS对4种氨基酸(L-半胱氨酸,L-胱氨酸和DL-同型半胱氨酸和L-蛋氨酸)中的硫含量进行测定,得到的4种氨基酸的检出限范围为0.047~0.058mg/L(以硫计),回收率为92%~128%。
由于蛋白质样品种类繁多,结构复杂,采用联用技术定量分析时需要使用与待测样品相匹配的标准物质保障量传和质控,但目前可使用的标准物质十分匮乏。同位素稀释质谱(IDMS)法是国际公认的权威定量分析方法,它只需要一种硫浓缩同位素即可实现不同基体的蛋白质中硫的准确测定[37]。Schaumloffel等[38]建立了HPLC-ICP-ID-MS测定肽中硫的方法,回收率为103%,相对标准偏差为2.1%。Wang等[39]采用HPLC柱后同位素稀释质谱技术,测定了牛血清蛋白、超氧化物歧化酶和金属硫蛋白中的硫,实现了对蛋白质中不同组成的定量测定。
2.3 环境科学
硫是石油、汽油、柴油等燃料中含量最高的杂质元素,是造成催化剂中毒和环境污染的主要原因[40]。Evans等[41]以硅作为内标元素,用HR-ICP-MS结合同位素稀释技术准确测定了柴油中的硫,方法的总不确定度为1%~2%。Heilmann等[42]采用ICP-ID-MS研究了两种样品前处理技术(微波消解和高效雾化器直接进样(DIHEN))对汽油、柴油、煤油等燃料中硫含量测定的影响,两种样品处理方法的测量检出限分别为4μg/g(微波消解)和18μg/g(DIHEN)。随后,Bowlyga等[43]又采用 LA 与ICP-MS联用的方法对化石燃料中的硫含量进行直接测定,方法检出限为0.04μg/g。
石油中含硫化合物主要是噻吩及其衍生物,它们容易挥发且含量相对较低,GC与ICP-MS联用常用于石油产品中含硫化合物的分析。研究表明,GC-HR-ICP-MS的方法检出限可达7μg/L,能够满足“无硫”汽油和轻油中噻吩及其衍生物的测定要求[44-45]。硫含量较高的石油产品中硫的形态分析和定量测量也可通过GC-ICP-MS方 法 实 现。Bouyssiere 等[46]使 用GC-ICP-CC-MS在30min内完成了石油、汽油等样品中不同形态硫的分离和测定。
2.4 食品科学
食品中的含硫化合物对食品的质量和特性有很大作用和影响。通过对不同含硫化合物(硫醇、硫化物、硫醚等)的分析可以鉴定不同类型的奶酪[47]。啤酒或葡萄酒中含硫化合物的量对酒的香味和质量有很大影响[48]。Ricardo等[49]测定了34种西班牙葡萄酒中的几种含硫物质含量,结果显示乙硫醇(EtSH)、二甲基硫醚(DMS)、硫酸二乙酯(DES)的含量普遍高于葡萄酒的香气阈值。Yu等[50]测定了几种市售葡萄酒中的含硫物质,结果表明,这些葡萄酒中H2S和MeSH(甲硫醇)的含量分别为0.48~9.26μg/L,此外,还检测到痕量二硫化物和三硫化物。硫同位素可用于啤酒的真伪鉴别和原产地溯源。Giner等[51]以硅同位素作内标,用MC-ICP-MS测定了26种不同品牌啤酒中的硫同位素变化,实验测得26种啤酒的δ(34S)在-0.2‰~13.8‰之间,测量不确定度≤2%,为啤酒品牌的鉴别以及食物或饮料中硫同位素组成的变化提供了科学依据。
2.5 化学计量标准
标准物质是我国计量法中依法管理的计量标准,作为量值传递的有效载体,对确保测量结果的可靠、有效及国际互认具有关键作用。国内外现有的硫有证标准物质的信息列于表2。目前,国内外能用于硫分析测量的计量标准十分有限,复杂基体样品(如石油化工产品、生物、食品等)以及硫形态、硫同位素方面的标准物质严重匮乏。
3 展望
近年来,ICP-MS分析技术已在硫总量、形态和同位素组成的分析测定中体现出了重要的使用价值。环境保护、食品安全、生命科学、矿产资源等领域对各种硫成分含量、同位素测定需求的增长为ICP-MS用于硫分析提供了广阔的发展空间。然而,由于各种类型的含硫样品基体复杂,进一步深入开展用于ICP-MS分析的样品前处理技术研究和优化,研发克服或降低ICP-MS测定中各种干扰的技术十分必要;在硫形态分析方面,液相色谱、离子色谱、气相色谱等分离技术与ICP-MS联用已获得了良好的效果,但对于硫形态复杂的样品,在测量方法学上还有待进一步探索和研究。在硫同位素测量方面,ICP-MS结合碰撞反应池技术或使用高分辨率模式为硫同位素组成变化研究提供了有效途径。另外,激光剥蚀技术与ICP-MS联用极大地提高硫的测定效率和样品原位分析的能力,相应的研究和应用也具有良好的发展前景。随着行业领域对各种硫成分分析测定需求的发展,应加快硫的多种特性量标准物质(典型基体、同位素、形态、浓缩稀释剂等)的研发,建立和完善相应的标准测量方法,不断提高计量标准的技术含量和品质,并加强其推广和使用,为硫测量量值的可比性和可靠性提供有效保障。
[1] GILL B C,LYONS T W,YOUNG S A,et al.Geochemical evidence for widespread euxinia in the Later Cambrian ocean[J].Nature,2011,469(7 328):80-83.
[2] WIND M,WEGENER A,EISENMENGER A,et al.Sulfur as the key element for quantitative protein analysis by capillary liquid chromatography coupled to element mass spectrometry[J].Angewandte Chemie International Edition,2003,42(29):3 425-3 427.
[3] CARROLL M R.Climate change:Volcanic sulphur in the balance[J].Nature,1997,389(6 651):543-544.
[4] BURAKHAM R,HIGUCHI K,OSHIMA M,et al.Flow injection spectrophotometry coupled with a crushed barium sulfate reactor column for the determination of sulfate ion in water samples [J].Talanta,2004,64(5):1 147-1 150.
[5] OHIRA S I,TODA K.Ion chromatographic measurement of sulfide,methanethiolate,sulfite and sulfate in aqueous and air samples[J].J Chromatogr A,2006,1 121(2):280-284.
[6] 中国石油大庆油田工程有限公司分析检测中心.GB/T 17606—2009原油中硫含量的测定[S].北京:中国标准出版社,2009.
[7] HOUK R S,FASSEL V A,FLESCH G D,et al.Inductively coupled argon plasma as an ion source for mass spectrometric determination of trace elements[J].Anal Chem,1980,52 (14):2 283-2 289.
[8] AMMANN A A.Inductively coupled plasma mass spectrometry (ICP MS):A versatile tool[J].J Mass Spectrom,2007,42(4):419-427.
[9] BEAUCHEMIN D.Inductively coupled plasma mass spectrometry[J].Anal Chem,2008,80(12):4 455-4 486.
[10] MASON P R D,KASPERS K,BERGEN M J.Determination of sulfur isotope ratios and concentrations in water samples using ICP-MS incorporating hexapole ion optics[J].J Anal Atom Spectrom,1999,14(7):1 067-1 074.
[11] BANDURA D R,BARANOV V I,TANNER S D.Detection of ultratrace phosphorus and sulfur by quadrupole ICPMS with dynamic reaction cell[J].Anal Chem,2002,74(7):1 497-1 502.
[12] WOLF K D,BALCAEN L,Van De WALLE E,et al.A comparison between HPLC-dynamic reaction cell-ICP-MS and HPLC-sector field-ICPMS for the detection of glutathione-trapped reactive drug metabolites using clozapine as a model compound[J].J Anal Atom Spectrom,2010,25(3):419-425.
[13] PROHASKA T,LATKOCZY C,STINGEDER G.Precise sulfur isotope ratio measurements in trace concentration of sulfur by inductively coupled plasma double focusing sector field mass spectrometry[J].J Anal At Spectrom,1999,14(9):1 501-1 504.
[14] RODRÍGUEZ-FERNÁNDEZ J,MONTES-BAY ÓN M,PEREIRO R,et al.Gas chromatography double focusing sector-field ICP-MS as an innovative tool for bad breath research[J].J Anal At Spectrom,2001,16(9):1 051-1 056.
[15] MENEGAÁRIO A A,GINE M F,BENDASSOLLI J A,et al.Sulfur isotope ratio (34S:32S)measurements in plant material by inductively coupled plasma mass spectrometry[J].J Anal Atom Spectrom,1998,13:1 065-1 067.
[16] CRADDOCK P R,ROUXEL O J,BALL L A,et al.Sulfur isotope measurement of sulfate and sulfide by high-resolution MC-ICP-MS[J].Chem Geol,2008,253(3/4):102-113.
[17] SCHAUMLÖFFEL D,THOLEY A.Recent directions of electrospray mass spectrometry for el-emental speciation analysis[J].Anal Bioanal Chem,2011,400(6):1 645-1 652.
[18] NARUKAWA T,KUROIWA T,CHIBA K.Mechanism of sensitivity difference between trivalent inorganic As species[As(III)]and pentavalent species[As(V)]with inductively coupled plasma spectrometry[J].Talanta,2007,73 (1):157-165.
[19] 黄志丁,王 军,逯 海,等.电感耦合等离子体质谱法测定硫时不同形态硫的影响[J].岩矿测试,2012,31(1):77-82.
[20] DIVJAK B,GOESSLER W.Ion chromatographic separation of sulfur-containing inorganic anions with an ICP-MS as element-specific detector[J].J Chromatogr A,1999,844(1/2):161-169.
[21] 范立民,寇贵德,侯飞龙.榆神低硫煤中硫含量特征及成因探讨[J].中国煤田地质,2003,15(2):12-13.
[22] MAKISHIMA A,NAKAMURA E.Determination of total sulfur at microgram per gram levels in geological materials by oxidation of sulfur into sulfate with in situ generation of bromine using isotope dilution high-resolution ICPMS[J].Anal Chem,2001,73(11):2 547-2 553.
[23] GUILLONG M,LATKOCZY C,SEO J H,et al.Determination of sulfur in fluid inclusions by laser ablation ICP-MS[J].J Anal Atom Spectrom,2008,23(12):1 581-1 589.
[24] SEO J H,GUILLONG M,HEINRICH C A.The role of sulfur in the formation of magmatichydrothermal copper-gold deposits[J].Earth Planet Sc Lett,2009,282(1/2/3/4):323-328.
[25] SEO J H,GUILLONG M,AERTS M,et al.Microanalysis of S,Cl,and Br in fluid inclusions by LA-ICP-MS[J].Chem Geol,2011,284(1/2):35-44.
[26] COPLEN T,BHLKE J,De BIEVRE P,et al.Isotope-abundance variations of selected elements:(IUPAC technical report)[J].Pure Appl Chem,2002,74(10):1 987-2 017.
[27] CAI C,LI H,QIN M,et al.Biogenic and petroleum-related ore-forming processes in Dongsheng uranium deposit,NW China[J].Ore Geol Rev,2007,32(1/2):262-274.
[28] BETTMER J,MONTES BAYON M,RUIZ ENCINAR J,et al.The emerging role of ICP-MS in proteomic analysis[J].J Proteomics,2009,72(6):989-1 005.
[29] AEBERSOLD R,MANN M.Mass spectrometry-based proteomics[J].Nature,2003,422(6 928):198-207.
[30] THOMAS W,MARTIN O,STEFAN W,et al.The role of the Kupferschiefer in the formation of hydrothermal base metal mineralization in the Spessart ore district,Germany:Insight from detailed sulfur isotope studies[J].Miner Deposita,2010,45(3):217-239.
[31] OLIVIER R,WAYNE C S,WOLFGANG B,et al.Integrated Fe-and S-isotope study of seafloor hydrothermal vents at East Pacific Rise 9-10°N[J].Chemical Geology,2008,252(3/4):214-227.
[32] SCHAUMLÖFFEL D.New ways in qualitative and quantitative protein analysis:Nano chromatography coupled to element mass spectrometry[J].J Trace Elem Med Bio,2007,21(S1):18-22.
[33] BALKHI S E,POUPON J,TROCELLO J M,et al.Human plasma copper proteins speciation by size exclusion chromatography coupled to inductively coupled plasma mass spectrometry.solutions for columns calibration by sulfur detection[J].Anal Chem,2010,82(116):6 904-6 910.
[34] HANN S,KOELLENSPERGER G,OBINGER C,et al.SEC-ICP-DRCMS and SEC-ICP-SFMS for determination of metal-sulfur ratios in metalloproteins[J].J Anal Atom Spectrom,2004,19(1):74-79.
[35] GINER M-S J,MORENO S F,HERRERO E P,et al.Evaluation of different analytical strategies for the quantification of sulfur-containing biomolecules by HPLC-ICP-MS:Application to the characterisation of34S-labelled yeast[J].J Anal At Spectrom,2010,25(7):989-997.
[36] YEH C-F,JIANG S-J,HSI T S.Determination of sulfur-containing amino acids by capillary electrophoresis dynamic reaction cell inductively coupled plasma mass spectrometry[J].Anal Chim Acta,2004,502(1):57-63.
[37] RAPPEL C,SCHAUMLOEFFEL D.The role of sulfur and sulfur isotope dilution analysis in quantitative protein analysis[J].Anal Bioanal Chem,2008,390(2):605-615.
[38] SCHAUMLOFFEL D,GIUSTI P,PREUD’HOMME H,et al.Precolumn isotope dilution analysis in nanoHPLC-ICPMS for absolute quantification of sulfur-containing peptides [J]. Anal Chem,2007,79(7):2 859-2 868.
[39] WANG M,FENG W,LU W,et al.Quantitative analysis of proteins via sulfur determination by HPLC coupled to isotope dilution ICPMS with a hexapole collision cell[J].Anal Chem,2007,79(23):9 128-9 134.
[40] CAUMETTE G,LIENEMANN C P,MERDRIGNAC I,et al.Element speciation analysis of petroleum and related materials[J].J Anal At Spectrom,2009,24(3):263-276.
[41] EVANS P,WOLFF-BRICHE C,FAIRMAN B.High accuracy analysis of low level sulfur in diesel fuel by isotope dilution high resolution ICPMS,using silicon for mass bias correction of natural isotope ratios[J].J Anal Atom Spectrom,2001,16(9):964-969.
[42] HEILMANN J,BOULYGA S F,HEUMANN K G.Accurate determination of sulfur in gasoline and related fuel samples using isotope dilution ICP-MS with direct sample injection and microwave-assisted digestion[J].Anal Bioanal Chem,2004,380(2):190-197.
[43] BOULYGA S F,HEILMANN J,HEUMANN K G.Isotope dilution ICP-MS with laser-assisted sample introduction for direct determination of sulfur in petroleum products[J].Anal Bioanal Chem,2005,382(8):1 808-1 814.
[44] HEILMANN J,HEUMANN K G.Development of a species-unspecific isotope dilution GC-ICPMS method for possible routine quantification of sulfur species in petroleum products[J]. Anal Chem,2008,80(6):1 952-1 961.
[45] HEILMANN J,HEUMANN K G.Development of a species-specific isotope dilution GC-ICP-MS method for the determination of thiophene derivates in petroleum products[J].Anal Bioanal Chem,2008,390(2):643-653.
[46] BOUYSSIERE B,LEONHARD P,FROCK D,et al.Investigation of the sulfur speciation in petroleum products by capillary gas chromatogra-phy with ICP-collision cell-MS detection[J].J Anal At Spectrom,2004,19(5):700-702.
[47] SABLÉS,COTTENCEAU G.Current knowledge of soft cheeses flavor and related compounds[J].J Agr Food Chem,1999,47(12):4 825-4 836.
[48] LANDAUD S,HELINCK S,BONNARME P.Formation of volatile sulfur compounds and metabolism of methionine and other sulfur compounds in fermented food[J].Applied microbiology and biotechnology,2008,77 (6):1 191-1 205.
[49] RICARDO L′OPEZ,CRISTINA L A,CACHO J,et al.Quantitative determination of wine highly volatile sulfur compounds by using automated headspace solid-phase microextraction and gas chromatography-pulsed flame photometric detection Critical study and optimization of a new procedure[J].Journal of Chromatography A,2007,1 143(1/2):8-15.
[50] YU F,MICHAEL C,QIAN.Sensitive quantification of sulfur compounds in wine by headspace solid-phase microextraction technique[J].Journal of Chromatography A,2005,1 080 (2):177-185.
[51] GINER MARTI NEZ-SIERRA J,SANTAMARIA-FERNANDEZ R,HEARN R,et al.Development of a direct procedure for the measurement of sulfur isotope variability in beers by MC-ICPMS[J].J Agr Food Chem,2010,58(7):4 043-4050.
