化学第2章官能团与有机化学反应烃的衍生物第2节(第1、2课时) 醇的化学性质教学案例
2013-04-29车丽荣
车丽荣
1.认识醇的典型代表物的组成和结构特点,知道醇与醛、羧酸之间的转化关系。
2.结合生产、生活实际了解烃的衍生物对环境和健康可能产生的影响,关注有机化合物的安全使用问题。
二、山东考试说明(与课标要求一致)
1.认识醇的典型代表物的组成和结构特点,知道醇与醛、羧酸之间的转化关系。
2.结合生产、生活实际了解烃的衍生物对环境和健康可能产生的影响,关注有机化合物的安全使用问题。
三、课标解读(教学目标)
1.通过【知识重温】回顾已学乙醇的化学反应,从而总结乙醇的部分化学性质。
2.通过分析醇的结构,结合前面的复习知道其化学反应主要涉及分子中碳氧键、氢氧键和碳氢键的断裂,根据醇的结构特点分析并总结乙醇的化学性质并能够熟练写出相关方程式和反应类型。
3.结合前面的学习,能够写出醇与烯烃、卤代烃、醛、酯等有机物之间的转化关系。
4.结合甲醇、乙醇在生产、生活实际中的应用,体会醇对环境和健康可能造成的影响,体现知识的重要性,从而激发学生学习的积极性。
四、教学评价
(一)课标评价
根据课标要求设计出4个教学任务,可以看出本节课的重点是醇的化学性质,教师在教学设计时要侧重醇的化学性质的探讨,设计足够的时间给学生理解醇反应的断键规律,并加强对应练习,充分体现本节课的重难点。
(二)历年考试试题评价
几乎每年的学业水平考试和高考都体现了乙醇的知识,重点考察乙醇的化学性质:取代反应(与金属钠、与羧酸的酯化反应、醇分子间的脱水反应)、消去反应、催化氧化。具体体现学业水平考试试题:
2010(山东省)
22.(8分)现有下列四种有机物:
分析:考察消去反应。
2008(山东省)
6.下列物质中加入金属钠不产生氢气的是
A.乙醇B.乙酸
C.水D.苯
分析:考察与金属钠的反应
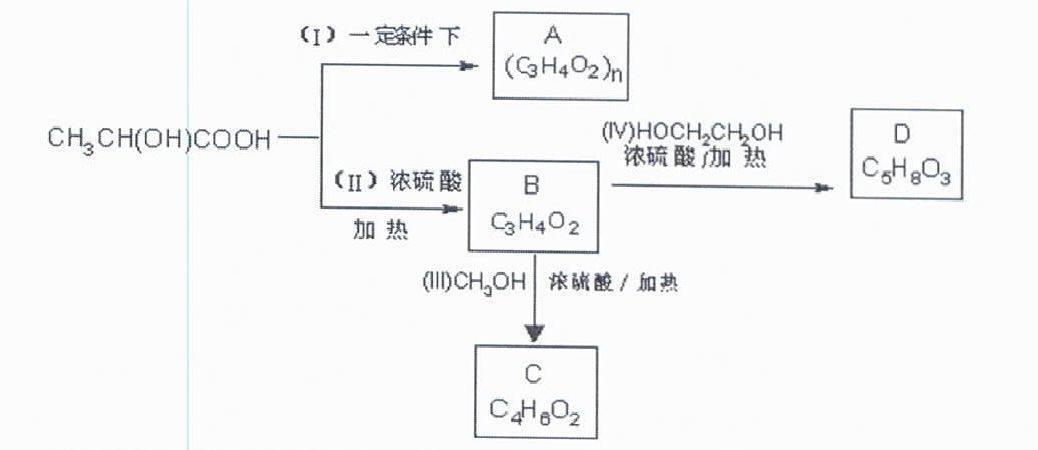
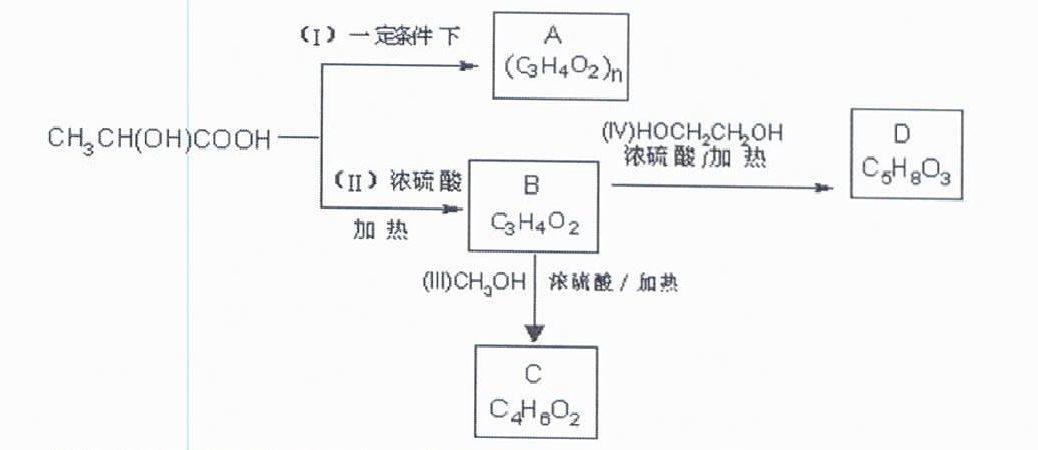
23.(9分)乳酸是酸奶的成分之一,乳酸可以用化學方法合成,也可以由淀粉通过生物发酵法制备,利用乳酸可以合成多种具有生物兼容性和环保型的高分子材料。乳酸已成为近年来人们的研究热点之一。乳酸的结构简式为CH3CH(OH)COOH,以下是采用化学方法对乳酸进行加工处理的过程:
请根据乳酸的性质和上述信息填写以下空白:
(1)写出乳酸与NaOH溶液反应的化学方程式:
;
(2)写出乳酸与浓硫酸共热生成C6H8O4的化学方程式:
;
(3)(II)的反应类型是。
分析:考察与羧酸发生酯化反应
(2)高考试题
(2010山东)
12.下列叙述错误的是
A.乙烯和苯都使溴水褪色,褪色的原因相同
B.淀粉、油脂、蛋白质都能水解,但水解产物不同
C.煤油可由石油分馏获得,可用作燃料和保存少量金属钠
D.乙醇、乙酸、乙酸乙酯都能发生取代反应,乙酸乙酯中的少量乙酸可用饱和Na2CO3溶液除去
分析:考察取代反应
(2012山东)
10.下列与有机物的结构、性质有关的叙述正确的是
A.苯、油脂均不能使酸性KMnO,溶液褪色
B.甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应
C.葡萄糖、果糖的分子式均为C6H12O6,二者互为同分异构休
D.乙醇、乙酸均能与Na反应放出H2,二者分子中官能团相同
分析:考察取代反应
2009(山东卷)
33.(8分)(化学-有机化学基础)
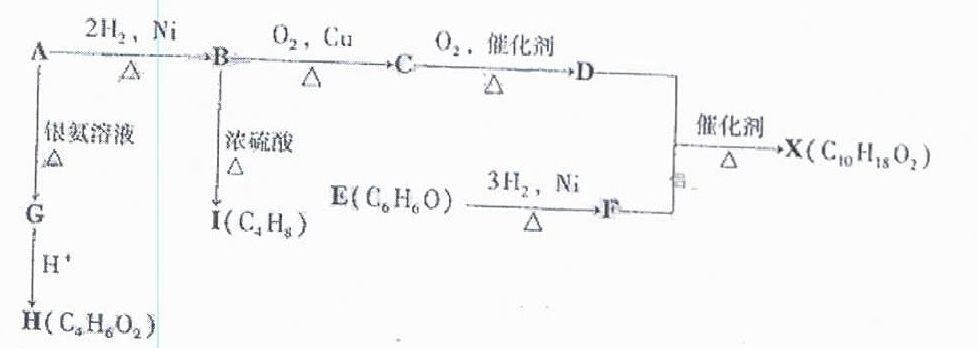
下图中X是一种具有水果香味的合成香料,A是有直链有机物,E与FeCl3溶液作用显紫色。
请根据上述信息回答:
(1)H中含氧官能团的名称是。B→I的反应类型为。
(2)只用一种试剂鉴别D、E、H,该试剂是。
(3)H与J互为同分异构体,J在酸性条件下水解有乙酸生成,J的结构简式为。
(4)D和F反应生成X的化学方程式为。
分析:考察与羧酸反应酯化反应、催化氧化反应。
(2012山东)
10.下列与有机物的结构、性质有关的叙述正确的是
A.苯、油脂均不能使酸性KMnO4溶液褪色
B.甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应
C.葡萄糖、果糖的分子式均为C6H12O6,二者互为同分异构体
D.乙醇、乙酸均能与Na反应放出H2,二者分子中官能团相同
分析:考察官能团和取代反应
五、学习目标
1.通过知识回顾,结合分析醇的结构特点总结醇的化学性质,能够熟练写出醇与烯烃、卤代烃、醛、酯等有机物相互转化的方程式。
2.结合资料介绍和生活实际能够列举醇在生产生活实践中的应用。
六、教材分析
(一)教材位置
本节在有机反应类型及反应规律的学习之后,学生已经具备了根据一定结构的有机化合物推测可能与什么样的试剂发生什么类型的反应、生成什么样的物质的思路和意识。本节内容是学生初次运用所学规律推测一类物质可能发生的反应,让他们用演绎法学习醇的性质并发展这种思路和方法,为后续学习打下基础。
(二)教材处理
对于醇的化学性质,通过回顾乙醇的化学性质推测醇的化学性质,从断键的角度推测产物,从而总结出醇消去、催化氧化反应的规律。
(三)与人教版教材的比较
编排的位置:
两个版本都是在介绍了烷烃、烯烃、苯及其同系物、卤代烃的基础上引入的,都是把醇作为烃的衍生物的第一种代表物进行介绍的,呈现的位置基本相同。
知识上的比较:
人教版对于醇的介绍从整体上分析比鲁科版相对简单,具体体现:
1.几种常见醇:人教版主要介绍了乙二醇和丙三醇的结构和物理性质的共性之处,对于甲醇的结构和物理性质没有介绍。
2.饱和一元醇:两个版本都对饱和一元醇的通式、沸点以及水溶性做了详细的介绍,通过表格数据的分析得出相关结论。但两个版本的切入点不同,鲁科版注重知识的系统性和完整性,人教版注重培养学生分析问题、解决问题的能力,注重联系生活实际。
3.醇的化学性质:两个版本都介绍了醇与金属钠、浓氢卤酸、消去反应、氧化反应,但知识的呈现方式不同,人教版注重实验的探究作用,对于醇分子间脱水的反应只是在资料卡片上出现,鲁科版则注重从官能团的角度进行分析,从断键上分析规律,帮助学生理解。
结论:通过两个版本的比较,进一步明确本节课的教学任务(重点知识):
1.乙二醇与丙三醇的结构和物理性质
2.饱和一元醇的通式、水溶性的规律、沸点的规律
3.醇与金属钠、浓氢卤酸的反应以及醇的消去反应、氧化反应的规律。
七、学情分析
学生在必修内容及前面章节内容的学习中,已经对乙醇的结构和性质有所了解,并且能够从结构上简单区分醇和酚,但是从结构上对性质进行推测方面的能力还不太熟练,尤其对断键位置与反应类型间的关系上不能很熟练区分。
八、教学重点、难点
根据醇的结构推测醇的性质,掌握醇的化学性质
九、教学策略:
课前准备:(学案导学)
根据已有知识和教材资料总结醇的化学性质,能够写出乙醇与金属钠的取代反应、乙醇的消去反应、乙醇的氧化反应的方程式。
课堂探究:(交流、检测、讲解、练习相结合)
通过课堂小测和交流订正检查学生对乙醇知识的掌握情况,结合乙醇的结构特点引导学生分析,帮助学生理解结构对于有机物性质的重要性,强化结构决定性质的理念,同时由乙醇的性质引导学生分别探讨1-丙醇或2-丙醇的性质,知识得到提升;结合对应训练巩固本节知识,体现知识的迁移应用。
十、教学过程中注意的问题
1.重点要突出。
2.注意课本知识的整合。课本上是从吸引电子能力的强弱角度入手分析醇的结构,教师应根据学生的理解能力进行分析,可以把此环节变为知识的总结来处理,学生掌握了醇的反应之后,再来看键的极性以及断键就更好理解了。
十一、教学过程
【教师活动】组织小组内交流预习内容,完成学习目标的1、2
【投影】学习目标1、2
1.醇、酚的区别;认识几种常见的醇
2.总结饱和一元醇的通式、物理性质
【学生活动】小组内交流预习作业,订正答案,提出质疑。
【教师活动】【投影】【目标1评价】
1.醇酚的区别(填序号)
下列物质属于醇类的是 属于酚类的是
【目标2评价】
2.饱和一元醇的物理性质
下列每组物质的沸点高低比较不正确的是()
A.乙二醇高于2-丙醇B.丁烷高于丙烷
C.乙醇高于甲醇D.乙醇低于丁烷
3.【学业水平考试试题】2010(山东省)
4.若从溴水中把溴萃取出来,可选用的萃取剂是
A.水 B.无水酒精 C.四氯化碳D.氢氧化钠溶液
【教师活动】学习目标3分析醇的结构特点掌握醇的化学性质
【學生活动】明确下一个学习任务。
【教师活动】
二、醇的化学性质
小组结合57页的【交流研讨】及以前的知识基础,以乙醇为例,预测醇能发生哪些类型的反应,反应时生成何种产物。
【学生活动】小组讨论,举出相应的实例,填写58页表格。
【学生活动】通过讨论分析,总结出醇在不同部位断键发生反应的类型:
⑴与金属钠发生取代反应
⑵与乙酸发生酯化反应
⑶消去反应
【教师活动】引导学生总结:羟基中的取代反应:引导学生从反应进行的条件和反应过程中断键的角度来区分分子内脱水和分子间脱水的联系和区别。
【练习巩固】写出1—丙醇发生反应的方程式
1.羟基的反应:
2.羟基中氢的反应:
3.氧化反应:
