甘油催化氢解制备丙二醇催化剂研究进展*
2013-04-07柳培吕志果王金金郭振美
柳培,吕志果,王金金,郭振美
(青岛科技大学化工学院,山东青岛 266042)
催化材料
甘油催化氢解制备丙二醇催化剂研究进展*
柳培,吕志果,王金金,郭振美
(青岛科技大学化工学院,山东青岛 266042)
摘要:简要概括了近些年生物柴油副产物甘油催化氢解制备丙二醇催化剂研究新进展,对甘油氢解分别采用贵金属催化体系和过渡金属催化体系的催化活性和选择性以及可能的机理进行了解释说明。采用贵金属Pt/WO3负载型催化剂、ReOx改性的Rh/SiO2、Ir/SiO2催化剂、贵金属催化体系中加入有机溶剂以及采用Cu-STA(硅钨酸)/SiO2的气相催化工艺等方式都能得到相对较多的1,3-丙二醇(收率最高为38%)。高分散的纳米铜基催化剂对甘油氢解有着较高的活性、选择性和稳定性,具有工业应用前景。纳米钴催化剂具有特定的形态和良好的催化效果颇受关注。
关键词:甘油;催化氢解;丙二醇
近年来,国际油价不断攀高,能源危机日益突显,促使世界各国的研究者积极寻找可替代且可再生的新能源,生物质是一种极有发展前景的生物能源。生物质来源于动物油脂、植物油脂等,通过酯交换反应生产的生物柴油具有生物可降解性、无毒、燃烧安全、沸点较高不易挥发、运输及储藏比石化柴油更安全等优点[1]。各国政府都在积极鼓励发展生物柴油产业,对于经济的可持续发展、推进能源替代、减轻环境压力、控制城市大气污染以及提供就业机会具有重要的战略意义[2]。随之而来的大量生物柴油副产物甘油过剩问题严重,粗甘油价格急剧下滑,因此副产物甘油的综合利用成为严峻且关键的问题。甘油生产高附加值的化学品(主要为丙二醇)是生物柴油生产工艺中不可或缺的关键点。丙二醇用途广泛,在医药工业中主要用作药物的溶解剂、渗透促进剂以及各类软膏的溶剂、软化剂、赋形剂;在食品和化妆品中用作调味品和色素的溶剂、香料的溶剂、烟草的增湿剂和防霉剂、抗冻剂等。丙二醇还是不饱和聚酯、环氧树脂、聚氨酯的重要原料。丙二醇(尤其是1,3-丙二醇)的生产采用化学法因原料毒性大、来源困难而受到限制,以甘油为原料的微生物发酵法虽然符合绿色化学要求,但酶的成活期短,成本很高。开发以甘油为底物通过催化氢解制备丙二醇的技术具有很大的竞争力和发展潜力,近年来已成为研究的热点。目前催化剂在甘油催化氢解中的作用及反应机理不尽相同,笔者就目前甘油氢解制丙二醇的催化剂研究进行回顾。
1 甘油催化氢解制备丙二醇的机理
甘油催化氢解机理一直处在研究探讨阶段,不同的催化剂体系其机理解释也不相同,但是一般来说,甘油氢解催化产物一般为1,2-丙二醇,副产物有正丙醇、甲醇和乙二醇等。因此在碱性条件下[3]的机理具有参考价值,见图1。首先,甘油分子吸附在催化剂表面可逆脱氢生成甘油醛或者其烯醇互变异构体,随后甘油醛或其烯醇互变异构体从催化剂表面脱附,在碱性环境中发生C—O键断裂,脱水生成2-羟基丙烯醛(随后加氢生成1,2-丙二醇),甘油醛或发生Retro-aldol反应,发生C—C键断裂生成甲醛和2-羟基乙醛,加氢生成乙二醇。

图1 甘油氢解碱性条件下的机理
2 甘油氢解贵金属催化体系
2.1单一贵金属催化体系
目前,工业上将氢气作为甘油氢解加氢的反应原料,还原为丙二醇需要一定的活性中心,众所周知,贵金属催化剂可以有效地激活氢分子,并且广泛地用于加氢催化反应中。近年,冯建等[4]采用浸渍法制备Ru/TiO2负载型催化剂,Ru均匀地分散在TiO2表面,在170℃、3 MPa、10%(质量分数)甘油水溶液条件下反应,甘油转化率为66.3%,丙二醇和乙二醇的选择性分别为47.7%和26.0%;当温度升高时会继续发生C—C键断裂,有较多的乙二醇产生,同时氢气压力过高也会降低1,2-丙二醇的选择性。M.A.Dasari等[5]使用Johnson Matthey催化剂公司的5%Ru/C、Ru/Al2O3催化剂,在1.38 MPa氢气低压、200℃、质量分数为80%甘油水溶液条件下反应24h,采用Ru/C催化剂的甘油转化率较采用Ru/Al2O3时高,分别为43.7%和23.1%,但是1,2-丙二醇的选择性却相反,分别为40.0%和59.7%。研究表明[6],Ru/C催化剂在温和的反应条件下主要产物为1,2-丙二醇,氢解过程中同时产生乙二醇,1,2-丙二醇的选择性没有超过70%。M.A.Dasari等[5]比较了各种商业催化剂的催化氢解性能:Pd/C活性较低;Pt/C对1,2-丙二醇有着较高的选择性(82.7%),并且收率也较高(28.6%);非贵金属Cu-Cr催化剂有着更高的活性和选择性(选择性为85.0%,收率为46.6%)。E.P.Maris等[7]报道了Pt/C催化剂对1,2-丙二醇的选择性高于Ru/C催化剂。I.Furikado等[8]比较了低温(120℃)下负载型贵金属(Rh、Ru、Pt、Pd/C、SiO2、Al2O3)的甘油氢解活性:Pd和Pt负载催化剂在温和条件下活性很低(转化率<1%);Rh/SiO2活性较其他的都高,甘油转化率最高为7.2%。
2.2贵金属+酸催化体系
研究得知,贵金属未添加其他组分时产物选择性较差,有多种手段可改进催化剂提高贵金属催化剂的选择性。T.Miyazawa等[6,9]研究了Ru/C+ Amberlyst15和Ru/C+Amberlyst70催化剂,活性炭负载的Ru催化剂比表面积小(约250 m2/g)却有着优良的反应性能,前驱物Ru(NO)(NO3)3在合适的温度下通入Ar气流后较商业Ru/C催化剂性能好,在120℃、8 MPa H2压力下反应10 h,甘油转化率为79.3%,1,2-丙二醇的选择性为74.7%。Amberlyst70较Amberlyst15热稳定性好,Ru/C+Amberlyst70可在高温下反应,在180℃、8 MPa H2压力下反应48.8 h,甘油转化率却下降为48.8%,1,2-丙二醇的选择性为70.2%,但是却有少量1,3-丙二醇生成(选择性为1.3%)。这说明高温有利于生成1,3-丙二醇,但是同时影响催化剂的活性以及容易发生C—C键断裂,发生过度氢解和降解形成小分子的脂肪醇。I. Gandarias等[10]研究了Pt负载在无定形硅铝载体上(Pt/ASA),在220℃、4.5 MPa H2压力下反应24 h,甘油转化率为19%,1,2-丙二醇和1,3-丙二醇的选择性分别为31.9%和4.5%,丙醇的选择性为53.8%。在氢解过程中产生H2,因此在N2压力下甘油的转化率和氢气压力下的转化率相差无几。A.Alhanash等[11]使用5%Rh/CsPW(Cs2.5H0.5[PW12O40])催化剂,在0.5 MPa H2低压、150℃下反应10 h,甘油转化率为21%,1,2-丙二醇的选择性为96%;在未通氢气条件下,Cs2.5H0.5[PW12O40]催化甘油有少量的丙酮醇生成,说明甘油脱水是发生在酸中心上的;5%Rh/ CsPW催化活性虽然没有5%Ru/CsPW好,但是对1,3-丙二醇有着更高的选择性;5%Rh/CsPW催化过程中没有乙二醇产生,说明该催化剂对C—C键的活性没有Ru催化剂好;研究中2%Pd/CsPW催化剂对甘油氢解反应没有活性。陈长林等[12]以磷钨杂多酸(HPW)为钨前驱体,用浸渍法制备系列具有不同Pt含量和不同HPW/ZrO2焙烧温度的Pt/HPW/ZrO2催化剂,通过各种手段表征催化剂的结构,在连续流动固定床反应器中考察该催化剂对甘油氢解的性能:负载量为2%Pt/HPW/ZrO2的催化剂,在4 MPa、130℃、质量分数为60%甘油水溶液、液空速为0.25h-1条件下,甘油转化率为53.4%,1,3-丙二醇的选择性为44.5%;100 h稳定性实验结果表明,该催化剂有着较好的稳定性。龚磊峰等[13]研究了Pt/WO3/ZrO2催化剂的溶剂效应,质子溶剂乙醇和水有利于甘油转化为1,3-丙二醇,并且使用混合溶剂1,3-丙二醇的选择性较高。刘龙杰等[14]采用蒸发诱导自组装法制备了介孔WO3负载Pt后应用于甘油催化氢解反应,在180℃、5.5 MPa氢气压力下反应12 h,甘油转化率为18.0%,1,3-丙二醇的选择性为39.2%。S.H. Zhu等[15]研究Pt-H4SiW12O40/SiO2催化剂,在200℃、6 MPa氢气压力、重时空速为0.045 h-1条件下,甘油转化率为81.2%,1,3-丙二醇的选择性为38.7%。
2.3贵金属+碱催化体系
根据甘油脱水机理可知,甘油脱水既可发生在酸性条件,也可发生在碱性条件。冯建等[3-4]研究了在Ru/TiO2催化体系中加入无机碱LiOH、NaOH、KOH、Li2CO3、Na2CO3、K2CO3等。研究表明,加入LiOH到催化体系,随着碱加入量的增加,甘油转化率和1,2-丙二醇的选择性也相应提高,达到甘油转化率最高为89.6%、1,2-丙二醇选择性为86.8%之后呈下降趋势。这一结果高于不加碱的单一贵金属催化剂。碱性物质的添加降低了乙二醇的选择性,说明碱的添加有利于抑制C—C键的断裂。同时研究了仅用LiOH催化甘油时甘油转化率极低。E.P. Maris等[7]研究了Ru/C和Pt/C催化剂中加入NaOH和CaO,在4 MPa H2压力、200℃下反应5 h,Pt/C中加入CaO较Ru/C加入CaO对1,2-丙二醇的选择性要好,分别为71%和46%,甘油转化率分别为40%和50%;加入NaOH的催化剂效果不及加入CaO的好,但是加入碱都能提高甘油氢解的速率,这和冯建等的研究一致。Z.Yuan等[16]研究了固体碱负载Pt催化剂:水滑石负载的Pt催化剂有很强的碱性,金属Pt高度分散,在无碱的水溶液中反应(3 MPa H2压力、220℃)20 h,甘油转化率为92.1%,1,2-丙二醇的选择性为93%,较E.P.Maris等研究的Pt/C中添加无机碱效果好。
2.4改性的金属氧化物+贵金属催化体系
Tomishige[17-18]课题组深入研究了改性的金属氧化物+贵金属催化剂并提出了反应机理。采用浸渍法制备Rh-ReOx/SiO2、Rh-MoOx/SiO2、Rh-WOx/SiO2催化剂。反应中用水作溶剂,添加Re、Mo和W到催化剂Rh/SiO2中,有利于提高甘油的转化率,同时也有相对多的1,3-丙二醇生成,尤其是加入Re,1,3-丙二醇的选择性更好。其中Rh-ReOx/SiO2催化剂对甘油氢解效果较其他催化剂好,在8 MPa H2压力、120℃下反应5 h,甘油转化率为79.0%,1,2-丙二醇的选择性为38.0%,1,3-丙二醇的选择性为13.8%,丙醇的选择性高达47.4%。但是Re添加过量也会降低甘油氢解性能,n(Re)/n(Rh)=0.5最为合适,该反应有效地抑制C—C键的断裂,但是过度氢解的丙醇的选择性较高。Y.Nakagawa等[18]研究了Ir-ReOx/SiO2催化剂,在n(Re)/n(Ir)=1、8 MPa H2压力、120℃条件下,反应开始时1,3-丙二醇的选择性可达67%± 3%;反应36 h时1,3-丙二醇的收率达到最大值38%,此时甘油的转化率为86%;随着反应时间的继续增加,甘油转化率接近100%,但是1,2-丙二醇和1,3-丙二醇相继发生氢解,丙醇选择性增加。
2.5有机溶剂作为反应介质的贵金属催化体系
专利文献[19]中,在有机疏质子溶剂中,在30MPa压力、200℃条件下,Rh(CO)2(acac)和H2WO4均相催化,1,3-丙二醇收率为21%。其中有机疏质子溶剂优选疏质子有机酰胺,例如:N,N-二甲基甲酰胺、N,N-二甲基乙酰胺、吡咯烷酮、1-甲基-2-哌啶酮、六甲基磷酰三胺以及四甲基脲等类似溶剂。J. Chaminand等[20]以H2WO4作为助催化剂加入到Rh/C催化剂中,用环丁砜作溶剂进行反应,甘油转化率为32%,1,3-丙二醇的选择性/1,2-丙二醇的选择性= 2,丙二醇的总收率为6%。T.Kurosaka等[21]研究了不同载体负载的Pt/WO3催化剂,采用依次浸渍制备。在1,3-二甲基-2-咪唑烷酮中反应,1,3-丙二醇的收率可达24.2%,但是甘油转化率较低。单一的Pt/ZrO2催化剂对1,3-丙二醇和1,2-丙二醇的选择性分别为2.2%和3.0%,用偏钨酸铵浸渍的Pt/WO3/ZrO2催化剂效果明显,Pt/WO3/ZrO2催化剂对形成1,3-丙二醇活性中心最大。加入某些有机溶剂、ZrO2和W较容易形成1,3-丙二醇。
3 甘油氢解过渡金属催化体系
3.1Cu催化体系
近年来,铜基催化剂在加氢催化剂研究领域较多,在甘油氢解加氢催化中,铜基催化剂对C—O键有着较高的活性,而对C—C键活性低,并且相对于其他贵金属催化剂而言,铜基催化剂以其低廉的价格和催化性能的稳定性颇受关注。M.A.Dasari等[5]研究的Cu-Cr催化剂催化氢解甘油反应获得了2006年美国绿色化学挑战奖,在200℃、1.38 MPa低压力、质量分数为80%甘油水溶液条件下,1,2-丙二醇的收率达到73%。张伟伟等[22]研究了纳米铜基催化剂催化氢解甘油反应,共沉淀法制备的CuO/SiO2纳米催化剂对甘油催化加氢制备1,2-丙二醇的反应具有很高的催化活性和选择性。在连续的固定床上,在200℃、1.0 MPa、n(H2)∶n(甘油)=30∶1、液空速为0.30 h-1条件下,甘油转化率为100%,1,2-丙二醇的选择性达到98.71%。该催化剂具有良好的稳定性,抗烧结性能好,在700 h的长时间运转过程中,催化剂的加氢活性变化不大,甘油转化率维持在95%~100%,1,2-丙二醇的选择性在96%左右。L. Guo等[23]研究了采用浸渍法制备γ-Al2O3和多种酸性分子筛(HY、13X、HZSM-5、Hβ)负载的铜基催化剂:γ-Al2O3负载的铜基催化剂对甘油催化氢解活性较高,在220℃、1.5 MPa H2压力下反应10 h,甘油氢解转化率为49.6%,1,2-丙二醇的选择性可达96.8%;分子筛作载体的铜基催化剂活性很低,有的几乎没有活性。黄志威等[24]采用沉淀凝胶法制备纳米Cu/SiO2催化剂,对比采用浸渍法制备的Cu/SiO2催化剂,在连续固定床反应器做200 h活性测试显示:在重时空速为0.25 h-1、n(H2)∶n(甘油)=22∶1、氢气压力为6.0 MPa、温度为180℃条件下,沉淀凝胶制备的纳米Cu/SiO2催化剂保持稳定的甘油转化率(80%±5%)和1,2-丙二醇的选择性(>98%),而浸渍法制备的Cu/SiO2催化剂,在不足100 h时甘油转化率已不到20%。并且研究了钠离子对Cu/SiO2催化氢解甘油性能的影响,沉淀凝胶法制备的Cu/SiO2催化剂,钠离子残余量越多,甘油的转化率和1,2-丙二醇的选择性就会越低,但是作为碱加入到催化剂中对甘油的活性有略微的促进作用,可能活性组分Cu也会随着钠离子的洗涤流失。黄龙等[25]研究了Cu/SiO2、Cu/ZnO/Al2O3、Cu/Cr2O3催化剂釜式催化氢解,在质量分数为60%甘油水溶液、5 MPa H2压力、200℃条件下反应10 h:Cu/ZnO/Al2O3催化剂展现了更优的催化性能,甘油转化率为20.4%,1,2-丙二醇的选择性达80%,其次是Cu/Cr2O3催化剂,甘油转化率和1,2-丙二醇的选择性分别为15.1%和73.8%。并且在连续的固定床上考察了Cu/ZnO/Al2O3催化剂,在重时空速为0.08 h-1、n(H2)∶n(甘油)=140∶1、压力为0.64 MPa、温度为190℃条件下,甘油转化率为96.2%,1,2-丙二醇的选择性达到92.2%,连续固定床反应器气相反应工艺更易于产生更多的1,2-丙二醇。进一步研究了甘油气相氢解制备1,3-丙二醇,采用固定床和气相反应工艺,制备Cu-STA/SiO2(STA为硅钨酸)酸-金属双功能催化剂,在重时空速为0.1 h-1、n(H2)∶n(甘油)=140∶1、压力为0.36 MPa条件下,甘油转化率为57.7%,1,3-丙二醇和1,2-丙二醇的选择性分别为31.2%和21.4%,根据NH3-TPD显示Cu-STA/SiO2催化剂表面酸中心数量较多[26]。在压力为0.54 MPa、温度为210℃条件下,甘油转化率为83.4%,1,3-丙二醇和1,2-丙二醇的选择性分别为32.1%和22.2%。M.Balaraju等[27]采用共沉淀法制备了Cu-ZnO催化剂,在n(Cu)∶n(Zn)=1∶1时,在质量分数为10%甘油水溶液、2 MPa氢气压力、200℃条件下反应16 h,1,2-丙二醇的选择性可达93%。
3.2Ni催化体系
A.Perosa等[28]用Raney镍(雷尼镍)催化剂催化氢解甘油,无添加剂和溶剂,在1 MPa H2压力、190℃条件下反应44 h,甘油转化率为97%,1,2-丙二醇的选择性为71%,同时有10%的CO2生成。黄龙等[25]制备Ni/SiO2和Ni/Al2O3催化剂,用高压釜评价催化剂性能,在5 MPa H2压力、200℃条件下反应10 h,甘油转化率分别为8.5%和32.3%,1,2-丙二醇的选择性分别为60.5%和55.1%。并且对Ni/Al2O3催化剂用固定床反应器进行评价,在重时空速为0.18 h-1、压力为0.10 MPa、n(H2)∶n(甘油)=70∶1、温度为190℃条件下,丙酮醇的选择性较高,甘油转化率为92.3%,1,2-丙二醇的选择性为43.6%,气体产物增多。当温度达到200℃时,甘油转化率为100%,1,2-丙二醇的选择性降为34.4%,同时也有较多的CO2和CH4等气体产生,这和A.Perosa等的研究一致。W.Q.Yu等[29]研究了Ni-Ce/AC催化剂催化氢解甘油,在25%(质量分数)的甘油水溶液、5 MPa氢气压力、温度为200℃条件下反应6 h,甘油转化率为90.4%。Ce添加到催化体系中改变了催化体系的还原性能,并且加速了甘油氢解生成丙酮醇。
3.3Co催化体系
相对Cu、Ni催化剂而言,Co催化剂研究较少。中国科学院大连化学物理研究所申文杰[30-32]课题组报道了系列纳米Co催化剂,在合成中用Ru作为异相剂、硬脂酸作为结构导向剂首次合成了Co纳米线,在220℃、5.2 MPa H2压力下,甘油转化率可达83%,1,2-丙二醇的选择性为56%。他们进一步研究Co纳米棒分级生长,合成了Co纳米化催化剂并应用于甘油氢解反应:Co纳米化催化剂较传统的纳米Co催化剂(Co纳米化催化剂与传统的纳米Co催化剂的合成方法不同)有着更优的甘油氢解催化性能(约为2.5倍)。中空的网状框架结构的Co催化氢解甘油反应也有着比较好的效果(转化率为35%,丙二醇的选择性为72%)。合成Co纳米催化剂的过程中使用硬脂酸一方面作为结构导向剂,另外一方面也是酸浸蚀剂。此外,研究CoNi纳米线,采用溶剂水热合成法,Ni作为异相成核剂,在多元醇中合成长约1 000 nm、直径为10 nm的CoNi纳米线。该催化剂应用于甘油氢解反应,在220℃、5.2 MPa H2压力下,甘油转化率为70%,1,2-丙二醇的选择性为49%。X.H.Guo等[33]研究了以MgO作为载体的纳米Co催化剂,研究了焙烧温度对甘油催化氢解活性的影响,结果显示:600℃焙烧的催化剂具有较高的活性,在200℃、2 MPa H2压力下,甘油转化率为44.8%,1,2-丙二醇的选择性为42.2%。
现在复合催化也是一种新趋势。I.Gandrias等[34]研究了Ni-Cu/Al2O3催化剂,Ni对C—C键的断裂有着较高的活性,而Cu对1,2-丙二醇有着良好的选择性,调配合适的Cu、Ni比例,在220℃、甲酸作为质子供体、无需供给氢气、氮气加压条件下反应24 h,甘油转化率达到90%,1,2-丙二醇的选择性为82%,大大优于单一的Ni催化剂,有效地控制了C—C键的活性,提高了C—O键的活性。
对比以上催化剂,现将部分有代表性的催化剂进行总结,见表1。
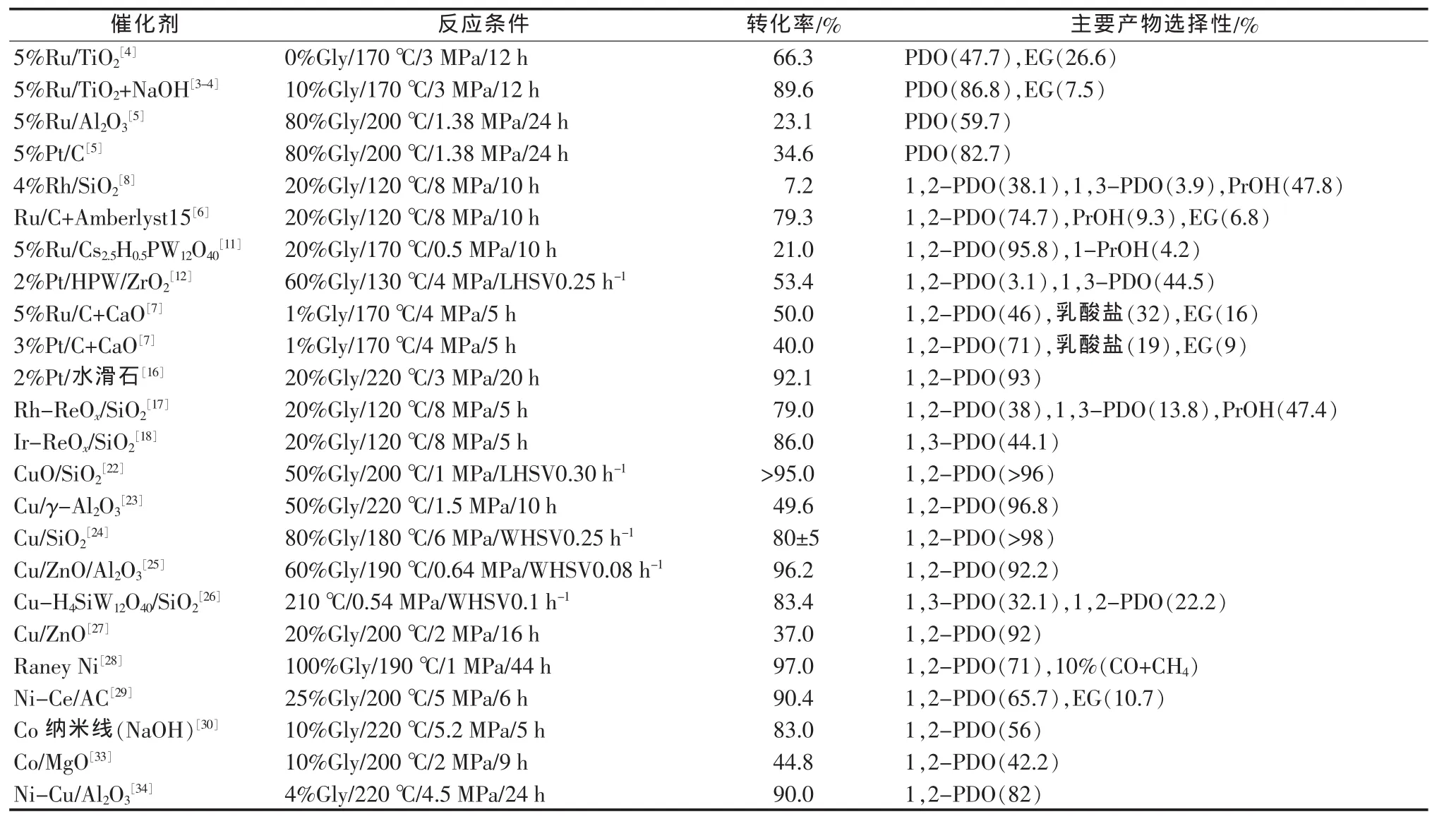
表1 一些有代表性的甘油氢解制备丙二醇催化剂体系及反应结果
4 结论与展望
近年来,甘油催化氢解制备丙二醇已成为研究热点,并取得了一定的研究成果。目前所采用的催化体系主要有贵金属催化体系和过渡金属催化体系。贵金属催化体系已由单一贵金属催化向多金属复合催化方向发展,并在制备1,3-丙二醇上取得突破进展,但存在副产物较多、活性较低、价格昂贵等缺点。以铜基催化剂为代表的过渡金属催化体系,在甘油催化氢解反应中具有更高的活性、选择性和稳定性,具有理想的工业应用前景。纳米Co催化剂具备特定的形态,表现出良好的催化性能,开辟了甘油氢解催化剂的新方向。无论是贵金属催化体系,还是过渡金属催化体系,加入助剂复合催化已成为一种趋势,并起到积极的作用。制备高分散、复合催化纳米级的铜基催化剂也是研究甘油氢解催化的新方向。
参考文献:
[1]宋如,钱仁渊,李成,等.甘油新用途研究进展[J].中国油脂,2008,33(5):40-44.
[2]Lin L,Zhou C S,Saritporn V,et al.Opportunities and challenges for biodiesel fuel[J].Appl.Energy,2011,88(4):1020-1031.
[3]Feng J,Wang J B,Zhou Y F,et al.Effect of base additives on the selective hydrogenolysis of glycerol over Ru/TiO2catalyst[J].Chem. Lett.,2007,36(10):1274-1275.
[4]冯建,熊伟,贾云,等.Ru/TiO2催化剂上甘油氢解制1,2-丙二醇[J].催化学报,2011,32(9):1545-1549.
[5]Dasari M A,Kiatsimkul P P,Sutterlin W R,et al.Low-pressure hydrogenolysis of glycerol to propylene glycol[J].Appl.Catal.,A,2005,281(1/2):225-231.
[6]Miyazawa T,Koso S,Kunimori K,et al.Development of a Ru/C catalyst for glycerol hydrogenolysis in combination with an ion-exchange resin[J].Appl.Catal.,A,2007,318:244-251.
[7]Maris E P,Davis R J.Hydrogenolysis of glycerol over carbon-supported Ru and Pt catalysts[J].J.Catal.,2007,249(2):328-337.
[8]Furikado I,Miyazawa T,Koso S,et al.Catalytic performance of Rh/ SiO2in glycerol reaction under hydrogen[J].Green Chem.,2007,9(6):582-588.
[9]Miyazawa T,Koso S,Kunimori K,et al.Glycerol hydrogenolysis to 1,2-propanediol catalyzed by a heat-resistant ion-exchange resin combined with Ru/C[J].Appl.Catal.,A,2007,329:30-35.
[10]Gandarias I,Arias P L,Requies J,et al.Hydrogenolysis of glycerol to propanediols over a Pt/ASA catalyst:the role of acid and metal sites on product selectivity and the reaction mechanism[J].Appl. Catal.,B,2010,97(1/2):248-256.
[11]Alhanash A,Kozhevnikova E F,Kozhevnikov I V.Hydrogenolysis of glycerol to propanediol over Ru:polyoxometalate bifunctional catalyst[J].Catal.Lett.,2008,120(3/4):307-311.
[12]陈长林,宋敏洁,秦丽珍.Pt/HPW/ZrO2催化甘油脱氧制取1,3-丙二醇[J].南京工业大学学报:自然科学版,2011,33(1):1-7.
[13]龚磊峰,吕元,丁云杰,等.Pt/WO3/ZrO2催化甘油选择性脱羟基制1,3-丙二醇反应的溶剂效应[J].催化学报,2009,30(12):1189-1191.
[14]刘龙杰,张艳华,王爱琴,等.介孔氧化钨担载Pt催化剂上甘油氢解制备1,3-丙二醇[J].催化学报,2012,33(8):1257-1261.
[15]Zhu S H,Zhu Y L,Hao S L,et al.Aqueous-phase hydrogenolysis of glycerol to 1,3-propanediol over Pt-H4SiW12O40/SiO2[J].Catal. Lett.,2012,142(2):267-274.
[16]Yuan Z,Wu P,Gao J,et al.Pt/solid-base:a predominant catalyst for glycerol hydrogenolysis in a base-free aqueous solution[J]. Catal.Lett.,2009,130(1/2):261-265.
[17]Shinmi Y,Koso S,Kubota T,et al.Modification of Rh/SiO2catalyst for the hydrogenolysis of glycerol in water[J].Appl.Catal.,B,2010,94(3/4):318-326.
[18]Nakagawa Y,Shinmi Y,Koso S,et al.Direct hydrogenolysis of glycerol into 1,3-propanediol over rhenium-modified iridium catalyst[J].J.Catal.,2010,272(2):191-194.
[19]Che T M.Production of propanediols:US,4642394[P].1987-02-10.
[20]Chaminand J,Djakovitch L A,Gallezot P,et al.Glycerol hydrogenolysis on heterogeneous catalysts[J].Green Chem.,2004,6(8):359-361.
[21]Kurosaka T,Maruyama H,Naribayashi I,et al.Production of 1,3-propanediol by hydrogenolysis of glycerol catalyzed by Pt/WO3/ ZrO2[J].Catal.Commun.,2008,9(6):1360-1363.
[22]张伟伟,吕志果,吴现印,等.纳米CuO/SiO2催化甘油氢解制备1,2-丙二醇反应研究[J].应用化工,2011,40(1):71-74.
[23]Guo L,Zhou J,Mao J,et al.Supported Cu catalysts for the selective hydrogenolysis of glycerol to propanediols[J].Appl.Catal.,A,2009,367(1/2):93-98.
[24]Huang Z W,Cui F,Kang H X,et al.Highly dispersed silica-supported copper nanoparticles prepared by precipitation-gel method:a simple but efficient and stable catalyst for glycerol hydrogenolysis[J].Chem.Mater.,2008,20(15):5090-5099.
[25]Huang L,Zhu Y L,Zheng H Y,et al.Continuous production of 1,2-propanediol by the selective hydrogenolysis of solvent-free glycerol under mild conditions[J].J.Chem.Technol.Biotechnol.,2008,83(12):1670-1675.
[26]Huang L,Zhu Y L,Zheng H Y,et al.Direct conversion of glycerol into 1,3-propanediol over Cu-H4SiW12O40/SiO2in vapor phase[J]. Catal.Lett.,2009,131(1/2):312-320.
[27]Balaraju M,Rekha V,Prasad P S Sai,et al.Selective hydrogenolysis of glycerol to 1,2 propanediol over Cu-ZnO catalysts[J].Catal. Lett.,2008,126(1/2):119-124.
[28]Perosa A,Tundo P.Selective hydrogenolysis of glycerol with raney nickel[J].Ind.Eng.Chem.Res.,2005,44(23):8535-8537.
[29]Yu W Q,Zhao J,Ma H,et al.Aqueous hydrogenolysis of glycerol over Ni-Ce/AC catalyst:promoting effect of Ce on catalytic performance[J].Appl.Catal.,A,2010,383(1/2):73-78.
[30]Liu Q Y,Guo X H,Chen J L,et al.Cobalt nanowires prepared by heterogeneous nucleation in propanediol and their catalytic properties[J].Nanotechnology,2008,19(36):365608.
[31]Liu Q Y,Guo X H,Li Y,et al.Synthesis of hollow Co structures
with netlike framework[J].Langmuir,2009,25(11):6425-6430.
[32]Liu Q Y,Guo X H,Wang T J,et al.Synthesis of CoNi nanowires by
heterogeneous nucleation in polyol[J].Mater.Lett.,2010,64(11):1271-1274.
[33]Guo X H,Li Y,Shi R J,et al.Co/MgO catalysts for hydrogenolysis of glycerol to 1,2-propanediol[J].Appl.Catal.A-Gen.,2009,371(1/2):108-113.
[34]Gandarias I,Requies J,Arias P L,et al.Liquid-phase glycerol hydrogenolysis by formic acid over Ni-Cu/Al2O3catalysts[J].J. Catal.,2012,290:79-89.
联系方式:lvzhiguo@qust.edu.cn
中图分类号:O643.36
文献标识码:A
文章编号:1006-4990(2013)09-0052-06
收稿日期:2013-03-18
作者简介:柳培(1984—),女,硕士研究生,从事催化剂的研究与开发。
通讯作者:吕志果
*基金项目:国家自然科学基金项目(20776071);山东省自然科学基金(ZR2009BL016)资助。
Research advances in catalyst of glycerol hydrogenolysis to prepare propanediol
Liu Pei,Lü Zhiguo,Wang Jinjin,Guo Zhenmei
(School of Chemical Engineering,Qingdao University of Science and Technology,Qingdao 266042,China)
Abstract:The recent research progress in the catalytic hydrogenolysis of glycerol,which is the main byproduct of biodiesel,
was briefly generalized.The catalytic activity and selectivity,as well as the proposed mechanisms of the noble metal catalyst and transition metal catalyst respectively used for glycerol hydrogenolysis,were summarized and illustrated.According to previous studies,a relatively large number of 1,3-propanediol(maximum yield up to 38%)could both be obtained by the technology that adding organic solvent into the catalytic systems,such as Pt/WO3supported catalyst,ReOx-modified Rh/SiO2,and Ir/SiO2,as well as the vapor phase catalytic process with Cu-STA(silicotungstic acid)/SiO2catalyst.Highly dispersed nano-sized Cu based catalyst had a higher activity,selectivity,and stability in the catalytic hydrogenolysis of glycerol to produce propanediol,which contributed a bright prospect in industrial production,and nano-sized Co based catalyst had drawn much attention due to a specific morphology and good catalytic effect.
Key words:glycerol;hydrogenolysis;propanediol
