风险管理与临床实验室质量改进
2013-03-01康凤凤王薇王治国
康凤凤,王薇,王治国
(北京医院卫生部临床检验中心,北京100730)
·述评·
风险管理与临床实验室质量改进
康凤凤,王薇,王治国
(北京医院卫生部临床检验中心,北京100730)
风险管理是系统地应用管理政策、程序和实践来完成风险的分析、评价、控制和监测的任务,以最小化不良事件的概率和影响。其核心过程是风险因素识别、风险估计、风险评价、风险控制、风险监测及故障调查的持续过程。临床实验室可使用风险管理工具,分析和评价检验全过程的故障,对不可接受的风险进行调查、控制和监测,促进临床检验的持续质量改进,保证患者的安全。
风险;风险管理;检验全过程;质量控制;质量改进
风险管理最早起源于保险业,目前主要用于航天业、汽车工业、企业管理等。近几年,国际标准化组织(ISO)、美国医疗机构评审联合委员会(JC)、美国临床和实验室标准协会(CLSI)先后颁布文件,建议将风险管理应用于临床实验室[1-7]。风险管理是系统地应用管理政策、程序和实践来完成风险的分析、评价、控制和监测的任务,帮助实验室对特定的过程建立特定的质量控制计划,使系统固有的质量控制、外部质量控制及其他质量控制程序达到最佳的平衡[3]。其核心过程是风险因素识别、风险估计、风险评价、风险控制、风险监测及故障调查的持续过程,通过合理经济地使用各种资源来监测和控制不良事件,以最小化概率和影响。对临床实验室而言,术语“风险”或“风险管理”可能会不适应,但日常工作中如新方法性能评价、失控调查、抱怨投诉处理等都属于风险管理[8]。图1描述了风险管理的具体流程。
1 风险因素识别
风险因素识别是风险管理的首要步骤,可通过查阅文献、厂家仪器试剂说明书、国内外颁布的标准、认可文件等[5],结合实验室具体环境进行分析。实验室过程流程图是识别风险因素的良好工具。临床实验室检验全过程包括分析前、分析中和分析后阶段,各个阶段都有可能出现差错[9,10]。例如分析前差错包括患者识别错误、诊断信息错误或无诊断信息、患者准备不当、采集容器或防腐剂错误、采集时间不当、采集量不足、运输条件或时间不正确等。分析中差错包括质控失败、设备或试剂差错、检测程序不当等。分析后差错包括结果延迟(尤其是危急值)、结果解释不当、报告传送错误等。临床实验室应谨慎地审核检验全过程,以识别所有风险因素。
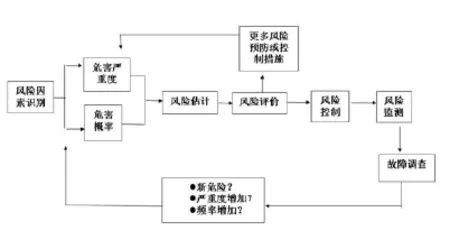
图1 风险管理流程图
2 风险估计和评价
风险估计包括风险出现的概率及其严重度。目前对于概率和严重度的衡量尺度还未达成一致。ISO 14971[7]文件关于概率和严重度为半定量描述:经常(每周1次),可能(每月1次),偶尔(每年1次),稀有(几年1次),不可能(整个使用期间1次);可忽略(暂时性不适),很小(暂时性伤害,不需要专业的医学干预),严重(需要专业的医学干预的伤害),危急(永久的或危及生命的伤害),灾难性(引起患者死亡)。与此不同,CLSI EP18-A2[4]文件采用了1~4等级评分制度。风险出现概率的估计应以实验室日常不良事件记录为基础,而严重度的估计应与临床共同协商决定。将风险估计结果与可接受风险标准进行比较,评价风险的可接受性。表1和表2分别为ISO14971和CLSI EP18-A2文件的风险评价模型,临床实验室应根据选择的概率和严重度衡量尺度选择对应的评价标准。

表1 风险可接受性矩阵表

表2 风险评分模型
3 风险控制与监测
风险控制是实验室最熟悉的部分,即对不可接受的或最严重的风险采取各种质量控制措施,包括室内质量控制、室间质量评价、人员培训、检测程序改进、整合设备固有监测系统等[11]。临床实验室应根据自身的实际情况,考虑当地监管认可要求、实验室环境等,采取合适的措施。传统质控品检测结合设备固有控制或其他控制过程是未来质量管理和质量保证的趋势。控制措施采取后应进行监测,比较风险是否降低,以评价控制措施的有效性。差错趋势、临床抱怨、患者投诉的监测是修正实验室质量控制计划和过程改进的良好资源。对监测过程总出现的不可接受风险,应调查其原因,从根本上降低剩余风险。
4 风险管理工具
目前已有很多成熟的风险管理工具可供临床实验室使用,如故障报告、分析和纠正措施系统(FRACAS),故障模式与影响分析(FMEA),故障树(FTA),帕累托图,鱼骨图等。以FMEA为例,简单介绍风险管理工具如何用于临床实验室[12]。FMEA方法学包括5个步骤:(1)选择研究过程,根据风险因素的严重度及出现概率,将风险最高的事件或过程作为研究对象;(2)召集多学科小组,最好包括具有特定知识、技能和经验的不同学科的专家;(3)采集和组织研究过程的信息,可利用流程图分析检测过程,同时参考监管认可要求、厂家说明等;(4)执行风险分析;(5)制定并实施控制和改进措施。表3为FMEA用于临床实验室核酸扩增检测的实例。
5 总结
风险管理有助于临床实验室综合实施传统室内质量控制、仪器固有控制系统和其他控制措施,使实验室检测过程中的各个风险降低至临床可接受水平。临床实验室可利用风险管理工具对检验全过程的故障进行分析、评价、调查、控制和监测,以实现持续质量改进,保证患者的安全。
[1]ISO.Medical laboratories-Particular requirements for quality and competence.ISO 15189[S].Geneva,Switzerland:International Organization for Standardization,2009.
[2]ISO.Risk management-Principles and guidelines.ISO31000[S]. Geneva,Switzerland:International Organization for Standardization, 2009.
[3]CLSI.Laboratory quality control based on risk management;approved guideline.CLSI document EP23-A[S].Wayne,PA:Clinical and Laboratory Standards Institute,2011.
[4]JC.Failure Mode and Effects Analysis in Health Care:Proactive Risk Reduction[S].Oakbrook Terrance,IL:The Joint Commission, 2010.
[5]CLSI.Risk Management Techniques to Identify and Control Laboratory Error Sources.CLSI document EP18-A2[S].Wayne,PA: Clinical and Laboratory Standards Institute,2009.
[6]ISO.Medicallaboratories-reductionoferrorthroughrisk management and continual improvement.ISO/TS 22367[S]. Geneva,Switzerland:International Organization for Standardization, 2008.
[7]ISO.Medical devices-Application or risk management to medical devices.ISO 14971[S].Geneva,Switzerland:International Organization for Standardization,2007.
[8]康凤凤,王治国.临床实验室质量控制中的风险管理[J].临床检验杂志,2012,30(7):539-542.
[9]Plebani M.Exploring the iceberg of errors in laboratory medicine [J].Clin Chim Acta,2009,404(1):16-23.
[10]Goswami B,Singh B,Chawla R,et al.Evaluation of errors in a clinical laboratory:a one-year experience[J].Clin Chem Lab Med, 2010,48(1):63-66.
[11]王治国.临床检验质量控制技术[M].北京:人民卫生出版社,2008.
[12]康凤凤,王治国.失效模式和效应分析在减少检验医学差错中的应用[J].中国医院,2012,16(9):37-39.

表3 FMEA在临床实验室核酸扩增检测中的应用
·读者·作者·编者·
2011年度《实验与检验医学》影响因子
据中国科技信息研究所、北京万方数据2012年版中国期刊引证研究报告,在“万方数据-数字化期刊群”基础上,结合中国科技论文与引文数据库(CSTPCD),以我国正式出版的各学科6000余种中英文期刊为统计源期刊,经统计分析,本刊2011年度影响因子为0.722。
《实验与检验医学》编辑部
Risk management and quality improvement in clinical laboratory
KANG Fengfeng,WANG Wei,WANG Zhiguo.National Center for Clinical Laboratory,Beijing Hospital,Ministry of Health,Beijing 100730,China
Risk management is the systematic application of management policies,procedures,and practices to fulfil tasks of analyzing,evaluating,controlling and monitoring risk to minimize the probability and impact of adverse events.The core process of risk management is the continuous process of identification,estimation,evaluation,control and monitoring of risk and failure investigation.There are many tools of risk management can be used to analyse and assess the total testing process.Unacceptable risk should be investigated,controlled,and monitored in order to promote continuous quality improvement and ensure patient safety.
Risk;Risk management;Total testing process;Quality control;Quality improvement
R446
A
1674-1129(2013)01-0001-03
10.3969/j.issn.1674-1129.2013.01.001
康凤凤(1988-),女,汉族,浙江宁波,北京协和医学院在读硕士,临床检验诊断学,研究方向为临床实验室质量管理。
王治国。
