4-氨基安替比林在盐酸溶液中对碳钢的缓蚀行为
2013-02-14蔡述兰谯康全任德虎何磊金张小兰
蔡述兰,谯康全,任德虎,何磊金,张小兰
(四川理工学院 化学与制药工程学院,自贡643000)
金属酸洗缓蚀剂是一种高效的金属防腐蚀试剂,在锅炉、管道等金属设备的清洗中应用广泛[1]。为研制出更高效的金属酸洗缓蚀剂,最有效的方法之一是以具有一定缓蚀性能的缓蚀剂分子为基础进行新分子合成或复配。其中以天然产物或生化试剂为切入点展开金属酸洗缓蚀剂的研究具有重要意义[2-3]。
4-氨基安替比林是一种可用于神经肝细胞培养的生化试剂,含有多个供电子结构,而供电子分子结构也正是酸洗缓蚀剂能在金属表面致密吸附的主要因素之一[3-5]。因此,本工作采用失重法、动电位扫描法、电化学阻抗谱研究了4-氨基安替比林在盐酸介质中对碳钢的缓蚀行为,研究其在酸性介质对金属的缓蚀性能和吸附情况,为更高效的金属酸洗缓蚀剂的分子结构研究奠定基础。
1 试验
1.1 药品与仪器
药品为4-氨基安替比林(AR,北京博瑞盛嘉化工技术有限公司,结构式见图1)。
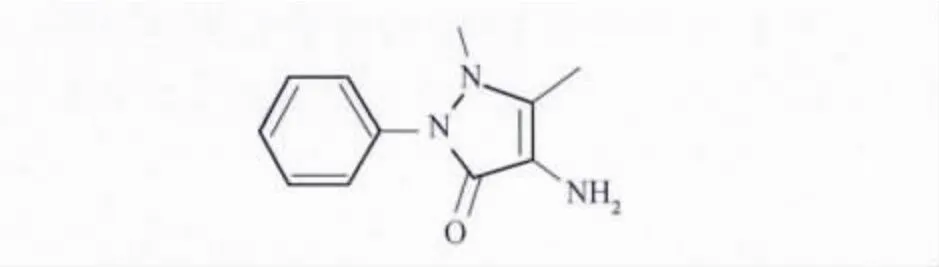
图1 4-氨基安替比林的分子结构图
仪器为CHI660D型电化学工作站(上海辰华仪器公司,采用三电极体系;工作电极为圆碳钢柱,工作面积为0.785cm2,非工作表面以环氧树脂涂封;参比电极为饱和甘汞电极(SCE);辅助电极为铂片电极)。
1.2 失重试验
大小为49.5mm×24.0mm×2.0mm的碳钢片用金相砂纸(干湿两用型)逐级打磨至1000#,蒸馏水冲洗、丙酮超声、室温干燥后称量,然后分别悬挂浸泡于25℃下含不同浓度4-氨基安替比林的1mol·L-1HCl溶液中,静置4h后取出钢片,除去腐蚀产物,再次用蒸馏水冲洗、丙酮超声脱脂,室温干燥后称量。
1.3 电化学试验
用金相砂纸将碳钢柱底工作面逐级打磨抛光至1000#,蒸馏水冲洗、丙酮超声,干燥后置于25℃下空白或含不同浓度4-氨基安替比林的1mol·L-1HCl溶液中,首先测定电化学阻抗谱,频率范围为100kHz~10mHz、扰动电位为±5mV;然后测定动电位极化曲线,扫描速率为1mV·s-1、扫描电位范围为开路电位±150mV。
2 结果与讨论
2.1 失重试验
在25℃的1mol·L-1HCl溶液中,利用失重法考察了不同浓度4-氨基安替比林对碳钢片的缓蚀效率,结果见表1。缓蚀效率计算见式(1):

式中:v0,vcorr分别为空白和含4-氨基安替比林溶液中钢片的腐蚀速率,单位为mg·cm-2·h-1。

表1 失重试验结果
由表1可知,4-氨基安替比林在HCl介质中对碳钢的缓蚀效果显著。浓度为5.00mmol·L-1时缓释效率就可达89.35%,且随着4-氨基安替比林浓度增加,腐蚀速度逐渐减小,缓蚀效率不断提高。当4-氨基安替比林浓度大于5.00mmol·L-1时缓蚀效率增幅明显减缓。
2.2 动电位极化曲线测试
25℃下,在不同浓度4-氨基安替比林的1mol·L-1HCl介质中,测定碳钢工作电极的动电位极化曲线(见图2),并利用CHI660D型电化学工作站软件获得电化学参数(见表2)。其中,缓蚀效率计算见式(2):
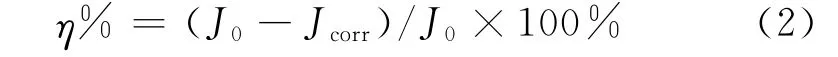
式中:J0,Jcorr分别为空白和含4-氨基安替比林溶液中钢柱底工作面的腐蚀电流密度,单位为μA·cm-2。

图2 不同浓度4-氨基安替比林动电位极化曲线图

表2 动电位测试主要电化学参数及缓蚀效率
由图2和表2可知:添加4-氨基安替比林后,碳钢的腐蚀电流密度显著减小,且随着4-氨基安替比林浓度增加,缓释效率不断提高,说明4-氨基安替比林在HCl介质中对碳钢有显著的缓蚀作用。当浓度小于5.00mmol·L-1时,随着缓蚀剂浓度的增加,缓蚀效率增加明显,而当浓度大于5.00mmol·L-1时,缓蚀效率增幅减弱,这表明4-氨基安替比林浓度为5.00mmol·L-1时在碳钢表面的吸附趋于饱和。随着4-氨基安替比林浓度增加腐蚀电位总体呈负移趋势,均较空白溶液的腐蚀电位低,但不显著,缓蚀剂类型受电位控制[6]。随4-氨基安替比林浓度增加阴极极化曲线和阳极极化曲线均向低电流方向移动,表明4-氨基安替比林同时抑制了阳极和阴极反应。4-氨基安替比林浓度的变化对βa影响不大,阳极极化曲线与空白盐酸溶液近似平行,而阴极极化曲线βc变化相对较大,且总体上随缓蚀剂浓度增加呈现小幅正移趋势,但偏离空白盐酸溶液的βc值不大。结合腐蚀电位及极化曲线变化规律,可认为4-氨基安替比林是以阴极控制更为明显的混合型缓蚀剂[7]。
2.3 电化学阻抗谱
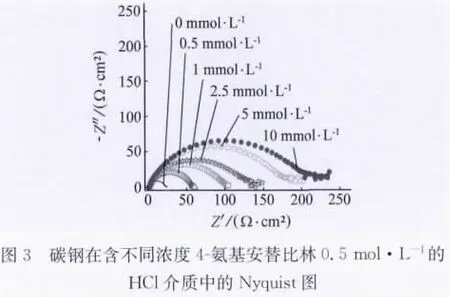
25℃下,在不同浓度4-氨基安替比林的1mol·L-1HCl溶液中,测定碳钢的电化学阻抗谱,结果见图3和图4。
由图3的Nyquist图可知:碳钢在不同浓度4-氨基安替比林的1mol·L-1HCl溶液中,阻抗谱相似,主要由直径较大的高频容抗弧组成,且随着4-氨基安替比林浓度增加,容抗弧直径呈增大趋势,表明4-氨基安替比林能有效降低碳钢在HCl介质中的腐蚀速度,原因可能是4-氨基安替比林分子吸附于碳钢表面阻挡了金属与腐蚀介质的接触。由图4的Bode图可知:在相位角曲线的高中频区出现了一个峰,说明碳钢在4-氨基安替比林的HCl溶液中进行了一个时间常数的腐蚀过程,即腐蚀反应受电极表面双电层电子传递过程控制[8]。在低频区,出现了小于0°的相位角曲线,表明缓蚀剂在碳钢表面可能存在吸附⇌脱附平衡过程[9]。在空白和含4-氨基安替比林溶液中,相位角图呈现类似形状,表明4-氨基安替比林吸附层没有改变空白HCl溶液中碳钢原有的腐蚀反应机制,这与极化曲线分析结果相符。

基于图3和图4的分析结果,采用ZVIEW软件拟合等效电路,其等效电路图及电化学阻抗谱主要参数分别见图5和表3,其中Rp为膜电荷转移电阻,单位为Ω·cm-2,电容元件CPE由CPE-T和CPE-P组成,CPE-T相当于电容,单位为μF·cm-2,CPE-P为弥散效应指数,取值范围为0.5~1[10]。缓蚀效率计算采用式(3):

式中:Rp0,Rpcorr分别为空白和含4-氨基安替比林的1mol·L-1HCl溶液中钢柱底工作面的Rp值。
由图5可知:双电层等效元件用CPE表示而不是纯电容,这是由于电极表面存在弥散效应,导致空白和含4-氨基安替比林溶液中的高频容抗弧均为压扁半圆(见图3)[11]。由表3可知:随4-氨基安替比林浓度增加CPE-T总体呈递减趋势,表明缓蚀剂分子取代钢表面的活性点数增多,介电常数较小的缓蚀剂分子取代介电常数较大的水分子的量增加,缓蚀剂吸附层更加致密,从而导致双电层电容总体呈现减小趋势,使得腐蚀反应更难以进行。由于碳钢电极表面存在弥散效应,空白和含4-氨基安替比林溶液中的CPE-P均小于1[8]。随4-氨基安替比林浓度增加,Rp逐渐增加,进一步表明钢的腐蚀受电极表面双电层电子传递过程控制。4-氨基安替比林浓度低于5.00mmol·L-1时,图3中的容抗弧直径和表3中的缓蚀效率均随4-氨基安替比林浓度的提高增幅明显,这种变化趋势与失重法、动电位极化曲线法测试结果相符。当4-氨基安替比林浓度高于5.00mmol·L-1时,缓蚀效率增幅明显减弱,当高于10.0mmol·L-1时,继续添加4-氨基安替比林,缓蚀效率无明显变化,说明4-氨基安替比林浓度为10.0mmol·L-1时在碳钢表面可能已形成较为完整的饱和吸附层。

图5 等效电路图

表3 电化学阻抗谱主要参数及缓释效率
2.4 缓蚀剂的吸附行为
将表1中数据用Langmuir,Temkin,Frumkin,Freundlich吸附等温式进行拟合。拟合结果表明Langmuir吸附等温式符合较好(见图6),Langmuir吸附等温式为:

式中:c为缓蚀剂浓度,mol·L-1;θ为表面覆盖度,由于4-氨基安替比林具有混合型缓蚀剂特征,因此θ可用缓蚀效率η%近似表示[8];k为常数,等于吸附平衡常数ka,L·mol-1。
由图6可知,拟合直线的R值为0.999 71,斜率为1.067,表明4-氨基安替比林在碳钢表面为单分子层吸附,而碳钢表面间作用力可能是导致直线斜率值略大于理论值1的主要因素,根据直线截距1/k可得ka=4 013L·mol-1,则吸附自由能(△Ga0)=-RTln(55.5ka)=-30.52kJ·mol-1>-40kJ·mol-1,表明4-氨基安替比林在碳钢表面吸附是一种介于物理吸附与化学吸附之间的混合型自发吸附[12]。
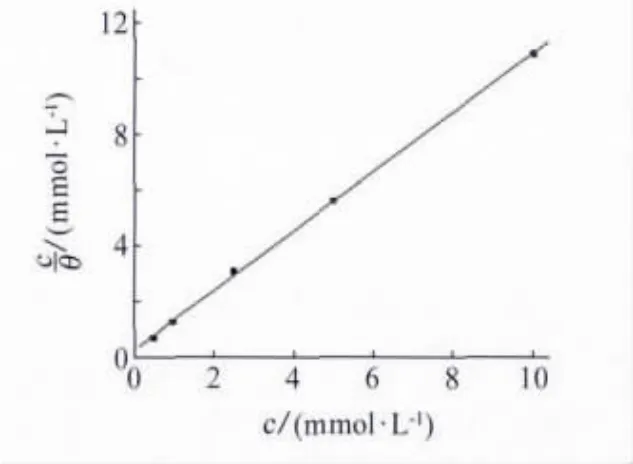
图6 c/θ与c的关系图
3 结论
(1)在温度为25℃、HCl浓度为1mol·L-1的介质中,4-氨基安替比林对碳钢有显著的缓蚀作用,并随4-氨基安替比林浓度的增加缓蚀效率增大,当4-氨基安替比林浓度仅为5.00mmol·L-1时,失重法获得的缓蚀效率高达89.35%,缓蚀剂吸附趋于饱和。
(2)在温度为25℃、HCl浓度为1mol·L-1的介质中,4-氨基安替比林在碳钢表面的吸附符合Langmuir吸附等温式,是一种介于物理吸附与化学吸附之间的混合型自发吸附。
(3)4-氨基安替比林在HCl介质中能同时抑制碳钢表面的阴极和阳极反应,缓蚀剂类型受电位控制,是一种以阴极控制更为明显的混合型缓蚀剂。
[1]Hasanova R,Bilgeb S,BilgiçS,et al.Experimental and theoretical calculations on corrosion inhibition of steel in 1MH2SO4by crown type polyethers[J].Corrosion Science,2010,52(5):984-990.
[2]Raja P B,Sethuraman M G.Natural products as corro-sion inhibitor for metals in corrosive media-a review[J].Materials Letters,2008,15(1):113-116.
[3]杨尚军,谭世语,张研.生物缓蚀剂的研究进展[J].表面技术,2006,35(1):12-13,73.
[4]Praveen B M,Venkatesha T V.Metol as corrosion inhibitor for steel[J].International Journal of Electrochemical Science,2009,4(1):267-275.
[5]Khaled K F.New synthesized guanidine derivative as a green corrosio inhibitor for mild steel in acidic solutions[J].International Journal of Electrochemical Science,2008,30(3):462-475.
[6]闫莹,李伟华,邢少华,等.新型杂环化合物在1M HCl中对Q235钢的缓蚀性能研究[J].腐蚀科学与防护技术,2007,12(6):414-418.
[7]王招娣,司云森,余强,等.一种曼尼希碱在酸性介质中对碳钢缓蚀行为的研究[J].表面技术,2011,40(1):59-62,80.
[8]曹楚南.腐蚀电化学原理(第三版)[M].北京:化学工业出版社,2008.
[9]陈文.碳钢缓蚀剂和铜基自组装膜的研究[D].重庆:西南大学硕士学位论,2012.
[10]赵丽娜,许淳淳.无机复合缓蚀剂对碳钢的缓蚀性能[J].腐蚀与防护,2008,29(8):460-463.
[11]Kissi M,Bourklah M,Hammouti B,et al.Establishment of equivalent circuits from electrochemical impedance spectroscopy study of corrosion inhibition of steel by pyrazine in sulphuric acidic solution[J].Applied Surface Science,2006,52(12):4190-4197.
[12]宋伟伟,张静,杜敏.新型不对称双季铵盐缓蚀剂在HCl中对Q235钢的缓蚀行为[J].化学学报,2010,69(16):1851-1857.
