溶胶凝胶法制备纳米二茂铁微粒及其电催化性能研究
2013-01-29宋诗稳甄延忠刘珍叶齐广才
宋诗稳, 于 浩, 甄延忠, 刘珍叶, 齐广才
(1.延安大学 能源与环境工程学院, 陕西 延安 716000; 2.延安大学 化学与化工学院, 陕西 延安 716000)
0 引言
二茂铁(Ferrocene,Fc)是一种具有芳香族性质的有机过渡金属化合物,其特殊的化学结构和优异的电催化活性在电化学传感器领域得到了广泛的应用[1-4].但Fc不易吸附于基础电极表面,而影响了修饰电极的稳定性[5].为解决这一问题,本文首先采用溶胶凝胶法制备出Fc微粒,再将其预先加入以甲基三甲氧基硅烷为硅源的溶胶中,制备了具有三维网状结构的无机多孔材料.甲基三甲氧基硅烷水解后失水缩聚成硅氧烷聚合物,同时将Fc填充于Si-O溶胶网络而形成SiO2-Fc凝胶.为进一步考察SiO2-Fc凝胶微粒的电催化活性,本文将SiO2-Fc凝胶微粒制成了化学修饰碳糊电极,研究了修饰电极对AA的电催化性能.研究表明:将Fc固载于溶胶凝胶中提高了修饰电极的稳定性与灵敏度,并改善了Fc的分散性.
1 实验部分
1.1 仪器和试剂
JSM-6700F型扫描电子显微镜用来说明Fc微粒的微观形貌.LK98BII型电化学工作站(天津兰力科公司)用来进行电化学实验.采用三电极系统电化学池,以修饰电极为工作电极,铂丝电极为辅助电级,饱和甘汞电极(SCE)为参比电极.文中电位值均是相对于饱和甘汞电极的电位.甲基三甲氧基硅烷(MTMOS,杭州硅宝化工),二茂铁(AR,西安化学试剂厂),高纯石墨粉(国药集团化学试剂有限公司,光谱纯).其它试剂均为分析纯试剂,水为二次蒸馏水.
1.2 电极的制备
1.2.1 Fc微粒的制备
将2 g二茂铁超声溶解于200 mL无水乙醇中,记为溶液a.在磁力搅拌下,将300 mL二次水逐滴加入a中,室温搅拌2 h,过滤黄色沉淀得到Fc溶胶,室温下溶胶经陈化后得到凝胶体,于60 ℃烘箱中蒸发掉多余溶剂,干燥后研磨既得Fc微粒.
1.2.2 sol-gel/Fc微粒的制备
向一干燥具橡胶塞的玻璃瓶内加入6.0 mL甲醇,0.4 mL浓HCl,4.0 mL MTMOS,超声5 min得均一的溶胶.向其中加入0.1 g Fc微粒,超声1 h,室温放置24 h后研细,即得sol-gel/Fc微粒.
1.2.3 碳糊电极的制备
修饰碳糊电极的制备:称取0.3 g sol-gel/Fc和0.9 g石墨粉于一10 mL小烧杯中,混合均匀后加入0.6 mL液体石蜡,充分搅拌直至得到均一的碳糊,将此碳糊装填入内径2 mm的聚四氟乙烯塑料管中,碳糊在管中的长度约为1 cm,并使管外留有少量的碳糊,从管的另一端插入一根细铜丝作为引线.电极使用前先在称量纸上仔细打磨至得到一光滑平整的电极表面,再用水充分冲洗,记为sol-gel/Fc/CPE.
裸碳糊电极的制备:制备方法与sol-gel/Fc/ CPE电极相似,但不加Fc,将石墨粉与液体石蜡按1.0 g∶0.5 mL的比例混合,记为裸CPE.
1.3 实验方法
循环伏安实验:将修饰电极(或裸CPE)表面冲洗干净后,置于一定的支持电解质溶液中以不同的扫描速率记录0.8 ~-0.2 V电位范围内的循环伏安图.
扫描电镜实验:用一薄层导电胶带将粉体微粒粘在样品台上,把样品台朝下使未与胶带接触的微粒脱落,再用洗耳球轻吹掉粘接不牢固的微粒,记录电镜图.
动力学计时安培实验:仔细冲洗电极表面,以修饰电极为工作电极,控制工作电极电位为一定值,向一连续搅拌的溶液中每隔一定时间加入一定量的AA,记录i-t曲线.
2 结果与讨论
2.1 sol-gel/Fc/CPE修饰电极的扫描电镜实验
图1(a)为以Fc为先驱体,以乙醇为互溶剂通过水解和缩聚反应制成的Fc微粒.当二次水逐滴加入先驱体与有机溶剂形成的均匀溶液,溶质释放出水和相应的醇,形成溶胶粒子,溶胶粒子进一步聚集生长而成凝胶[6].由图1(a)可知,部分Fc微粒直径小于1μm,但团聚严重,这是由于先驱体水解后生成次生粒子时聚合速度过快.为解决这一问题,本文将1.2.1中制得的Fc微粒超声分散于MTMOS的溶胶结构中.图1(b),(c)分别为所得sol-gel/Fc微粒在10 000倍与30 000倍放大倍数下的SEM图.可以看出,MTMOS失水缩聚后形成了具有三维管状结构的硅氧烷聚合物,凝胶过程中Fc均匀地填充于Si-O溶胶网络结构中.形成SiO2-Fc凝胶后,Fc纳米粒子的团聚现象得到了明显改善,粒径基本小于300 nm (图1(c)),这种形貌特征为提高修饰电极的稳定性及电催化活性提供了可能.MTMOS在酸性条件下可发生水解[7],为使反应在均相体系中进行,实验选择浓盐酸为催化剂,甲醇为反应体系的共溶溶剂.实验选择溶胶液的组成为6.0 mL甲醇+0.4 mL浓HCl+4.0 mL MTMOS.

(a) Fc微粒放大10 000倍的SEM图

(b) sol-gel/Fc微粒放大10 000倍的SEM图

(c) sol-gel/Fc微粒放大30 000倍的SEM图图1 扫描电镜图
2.2 sol-gel/Fc/CPE的电化学性质
由图2可知,在0.1 mol/L PBS中,当扫速为10~100 mV/s时,阴、阳极峰电位基本不随扫速变化而改变,峰电流与扫速的一次方呈线性关系(图 2(a)),表明该电极过程是一表面控制的可逆过程[8].
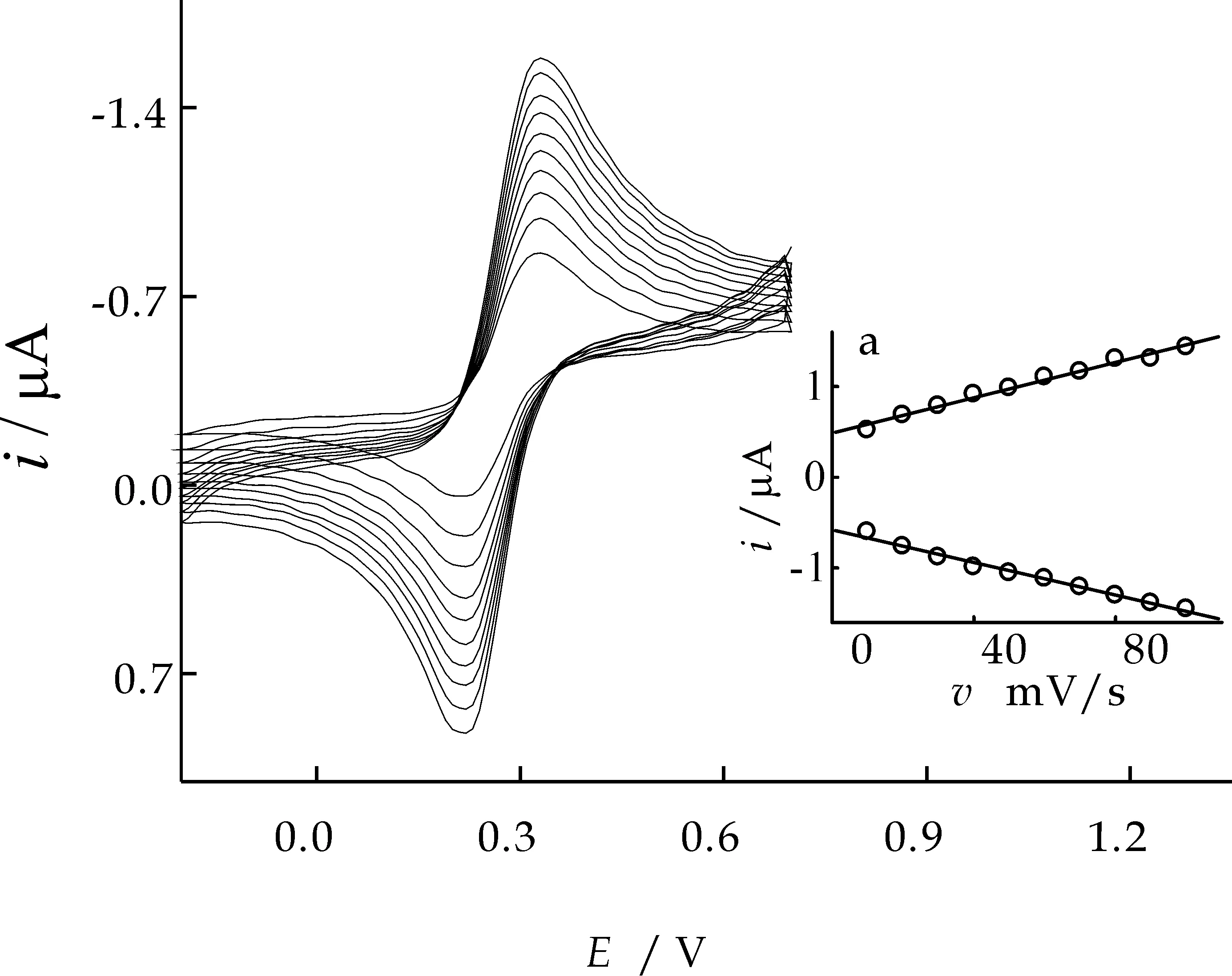
图2 电位扫描速率对sol-gel/Fc/CPE峰电流和峰电位的影响
2.3 sol-gel/Fc/CPE修饰电极的电催化活性
采用循环伏安法研究了修饰电极的电催化氧化性能(如图3所示).图中曲线a为sol-gel/Fc/CPE电极在0.1 mol/L PBS中的循环伏安图,b,c分别为裸CPE与sol-gel/Fc/CPE在4.0×10-4mol/LAA中的循环伏安图.可以看出,加入 AA后,裸CPE上氧化峰出现在较高电位处,灵敏度很低,而在sol-gel/Fc/CPE电极上,随着AA的加入阳极峰电流迅速增加,阴极峰电流明显减小.
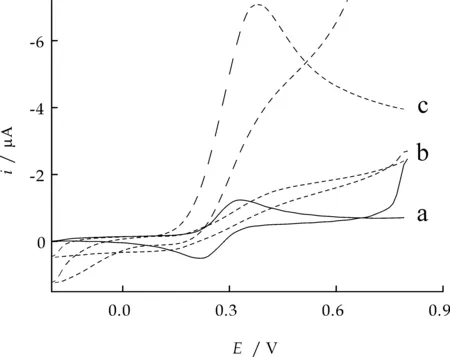
a:sol-gel/Fc/CPE在0.1 mol/L PBS中的伏安曲线; b, c:裸CPE与sol-gel/Fc/CPE在4.0×10-4 mol/L AA中的伏安曲线图3 AA在sol-gel/Fc/CPE和裸CPE上的循环伏安图
过电位的降低和电流响应的增大说明Fc在该反应体系中作为电子媒介体,可催化AA的氧化,随着AA浓度的增加,氧化态Fc立即又被AA所还原,所以修饰电极氧化电流增大,还原电流减小[9].对于一定浓度的AA,在一定扫速范围内催化电流与v1/2成正比 (图4(a)),随着扫速的增加,则偏离该线性关系.原因在于,在有限的时间内电极表面氧化态的Fc来不及被AA还原,故生成的还原态Fc少,阳极峰电流增幅随之减小.上述现象表明该电催化过程由AA向电极表面的扩散速度控制且催化电流与AA的浓度有关[10].
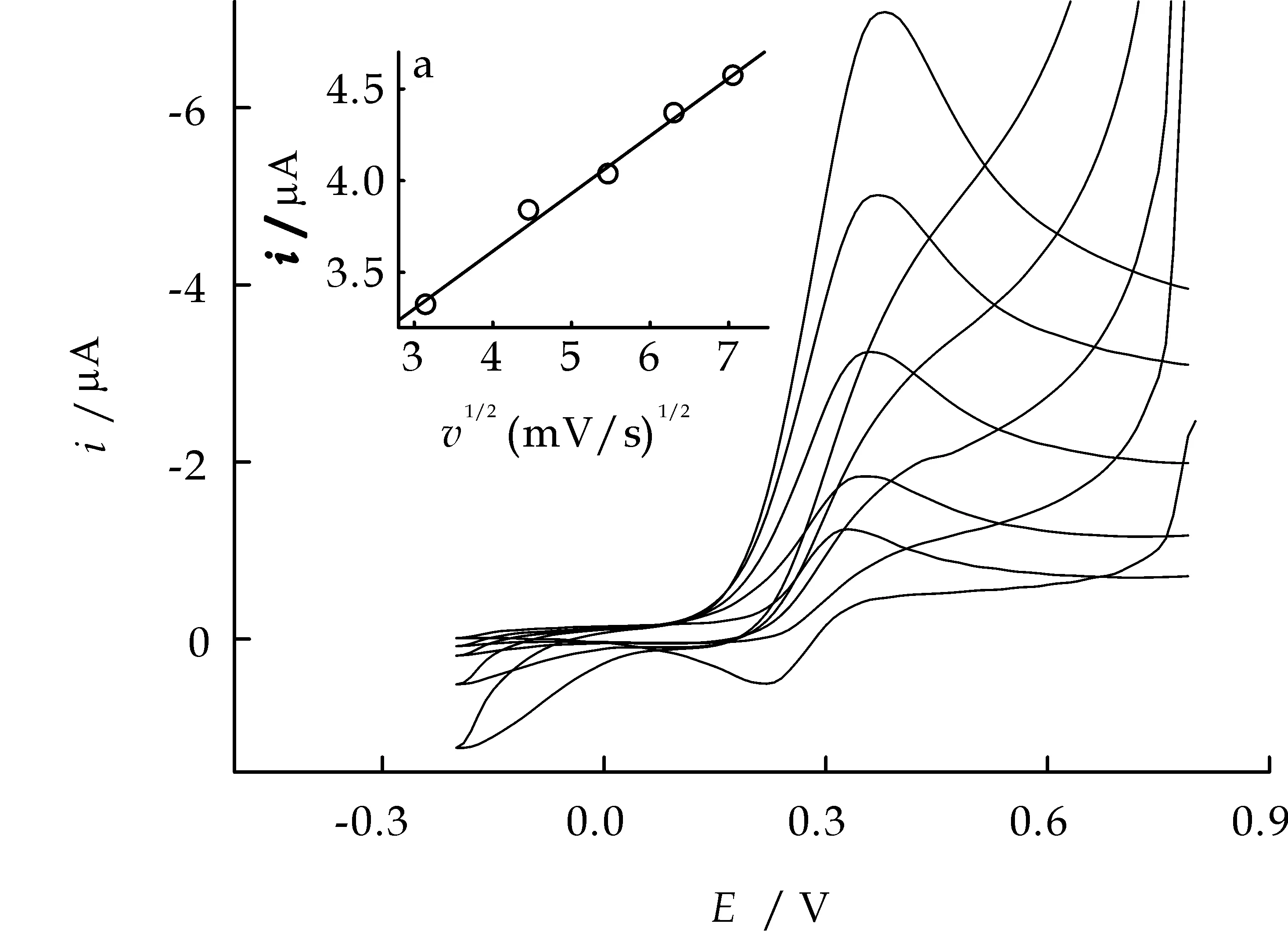
c(AA):0.0, 1.0, 2.0, 3.0, 4.0×10-4 mol/L; v:50 mV/s; a:i-v1/2; c(AA): 3.0×10-4 mol/L; v:10 ~ 50 mV/s图4 不同浓度AA在sol-gel/Fc/CPE上的循环伏安图
2.4 催化反应速率常数的测定
采用计时安培法测定了AA的扩散系数及催化反应的速率常数[11,12].图5为不同浓度AA的计时安培曲线,以i-t-1/2曲线线性关系的斜率对AA浓度作图(如图5(a)所示),扩散系数为2.15×10-5cm2/s.以Icat/IL-t1/2曲线斜率对AA浓度平方根作图(如图5(b)所示),求得异相催化反应速率常数为1.23×103L/mol s.
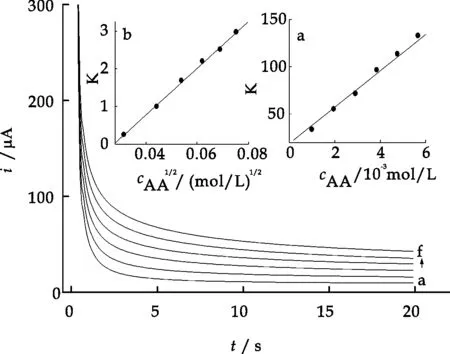
c(AA) a~f: 0.99, 1.96, 2.91, 3.85, 4.76, 5.66×10-3 mol/L;E: -0.2 ~ 0.45 V图5 不同浓度AA在sol-gel/Fc/CPE上的计时安培图
2.5 安培法检测AA
动力学计时安培实验研究表明,当以0.1 mol/L PBS为测定介质,控制工作电极电位为0.45 V时,AA浓度与其电流响应在3.0×10-6~2.5×10-3mol/L范围内有良好的线性关系(r=0.996 6),检出限为1.0×10-6mol/L,响应时间小于5 s(如图6(b)所示).
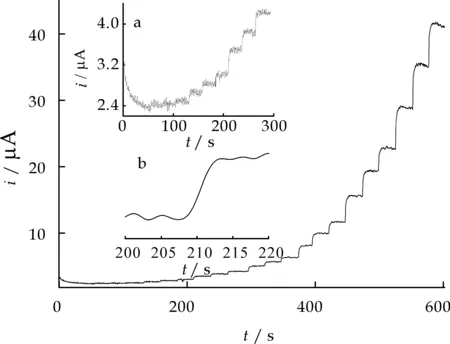
工作电位: 0.45 V;底液: 0.1 mol/L PBS;AA加入量:3.0×10-5, 5.0×10-5, 1.0×10-4, 3.0×10-4, 5.0×10-4, 1.0×103, 3.0×10-3 mmol各3次图6 sol-gel/Fc/CPE的安培响应
2.6 修饰电极的稳定性与重现性
采用循环伏安法研究了sol-gel/Fc/CPE的稳定性和重现性.在0.1 mol/L PBS中,当扫速为50 mV/s时,平行测定10次1.0 mmol/L AA的相对标准偏差为5.6%,电极于室温下放置30 d后重新测试AA的响应电流几乎不变,表明修饰电极对AA的测定具有较好的稳定性和重现性.同一批次制作的5支电极经相同的前处理后,其电流响应的相对标准偏差不超过6%,当扫速为50 mV/s时,在0.8 ~ -0.2 V电位范围内经过50圈的连续电位循环后,峰电流的降低值不超过5%,表明该电极具有良好的稳定性.
3 结束语
采用两步溶胶凝胶法制备了sol-gel/Fc纳米粒子并将其制成化学修饰碳糊电极,研究了该电极的电催化性能.结果表明,Si-O的凝胶网络显著提高了Fc微粒的分散性及稳定性,Fc纳米粒子粒径约为300 nm.所制备的sol-gel/Fc/CPE修饰电极对AA的氧化具有明显的催化活性,在生物电化学传感器制作方面具有潜在的应用价值.
[1] Tauchman J.,tP..Preparation and structural characterisation of a novel ferrocene-amino acid conjugate[J].Inorganic Chemistry Communications,2010,13(1):149-152.
[3] 苏 敏,李 晴,王亚光,等.二茂铁修饰卟啉及含氟卟啉的光物理与电化学性质[J].有机化学,2013,33(4):815-819.
[4] 毛燕妮,刘淑娟,廖桢葳,等.氨基-β-环糊精-石墨烯-二茂铁修饰电极对多巴胺的电化学行为研究[J].功能材料,2012,43(8):976-979.
[5] Brooks S.L.,Ashby R.E.,Turner A.P.F.. Development of an on-line glucose sensor for fermentation monitoring[J].Biosensors,1988,3(1):45-56.
[6] 陈登福.溶胶-凝胶法制备纳米二氧化钛颗粒的研究[C]//全国冶金物理化学学术会议专辑.郑州:中国稀土学报,2004:550-554.
[7] 曹 兵,朱从善.采用有机改性硅醇盐甲基三乙氧基硅烷制备无支撑孤立膜[J].硅酸盐学报,1998,26(6):768-772.
[8] Bean L.S.,Heng L.Yook.,Yamin B.Mohd.,et al.The electrochemical behaviour of ferrocene in a photocurable poly(methyl methacrylate-co-2-hydroxylethyl methacrylate) film for a glucose biosensor[J].Bioelectrochemistry,2005,65(2):157-162.
[9] 邓湘辉,阚显文,尉 艳,等.二茂铁/L-半胱氨酸修饰电极的电化学行为及电催化性能[J].物理化学学报,2005,21(12):1 399-1 402.
[10] Sheng Q.L.,Yu H.,Zheng J.B..Sol-gel derived terbium hexacyanoferrate modified carbon ceramic electrode:electrochemical behavior and its electrocatalytical oxidation of ascorbic acid[J].Journal of Electroanalytical Chemistry,2007,606(1):39-46.
[11] Bard A.J.,Faulkner L.R..Electrochemical methods,fundamentals and applications[M].2nd Edition.New York:John Wiley & Sons.Inc, 2001:163.
[12] Pournaghi-azar M.H.,Sabzi R..Electrochemical characteristics of a cobalt pentacyano- nitrosylferrate film on a modified glassy carbon electrode and its catalytic effect on the electrooxidation of hydrazine[J].Journal of Electroanalytical Chemistry,2003,543(2):115-125.
