人工低温胁迫条件下菲油果各项生理指标的变化
2013-01-05袁德义
唐 丽,张 瑜,袁德义
(中南林业科技大学,湖南 长沙 410004)
人工低温胁迫条件下菲油果各项生理指标的变化
唐 丽,张 瑜,袁德义
(中南林业科技大学,湖南 长沙 410004)
为了探讨菲油果的抗寒特性,以引种的Coolidge和Mammoth 2个菲油果新品种成熟叶为试验材料,在人工低温胁迫条件下,对不同低温条件下叶片电导率、可溶性糖、游离脯氨酸(Pro)、超氧化物歧化酶(SOD)、过氧化物酶(POD)、丙二醛(MDA)等几个生理指标的变化情况进行研究。结果表明:在一定的温度范围内,不同品种的菲油果叶片的电导率均随着温度的降低而增大;可溶性糖含量和游离脯氨酸(Pro)随着温度的降低而增加,人工越冬过程中不同品种的菲油果的游离脯氨酸(Pro)呈有规律的变化;细胞内的保护酶(SOD、POD)都表现为随着温度的降低,其活性增强;方差分析结果显示,不同品种的菲油果相对电导率、丙二醛(MDA)、游离脯氨酸(Pro)、过氧化物酶(POD)差异达到显著水平,不同温度间电导率、可溶性糖、丙二醛(MDA)、游离脯氨酸(Pro)、过氧化物酶(POD)、超氧化物歧化酶(SOD)差异达到极显著水平,不同品种间的超氧化物歧化酶(SOD)差异不显著。
菲油果;人工低温胁迫;生理指标;抗寒性
菲油果Feijoa sellowiana,桃金娘科Myrtaceae菲油果属Feijoa常绿灌木或小乔木[1]。低温危害是植物栽培生产过程中常见的一种自然灾害,它不仅能够给植物生长造成严重的伤害,严重时甚至会导致植株的死亡,给生产带来严重的损失[2]。到目前为止,有关植物抗寒性的研究报道很多[3-8],但是大部分都是关于蔬菜、果树等园艺资源和大棚农作物展开的。
菲油果是一种集绿化、食用、观赏于一体的新兴园林树种,具有广泛的发展前景。目前,国内对于菲油果的研究不多,大部分对菲油果的研究建立在扦插、组织培养、药用价值及光合特性等方面[9-16],目前尚未对菲油果的抗寒性进行深入的研究。因此,本试验在人工低温胁迫条件下,研究菲油果抗寒性指标,探索其抗寒机理,从而更好地掌握其抗寒的特点,以期为菲油果的引种、选种、扩大栽培提供理论支持。
1 材料与方法
1.1 试验时间、地点
试验于2010年5月~2011年10月在中南林业科技大学植物园进行。该试验地的年平均气温为17.2~18.1 ℃,1月为全年平均温度最低月份,其平均气温为4.3~5.2 ℃,9月的平均气温为25.1~38.5 ℃,年积温为5 457 ℃,全年无霜期约275 d,年均降水量1 361.6 mm。
1.2 试验材料
菲油果树高1.5 m左右,树体健壮,生长势一致,开花结果正常。在菲油果植株上随机采取位于中上部生长一致的叶片,采集后立即用湿纱布包裹好,装入密封塑料袋中带回实验室。
1.3 试验方法
1.3.1 试验设计
于2010年5月~2010年10月的每月下旬采样,测定菲油果人工低温胁迫状况下的生理指标。将叶片用蒸馏水冲洗3次后,用吸水纸吸干水分。将叶片分为6组,置于密封塑料袋中进行低温处理。放入低温的冰箱或人工气候室内,设置的温度梯度为5、0、-5、-10、-15、-20 ℃。首先降温至5℃预冷12 h,然后从0℃开始降温,降温速度为1℃/h。并将低温处理后的样品置于5℃的冰箱内解冻24 h后取出待用。
1.3.2 测定方法
电导率采用电导仪测定;可溶性糖采用蒽酮比色法测定;超氧化物歧化酶(SOD)活力采用氮蓝四唑(NBT)法测定;过氧化物酶采用愈创木酚显色法[17]测定;丙二醛(MDA)参照邹琦方法测定;脯氨酸采用张殿忠等的磺基水杨酸提取,酸性茚三酮显色。上述试验均重复3次。
1.3.3 试验仪器
主要有:北京华瑞博远DDS-307精密型电导仪、分光光度计、电炉、铝锅、20 mL刻度试管、刻度吸管、记号笔、吸水纸适量。
1.3.4 统计分析
原始数据的合成、统计以及图表制作使用Microsoft Excel、Word 2007软件处理;数据统计分析采用SPSS统计分析软件。
2 结果与分析
2.1 不同低温处理菲油果细胞膜质膜透性的变化
由图1可知:人工低温胁迫下的2个品种菲油果叶片的相对电导率变化趋势均为上升的趋势。温度在降到0℃以下时,2个品种菲油果的相对电导率变化均不明显,随着低温胁迫温度的降低,膜透性逐渐增大,但是,膜受损的程度因品种而异。当温度达到-10 ℃时,2个品种菲油果的相对电导率分别为44.33%和53.83%;当温度下降到-15 ℃时,相对电导率分别为53.33%和60.98%,之后随着温度的降低,电导率变化不大,已经趋于平缓的状态。根据相对电导率达到50%时的温度作为半致死温度的判定[11-12],在-10℃时,Mammoth的相对电导率为53.83%,已经高于50%,其半致死温度应该在-10℃左右;在-15℃时,Coolidge的相对电导率为53.33%,同样高于50%,其半致死温度应该在-15℃左右。其研究表明2个品种菲油果的膜透性已经被完全破坏,并且膜透性的破坏是不可逆转的。

图1 不同温度处理菲油果叶片电解质外渗率的影响Fig.1 Effects of different low temperature treatments on electrolyte leakage of F. sellowiana leaves
对不同品种的菲油果叶片中电解质的外渗进行了方差分析,结果表明不同品种的菲油果叶片中的电解质的外渗差异显著,已经达到了极显著水平(见表1)。

表1 不同温度处理对菲油果叶片电解质外渗率影响的方差分析†Table 1 ANOVA on electrolyte leakage of F. sellowiana leaves with low temperature treatments
2.2 不同低温处理菲油果可溶性糖的变化
由图2可看出,可溶性糖的变化趋势总体上呈增加趋势,但是不同品种的菲油果变化幅度不相同。Coolidge在5~-15 ℃之间,可溶性糖含量一直呈现出上升的趋势,其中在5~-10℃时的变化幅度不大,相对比较稳定。当温度达到-10 ℃时,2个品种的菲油果叶片中可溶性糖的含量分别为15.56和 16.62 mg·g-1。但是 Coolidge在 -10 ~ -15 ℃时,所增加的幅度最大,此时可溶性糖的含量为19.93 mg·g-1;Mammoth在 -5~ -10 ℃时,可溶性糖含量上升的幅度最大,其含量为16.51 mg·g-1。可溶性糖含量上升幅度较大的原因可能是过低的温度使细胞遭到破坏,导致可溶性糖大量的积累。

图2 不同温度处理菲油果叶片可溶性糖含量的变化Fig. 2 Soluble sugar content changes of F. sellowiana leaves with low temperature treatments
对不同温度所处理的不同品种的菲油果叶片中可溶性糖的含量进行了方差分析,结果表明不同品种的菲油果叶片中的可溶性糖含量呈显著差异,不同温度处理间可溶性糖已达到了极显著水平(见表2)。

表2 不同温度处理下菲油果叶片可溶性糖含量的方差分析Table 2 ANOVA on soluble sugar contents of leaves F.sellowiana with different temperature treatments
2.3 不同低温处理菲油果丙二醛(MDA)的变化
如图3所示,在人工模拟低温的环境下,菲油果2个品种叶片中的MDA含量随着温度的降低呈现出先上升后下降的趋势, 2个品种的菲油果均在-5 ℃时丙二醛(MDA)的含量有明显上升的趋势,此时丙二醛(MDA)的含量分别为5.45和5.86 μmol·g-1;当温度达到 -15 ℃时,Coolidge 中丙二醛(MDA)含量又出现了一次大幅度的上升,此时的丙二醛(MDA)含量为 10.07 μmol·g-1,之后便随着温度的降低变化不大;Mammoth在温度达到-10 ℃时,MDA含量出现了较大幅度的上升,此时的含量为 8.97 μmol·g-1,在 -10 ℃之后,随着温度的降低,其丙二醛(MDA)的含量变化不大。从菲油果的2个不同品种叶片中丙二醛(MDA)的含量来看,Mammoth中丙二醛(MDA)的含量明显高于Coolidge。原因可能是过低的温度所引起的膜质过氧化,从而产生更多的丙二醛(MDA),大量的丙二醛(MDA)积累已经对细胞造成了毒害。由此可见,Coolidge的抗寒性要强于Mammoth的抗寒性。

图3 不同温度处理菲油果叶片可MDA含量的变化Fig.3 MDA content changes of F. sellowiana leaves with low temperature treatments
对不同温度所处理的不同品种的菲油果叶片中丙二醛(MDA)的含量进行了方差分析,结果表明不同品种的菲油果叶片中丙二醛(MDA)含量达到了显著水平,不同温度处理的叶片中丙二醛(MDA)含量已经达到了极显著水平(见表3)。

表3 不同温度处理下菲油果叶片MDA含量的方差分析Table 3 ANOVA on MDA content of F. sellowiana leaves with different temperature treatments
2.4 不同低温处理菲油果游离脯氨酸(Pro)的变化
图4所示,2个菲油果的品种中游离脯氨酸含量大体上呈先上升后下降的趋势。2个品种菲油果叶片中游离脯氨酸(Pro)的含量均在5~-5 ℃之间基本处于稳定状态,变化不大,均在-10 ℃时出现幅度较大的上升趋势,此时2个品种菲油果叶片中游离脯氨酸(Pro)的含量分别为9.82和9.67 μg·g-1,相差不大;之后,Mammoth叶片中游离脯氨酸(Pro)的变化不明显,而Coolidge在-15 ℃时达到高峰,此时的游离脯氨酸(Pro)含量为12.19 μg·g-1,在降温的后期变化不明显。
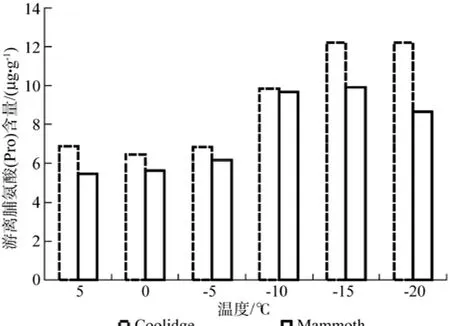
图4 不同温度处理菲油果叶片游离脯氨酸(Pro)含量的变化Fig.4 Proline content changes of F. sellowiana leaves with low temperature treatments
对不同温度所处理的不同品种的菲油果叶片游离脯氨酸(Pro)的含量进行了方差分析,结果表明不同品种的菲油果叶片中游离脯氨酸(Pro)的含量达到了显著水平,不同温度处理的叶片游离脯氨酸(Pro)含量已经达到了极显著水平(见表4)。
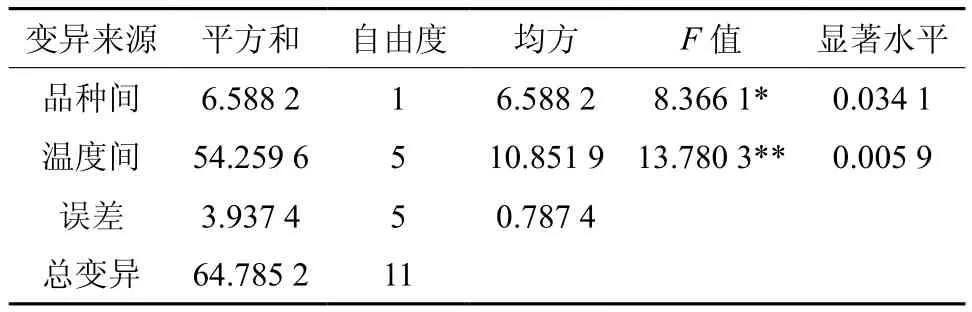
表4 不同温度处理下菲油果叶片游离脯氨酸含量的方差分析Table 4 ANOVA on proline content of F. sellowiana leaves with different temperature treatments
2.5 不同低温处理菲油果超氧化物歧化酶(SOD)的变化
氧化物歧化酶(SOD)在2个菲油果品种中的变化趋势大体为先上升或下降的趋势(见图5)。Coolidge中氧化物歧化酶(SOD)的活性随着温度的降低,活性随之升高,在-15 ℃时达到最大值后迅速降低,其最大值为10.33 mg·g-1;Mammoth叶片中氧化物歧化酶(SOD)活性相比Coolidge对低温较为敏感,在初次遭遇低温0 ℃时,其活性迅速上升,当温度达到-10 ℃时其活性达到最大值,此时的最大值为7.81 mg·g-1,同期Mammoth叶片中氧化物歧化酶(SOD)活性的上升幅度也达到了最大值,之后其活性便迅速下降。说明了随着温度的降低,刺激了氧化物歧化酶(SOD)的活性,但是当低温温度达到一定的临界值时,植物体内的氧化物歧化酶(SOD)便开始迅速地下降,其清除活性氧和自由基的功能甚至会随之消失。

图5 不同温度处理菲油果叶片SOD活性的变化Fig.5 SOD activities changes of F. sellowiana leaves with low temperature treatments
对不同温度所处理的不同品种的菲油果叶片超氧化物歧化酶(SOD)的含量进行了方差分析,结果表明不同品种的菲油果叶片中的超氧化物歧化酶(SOD)差异不显著,不同温度处理的叶片超氧化物歧化酶(SOD)含量差异极显著(见表5)。

表5 不同温度处理下菲油果叶片SOD活性方差分析Table 5 ANOVA on SOD content of F. sellowiana leaves with different temperature treatments
2.6 不同低温处理菲油果过氧化物酶(POD)的变化
图6所示:Coolidge的过氧化物酶(POD)在0~-10 ℃时呈缓慢上升的趋势,-10~-15 ℃时迅速上升,并且此时的上升幅度达到最大值,此时的最大值为2.1 mg·g-1,之后,便随着温度的降低而迅速的下降,其原因可能是由于温度过低,使细胞内遭到破坏,导致过氧化物酶(POD)的活性下降;Mammoth在初次遭遇低温时(0℃)便出现上升的趋势,其原因是对低温的一种防御能力,直至温度降低至-10 ℃时,达到其活性的最大值,此时的最大值为1.67 mg·g-1,在-10℃之后便一直呈下迅速地降趋势。由图6可知,2个菲油果品种不同低温处理后的叶片中氧化物酶(POD)酶的活性Coolidge明显高于Mammoth。

图6 不同温度处理菲油果叶片POD活性变化Fig.6 POD activities changes of F. sellowiana leaves with low temperature treatments
对不同温度所处理的不同品种的菲油果叶片过氧化物酶(POD)的含量进行了方差分析,结果表明不同品种的菲油果和不同温度处理的叶片中过氧化物酶(POD)均差异显著(见表6)。

表6 不同温度处理下菲油果叶片POD活性的方差分析Table 6 ANOVA on POD content of F. sellowiana leaves with different temperature treatments
3 结论与讨论
在人工低温越冬的低温条件下,所研究的2个品种菲油果叶片相对电导率、可溶性糖的含量、丙二醛(MDA)的含量、游离脯氨酸(Pro)的含量、超氧化物歧化酶(SOD)的活性、过氧化物酶(POD)的活性等指标均呈现先上升后下降的趋势。其结果与自然越冬低温条件及前人的研究结果一致[20-21]。
人工低温胁迫的环境条件下,相对电导率的变化趋势大体上呈现出随着温度的降低而上升的趋势,说明人工低温胁迫对细胞膜的伤害是不可逆转的。
当温度还是下降时,菲油果叶片中的可溶性糖含量没有出现明显的上升趋势,其原因可能是经过低温锻炼后,已对温度不敏感,还没有做出相应的反应。但是随着温度的降低,也出现了先上升后下降的趋势,当温度达到阈值时,随着温度的降低,可溶性糖的含量也随之降低,其原因可能是过低的温度需要消耗大量的可溶性糖或者是已经对植物的细胞造成了损害,植物体内已经不能产生足够的可溶性糖来抵御低温寒冷。与杜玉娉、左宝峰(雪松)、王连翠、田娟等人的研究结果一致[22-27]。
在人工低温处理的条件下,2个品种菲油果叶片中的丙二醛(MDA)含量大体上呈先上升后下降再上升的趋势,但是2个品种菲油果叶片中的丙二醛(MDA)含量所上升的幅度有所不同,是由于2个品种菲油果对温度的敏感程度不一样,进而导致膜质过氧化的程度不同。期间2个品种中菲油果叶片中的丙二醛(MDA)含量有所下降,是由于机体的自我调节和抵抗能力,出现了MDA含量降低;之后随着温度的降低,丙二醛(MDA)的含量一直上升,Coolidge上升的波动不大,其原因可能是体内一些应激蛋白的调节作用,使保护酶的活性趋于稳定或不再急剧下降,从而MDA含量也就不再持续增加而呈现波动状态,而Mammoth的丙二醛(MDA)含量一直上升,表明膜质过氧化作用的加强。
菲油果叶片中的游离脯氨酸(Pro)的含量变化大体上呈先上升后下降的趋势,其中Coolidge叶片中的游离脯氨酸(Pro)含量在期间也出现了略微下降的情况,之后便出现了大幅度的上升现象。其原因可能是随着温度的下降,由于氨基酸的合成受抑制和游离脯氨酸的合成对低温的响应机制不同而造成的。因此,游离脯氨酸(Pro)可以作为鉴定不同品种菲油果抗寒性的指标之一。与姜春秋、吴娜、宋丽华、宋永艳等人的研究结果一致[18-25]。
超氧化物歧化酶(SOD)活性的变化大体上呈先上升后下降的趋势,其原因可能是由于自身机体内达到了短暂的动态平衡状态,之后随着温度的继续降低,其活性也随之增强;之后2个品种菲油果叶片中超氧化物歧化酶(SOD)活性都有相对较大幅度的降低,是因为过低的温度最终打破了菲油果体内的代谢平衡,使其酶的活性下降,进而清除自由基的能力也随之减弱,与此同时,膜系统的功能和结构也都遭到了破坏。
菲油果品种叶片中过氧化物酶(POD)的活性均表现出先上升后下降的趋势,在低温胁迫的初期,过氧化物酶(POD)的活性变化不大,但是随着温度的降低,其活性也随之增强,Coolidge在-15℃时、Mammoth在-10℃时过氧化物酶(POD)的活性均达到最大值,之后随着低温胁迫温度的下降其活性便开始下降,原因是处于过低温度下,细胞的结构受了到严重伤害,其完整性也受到破坏,过氧化物酶(POD)清除活性氧自由基的能力下降,导致有毒物质含量的大量积累,膜系统结构和功能受到损伤。因此,可知Coolidge 的抗寒性要强于Mammoth的抗寒性。
人工低温处理不仅可以自由地控制试验的条件,还可以排除自然温度变化的复杂性,重要的是人工低温处理可以作为模拟温度骤降的适生环境,并且是一个对自然低温温度的补充[28],用来反映植物受到不同程度的低温胁迫时生理状态的反应。这样的实验设计可以充分地弥补自然越冬过程中温度降低的不足,可以更加深入地探索植物抵御低温寒冷的适应性和反应状况。
[1] 张连全.庭院绿化新秀——菲油果[J].园林,2005,(2):25.
[2] 和红云,田丽萍,薛 琳.植物抗寒性生理生化研究进展[J].天津农业科学,2007,13(2):10-13.
[3] 黄希莲.贵州市绿蓠植物耐热抗寒性研究[D].贵阳:贵州师范大学,2008:84-86.
[4] 司剑华,卢素锦.低温胁迫对5种柽柳抗寒性生理指标的影响[J].中南林业科技大学学报,2010,30(8):78-81.
[5] 张学明.桉树在低温胁迫下的膜脂过氧化作用和膜伤害[J].经济林研究,1994,12(增刊):12-14.
[6] 夏清柱,万 仁,刘惠民,等.人工低温胁迫下腰果叶片生理生化指标的变化[J].经济林研究,2012,30(2):28-32.
[7] 阚文清,邱运亮.人工低温桉树组培芽丛过氧化物酶同工酶酶谱的变化[J].经济林研究,1994,12(增刊):10-11.
[8] 杨立学,王海南,张 琳,等.低温层积过程中紫椴种子内源激素含量的变化[J].经济林研究,2012,30(2):15-18.
[9] 王 丹,刘仁道,任少雄.食用、观赏兼用果树新种类费约果引种的气候适应性分析[J].中国南方果树,2007,36(6):39-41.
[10] 韩玉洁,殷丽清,张于卉,等.费约果的引种栽培及应用[J].上海交通大学学报农业科学版,2009,28(6):631-634.
[11] 范仲先.可观可食致富树——菲油果[J].农业实用科技信息,2008,(10):50.
[12] 范仲先.可观可食树——菲油果[J].资源开发与市场,2008,24(5):393.
[13] 任少雄,王 丹,张 猛,等.世界各国费约果育种进展及主要栽培品种[J].中国南方果树,2008,37(5):30-32.
[14] 福井正夫.菲油果的生物学特性与栽培技术[C]//农业技术大系果树篇——特产果树,2009:42-50.
[15] 邓文韬,张日清,袁德义.植物生长调节剂对菲油果嫩枝扦插生根的影响[J].中南林业科技大学学报,2011,31(3):60-63.
[16] 曾艳玲,袁德义,范晓月,等.菲油果离体快繁再生无菌植株研究[J].经济林研究,2012,30(4):97-100.
[17] 李合生.植物生理生化实验原理和技术[M].北京:高等教育出版社,2000:134-260.
[18] 王富荣.植物抗寒性指标的种类及其应用[J].植物生理学通报, 1987,(3):49-55.
[19] 缴丽莉,路丙社,白志英,等. 四种园林树木抗寒性的比较分析[J]. 园艺学报,2006,33(32):667-670
[20] 陈 贵,胡文玉,谢甫绨,等.提取植物体内的MDA的溶剂及MDA作为衰老指标的探讨[J].植物生理学通讯,1991,27(1): 44-46.
[21] Hare P D, Cress W A, van Staden J. Dissecting the roles of osmolyte accumulation during stress[J].Plant Cell Environ.,1998, 21:535-553.
[22] 孙昌祖,刘家琪.低温胁迫对青杨叶片O-2、MDA、膜透性、叶水势及保护酶的影响[J].内蒙古林学院学院,1998,3(2):31-36.
[23] 车代弟,王军虹,刘慧民.丰花月季抗寒生理指标和抗寒性的关系[J].北方园艺,2000,(2):57.
[24] 詹福建,巫光宏,黄卓烈,等.马占相思树对低温冻害的抗性研究[J].林业科学,2003,39(1):56-61.
[25] 魏 娜,欧小平,董 丽.10种宿根花卉抗寒性研究初报[J].中国农学通报,2008,24(7):314-317.
[26] 田 娟.20个紫薇品种抗寒性比较研究[D].北京:北京林业大学, 2009.
[27] 吴 娜.卫矛科三种常绿阔叶植物抗寒性研究[D].保定:河北农业大学,2006.
[28] 刘 冰.花椒抗寒性研究[D].兰州:甘肃农业大学,2005:89-90.
Study on physiological indexes of Feijoa sellowiana in artificial low temperature stress environment
TANG Li, ZHANG Yu, YUAN De-yi
(Central South University of Forestry & Technology, Changsha 410004, Hunan, China)
∶ In order to study the cold resistance characteristics of Feijoa sellowiana, the mature leaves of two F. sellowiana species(introduced Coolidge and Mammoth in artificial low temperature stress environment) were selected as the test materials, the physiological indexes such as electrical conductivity, soluble sugar and free proline (Pro), superoxide dismutase (SOD), peroxidase(POD) and malondialdehyde (MDA) were investigated. The results show that in a certain temperature range, the electrical conductivities,the content of soluble sugar and free proline (Pro) of different species of F. sellowiana increased with decreasing temperatures; In the process of artificial over-wintering, the free proline (Pro) of different kinds of F. sellowiana showed regular changes, the activity of protective enzymes (SOD, POD) inside the cells were enhancing with reducing temperatures. The variance analysis results show that the variance differences of relative conductivity, malondialdehyde (MDA), free proline (Pro), peroxidase (POD) between different species reached significant levels, and the electrical conductivity, soluble sugar, malondialdehyde (MDA), free proline (Pro), peroxidase (POD)and superoxide dismutase (SOD) indexes reached extremely significant level between different temperatures. There was no significant difference between the superoxide dismutase (SOD) in different species.
∶ Feijoa sellowiana; artificial low-temperature stress; physiological indexes; cold resistance
S722.7
A
1673-923X(2013)11-0008-06
2013-04-25
“948”引进国际先进林业科学技术项目“菲油果品种及栽培新技术引进”(2008-4-06)
唐 丽(1966-),女,湖南祁阳人,教授,博士,主要从事森林培育及观赏园艺的教学与科研工作;E-mail:lily0286rose@163.com
[本文编校:谢荣秀]
