铝电解电容器用铝箔发孔腐蚀工艺的研究
2012-12-28杜海燕梁晓鹏柴敏平
杜海燕, 梁晓鹏, 徐 晶, 柴敏平, 邓 顺
(江西理工大学冶金与化学工程学院,江西 赣州 341000)
铝电解电容器用铝箔发孔腐蚀工艺的研究
杜海燕, 梁晓鹏, 徐 晶, 柴敏平, 邓 顺
(江西理工大学冶金与化学工程学院,江西 赣州 341000)
采用电化学方法,找到了阳极发孔腐蚀的影响因素.采用正交实验,研究了HCl+H2SO4体系中腐蚀液组成、腐蚀电流密度、腐蚀温度以及腐蚀时间对铝箔性能的影响.结果表明:当选取ψ(HCl∶H2SO4)为1∶3,电流密度为0.25 A/cm2,腐蚀温度为70℃,腐蚀时间为105 s时,可以获得较优比容的腐蚀箔,比容值为110.8 μf/cm2,为铝箔腐蚀的研究提供了一定的科学依据.
铝电解电容器;腐蚀箔;直流腐蚀工艺
近年来随着电子产业的迅速发展,电解电容器作为电子产品中不可或缺的元件被大量生产和广泛应用,而其中铝电解电容器以其电容量大,体积较小,重量较轻且价格较便宜而被大量使用于储存能量,音频耦合以及隔断直流等方面.同时,随着信息产业的不断发展,手机,显示器,主板的更新换代使得铝电解电容器的市场更加扩大化,尤其是通讯产品、计算机、家电等整机产品市场的急剧扩大,对电解电容器的需求也急剧上升,极大地加速了电极箔产业的发展,同时对电解电容器的小型化、片式化、高性能化的要求也越来越迫切,对电极箔的制造业也提出了更高的技术和质量要求,对腐蚀铝箔的性能、可靠性的要求也越来越高[1-4].
除光箔自身质量外,铝电解电容器用铝箔腐蚀工艺则是腐蚀箔能否获得高比容和高性能关键所在[5].为了获得令人满意的性能,腐蚀工艺总类繁多,但是一部分工艺对于环保要求很难保证.由于硫酸-盐酸体系对环境的污染小,目前行业内多用这一体系作阳极腐蚀[6].但是该体系尚有不足:除了工艺过程的不当而使得箔面质量不稳定;同时中高压铝箔的真实腐蚀系数较实用极限腐蚀系数还有很大的提升空间[7].于是,选择采用单因素实验和正交实验相结合的方法,研究了相关工艺参数,试图寻找最佳工艺条件.
1 实验材料与方法
1.1 实验材料
铝箔:实验选用国产110 μm厚,纯度为99.99%的电解电容器阳极用铝光箔.
主要试剂:NaOH,H3PO4,H2SO4,HCl.
1.2 实验方法
(1)将平整的光箔剪裁成2×2 cm2样片,在30℃、0.1 mol/L的NaOH水溶液中预处理30 s.经过预处理的光箔在去离子水中清洗后,于去离子水中放置以备用.
(2)对预处理过的铝箔进行发孔腐蚀[8].在发孔过程中,铝箔作为阳极,为使铝箔发孔均匀,需采用经过处理的均匀孔状石墨板作为阴极,且铝箔和石墨板等距、平行.首先进行单因素实验:选择含有Cl-的酸作为腐蚀液(主要是盐酸和硫酸,辅以少量缓蚀剂和添加剂),两种酸的浓度、温度、时间、电流密度等随实验的不同而改变.然后在单因素实验基础上采用正交实验方法,研究影响阳极发孔腐蚀的工艺参数.
(3)将发孔后的腐蚀箔于1 mol/L的硝酸溶液中进行扩孔腐蚀,温度选择85℃,恒温10 min.
(4)将样片在去离子水中煮沸,维持3 min.目的是为了在铝箔表面形成一层高温水合氧化膜,起到预赋能的作用.
(5)将预赋能后的样片于低温浓磷酸中浸泡5 min,作形成化处理.
(6)将形成化处理后的铝箔裁剪成暴露面积为1 cm2的圆形,进行恒电流充放电测定比电容.
1.3 比容测定方法
恒电流充放电测试使用荷兰电化学工作站(IVIUMSTAT)进行测试,运用传统的三电极体系,其中参比电极为饱和甘汞电极,铂电极为辅助电极,工作电极暴露面积为1 cm2.采用计时电位法,测定基片在0.15 mol/L (NH4)2SO4溶液中的充放电曲线.充放电面积比电容的计算公式为:
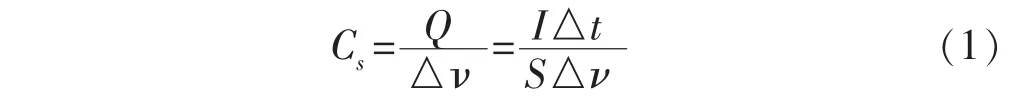
其中Cs为面积比电容,F/cm2;Q为充放电时的电荷量;I为充放电电流;△t为充、放电时间;S为材料的测试面积,cm2;△V为放电时间内的压降.
1.4 极化曲线测定方法
极化曲线的测量采用荷兰电化学工作站(IVIUMSTAT)进行测试,运用传统的三电极体系,其中参比电极为饱和甘汞电极,铂电极为辅助电极,工作电极(铝箔)暴露面积为1 cm2.先测量腐蚀体系的开路电位,在其基础上采用线性扫描法中的恒电流模式测量体系的极化曲线.
2 结果与分析
2.1 单因素实验分析
2.1.1 腐蚀液组分比例对腐蚀铝箔性能的影响
恒定电流密度为0.3 A/cm2,时间60 s、腐蚀温度65℃时,固定HCl的量为1 mol/L[9]、选取不同H2SO4的量得表1数据,由表1通过式(1)计算出比容值作图,如图1,添加量在3 mol/L时得到极大值.
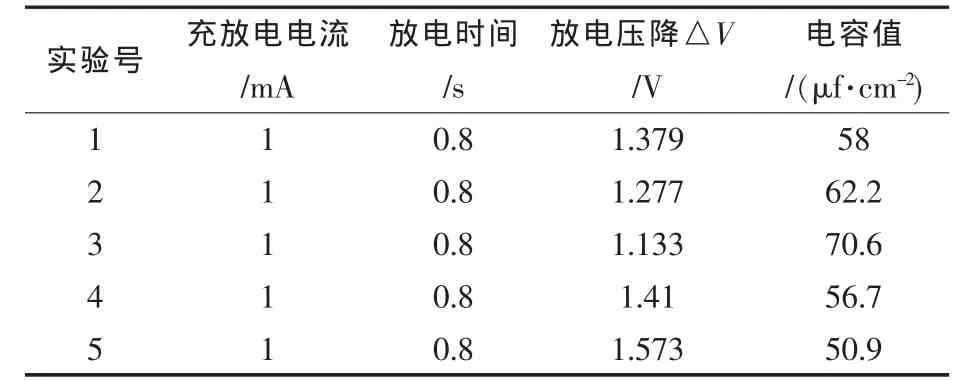
表1 腐蚀液组分实验数据表
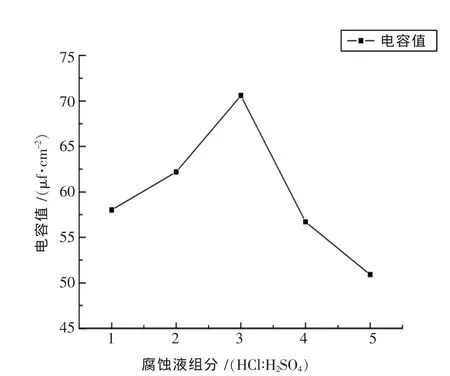
图1 腐蚀介质组成对腐蚀铝箔比容的影响
腐蚀液组分比例对腐蚀铝箔性能的影响结果见图1.由图1可以看出腐蚀液中硫酸的量增加的过程中,腐蚀箔的比容出现一个峰值,当继续加硫酸的量时,铝箔比容加速减小.这是因为在腐蚀过程中Cl-作为点蚀离子在铝箔表面点蚀成核后,若想要从蚀孔转化成隧道孔,不仅需要蚀孔内壁溶解面的变化,还需要蚀孔内部选择性钝化,在钝化过程中氧化性酸起到关键作用.当硫酸量提高时有利于内壁成膜,铝箔在不同腐蚀介质组成中的tafel曲线如图2所示,所以铝箔的比容相应的也会增大.
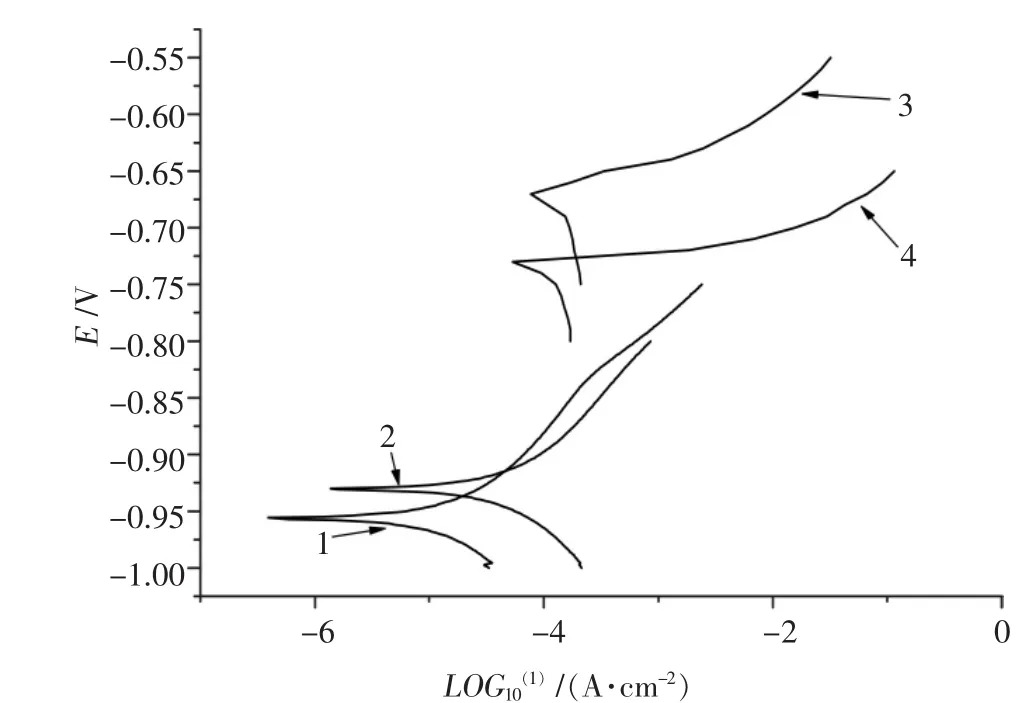
图2 铝箔在不同腐蚀介质组成中的tafel曲线
图2中曲线1、2、3、4分别对应着腐蚀液组成ψ(HCl∶H2SO4)为 1∶1、1∶2、1∶3、1∶4 时在测定开路电位的基础上测量到的tafel曲线图.从图4中可以看到:在H2SO4的量较少时,体系的自腐蚀电位较低,逐渐加入H2SO4后,体系自腐蚀电位升高.说明H2SO4在体系中起到了一定的缓蚀钝化作用.但是继续添加H2SO4时,自腐蚀电位又降低了,原因是不断添加H2SO4时,体系中H+的浓度不断增加,酸性增强,腐蚀加剧,氧化性酸形成的钝化膜被侵蚀不能再起到保护铝基体的作用,所以H2SO4的量要选择适当.因此在腐蚀液组成达到 ψ( HCl∶H2SO4)=1∶3 时,腐蚀箔会出现一个极值比容[10-11].
2.1.2 腐蚀电流密度对腐蚀铝箔比容的影响
在 70 ℃条件下,ψ(HCl∶H2SO4)为 1∶3、腐蚀时间为60 s时,选取不同腐蚀电流密度实验,得到数据,依照2.1.1的方法通过公式(1)计算出比容值作图,如图3所示,比容存在一个极值.
侵蚀电流密度可以影响铝箔蚀孔的尺寸,改变电流密度可以使铝箔获得不同的起始发孔密度和电容量.增大电流时比容提高,但电流过大时比容反而会下降.这是因为增加电流时,铝箔的电化学反应速度加快,使得铝箔初始蚀孔生长速率增大、发孔密度大.因此,腐蚀箔比表面积增加,表现为比容提高.当电流过大时,初始蚀孔中 Al3+浓度增加过快、容易达到饱和,使孔停止生长,而后续电流则用于继续发孔,使得铝箔表面出现并孔和坍塌现象,其电容反而下降[12].
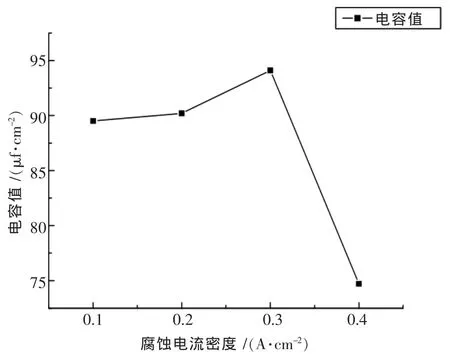
图3 腐蚀电流密度对腐蚀铝箔比容的影响
2.1.3 腐蚀温度对铝箔比容的影响
恒定电流密度为 0.2 A/cm2,Ψ(HCl∶H2SO4)为 1∶3、腐蚀时间为60 s时,选取不同腐蚀温度,计算所得数据作得图4,比容在温度为70℃左右同样存在一个极值.
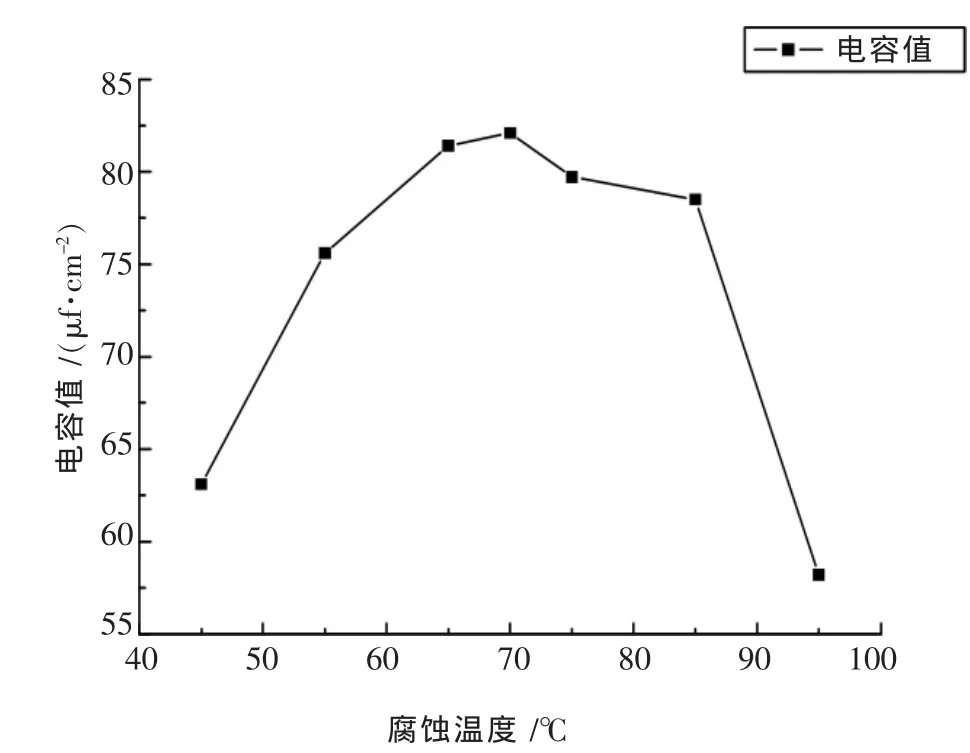
图4 腐蚀温度变化对腐蚀铝箔比容的影响
铝箔表面点蚀成核后,腐蚀主要在小孔内进行.当腐蚀温度较低时,铝箔表面氧化膜很薄,对基体的保护能力低,于是产生了孔径大且密度小的蚀坑,这样的腐蚀箔扩面面积有限,所以电容值较小;而当腐蚀温度较高时,铝箔产生的蚀孔孔径较小、密度较大,但是腐蚀进一步进行时,小孔可能会出现堵塞,孔壁之间出现坍塌、并孔(如图5),表现为铝箔电容增长缓慢或者不升反降(如图4)[13].
2.1.4 腐蚀时间对铝箔比容的影响
恒定电流密度为 0.2 A/cm2, ψ (HCl∶H2SO4)为1∶3、腐蚀温度60℃时,选取不同腐蚀时间得到图6,时间在105 s左右出现比容的极值.

图5 不同温度下的铝箔表面形貌
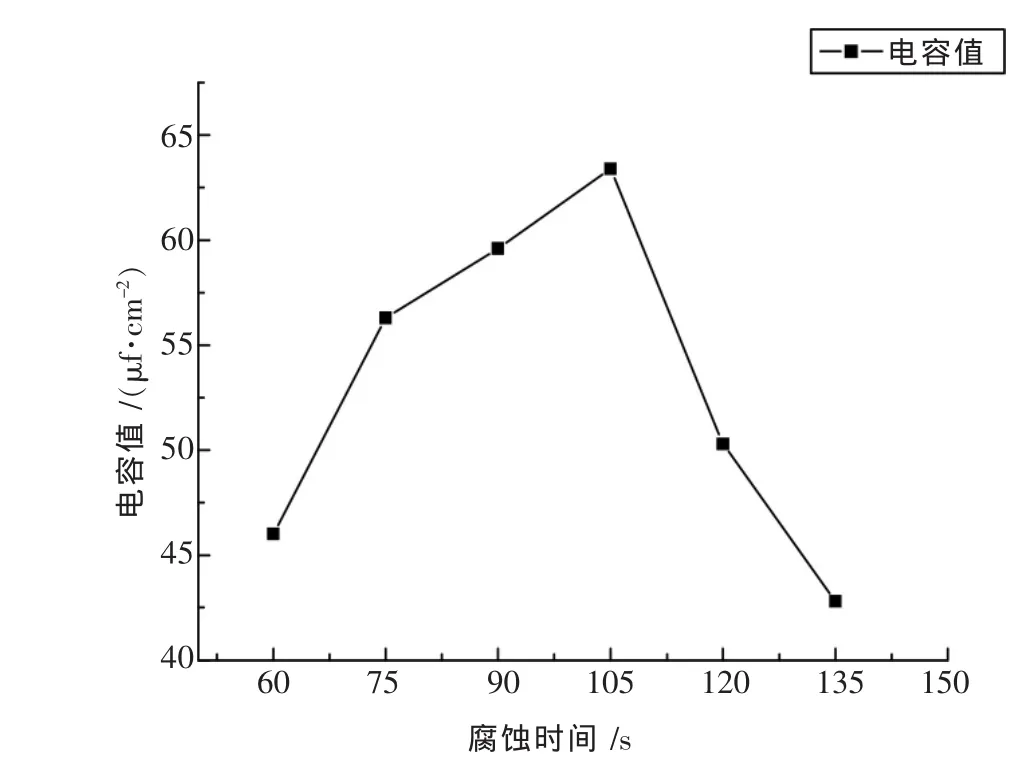
图6 腐蚀时间变化对腐蚀铝箔比容的影响
蚀孔在电化学腐蚀过程中并不是随机的,而是择优引发.一般首先引发的是表面有缺陷或者杂质富集区.随着腐蚀时间的增加,铝箔表面的氧化膜逐渐被溶解,腐蚀区域渐渐增大至整个表面,铝箔比表面积相应增大,所以比容值也相应变大.但是,继续延长腐蚀时间,铝箔表面的腐蚀量越来越大,直观现象表现为铝箔周边断裂、铝箔变薄、穿孔直至完全溶解,电容方面表现为电容值突然下降.
2.2 铝箔发孔腐蚀的正交试验
2.2.1 发孔腐蚀的正交试验
在单因素实验的基础上,为了进一步得到较优工艺,选取适当因素条件进行了一组L9(34)的正交实验,正交试验表如表2.
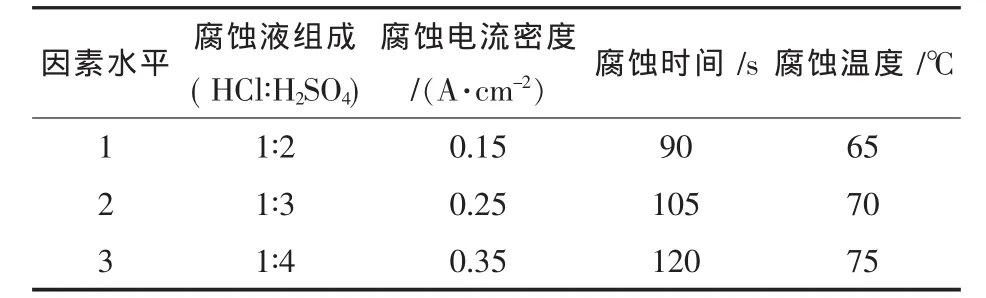
表2 腐蚀工艺正交实验因素表
采用表2的正交腐蚀工艺作实验得到结果表3,表 3 中 K1,K2,K3为平均值.
铝单质及其合金具有极强的自钝化性质.同时,在含有卤素离子的酸性溶液中(如Cl-、F-)可以发生小孔腐蚀.小孔腐蚀包括两个过程:①小孔的发生,Cl-吸附在铝表面尤其是氧化膜缺陷处,通阳极电流时电位变正,Cl-的吸附增强,当电位超过击破电位,膜的薄弱处被击破,表面上有小孔形成;②小孔的生长,孔壁处在钝化状态,小孔前沿处活性溶解状态,直到孔中Al3+浓度达到饱和,小孔停止生长[14].表2实验是通过对各因素水平的改变影响上述两个过程,从而达到优化铝箔腐蚀工艺的效果.
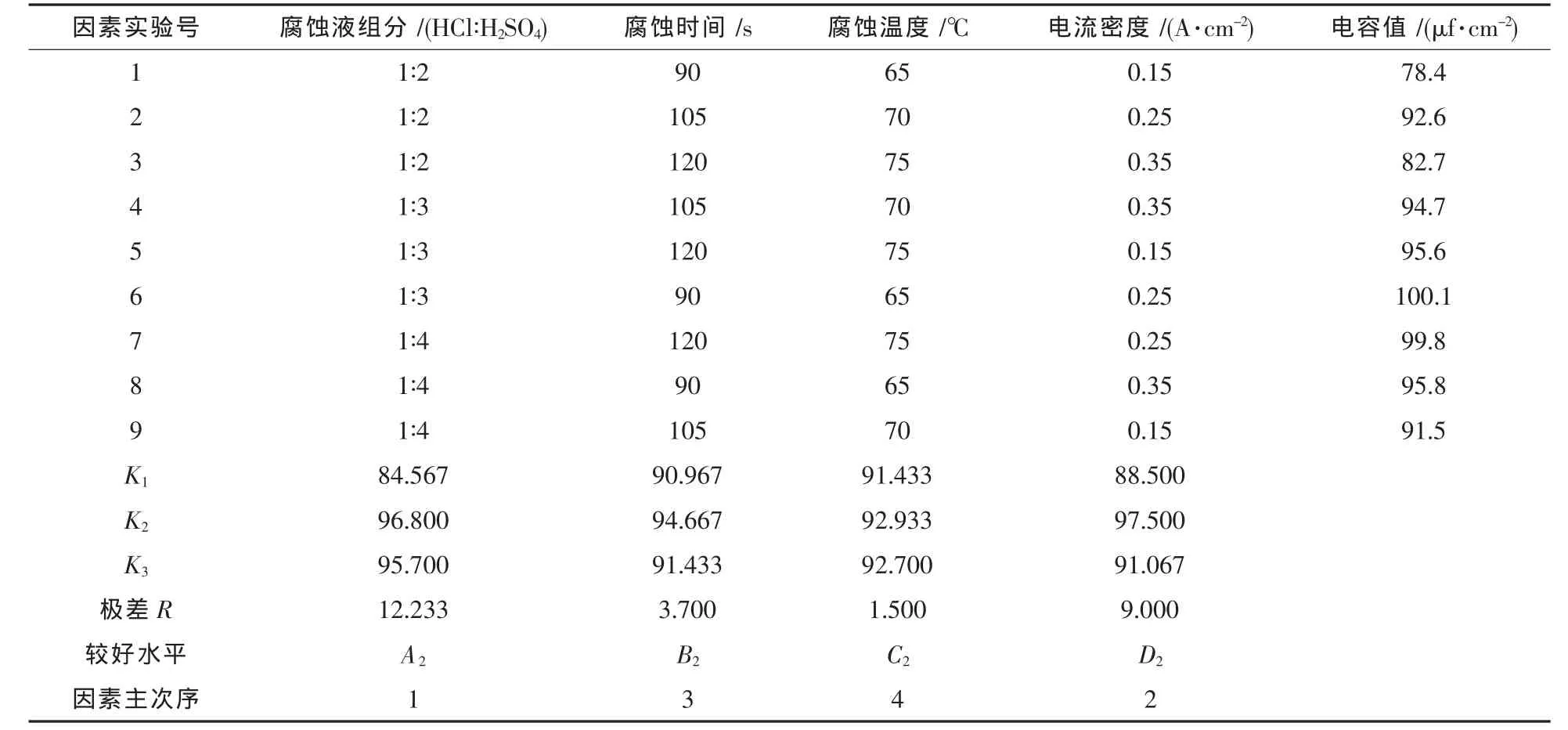
表3 腐蚀工艺实验结果
从表3正交实验数据中,可以看出各因素对铝箔腐蚀的效果不尽相同.腐蚀液组成和腐蚀电流密度对铝箔腐蚀影响较温度和时间大.
根据表3,我们可以得到较优工艺A2B2C2D2,即当腐蚀液组分为1∶3、腐蚀电流密度为0.25 A/cm2、温度为70℃、腐蚀时间为105 s时,可以达到较优实验效果.
2.2.2 较优工艺的重复性实验
为了确定该实验方案的效果,采用恒定电流密度为 0.2 A/cm2、ψ(HCl∶H2SO4)为 1∶3、腐蚀温度 70 ℃、腐蚀时间为105 s,作了5次重复性实验,得到结果如表4所示.

表4 重复性实验结果
按照以上重复性实验所得电容值的平均值,即C=(109.7+113.7+116.2+106.8+107.6)/5=110.8 μf/cm2RSD=3.64%,符合重复性实验要求.
3 结 论
(1)本实验采用单因素实验法和正交实验法,通过对铝电解电容器用阳极铝箔在HCl+H2SO4体系中发孔腐蚀的研究,得到一组较优工艺参数,即当腐蚀液组分为 1∶3、腐蚀电流密度为 0.25 A/cm2、温度为70℃、腐蚀时间为105 s时,可以达到较优实验效果.
(2)通过该工艺参数进行重复性实验得到比容值为 110.8 μf/cm2.
(3)采用电化学方法,测量得到不同组分条件下的极化曲线,科学的解释了HCl+H2SO4体系中H2SO4作为缓蚀剂时须选择一个适当的量.
(4)实验只对铝电解电容器用铝箔发孔腐蚀工艺进行了初步的研究,有关铝箔扩孔、化成等方面的研究有待进一步深入探索.
[1]毛卫民,何业东.国产电解电容器用铝箔的发展与展望[J].世界有色金属,2005(8):23-27.
[2]徐友龙.铝电解电容器技术的新进展[J].电子元件与材料,2008,27(9):5-7.
[3]梁霞妹,铁绍龙.高比容铝电解电容器关键技术进展[J].科技导报,2008, 26(7):78-83.
[4]阎康平,罗泸蓉,涂铭旌.中高压阳极铝箔直流电扩面侵蚀研究[J].四川大学学报:工程科学版,2000,27(2):32-35.
[5]王 跃,翁德明,黄新民.电解电容器用铝箔腐蚀工艺研究[J].电子元件与材料,2008,27(8):39-42.
[6]郭 敏,王兰东.几种电子铝箔腐蚀技术的简介[J].新疆有色金属,2000(1):35-36.
[7]班朝磊,何业东.中高压电子铝箔腐蚀系数的研究[J].电子元件与材料,2007,26(8):28-30.
[8]杨邦朝,肖占文.预处理对铝箔电蚀特性的影响[J].电子元件与材料,1997,16(3):1-9.
[9]Vetter H J,Strenhblow H H.Conference on localized corrosion houston[J].National Association of Corrosion Engineers,1974,40(7):107-113.
[10]McCafferty E.Sequence of steps in the pitting of aluminum by chlorideions[J].Corrosion Science,2003,45(8):1421-1438.
[11]McCafferty E.A surface charge model of corrosion pit initiation and of protection by surface alloying[J].Journal of the Electrochemical Society,1999,146(8):2863-2869.
[12]Alwitt R S,Uchi H,Beck T R,et al.Electrochemical tunnel etching of aluminum[J].J Electrochem Soc,1984,131(1):13-17.
[13]王 刚,闫康平,严季新.硫酸/盐酸比例和Al3+含量对铝箔隧道孔生长的影响[J].电子元件与材料,2003,22(10):10-12.
[14]沈行素,单义斌.铝电解电容器铝箔腐蚀工艺的进展及有关的电化学问题[J].电子元件与材料,1993,12(2):10-17.
On the etching process of aluminum foil for high-voltage electrolytic capacitors
DU Hai-yan,LIANG Xiao-peng,XU Jing,CHAI Min-ping,DENG Shun
(School of Metallurgical and Chemical Engineering,Jiangxi University of Science and Technology,Ganzhou 341000,China)
Electrochemical method and orthogonal design were used to study influencing factors of surface anode corrosion foil.Corresponding factors were investigated such as concentration of etching solution,current density,temperature,and corrosion time which affect on performance of aluminum foil in the system of sulfuric acid and hydrochloric acid.The optimal corrosion conditions were chosen through orthogonal test that corrosion temperature is 70 ℃,Ψ (HCl∶H2SO4)=1∶3,current density is 0.25 A/cm2,and corrosion time is 105 sec,et al.The results show that:corrosion foil of high specific volume can be got and specific electric-capacity is as high as 110.8 μf·cm-2.This study can provide scientific basis for the follow-up corrosion research of aluminum foil.
aluminum electrolytic capacitor;corrosion foil;DC corrosion process
TM535
A
1674-9669(2012)01-0027-05
2011-11-12
东莞通旺达五金制品有限公司科技项目
杜海燕(1963- ),女,教授,主要从事石油管材的腐蚀与防护及工业电化学方向研究,E-mail:dhyboy@163.com.
