以钛精粉为载体由CO歧化反应制备纳米碳管
2012-12-23司新国鲁雄刚危雪梅
司新国,鲁雄刚,肖 玮,危雪梅
(1.上海大学材料学院,上海市现代冶金与材料制备重点实验室,上海200072; 2.河北钢铁集团唐钢公司,河北唐山063020)
以钛精粉为载体由CO歧化反应制备纳米碳管
司新国1,2,鲁雄刚1,肖 玮1,危雪梅1
(1.上海大学材料学院,上海市现代冶金与材料制备重点实验室,上海200072; 2.河北钢铁集团唐钢公司,河北唐山063020)
以攀枝花钛精粉为载体,使用大载荷热重分析仪,在H2和CO混合气中,研究了纳米碳管的制备工艺.利用热重分析(TG)、气相色谱分析(GC)、扫描电镜(SEM)、比表面积(BET)、透射电镜(TEM)和X射线衍射(XRD)对工艺过程中产物相组成及其微观形貌进行了表征.结果表明:攀枝花钛精粉在H2-CO气氛中,由于气基还原和析碳作用,其热重曲线首先随时间的延长而逐渐降低,达最低点后逐渐升高;生成纳米碳管的最佳工艺参数是钛精粉首先经过还原制备还原产物,其相主要由Fe和M3O5固溶体组成;随后在体积浓度80%的一氧化碳气氛中逐渐降温,温度达550℃时恒温2 h;制备的纳米碳管量约是原矿粉质量的3.5倍,直径小于100 nm、比表面积约151 m2/g;纳米碳管的产生是以铁为析碳基体,且还原产物中其他矿相有效阻止了铁颗粒的团聚,其生长是吸附-反应-产物扩散的过程.
钛精粉;碳纳米管;生长机理;歧化反应
1991年,日本NEC公司Iijima S教授使用高分辨透射电镜在电弧蒸发石墨的阴极沉淀物中发现了纳米碳管[1],其结构是由类石墨平面卷曲而成的纳米级中空管,其中每个碳原子在sp2轨道杂化后,与周围3个碳原子完全键合,其直径在几十个纳米之内,轴向长度可达几十微米甚至更长,被认为是目前世界上“最小的试管”材料[2-3].由于此特殊结构,纳米碳管具有优异的导电、导热性能和机械强度,展现出广泛的应用潜力,成为物理学、材料学等领域的研究热点之一[4-7].目前合成纳米碳管的主要方法有电弧法、固相热分解法、激光法和化学气相沉积法.其中化学气相沉积法制备方法简单,条件易于控制,可大规模生产,同时产物杂质含量少,引起了研究者的重视,成为制备纳米碳管的主要方法[8-11].
在化学气相沉积法中,通常以单金属或双金属的活性组分为载体,以碳氢化合物气体或者CO为碳源制备纳米碳管[12].其中CO歧化反应的研究早于纳米碳管的发现,研究表明高温抑制CO的歧化反应[13];气态水的存在能提高CO的转化率[14-15].因此可考虑利用部分氢气还原氧化物制备CO歧化反应载体的方式实现纳米碳管的制备.
我国钛资源丰富,资料显示[16-17],以二氧化钛的储量计,约 24.84亿吨,占世界总量的38.85%,居首位,主要以钛铁矿相形式赋存于钛精粉中[18].目前,绝大多数资源被作为生产富钛料或者高钛渣的原料,其生产工艺特点是污染大、能耗高、效率低[19].
结合以上两点,本文以攀钢集团攀枝花钢铁研究院提供的钛精粉为载体,在氢气和一氧化碳混合气条件下,由CO的歧化反应成功制备了纳米碳管.该方法具有工艺简单、产量大、成本低等优点,制备出的纳米碳管具有良好的性能.
1 试验
1.1 原料及气体规格
试验用载体钛精粉由攀钢钢铁研究院提供,其化学成分见表1.试验过程中气体规格见表2,其中氢气和一氧化碳是反应气,氩气是保护气.

表1 钛精粉化学成分(质量分数/%)

表2 试验所用气体规格
1.2 试验设备与研究方法
实验主体设备是美国产大载荷热重分析仪,型号Cahn Thermax700.反应器为圆柱形坩埚,内径15 mm,高25 mm.
首先将钛精粉置于热重分析仪的反应器中,并通入Ar;然后按照试验方案配入反应气,并运行温度程序,升温速度 10℃/min,降温速度5℃/min;最后降至室温,切换为氩气,取样并分析其矿相和微观结构.试验过程中采用色谱分析仪对尾气成分进行定量检测.
1.3 表征方法
1)X射线衍射:将实验样品球磨至100 nm,采用CuKα射线,电压和电流40 kV×200 mA,以8℃/min的扫描速度,在10°~90°测试样品的矿相组成.
2)扫描电镜:在工作电压为15 kV,分辨率2.2 nm的条件下,观察实验样品的表面形貌、孔结构及其元素分布现象.
3)透射电镜:通过场发射透射电镜(工作电压150 kV)观察制备纳米材料的微观结构.
4)气体成分:使用GC9160气相色谱检测尾气中的氢气、一氧化碳、二氧化碳等气体含量,在实验过程中取样和分析时间间隔是15 min.
2 结果与讨论
2.1 气体体积浓度对TG曲线的影响
图1(a)是不同体积浓度配比,即一氧化碳体积浓度步长值10%,钛精粉还原过程中质量随反应时间和温度的变化.
由图1(a)可知TG曲线具有相似的特点,首先钛精粉发生还原反应,由于失氧而质量逐渐降低,且失质量随CO体积浓度的增加而减小;当达最低点后,曲线变化相反,即随时间的延长质量逐渐增加,这主要是一氧化碳发生歧化反应产生碳沉积的原因.
图1(a)表明最终产物质量变化与CO体积浓度有关,首先随其体积浓度的增加而增加,当体积浓度是80%时,质量达最大,而后逐渐减小.对CO体积浓度为80%条件下的热重曲线进行微分处理,得质量变化率随温度的变化曲线,即图1 (b),可知在增重过程中,温度降至500~600℃,其速率达最大变化区域,即3.8 mg/min左右.因此从增质量上考虑,气体体积浓度80%CO,恒温温度500~600℃较合理.为确定其他参数,温度取一中间固定值,即550℃.

图1 不同气体组成下钛精粉的TG分析
2.2 恒温时间的影响
为了考察550℃、CO体积浓度80%条件下的增重变化,设计试验,降温至550℃,恒温6 h,其TG曲线如图2所示.由图2可知恒温2 h,增重达最大值,增重约450%,即质量约是原钛精粉的3.5倍,继续延长反应时间其质量不变,因此合理的恒温时间是2 h.
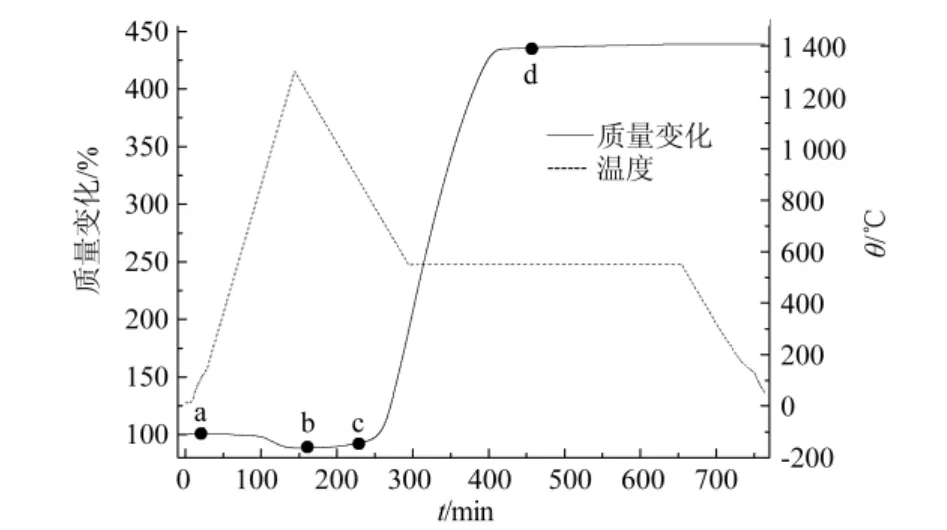
图2 恒温时间对TG曲线的影响
2.3 反应过程中相变化
为了研究反应过程中的物相转变,在图2中a、b、c、d处进行取样分析,结果如图3所示.图3表明钛精粉原料主要由Fe2O3和FeTiO3组成;随温度升高,两相开始发生还原反应,在质量最低处,即 b处,还原结束,还原产物主要由 Fe和M3O5固溶体组成(图3曲线b),结合失质量和钛精粉原料化学成分,产物中Ti部分仍以+4形式存在;在降温过程中,质量增加比较缓慢的部分,即c处,由于一氧化碳的作用,产物中有渗碳体相产生,其他相不变;最后在恒温段(d处),在产物上层取样,结果表明该物质是单质碳,无其他物质,因此可知热重曲线升高主要是由碳沉积引起.

图3 还原过程中XRD分析结果
2.4 化学成分对析碳的影响
为了说明上述试验的析碳机理,在图2试验条件下,考察了还原过程中所有矿相的影响,试验结果如图4所示.其中高钛渣是b点处样品(图2)采用湿法去除了金属Fe的产物.由图4可知:TiO2和去除金属铁的矿相在CO体积浓度80%的试验条件下,不会产生增重现象,即未生成单质碳;金属铁相和含铁的TiO2相,出现增重现象,可知碳的析出是因为有单质铁的存在;试验过程中发现,当采用纯金属铁粉时,除生成少量的碳外,铁粉发生团聚现象,而在含有铁的TiO2中,铁粉未团聚,且碳量显著较高.因此保持金属铁的弥散,利于单质碳的生成.

图4 不同物质的析碳TG曲线
2.5 微观结构分析
对图2中a、b、c处的试验样品进行微观形貌和能谱分析,如图5(d)、(e)和表3所示.图5和能谱分析表明,金属铁颗粒不规则地分散在还原产物表面,未发生团聚现象;在不存在金属铁的位置处开始阶段未发现单质碳,进一步证明铁是析碳的基体;随着时间的延长,最后在还原产物周围生成大量的碳材料,析碳量明显高于图4的每一种情况,说明钛精粉还原产物可作为制备碳的原料;碳的扫描电镜照片(图5(d))和透射电镜照片(图5(e))表明碳单质直径大部分小于100 nm,且每一个细纤维均呈长度大于600 nm的管状,比表面积是151 m2/g,因此可以推断最终产物是纳米碳管.

图5 反应过程中微观结构的变化

表3 能谱分析结果
2.6 尾气成分检测
反应过程中尾气气相色谱检测结果见图6.可知尾气成分主要由CO、CO2、H2和微量CH4组成,在加上C及反应管冷却端的冷凝H2O,可断定主要反应物种数是5(CH4体积浓度近似于0,因此忽略),根据热力学计算,500~600℃时,能自发进行的反应式(1)~(4).

图6 尾气成分分析
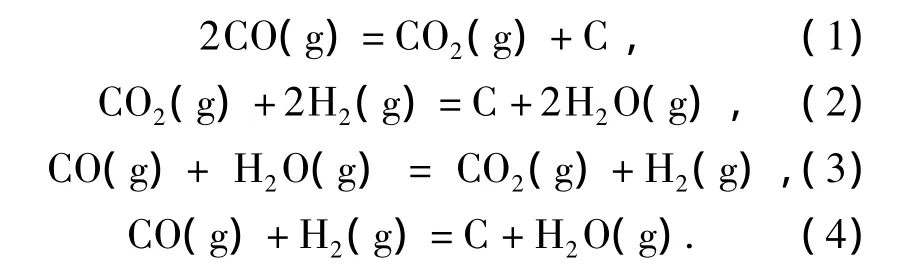
在图6中取纳米碳管生成过程中某一时刻的尾气体积浓度,结果是58%CO、18%CO2、19%H2以及少量忽略不计的CH4.其起始气体反应的气体积浓度是80%CO和20%H2.由图6可以看出:析碳过程中CO和CO2相互映衬,此消彼长,且式(1)~(4)中CO2的来源只能首先是由反应1提供,根据此式的平衡方程可以计算出尾气中CO体积浓度约59%,与检测结果相差1%;如H2未参与反应,则 H2体积浓度是23%,而结果是19%;且在反应器冷却段发现液态水,因此可以断定H2参与了还原过程.若仅存在反应2和反应4,H2体积浓度可以逐渐降低,但总气体量相应减小,CO2体积浓度会偏高;假设不成立,必然存在增加CO2含量的反应,即式(3).因此纳米碳管的生成过程是以CO歧化反应为主体、兼有部分H2参与的复杂过程.结合图1(a)中反应气体积浓度对纳米碳管生成量的影响,可以解释为氢气参与时利于气相扩散,促使CO的歧化反应,与Ghorbani等的研究结果一致[19];如H2含量过高,会降低体系中一氧化碳的体积浓度,对反应1不利,水吸附在固体还原产物表面,阻碍气相扩散,降低反应物体积浓度,因而氢气体积浓度也不宜过高,从具体的实验结果看,体积浓度20%比较合理.
2.7 纳米碳管的生长机理
结合前文分析可知,纳米碳管的生成,即析碳过程,是一个吸附-反应-扩散的过程,见图7,即反应气首先在气流的带动下向钛精粉还原产物层移动,并吸附在金属铁表面,以金属铁颗粒为基体发生气固相转变反应,随后产生的气体脱离产物层向外扩散,同时生成的碳颗粒逐渐沉积在纳米碳管的管壁或者管的前部,使其长粗或长大.但随着纳米碳管的逐渐增加,作为催化剂的金属铁颗粒与反应气被隔离开,因此该条件下纳米碳管的生长不是无限期长大过程,在产物足够多时,反应会自动终止,在本实验条件下,2 h为宜.

图7 纳米碳管的生长机理示意图
3 结论
1)钛精粉必须被还原为含单质铁的还原产物,且金属铁粒子与其他矿相彼此镶嵌,最后以还原产物为基体制备纳米碳管;
2)制备纳米碳管的最佳工艺参数是:气体配比为H2体积浓度20%和CO体积浓度80%,反应温度550℃、反应时间2 h,最终纳米碳管直径小于100 nm,比表面积约151 m2/g;
3)矿相和微观分析表明铁是纳米碳管的产生基体,还原产物中其他矿相能够有效阻碍铁颗粒的团聚,利于材料制备;纳米碳管的生长是吸附-反应-产物扩散的过程.
[1] IJIMA S.Helical microtubules of graphitic carbon[J].Nature,1991(354):56-58.
[2] 王茂章,李峰,杨全红,等.由不同碳源合成及制备纳米碳管的进展[J].新型炭材料,2003,18(4): 251-264.WANG Mao-zhang,LI Feng,YANG Quan-hong,et al.Advances in synthesizing and preparing carbon nanotubes from different carbon sources[J].New Carbon Materials,2003,18(4):251-264.
[3] 李峰,白朔,成会明.纳米碳管[J].新型炭材料,2000,15(3):79-80.LI Feng,BAI Su,CHENG Hui-ming.Carbon nanotubes[J].New Carbon Materials,2000,15(3):79-80.
[4] HENNING T H,SALAMA F.Carbon in the universe[J].Science,1998,282(12):2204-2210.
[5] 古玲,赵建国.化学气相沉积工艺制备绳状纳米碳管的研究[J].碳素技术,2011,30(2):6-8.GU Ling,ZHAO Jian-guo.Preparation of carbon nanotube ropes by chemical vapor deposition[J].Carbon Techniques,2011,30(2):6-8.
[6] CHEN W X,TU J P,WANG L Y,et al.Tribological application of carbon nanotubes in a metal-based composite coating and composites[J].Carbon,2003,41 (2):215-222.
[7] LI Z,YING Z,LIU M,et al.Preparation and tensile properties of MW/polypropylene composite fibers by melt spinning[J].New carbon materials,2005,20 (2):108-114.
[8] 应永飞,严新焕,王文静,等.CVD一步法制备纳米碳管的研究[J].材料科学与工程学报,2003,21 (2):233-235.YING Yong-fei,YAN Xin-huan,WANG Wen-jing,et al.One step synthesis for carbon nanotubes using CVD Method[J].Journal of Materials Science and Engineering,2003,21(2):233-235.
[9] CAO Z L,WANG J N,DING D Y,et al.Fast growth of well-aligned carbon nanotubes by chemical wapor deposition on plain glass[J].New carbon materials,2003,18(1):48-52.
[10] 刘畅,成会明.电弧放电法制备纳米碳管[J].新型炭材料,2001,16(1):67-71.LIU Chang,CHENG Hui-ming.Synthesis of carbon nanotubes by electric arcmethod[J].New Carbon Materials,2001,16(1):67-71.
[11] WOLFGANG K M,ANA M B,MARTINEZ M T.Production of carbon nanotubes:the light approach[J].Carbon,2002,40(10):1685-1695.
[12] 李克,聂聪,吕功煊,等.Ni-Sm-MgO催化热解CO制备碳纳米管[J].分子催化,2005,19(6): 419-424.LI Ke,SHE Cong,LÜ Gong-xuan,et al.Synthesis of carbon nanotubes by catalytic disproportionation of CO over a Ni-Sm-MgO catalyst[J].Durnal of Molecular Catatysis(China),2005,19(6):419-424.
[13] 李春义,余长春,沈师孔.CO在Ni/Al2O3催化剂上的歧化和氧化反应[J].催化学报,1998,19(5): 463-466.LI Chun-yi,YU Chang-chun,SHEN Shi-kong.Disproportionation and oxidation reactions of CO over Ni/ Al2O3[J].Chinese Journal of Catalysis,1998,19 (5):463-466.
[14] GHORBANI H,RASHIDI A M,RASTEGARI S,et al.Mass production of multi-wall carbon nanotubes by metal dusting process with high yield[J].Materials Research Bulletin,2011,46:716-721.
[15] LU S H,ZHANG C,LIU Y.Carbon nanotube supported Pt-Ni catalysts for preferential oxidation of CO in hydrogen-rich gases[J].International Journal of Hydrogen Energy,2011,36:1939-1948.
[16] 杨绍利,盛继孚.钛铁矿熔炼钛渣与生铁技术[M].北京:冶金工业出版社,2006.YANG Shao-li,SHENG Ji-fu.Technology of Titanium Slag and Pig Iron from Iimenite Smelting[M].Beijing,Metallurgical Industry Press,2006.
[17] ZHANG L,ZHANG L N,WANG M Y,et al.Precipitation selectivity of perovskite phase from Ti-bearing blast furnace slag under dynamic oxidation conditions[J].Journal of non-crystalline solids,2007,353(22/ 23):2214-2220.
[18] 吴贤,张健.中国的钛资源分布及特点[J].Ti工业进展,2006,23(6):8-12.WU Xian,ZHANG Jian.Geographical distribution and characteristics of titanium resources in china[J].Titanium industry progress,2006,23(6):8-12.
[19] 孙艳.高钙镁钛铁矿制取高品质富钛料新工艺研究[D].昆明:昆明理工大学,2006.SUN Yan.High rich titamium materials prepared from ilmenite with rich calcium and magnesium[D].Kunming:Kunming university of science and technology,2006.
Preparation of carbon nanotubes from ilmenite concentrate carrier by disproportionation of carbon monoxide
SI Xin-guo1,2,LU Xiong-gang1,XIAO Wei1,WEI Xue-mei1
(1.Shanghai Key Laboratory of Modern Metallurgy and Materials Processing,School of Materials Science and Engineering,Shanghai University,Shanghai 200072,China;2.Hebei Iron and Steel Group Tangshan Steel Company,Tangshan 063020,China)
A preparation technology of carbon nanotubes was studied in hydrogen and carbon monoxide by heavy loading thermogravimetric analysis,using Panzhihua ilmenite concentrate as catalysts.During the process,the phase composition and microstructures of the products were characterized by means of thermogravimetry,gas chromatographic analysis,scanning electron microscopy,specific surface area,transmission electron microscope and X-ray diffraction.The results indicated that the weight of ilmenite concentrate decreased firstly and then increased gradually with reaction time under H2-CO atmosphere owing to gas-basis reduction and deposition of carbon.The optimal process was that the reductive products with Fe and M3O5solid solution phase were prepared by reduction of titanium concentrate,and the temperature was decreased in 80%carbon monoxide gradually and kept 550℃ for 2 h.The carbon nanotubes,which were less 100 nm of diameter and 151 m2/g of specific surface,were about 3.5 times than the ilmenite concentrate.The iron was regarded as matrix material of producing of carbon nanotubes and its agglomeration was prevented by other mineral phase owing to mutual infiltration.Growth of carbon nanotubes were controlled by adsorption,reaction and diffusion during the process.
titanium concentrate;carbon nanotubes;growth mechanism;disproportionation
TE09 文献标志码:A 文章编号:1005-0299(2012)06-0018-05
2011-11-09.
国家自然科学基金资助项目(51074105,51225401);上海大学研究生创新基金资助项目(A.16-0110-09-704).
司新国(1980-),男,博士研究生;
鲁雄刚(1969-),男,教授,博士生导师.
鲁雄刚,E-mail:luxg@shu.edu.cn.
(编辑 程利冬)
