MRI对门静脉海绵样变性的诊断价值
2012-12-08NIULei
牛 磊 NIU Lei
朱蒙蒙1 ZHU Mengmeng
王明皓1 WANG Minghao
崔 文1 CUI Wen
刘圆圆1 LIU Yuanyuan
朱 斌2 ZHU Bin
2.南京大学医学院附属鼓楼医院 江苏南京 210008
门静脉海绵样变性(cavernous transformation of portal vein, CTPV)的诊断多依靠彩色多普勒超声、CT、数字减影血管造影(DSA)等方法。近年随着MRI技术的快速发展,MRI能清晰显示CTPV的病变,越来越受到临床关注。本文回顾性分析宿迁市人民医院29例CTPV患者的资料,并结合CTPV的病因及发病机制,探讨CTPV的MRI表现特征,评价MRI对CTPV的诊断价值及临床意义,旨在提高对该病的认识。
1 资料与方法
1.1 一般资料 2004-01~2010-12宿迁市人民医院临床诊断为CTPV的29例患者,其中男性20例,女性9例;年龄33~72岁,平均46岁。CTPV同时伴有原发性肝癌伴门静脉癌栓形成19例,肝硬化门脉高压5例,脾切除术后4例,Budd-Chiari综合征1例。所有病例均经手术病理或DSA证实。
1.2 仪器与方法 使用德国西门子公司Magnetom Avanto Tim(76×18)1.5T超导磁共振系统。采用体部表面线圈。受检者仰卧于检查床上,训练呼吸后进行上腹部MRI平扫,接着进行增强扫描。常规平扫序列,T1WI轴位、T2WI轴位、T2WI脂肪抑制序列,半傅立叶单次激发快速序列(half-fourier single-shot fast sequence, HASTE)冠状位,真实稳态进动快速成像(true fast imaging with steady state precession,True-Fisp)冠状位,层厚6mm,层间距1.2mm。增强扫描采用西门子VIBE,T1WI压脂序列,层厚3mm,层间距0.8mm,视野(FOV)380mm,TR 4.89mm,TE 2.38mm。对比剂为钆喷替酸葡甲胺(Gd-DTPA),用量0.1mmol/kg,使用高压注射器注射,分别行动脉期、静脉期、延迟期三期扫描。
2 结果
2.1 门静脉栓塞的部位 29例CTPV中门静脉主干CTPV 15例,门静脉主干及左右分支均受累8例,单纯左右分支受累6例。
2.2 门静脉系统栓塞的表现 本组全部病例均见门静脉主干及其分支闭塞和(或)狭窄,正常门静脉结构消失,门静脉结构走行区结构紊乱。门静脉主干和(或)其分支因栓子闭塞和(或)狭窄20例,其中癌栓17例,T1WI均呈等低信号,T2WI呈等高信号,增强扫描示不同程度的强化;血栓7例,T1WI呈高信号,T2WI呈高信号,增强扫描示无强化。门静脉受侵闭塞和(或)狭窄5例(图1~10)。
2.3 门静脉侧支循环异常强化 平扫示门静脉走行区可见侧支循环静脉形成的团块样或网状软组织密度影,肝门部正常结构模糊紊乱(图1~5)。增强扫描示门静脉及延迟期上述软组织影明显强化,为扩张迂曲的类海绵状血管结构(图9、10)。局部包绕胆总管,呈现所谓“假胆管癌征”。
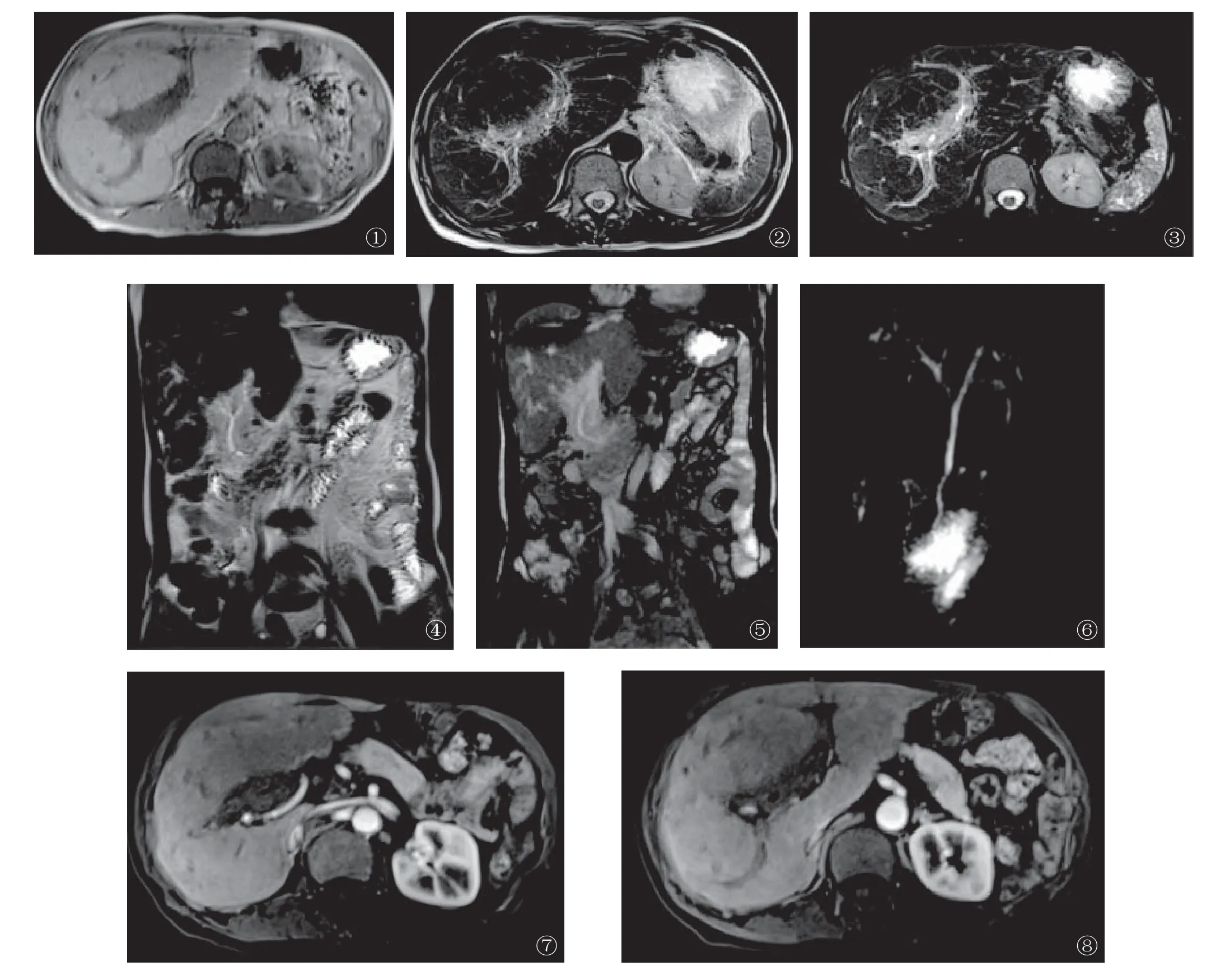
图1~10 患者女性,50岁,脾切除术后3年。图1 平扫T1WI门脉主干及分支增粗、迂曲,肝形态改变,肝左外叶萎缩,尾状叶及左内叶增生。图2、3 分别为T2WI、FS轴位,正常门静脉的流空影消失,其周包绕类海绵状血管影。图4、5 分别为T2WI、True-Fisp冠状位,肝门处结构紊乱,见团块状软组织信号灶,正常门静脉结构消失,胆总管被包绕,呈现“假胆管癌征”。图6 磁共振胰胆管成像(magnetic resonance cholanggiopancreatography,MRCP),胆总管狭窄,肝内外胆管无扩张。图7、8 肝动脉期扫描,肝边缘可见一过性条状、片状异常强化,可见与门静脉伴行的肝动脉分支增粗

图9、10 肝静脉期与延迟期扫描,平扫肝门处所见团块状软组织、门静脉走行区呈明显异常强化,类似海绵状,正常门静脉管腔影消失,肝实质强化趋于一致
2.4 肝实质一过性灌注异常 本组18例(62%)显示肝一过性灌注异常。其表现为肝动脉期肝周边或局部见均匀带状、小片状异常强化影,肝门区强化不明显(图7、8)。有时可见局部肝动脉血流增多,血管增粗、扭曲。门静脉期周边肝实质趋于均匀强化(图9)。
2.5 肝形态改变 肝左外叶萎缩,尾状叶及左内叶增生,可见明显的萎缩-增生复合体(atrophy-hypertrophy complex,AHC),本组3例。26例有不同程度的肝硬化表现,肝外形不规整,呈浅波浪状。
2.6 肝原发性病变MRI表现 原发性肝癌伴门静脉癌栓形成19例,三期扫描呈快进快出强化特征,病灶与肝内门脉分支分界不清,肝硬化门静脉高压表现5例,脾切除术后4例,Budd-Chiari综合征1例表现为下腔静脉肝段闭塞。
3 讨论
3.1 CTPV的概念及病因 CTPV是因门静脉主干和(或)其分支狭窄或阻塞,致使门静脉压力增高,门静脉周围侧支循环代偿,以及受阻门静脉再通所致的病变。由于门静脉周围代偿增生的血管在病理标本上呈类海绵状血管瘤样表现,所以命名为门静脉海绵样变性[1],是机体为保证肝血流量和肝功能正常的一种代偿性病变。
CTPV分为原发性和继发性,儿童CTPV多为原发性,指门脉结构先天性发育异常,门静脉管腔结构狭窄或闭塞。成人CTPV多为继发性,门脉系统由于各种致病因素导致门静脉血流受阻,血流量及血流状态改变,最终导致门静脉周围侧支循环代偿增生、门静脉再通。致病因素多为门静脉癌栓、血栓、感染、脾切除术(本组4例)等。
3.2 CTPV的发病机制及病理过程 门静脉主干及分支完全或部分栓塞后,门脉供血减少,为了代偿肝的供血,肝动脉增粗,门静脉周围侧支循环建立,这种代偿一般发生在肝的边缘,肝的边缘区一般为海绵样变性的门静脉侧支供血,这样门脉系统远部压力下降,可以回到正常压力,使肝的血液重新分布,改善肝营养供应,可以保持肝的正常功能及其代谢[2]。
3.3 CTPV的MRI表现 MRI平扫时可见门静脉闭塞,闭塞门静脉周围可见由侧支静脉形成的团块状、网状异常软组织信号影。闭塞或阻塞的门静脉走行区可见类海绵状的侧支代偿增生血管影,内部血流方向不一致[3]。MRI门静脉期及延迟扫描,其强化程度与相连血管一致。
CTPV还可以出现肝动脉分支代偿增粗、动脉期异常灌注、肝形态的变化[4]以及“假胆管癌征”[5]等征象:①肝左、右动脉分支增粗表明肝动脉供血增加。②动脉期肝一过性灌注为特征性表现,动脉期一过性片状异常强化,门静脉期迅速消失。③Schweizer等[6]的研究进一步说明门静脉血供异常对肝的形态有重要影响,虽然肝动脉可以代偿增粗供血,但是其营养因子较门静脉含量低,仍然改变不了CTPV对肝形态的改变。肝尾状叶及左内叶距离门静脉较近,所以其血供得以维持。④出现“假胆管癌征”应考虑CTPV的存在及压迫胆系的可能。“假胆管癌征”是指在经内镜逆行胰胆管造影(endoscopic retrograde cholangiopancreatography,ERCP)时可见胆管不规则状、结节状的外压性改变,脾形态增大。
3.4 MRI对CTPV的诊断价值与其他方法比较 血管造影、CT、彩色多普勒超声及MRI等对CTPV的诊断价值各不相同。血管造影是诊断CTPV的“金标准”,但其为有创性检查,有一定的风险,应用受到一定的限制。目前多层螺旋CT(MSCT)在CTPV的诊断方面应用较多,但因其X线的辐射及软组织的分辨率较低而使其应用受到限制。超声是诊断CTPV的常用检查方法,既安全又可靠,但是它仍然受一些因素(如患者体型肥胖、肠道气体干扰、操作者的经验等)的制约。
随着MRI技术的发展,在腹部血管病变方面,尤其西门子“无极成像”VIBE序列具有独特的优势,与DSA具有很好的一致性,是显示CTPV的优化序列。单次屏气状态下,VIBE即可轻松完成各向同性T1三维脂肪抑制成像,提供良好的空间分辨率和脏器解剖与血管的细腻对比。原始数据经最大密度投影(MIP)和多平面重组(MPR)快速重建后,可展示任意层面上扫描部位的精细结构,信噪比和对比度均与原始图像无差异。其平均层厚仅为2mm,扫描时间足够短,可以很好地应用于动态增强成像,对腹部、盆腔结节状等病变的发现和鉴别十分有益。
MRI平扫可以显示流空的血管影,增强可以观察门静脉的栓塞程度、侧支循环情况、动脉期的异常灌注、肝的形态改变,MRCP可以直观显示胆总管的情况。
综上所述,MRI可以更好地显示门静脉栓塞、肝异常灌注以及血流变化所致形态改变,对诊断CTPV具有重要意义。
[1]李康, 吕富荣, 马千红, 等.64层螺旋CT门静脉成像诊断门静脉海绵样变性.中国医学影像技术, 2009, 25(6):1050-1052.
[2]梁颖, 蒋涛, 王亚杰, 等.螺旋CT评价门静脉海绵样变性及其侧支循环的特点.中国医学影像技术, 2008,24(7): 1076-1079.
[3]葛玲五, 严森祥, 许顺良, 等.门静脉海绵样变性三维动态增强磁共振血管成像的诊断及其价值.浙江大学学报:(医学版), 2008.37(2): 203-207.
[4]Vilgrain V, Condat B, Bureau C, et al.Atrophy-hypertrophy complex in patients with cavernous transformation of the portalvein: CT evaluation.Radiology, 2006, 241(1): 149-155.
[5]Bayraktar Y, Harmanci O, Ersoy O, et al.Portal double ductopathy sign in patients with portal vein cavernous transformation.Hepatogastroenterology, 2008, 55(85):1193-1200.
[6]Schweizer W, Duda P, Tanner S, et al.Experimental atrophy/hypertrophy complex (AHC) of the liver: portal vein,but not bile obstruction, is the main driving force for the development of AHC in the rat.J Hepatol, 1995, 23(1): 71-78.
