瘤内注射用姜黄素温敏凝胶的处方筛选及pH值的确定
2012-12-03高萌张成鸿鲍旭蒋妮何艳田舸田燕大连医科大学药学院辽宁大连6044大连医科大学形态学实验室辽宁大连6044大连儿童医院药剂科辽宁大连600
高萌,张成鸿,鲍旭,蒋妮,何艳,田舸,田燕#(.大连医科大学药学院,辽宁大连6044;.大连医科大学形态学实验室,辽宁大连 6044;.大连儿童医院药剂科,辽宁大连 600)
经皮无水乙醇注射疗法(percutaneous ethanol injection therapy,PEIT)是一种应用广泛、疗效肯定的瘤内注射疗法,尤其对于肿瘤直径≤3 cm的肝癌有很好的治疗效果。但乙醇会从针孔外漏到肝包膜外而引起剧烈疼痛,或经小血管进入循环系统引起不良反应,对肝组织的毒性较大,不适于肝功能差的患者。据文献[1]报道,若将药物制备成温度敏感型原位凝胶(以下简称温敏凝胶)并采用瘤内注射的给药方式,既可以避开首关效应以及在消化道和胃肠道中的降解,减轻化疗药物的不良反应,又克服了瘤内注射液体制剂易扩散的缺点,达到靶向给药和延缓药物释放的目的。因此,笔者选择药用辅料泊洛沙姆为基质制备瘤内注射用姜黄素温敏凝胶,在弥补PEIT不足的前提下,达到更好的治疗效果。
温敏凝胶在贮藏条件(4℃)下是自由流动的液体,进入体内后可在注射部位发生相转变形成半固体状态凝胶,能达到局部给药或延缓药物释放的目的[2]。其中,用泊洛沙姆407(P407)制备的凝胶表面光滑柔软,在注射部位没有明显的异物感、无毒无刺激、生物相容性好[3],是常用的制备温敏凝胶的辅料。姜黄素(Curcumin)是中药姜黄中的有效成分,具有抗肿瘤、抗炎、抗氧化、抗菌、保肝等多种药理活性[4],是一种高效低毒的天然抗癌药物,对小鼠腹水型肝癌高淋巴道转移细胞株有很强的抑制作用[5]。有关姜黄素制剂的报道较少,其主要原因是姜黄素水溶性差、不稳定且易降解[6],故体内吸收差。笔者选择P407、P188为基质,聚乙二醇400(PEG400)、1,2-丙二醇、磷酸盐缓冲液为溶剂,通过正交试验筛选姜黄素温敏凝胶的最佳处方,通过稳定性试验确定其最适宜pH值,从而提高姜黄素的稳定性,为制备姜黄素制剂提供试验依据,使其具有更好的开发和应用前景。
1 仪器与试药
1100型高效液相色谱(HPLC)仪(美国安捷伦公司);Krom Asil C18柱(大连江申分离科学技术公司);NDJ-7旋转式黏度计、FA1104万分之一电子天平(0.1 mg),均购于上海精密科学仪器有限公司;501超级恒温器(上海市实验仪器厂);79-1磁力加热搅拌器(金坛市医疗仪器厂);PB-20标准型pH计(北京赛多利斯仪器系统有限公司)。
姜黄素原料药(陕西森弗生物技术有限公司,纯度:95%,批号:20101213);姜黄素标准品(成都曼思特生物科技有限公司,纯度:98%,批号:20110302);P407(批号:119 K0073)、P188(批号:129 K0055),均购于美国Sigma公司;PEG400(分析纯,天津市福晨化学试剂厂,批号:20080701);1,2-丙二醇(分析纯,天津市化学试剂一厂,批号:990428);乙腈(色谱纯,美国Tedia公司,批号:1009262);冰醋酸(色谱纯,天津市科密欧化学试剂有限公司,批号:20090706);姜黄素温敏凝胶(大连医科大学药剂学教研室自制,批号:20110301、20110302、20110303,规格:2 mg·mL-1)。
2 方法与结果
2.1 色谱条件[7]
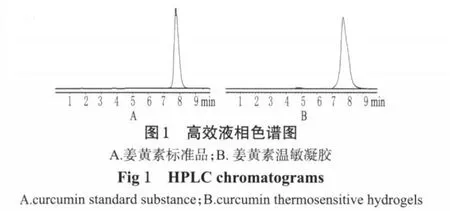
色谱柱:以十八烷基硅烷键合硅胶为黏合剂的Krom AsilC18柱(150mm×4.6mm,5μm);流动相:乙腈-2%冰醋酸(58∶42);检测波长:430 nm;流速:1 mL·min-1;柱温:室温;进样量:20 μL。理论板数按姜黄素峰计算应不低于4000。精密量取姜黄素标准品5 mg和姜黄素温敏凝胶适量(含姜黄素约5 mg),分别置50 mL量瓶中,用流动相溶解并稀释至刻度,按上述色谱条件分别进样。结果,姜黄素保留时间在7.7 min左右,分离度符合要求。色谱见图1。
2.2 姜黄素温敏凝胶的处方筛选
2.2.1 姜黄素温敏凝胶的制备[8,9]分别称取处方量P407、P188,加入60 mL磷酸盐缓冲液溶解,在4℃冰箱中放置至溶液澄明,为A液。精密称定处方量姜黄素,溶于处方量PEG400和1,2-丙二醇中,超声至完全溶解,为B液。将B液完全转移至A液中,所得溶液为C液,在C液中加入磷酸盐缓冲液至100 mL,在4℃放置至C液完全澄清,调节至所需pH值,即得(规格:2 mg·mL-1)。
2.2.2 胶凝温度的测定[10]采用搅拌子法,在西林瓶中装入温敏凝胶溶液10mL和搅拌子,插入精度为0.1℃的精密温度计,温度计的水银球完全浸没在凝胶溶液中。将其放入低温(10℃)水浴中,保持水浴持续缓慢升温,使凝胶的温度上升速率约为(1~2)℃·min-1。将磁力搅拌子完全停止转动的温度定义为胶凝温度。
2.2.3 黏度的测定[9]取凝胶样品溶液15 mL置样品管中,用循环水浴使其升温至40℃以上,再以(1~2)℃·min-1的速率缓慢冷却至10℃,选择合适量程的悬吊式转子测定不同温度下的黏度,从40℃开始,温度每下降1℃记录一个黏度值。
2.2.4 姜黄素的最大溶解度 精密量取不同配比的1,2-丙二醇、PEG400适量,置烧杯中,磷酸盐缓冲液加至100 mL,在超声溶解状态下,用减量法逐渐加入适量姜黄素至最大饱和为度(10~15 min内不再溶解为准),平行制备5个样品,按“2.1”项下色谱条件测定含量,求出平均值,结果见表1。
结果表明,姜黄素在10%PEG400、14%1,2-丙二醇中的溶解度最大,即(2.447±0.121)mg·mL-1,大大提高了姜黄素的溶解度。
表1 姜黄素的最大溶解度测定结果(±s,n=5)Tab 1 Maximum dissolution rate of curcumin(±s,n=5)

表1 姜黄素的最大溶解度测定结果(±s,n=5)Tab 1 Maximum dissolution rate of curcumin(±s,n=5)
PEG400/%6810810610861,2-丙二醇/%101214141012121410最大溶解度/mg·mL-11.605±0.1052.026±0.0032.447±0.1212.197±0.1182.105±0.0081.776±0.1072.276±0.1312.197±0.0061.605±0.145
2.2.5 含药量的测定 精密称取姜黄素标准品5 mg,置于25 mL量瓶中,甲醇稀释至刻度,得浓度为0.2 mg·mL-1的标准品贮备液,精密量取姜黄素标准品贮备液200、400、800、1600、3200、6400 μL,置于10 mL量瓶中,用甲醇稀释至刻度,配成浓度分别为4、8、16、32、64、128μg·mL-1的系列标准溶液。按“2.1”项下色谱条件进样测定,平行测定3次,每次进样量20 μ L。以峰面积积分值(A)为纵坐标,姜黄素检测浓度(c)为横坐标,进行线性回归,得回归方程为A=113.2 c+82.177(r=0.9993)。精密量取200µL姜黄素温敏凝胶置10 mL量瓶中,甲醇定容。混匀后按上法测定,根据回归方程计算姜黄素温敏凝胶中姜黄素的含量。
2.2.6 正交试验优选处方 通过预试验中单因素试验结果,选择P407的浓度(A)、P188的浓度(B)、PEG 400的浓度(C)、1,2-丙二醇的浓度(D)为考察因素,以胶凝温度(T)、黏度(η)和含药量的综合评分为评价指标(评分方法:(1)T:由于人体的正常体温范围为36~37℃,故胶凝温度在此范围内者得100分,每低于36℃或高于37℃为1℃者扣5分,若转子无停止则记为0分。(2)η:以正交试验结果中胶凝温度时的黏度为标准,<10 mPa·s者为100分,10~20 mPa·s者为90分,20~30 mPa·s者为80分,30~40 mPa·s者为70分。(3)含药量:以正交试验结果中含量最高者为满分100分,每低于此含量0.1 mg者扣5分。(4)综合评分:综合评分=胶凝温度记分×50%+黏度记分×20%+含量记分×30%)。采用L9(34)正交表安排试验,测定评价指标,计算每次试验得分确定最佳配比,每个试验重复3次。用SPSS 11.5统计软件,多组资料采用方差分析,两组间比较采用t检验。因素水平见表2;正交试验结果见表3;方差分析结果见表4。
由表3、表4可知,4种因素对工艺均有显著性影响(P<0.05或P<0.01),其影响大小为A>C>D>B,即P407浓度为影响姜黄素温敏凝胶性质的主要因素,其次是PEG400浓度,再次为1,2-丙二醇浓度,最后是P188浓度。较好的组合为A2B2C2D2,即P407浓度为20%、P188浓度为4%、PEG400的浓度为8%、1,2-丙二醇的浓度为12%。
2.3 姜黄素温敏凝胶最适宜pH值的确定
2.3.1 不同pH值下姜黄素温敏凝胶的标准曲线 配制pH值分别为5.5、6.0、6.5、7.0、7.5的磷酸盐缓冲溶液,按“2.2.6”项下最终确定的处方量制备不同pH值的姜黄素温敏凝胶。待凝胶充分混匀溶解之后,用pH计调pH值为6.0、6.5、7.0、7.5、8.0,为不同pH值下的姜黄素的贮备液。精密量取各姜黄素贮备液0.5、1.0、2.0、4.0、8.0 mL,置于100 mL量瓶中,用甲醇定容,混匀后按“2.1”项下色谱条件测定,以峰面积积分值(A)为纵坐标,姜黄素检测浓度(c)为横坐标,制备各pH值下姜黄素的标准曲线,结果见表5。

表2 因素水平Tab 2 Factors and levels

表3 正交试验结果Tab 3 Results of orthogonal test

表4 方差分析结果Tab 4 Results of variance analysis

表5 不同pH值姜黄素温敏凝胶的标准曲线Tab 5 The standard curves of Curcumin thermosensitivehydrogels with different pH values
结果表明,在不同pH值的姜黄素温敏凝胶中姜黄素检测浓度在10~160 μg·mL-1范围内与峰面积积分值呈良好线性关系。
2.3.2 姜黄素降解速率的测定 将“2.3.1”项下制备的不同pH值下的姜黄素温敏凝胶置于4℃冰箱中,于1、2、3、4、6、10、14、20d时分别取200µL不同pH值的姜黄素温敏凝胶至10 mL量瓶中,用甲醇定容。混匀后按“2.1”项下色谱条件测定,根据标准曲线方程计算姜黄素浓度(c),以c(μg·mL-1)对时间t(d)作图,求不同pH值姜黄素温敏凝胶的降解速率常数(k)、半衰期(t1/2),结果见表6。

表6 不同pH值姜黄素温敏凝胶的降解方程及速率Tab 6 The degradation equations and degradation rates of Curcumin thermosensitive hydrogels with different pH values
结果表明,在4℃时,姜黄素温敏凝胶随时间的降解符合为零级动力学过程。不同pH值的姜黄素温敏凝胶的动力学方程、k、t1/2均不相同,随着pH值的升高,k加大。当pH值为6.0时,t1/2=150.93 d,表明pH值为6.0时姜黄素温敏凝胶稳定,且稳定性明显优于姜黄素溶液(t1/2=433.1h[5]),而当pH≥6时,姜黄素温敏凝胶的降解速率加快,故将姜黄素温敏凝胶的pH定为6.0。
综上所述,拟定姜黄素温敏凝胶的处方为0.2%姜黄素、20%P407、4%P188、12%1,2-丙二醇、8%PEG400、磷酸盐缓冲液加至100 mL,调pH值为6.0。
2.4 工艺验证试验
按上述最佳处方制备3批姜黄素温敏凝胶(批号:20110301、20110302、20110303),分别测定其T、在胶凝温度(36.5℃)时的η以及姜黄素的含量。结果,各指标分别为(36.5± 0.41)℃(n=3)、(823± 6.23)mPa·s、(0.207±0.0021)%(即剂量为2.07 mg·mL-1),姜黄素温敏凝胶规格为2 mg·mL-1,所测姜黄素含量在常规含量限度范围内(1.8~2.2 mg·mL-1),含量符合规定。
3 讨论
药物辅料泊洛沙姆是由聚氧化乙烯与聚氧化丙烯组成的嵌段共聚物(PEO-PPO-PEO),由于聚氧乙烯链的相对亲水性和聚氧丙烯链的相对亲油性,使其具有表面活性,属于非离子型表面活性剂。多数泊洛沙姆在较高浓度时可以形成水凝胶,主要是由于分子间形成氢键的结果[11]。以P407为例,当其浓度高于15%时,可以形成凝胶。正交试验结果表明,随着P407浓度的增加,胶凝温度下降;与此相反,随着P188浓度的增加,胶凝温度则上升。加入溶剂1,2-丙二醇后,胶凝温度降低,黏度升高,主要是因为1,2-丙二醇也可以与泊洛沙姆形成分子间氢键,形成更大的分子。加入溶剂PEG400后,胶凝温度升高,黏度下降,PEG400的分子结构与泊洛沙姆相似,且水溶性优于泊洛沙姆,故使泊洛沙姆的水溶性降低,当PEG400浓度过高时则无法形成凝胶。试验证明,P407浓度若为18%,当PEG400的浓度大于15%时,不能形成凝胶,即无胶凝温度。本试验根据正交试验结果,筛选出了最佳处方,既有适宜的胶凝温度及黏度,又提高了姜黄素的含量,同时改善了姜黄素的稳定性,克服了其水溶性差的缺点,进而可提高姜黄素在体内的生物利用度,使其具有更大的开发和应用价值。
[1]陈 喆,翟笑枫,蒋 栋,等.去甲斑蝥素-泊洛沙姆407缓释剂和无水乙醇的肝癌瘤内注射疗效比较[J].第二军医大学学报,2001,22(7):606.
[2]金璐燕,李 娟.泊洛沙姆407在制剂中的应用进展[J].药学与临床研究,2009,17(3):231.
[3]杜广增,赵浩如.Poloxamer407温敏性即型凝胶的制备和应用进展[J].药学进展,2008,3(4):163.
[4]胡 静,李 立.姜黄素药理作用研究现状[J].检验医学与临床,2007,4(12):1186.
[5]张宏颖,刘春平,唐建武,等.姜黄素对小鼠腹水型肝癌高淋巴道转移细胞株(HCa-F)生物学行为的影响[J].中草药,2005,36(11):1663.
[6]韩 刚,霍 文,李秋影,等.姜黄素的稳定性研究[J].中成药,2007,29(2):291.
[7]顾吉晋,邓英杰,王 浩,等.RP-HPLC法测定大鼠血浆中姜黄素含量[J].成都医学院学报,2009,4(4):241.
[8]申献玲,胡 燕,雷 露,等.美洛昔康温敏性水凝胶的制备及质量控制[J].中国药房,2008,19(25):1069.
[9]高 斐,王东凯,罗 立,等.左氧氟沙星热敏型眼用凝胶的研制及体外释放研究[J].中国药房,2005,16(14):1057.
[10]宋 涛,王东凯,高 红,等.利巴韦林鼻用温敏凝胶热力学和流变学性质研究[J].中国医药工业杂志,2006,37(8):540.
[11]王明坤,方晓玲.泊洛沙姆在药剂学中的应用[J].中国医药工业杂志,2002,33(12):621.
