改进共沉淀法制备LiCo1/3Ni1/3Mn1/3O2正极材料
2012-11-30谌谷春唐新村王志敏
谌谷春,唐新村,2,王志敏
(1.中南大学 化学化工学院,有色金属资源化学教育部重点实验室,湖南 长沙,410083;2.中南大学 粉末冶金国家重点实验室,湖南 长沙,410083)
LiCoO2作为锂电池的主流正极材料,由于其存在实际比容量偏低、资源短缺、价格高、热稳定性能差等缺陷[1−2],限制了它的进一步发展,LiCoO2正极材料在市场上占主导地位的格局已发生改变。近年来,市场上涌现出一批新型材料,例如LiNiO2,LiMn2O4,磷酸铁锂和镍钴锰酸锂等。LiNiO2比 LiCoO2便宜,实际比容量可达到200 mA·h/g,自放电率低,对环境无污染,但是Ni2+很难氧化成Ni3+,导致LiNiO2很难合成,且安全性也差[3−5];LiMn2O4具有较高的功率和能量密度,性价比高,无污染,但是由于Mn3+容易发生 Jahn–Teller效应导致容量衰减严重[6−7];磷酸铁锂虽然价格低廉,对环境友好,循环性能优异,但其容量较低,电导率小,大电流放电时容量衰减较大[8−9]。而镍钴锰酸锂正极材料具有比容量较高、价格低、安全性和循环性能好等优点,不仅被认为是最有潜力替代LiCoO2的正极材料,而且也被认为是发展成动力锂电池最有竞争力的候选材料[10]。目前,合成LiCo1/3Ni1/3Mn1/3O2的主要方法有高温固相法、溶胶凝胶法、共沉淀法和喷雾热分解法[11−14]等,但是适应于工业化生产的主要是高温固相法和共沉淀法。高温固相法虽然工艺简单,但是原料混合均匀程度有限,需要在高温下反应较长时间,合成的产物通常颗粒大小不均匀、晶粒形状不规则、晶界尺寸较大以及电化学性能不容易控制。共沉淀法是目前研究的最多的方法,这种方法可以使金属离子间的接触充分,基本上能达到原子级反应水平,样品的形貌易于控制,粒径分布均匀,导致电化学性能稳定,且产品的重现性好。但传统的共沉淀法较难获得振实密度高和形貌较好的产品。本文作者采用改进的氢氧化物共沉淀法制备LiCo1/3Ni1/3Mn1/3O2正极材料。选用 NiSO4,CoSO4和MnSO4为原料,以NaOH为沉淀剂,NH3·H2O为络合剂,PEG为分散剂,在 N2氛围保护下,制备得到了球形的Ni1/3Co1/3Mn1/3(OH)2前驱体,与LiOH研磨煅烧,即得到产品LiCo1/3Ni1/3Mn1/3O2。
1 实验
1.1 正极材料的制备及表征
将NiSO4,MnSO4和CoSO4配成2 mol/L的混合溶液,采用NaOH为沉淀剂,NH3·H2O做络合剂,聚乙二醇(PEG)为分散剂,在惰性气体保护下,搅拌反应12 h,控制反应温度在50 ℃。反应完后,过滤烘干,得到Ni1/3Co1/3Mn1/3(OH)2前驱体(对于传统的共沉淀法来说,实验过程中不需加入NH3·H2O和PEG,其他的实验条件均相同)。取适量的前驱体与一定比例的LiOH混合研磨,然后置于马弗炉中,450 ℃预煅烧4 h,再升温至900 ℃煅烧12 h,得到LiCo1/3Ni1/3Mn1/3O2正极材料。采用Rigaku D/ Max2500VB+X线衍射仪(XRD)进行物相分析,用场发射扫描电镜(FE-SEM,FEI Sirion)进行形貌分析。
1.2 测试电池的组装
取正极活性物质、乙炔黑和聚偏氟乙烯(PVDF)按质量比 85:5:10的比例制浆,涂在不锈钢网上,制成正极。用金属锂片作为测试电池的负极,电解液为1 mol/L的LiPF6/EC+DEC(体积比为1:1)溶液,聚丙烯微孔膜为隔膜,在充满氩气的手套箱中组装成扣式电池。用Land CT2001A电池测试仪在室温(25℃左右)进行恒流充放电测试,充放电电流密度为 32 mA/g(0.2C),充放电电压控制在2.80~4.25 V。
2 结果与讨论
2.1 XRD分析
图 1所示为用 2种方法制备得到的LiCo1/3Ni1/3Mn1/3O2的XRD谱(样品A和B分别为改进共沉淀法和传统共沉淀法制得的产品LiCo1/3Ni1/3Mn1/3O2)。从图1可以看出:(006)/(102)与(108)/(110)2组衍射峰分裂明显,表明这2种材料均具有有序的层状α-NaFeO2结构[15],Li占据3a位置,过渡金属M(M=Ni,Co,Mn)占据3b位置,O原子占据 6c位置,且图谱中不存在杂相,这与文献[5]中报道的LiCo1/3Ni1/3Mn1/3O2的谱图完全相同。表1所示为2种方法合成的LiCo1/3Ni1/3Mn1/3O2晶胞参数。
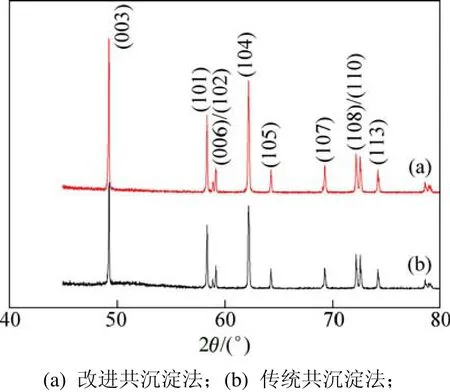
图1 改进共沉淀法和传统共沉淀法制备的LiNi1/3Co1/3Mn1/3O2的XRD谱Fig.1 XRD patterns of LiNi1/3Co1/3Mn1/3O2 powders prepared by improved coprecipitation method and conventional coprecipitation method

表1 样品A和B的晶胞参数Table 1 Lattice parameters of samples A and B
据文献[16]报道,c/a越大,材料的层状结构更优异,越有利于锂离子在层间的脱嵌。由表1可知:样品 A的 c/a较高,表明由改进共沉淀法制得的LiCo1/3Ni1/3Mn1/3O2具有更好的层状结构。由于Li+和Ni2+的半径相近,所以在LiCo1/3Ni1/3Mn1/3O2中很容易发生离子混排。一般用I(003)/I(104)峰强比来表征阳离子混排程度,该值越大,表明阳离子混排效应越小[3],越有利于提高材料的电化学性能,A样品的I(003)/I(104)峰强比B样品的高,表明A样品中阳离子混排程度更小。因此,可以推断改进共沉淀法制得的LiCo1/3Ni1/3Mn1/3O2是较理想的产品,可表现出更优异的电化学性能。
2.2 SEM分析
图2所示为改进共沉淀法与传统共沉淀法所制备的前躯体的SEM图。从图2(c)可以看出:由传统共沉淀法所制备的前驱体呈不规则形状,大小不一,排列无序,颗粒之间有团聚现象产生。而通过图2(a)可知:由改进共沉淀法制备得到的前躯体呈球形颗粒,粒径较为均一,约为2 μm,颗粒之间排列紧凑,没有发生团聚;图2(b)是图2(a)的高倍率扫描电镜图,从图2(b)可以更加清晰地看到:前驱体的球形颗粒是由球形和片状的一次颗粒组装而成,其中,球形的一次颗粒粒径在5 nm左右,整个二次颗粒的表面可看到空隙,这极有可能是一次颗粒在组装过程中所导致的,这种空隙的存在有利于锂离子的脱嵌,能使材料保持较好的循环稳定性。
图3所示为改进共沉淀法与传统共沉淀法制备得到的产品LiCo1/3Ni1/3Mn1/3O2的SEM图。从图3可以看出:煅烧后,由改进共沉淀法制备得到的LiCo1/3Ni1/3Mn1/3O2颗粒仍呈球形形貌,颗粒表面存在空隙。测试对比2种产品的振实密度,可以发现后者的振实密度高达 2.78 g/cm3,明显高于前者的 2.04 g/cm3,也高出文献的报道值(1.8~2.4 g/cm3)[17]。振实密度是电池材料的一个重要指标,较高的振实密度可以较大程度地提高锂电池的体积比能量[10,16],因此,可以推测由改进共沉淀法制备得到的产品LiCo1/3Ni1/3Mn1/3O2具有更优异的电化学性能。
2.3 电化学性能分析

图2 改进共沉淀法和传统共沉淀法制备的前躯体的SEM像Fig.2 SEM images of precursors by improved coprecipitation method and traditional coprecipitation method
图 4所示为 2种方法合成的 LiCo1/3Ni1/3Mn1/3O2首次充放电曲线(0.2C,2.80~4.25 V)。从图4可以看出:在室温条件下,改进共沉淀方法制备的LiCo1/3Ni1/3Mn1/3O2正极材料的充放电比容量(185.2和158.3 mA·h/g)比传统方法制备的正极材料(155.7和127.3 mA·h/g)的高,如此大的性能差异可能是由于材料的形貌和结构,以及其他的物化性质的不同所致。用改进共沉淀方法制备的 LiCo1/3Ni1/3Mn1/3O2具有球形二次颗粒的形貌,颗粒之间没有团聚。一次颗粒由于粒径小,缩短了Li+在正极材料中迁移的时间,提高了迁移的效率。又由于球形颗粒具有更高的振实密度,因此,综合这些因素,改进方法后制得的LiCo1/3Ni1/3Mn1/3O2具有更高的充放电容量。此外,通过对比两者的库仑效率发现:2种材料的不可逆容量损失均较大,这极有可能是由于电极表面固体电解质膜(SEI)的生成引起的[18]。

图3 改进共沉淀法和传统共沉淀法和制备的LiCo1/3Ni1/3Mn1/3O2的SEM像Fig.3 SEM images of precursors by improved coprecipitation method traditional coprecipitation method
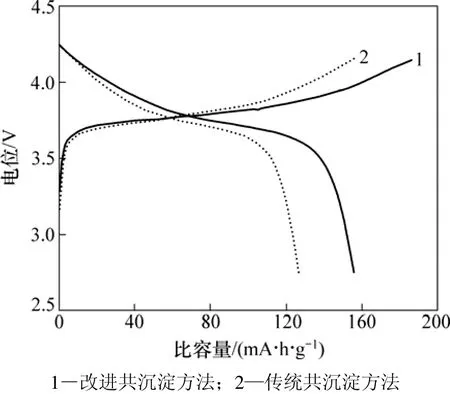
图4 LiCo1/3Ni1/3Mn1/3O2第1次循环的充放电曲线Fig.4 Initial charge and discharge curves ofLiCo1/3Ni1/3Mn1/3O2 cathodes
图 5所示为2种方法制备的 LiCo1/3Ni1/3Mn1/3O2循环性能曲线(0.2C,2.80~4.25 V)。由图5可知:30个循环后,改进共沉淀方法制备的LiCo1/3Ni1/3Mn1/3O2正极材料放电比容量为142.8 mA·h/g,而传统共沉淀方法制备的 LiCo1/3Ni1/3Mn1/3O2正极材料放电比容量仅为99.1 mA·h/g,前者的容量保持率为90.2%,显著优于后者的 77.8%。循环性能的优异可能归功于其特有的具有空隙的球形形貌,由于空隙的存在,电解液能够很容易进入这些空隙,并渗透进球形颗粒的内部,直接和球体内部的晶粒接触,这样可以大大降低 Li+在材料中扩散的阻力,有利于Li+的脱嵌。此外,还可能是因为其具有更好的结晶性,更加完美的层状结构和较小的阳离子混排率,这在 XRD图谱分析中得到了验证。
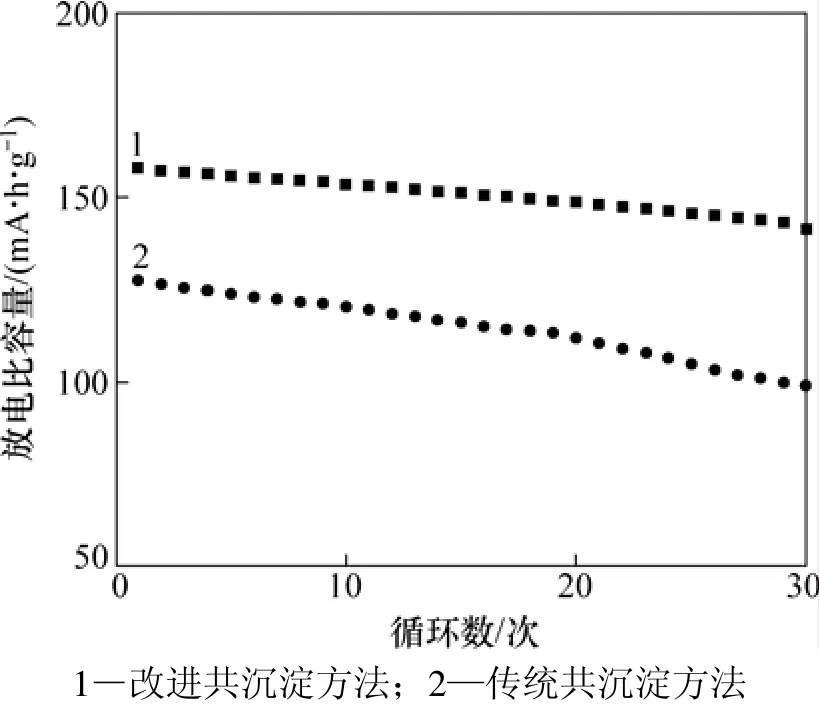
图5 LiCo1/3Ni1/3Mn1/3O2的循环性能曲线Fig.5 Cycling performance curves of LiCo1/3Ni1/3Mn1/3O2 cathodes
3 结论
(1)通过在传统共沉淀方法的基础上添加络合剂(NH3.H2O)和分散剂(PEG),采用这种改进的共沉淀方法制备得到了LiCo1/3Ni1/3Mn1/3O2正极材料。
(2)运用XRD和SEM等分析手段对2种方法制备的产品进行表征,发现用改进共沉淀法制得的LiCo1/3Ni1/3Mn1/3O2呈球形二次颗粒,具有更优异的层状结构,更高的振实密度(2.78 g/cm3)以及更好的电化学性能,在充放电倍率为0.2C,电压范围为2.80~4.25 V的条件下,它的首次充、放电比容量分别为 185.2和 158.3 mA·h/g,30次循环后的容量保持率高达90.2%。
[1]Yoshio N.Lithium ion secondary battery technologies,present and future[J].Macromol Symp,2000,156:187−193.
[2]Noboru O.Lithium polymer battery with high energy density[J].Macromol Symp,2000,156:171−178.
[3]苏继桃,苏玉长,赖智广,等.LiCo1/3Ni1/3Mn1/3O2正极材料的制备及其表征[J].中南大学学报:自然科学版,2008,39(2):1703−1708.SU Ji-tao,SU Yu-chang,LAI Zhi-guang,et al.Preparation and characterization of LiCo1/3Ni1/3Mn1/3O2cathode material[J].Journal of Central South University:Science and Technology,2008,39(2):1703−1708.
[4]Armstrong A R G.Synthesis of layered LiMnO2as an electrode for rechargeable lithium batteries[J].Nature,1996,381(6582):499−500.
[5]Yabuuchi N,Ohzuku T.Novel lithium insertion material of LiCo1/3Ni1/3Mn1/3O2for advanced lithium-ion batteries[J].Journal of Power Sources,2003,119/120/121:171−174.
[6]Xia Y,Sakai T,Fujieda T,et al.Correlating capacity fading and structural changes in Li1+yMn2−yO4spinel cathode materials:A systematic study on the effects of Li/Mn ratio and oxygen deficiency[J].J Electrochem Soc,2001,148(7):A723−A729.
[7]Piszora P,Paszkowicz W,Baehtz C,et al.X-ray diffraction studies on the nature of the phase transition in the stoichiometric LiMn2O4[J].J Alloys Compd,2004,382(1/2):119−122.
[8]Padhi A K,Nanjundaswamy K S,Goodenough J B.Phospho-olivines as positive-electrode materials for rechargeable lithium batteries[J].J Electrochem Soc,1997,144(4):1188−1194.
[9]Kim H S,Cho B W,Cho W I.Cycling performance of LiFePO4cathode material for lithium secondary batteries[J].J Power Sources,2004,132(1/2):235−239.
[10]张宝,张明,李新海,等.锂离子电池正极材料LiCo0.1Ni0.45Mn0.45O2合成及电化学性能[J].中南大学学报:自然科学版,2008,39(1):75−79.ZHANG Bao,ZHANG Ming,LI Xin-hai,et al.Synthesis and electrochemical properties of LiCo0.1Ni0.45Mn0.45O2cathode material for lithium ion batteries[J].Journal of Central South University:Science and Technology,2008,39(1):75−79.
[11]Yasuhiro F,Hiroshi M,Naoto Si,et al.Structural and electrochemical properties of LiNi1/3Co1/3Mn1/3O2:Calcination temperature dependence[J].J Power Sources,2007,171(2):894−903.
[12]Kima J H,Parkb C W,Sun Y K.Synthesis and electrochemical behavior of Li[Li0.1Ni0.35-x/2CoxMn0.55-x/2]O2cathode materials[J].Solid State Ionics,2003,164:43−49.
[13]Lee M H,Kang Y J,Myung S T,et al.Synthetic optimization of LiNi1/3Co1/3Mn1/3O via co-precipitation[J].Electrochimica Acta,2004,50:939−948.
[14]Sung W O,Sang H P,Park C W,et al.Structural and electrochemical properties of layered Li[Ni0.5Mn0.5]1−xCoxO2positive materials synthesized by ultrasonic spray pyrolysis method[J].Solid State Ionics,2004,171:167−172.
[15]苏继桃,苏玉长,赖智广,等.锂离子电池正极材料LiCo0.4Ni0.3Mn0.3O2的制备及性能[J].中南大学学报:自然科学版,2008,39(1):18−22.SU Ji-tao,SU Yu-chang,LAI Zhi-guang,et al.Synthesis and properties of LiCo0.4Ni0.3Mn0.3O2cathode material for Li-ion batteries[J].Journal of Central South University:Science and Technology,2008,39(1):18−22.
[16]ZHANG Xiang-feng,WEN Zhao-yin,YANG Xue-lin,et al.Synthesis and electrochemical behavior of a new layered cathode material LiCo1/2Mn1/3Ni1/6O2[J].Mater Res Bull,2006,41(3):662−666.
[17]LUO Xue-fang,WANG Xian-you,LI Liao,et al.Synthesis and characterization of high tap-density layered LiNi1/3Co1/3Mn1/3O2cathode material via hydroxide co-precipitation[J].J Power Sources,2006,158(1):654−658.
[18]WEN Jian-wu,ZHANG Da-wei,TENG Yuan-cheng,et al.One-step synthesis and improved electrochemical performance of LiCo1/3Ni1/3Mn1/3O2by a modified radiated polymer gel method[J].Electrochim Acta,2010,55(7):2306−2310.
