新型2-硝基亚氨基咪唑烷和2-氰基亚氨基-1,3-噻唑烷衍生物的合成及其抗真菌活性
2012-11-21赵浩宇侯太平
孙 秋, 赵浩宇, 侯太平
(1. 四川大学 a. 华西药学院 靶向药物及释药系统教育部重点实验室;b. 生命科学院 生物资源与生态环境教育部重点实验室,四川 成都 610064)
在全球范围类,农作物由于植物病害产量剧烈减少,其中由植物病原菌引起的损失占了相当大的一部分[1~4]。水稻纹枯病、小麦赤霉病、苹果腐烂病和葡萄黑豆病是影响农作物的常见病害,发生范围广,危害损失大。通过化学农药对植物病菌进行防治,是目前生产上最主要的手段[5]。但是,随着这类化合物的使用时间的延长,病害菌的抗性也越来越强,导致了该类杀菌剂活性降低,甚至在一些地区丧失了杀菌能力[6]。因此,研发新型的杀菌剂具有非常重要的意义。
在抗真菌农药创制过程中发现,N-{1-[3-(4-溴-2-甲基)丙烯酰]咪唑烷-2-亚基}硝酰胺(Ⅰ)和N-{3-[2-氧代-2-(吡咯烷-1-基)乙基]噻唑烷-2-亚基}氰胺(Ⅱ)具有良好的抗真菌活性,且目前对该类化合物的抗真菌活性尚未见报道。
本文以芳甲酰氯(4a~4g),芳乙酰氯(5a~5c)2-硝基亚胺咪唑烷和2-氰基亚胺1,3-噻唑烷为主要原料,设计并合成了5个新型的2-硝基亚氨基咪唑烷(1a~1e)和10个新型的2-氰基亚氨基-1,3-噻唑烷衍生物(2a~2g和3a~3c, Scheme 1),其结构经1H NMR和13C NMR表征。并对其进行了初步的生物活性测试。

1 实验部分
1.1 仪器与试剂
Bruker AV 400 Hz型核磁共振仪(CDCl3或DMSO-d6为溶剂,TMS为内标)。
薄层色谱用硅胶GF254和柱层析用硅胶(300目~400目),青岛海洋化工厂;水稻纹枯病菌、小麦赤霉病菌、苹果腐烂病菌和葡萄黑豆病菌,四川省农科院;所用试剂均为分析纯,其中CH2Cl2经干燥重蒸处理。
1.2 合成[7]
(1) 4的合成(以4c)为例
在干燥的反应瓶中加入4-甲基肉桂酸432.4 mg(2 mmol), N2保护下滴加DMF 1滴~2滴;加入CH2Cl25 mL,于0 ℃搅拌使其完全溶解;缓慢滴加草酰氯0.17 mL(2 mmol),滴毕,于室温反应2 h~3 h。减压浓缩后用CH2Cl2(5 mL)稀释得含4c的CH2Cl2溶液A。
用类似的方法合成4a,4b,4d~4g的CH2Cl2溶液。
(2) 5的合成(以5b为例)
在干燥的反应瓶中加入吗啉0.20 mL(2.3 mmol), N2保护下加入CH2Cl25 mL,搅拌下于0 ℃缓慢滴加氯乙酰氯0.16 mL(2 mmol),滴毕,反应2 h~3 h。减压浓缩后用CH2Cl2(5 mL)稀释得含5b的CH2Cl2溶液B。
用类似的方法合成5a和5c的CH2Cl2溶液。
(3) 1和2的合成(以1c为例)
在干燥的反应瓶中加入2-硝基亚氨基咪唑烷, N2保护下加入CH2Cl210 mL,搅拌使其完全溶解;滴加Et3N 0.05 mL(0.35 mmol),滴毕,反应5 min;冰水浴冷却,缓慢滴加溶液A,滴毕,于室温反应至终点(TLC跟踪)。减压浓缩后经硅胶柱层析[洗脱剂:A=V(石油醚) ∶V(乙酸乙酯)=2 ∶1]分离得(E)-N-{3-[(E)-3-p-甲苯丙烯酰]2-亚咪唑烷基)硝酰胺(1c)。
用类似的方法合成1a,1b,1d~1e。
用2-氰基亚氨基-1,3-噻唑烷替代2-硝基亚氨基咪唑烷,用类似的方法合成2a~2g。
(4) 3的合成(以3b为例)
在干燥的反应瓶中加入2-氰基亚氨基-1,3-噻唑烷260.2 mg(2 mmol), N2保护下加入CH2Cl210 mL,搅拌使其完全溶解;滴加Et3N0.05 mL(0.35 mmol),滴毕,搅拌5 min。冰水浴冷却下,缓慢滴加溶液B,滴毕,于室温反应30 min;回流反应至终点(TLC跟踪)。减压浓缩后经硅胶柱层析(洗脱剂:A=1 ∶1)分离得(Z)-N-{3-[2-(吗啉-4)-2-氧乙基]2-亚噻唑烷基}氨基腈(3b)。用类似的方法合成3a和3c。
合成1~3的实验结果见表1, NMR数据见表2。
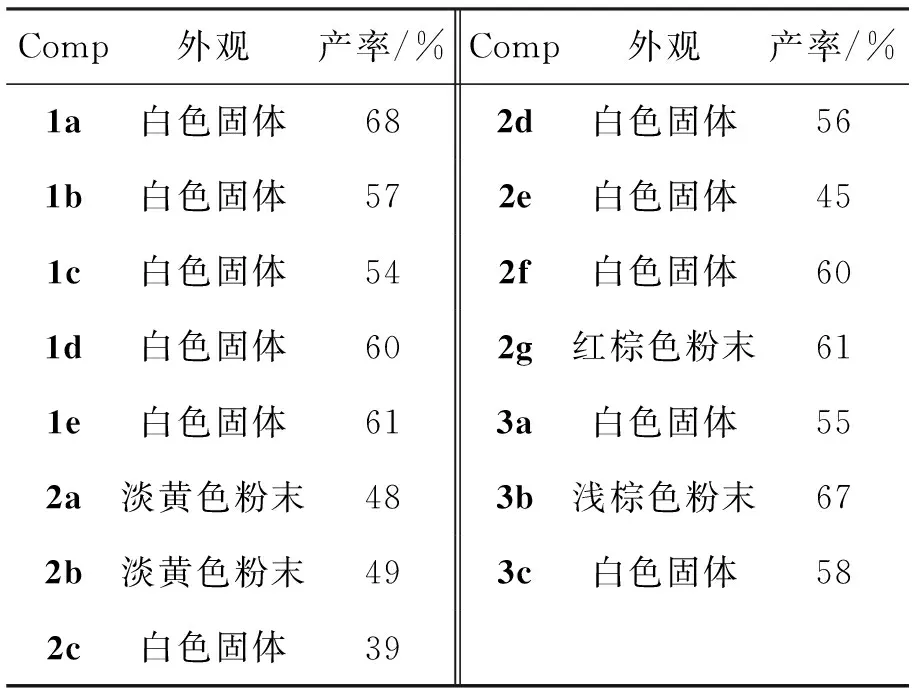
表1 合成1~3的实验结果Table 1 Experimental results of synthesizing 1~3

表2 1~3的NMR数据Table 2 NMR data of 1~3
续表2

Comp1H NMR δ(J/Hz)13C NMR δ2c2.40(s, 3H), 3.41~3.45(m, 2H), 4.47~4.50(m, 2H), 7.23(d, J=8.0, 2H), 7.49(d, J=8.0, 2H), 7.63(d, J=15.2, 1H), 7.83(d, J=15.6, 1H)21.6, 27.0, 49.0, 114.4, 117.1, 128.7, 129.8, 131.5, 141.7,147.5, 165.0, 176.72d2.11(s, 3H), 3.49(t, J=7.2, 2H), 4.33~4.36(m, 2H), 6.92(s, 1H), 7.24-~7.26(m, 2H), 7.54(d, J=8.4, 2H)15.5, 27.6, 52.2, 114.2, 118.8, 122.8, 131.0, 131.7, 132.4, 133.9, 135.9, 171.0, 176.52e2.24(s, 3H), 3.48~3.51(m, 2H), 4.44~4.47(m, 2H), 7.09(d, J=8.4, 2H), 7.24(d, J=8.4, 1H), 7.29(d, J=2.0, 1H), 7.32(d, J=8.4, 2H), 7.43(d, J=2.0, 1H)8.9, 28.0, 52.4, 114.2, 118.3, 126.5, 128.0, 129.0, 130.3, 130.5, 130.7, 133.0, 135.1, 135.7, 136.2, 142.7, 145.1, 162.9, 176.92f3.48~3.52(m, 2H), 4.36~4.40(m, 2H), 7.12~7.14(m, 1H), 7.71~7.74(m, 2H)27.8, 53.3, 114.2, 127.8, 134.8, 135.3, 135.5, 161.9, 177.12g3.49(t, J=3.2, 2H), 4.31(s, 2H), 4.33(t, J=3.2, 2H), 6.97(t, J=7.6, 1H), 7.07(t, J=8.0, 1H), 7.35(d, J=8.0, 1H), 7.46(d, J=8.0, 1H), 7.20(d, J=2.0, 1H), 7.35(d, J=8.0, 1H), 7.46(d, J=8.0, 1H), 10.95(s, 1H)27.2, 34.3, 52.5, 106.7, 111.6, 115.0, 118.6, 119.0, 121.2, 124.6, 127.5, 136.3, 170.7, 178.33a1.57~1.67(m, 6H), 3.35(t, J=5.2, 2H), 3.42~3.46(m, 2H),3.52~3.54(m, 2H), 4.02~4.05(m, 2H), 4.25(s, 2H)24.3, 25.4, 26.3, 27.7, 43.2, 46.0, 47.2, 53.8, 117.2, 163.6, 175.33b3.44~3.49(m, 4H), 3.60~3.63(m, 2H), 3.70~3.74(m, 4H), 4.03~4.07(m, 2H), 4.26(s, 2H)27.6, 42.1, 45.2, 46.9, 53.7, 66.2, 66.5, 117.0, 164.1, 175.43c1.85~1.92(m, 2H), 1.98~2.05(m, 2H), 3.43~3.50(m, 6H), 4.09(t, J=7.6, 2H), 4.17(s, 2H)24.1, 26.1, 27.7, 45.9, 46.1, 47.9, 53.8, 164.0, 175.3
2 结果与讨论
参照文献[8,9]方法作抑菌活性测试,在150 mL三角瓶加入PDA培养基60 mL,灭菌备用。用0.05% Tween 20灭菌水配成浓度为20 mg·L-1的待测药样,加入培养基中,于45 ℃~50 ℃充分摇匀后倒入直径为9 cm的灭过菌的培养皿中,每组三个重复,以等量的溶剂为空白对照。以打孔器(内径4 mm)将生长正常的菌落打孔制成若干菌饼备用,用接种针将菌饼移接到平板中央,每个培养皿接一个菌饼,置于27 ℃饱和湿度恒温培养箱中培养,待对照组长满时,测量菌落的直径。每个菌落用十字交叉法测量2次,以平均数代表菌落的大小,计算相对抑制率[抑制率=(直径空白-直径药样/直径空白)×100%]。
将待测药样用丙酮溶解,采用二倍稀释法制备各种浓度培养基,在无菌操作下接种上述新鲜菌种,每组设三个重复组,于27 ℃倒置培养,待菌落直径长到平板的2/3时,采用十字交叉法测量直径,再将六个数据平均,计算EC50值。
1~3对水稻纹枯病菌(A),小麦赤霉病菌(B)、苹果腐烂病菌(C)和葡萄黑豆病菌(D)的抑菌活性见表3。从表3可见,在浓度为20 mg·L-1时,除3a和3b外,其余15个2-硝基亚氨基咪唑烷类和N-氰基噻唑烷类衍生物均具有一定的抑菌活性。在浓度为0.02 mg·mL-1下,1d和2d对A的抑制率分别为44.15%, 58.97%;1e和2e对B的抑制率分别为48.91%, 54.46%,对C的抑制率分别为70.69%, 80.63%,对D的抑制率分别为58.87%, 62.02%。由于1e和2e表现出良好的抑菌活性,故进一步测定了他们对C和D的EC50值。结果表明,1e和2e对C的EC50分别为4.5 mg·L-1, 8.6 mg·L-1,对D的EC50分别为11.7 mg·L-1, 14.3 mg·L-1。1e和2e对D的EC59均优于阳性对照药多灵多(对C和D的EC50分别为1.6 mg·L-1, 33.4 mg·L-1)。

表3 1~3的抑菌活性*Table 3 Antifungal activities of 1~3
*c0.02 mg·mL-1; A:水稻纹枯病菌; B:小麦赤霉病菌; C:苹果腐烂病菌; D:葡萄黑豆病菌
3 结论
设计并合成了5个新型的2-硝基亚氨基咪唑烷衍生物(1a~1e)和10个新型的2-氰基亚氨基-1,3-噻唑烷衍生物(2a~2g和3a~3c)。生物活性测试结果表明,在浓度为20 mg·L-1时,除3a和3b外,其余化合物对水稻纹枯病菌,小麦赤霉病菌,苹果腐烂病菌和葡萄黑豆病菌均有一定的抑菌活性。其中1e和2e具有抗菌农药的开发潜力,与其他2-硝基亚氨基咪唑烷类和N-氰基噻唑烷类衍生物比较,卤素原子可能是影响该类化合物抗真菌活性的重要因素。1d和2d都含有一个溴原子,1e和2e含有三个氯原子。另外,1e和2e中均含有额外的一个吡唑环,这也可能是其活性高于其他衍生物的重要因素。以上构效关系的初步讨论将有助于此类抑菌活性更高的化合物的设计与合成。目前,基于1e和2e的化合物的结构修饰与合成的研究正在进行当中。
[1] Agrios G N. Significance of Plant Diseases[M].In Plant Pathology,4th ed.San Diego:Academic Press,1997.
[2] Lee S E, Kim J E, Lee H S. Insecticide resistance in increasing interest[J].Agric Chem Biotechnol,2001,44(1):105-112.
[3] Benner J P. Pesticidal compounds from higher plants[J].Pestic Sci,1993,39:95-102.
[4] Swain T. Secondary compounds as protective agents[J].Annu ReV:Plant Physiol,1977,28:479-501.
[5] 马青,崔鸿文,仇贵生. 速保利防治黄瓜白粉病效果研究[J].西北农业大学学报,1997,25(1):36-40.
[6] 司乃国,张宗俭,刘君丽,等. 创制杀菌剂啶菌恶唑生物活性及应用研究(1)—番茄灰霉[J].农药,2004,43(1):16-18.
[7] Charles D H, Kenneth W.C-alkylation andO-alkylation in the synthesis of substituted furioic acids[J].J Am Chem Soc,1948,70:739-741.
[8] 周丽,高飞,滕云,等. 17种高原草地有毒植物对植物病原真菌生物活性的初步研究[J].四川大学学报:自然科学版,2008,45(1):215.
[9] 张宗俭. 创制农药的开发及生物活性筛选的原则和方法[C].第四届全国青年植物保护科技工作者学术研讨会,大连:中国科学技术出版社,2003.
