改性炭对磺胺甲噁唑的吸附及解吸特性
2012-11-14万俊力邓慧萍
万俊力,邓慧萍
(同济大学 长江水环境教育部重点实验室,上海 20009)
最近研究报道[1-5],在水源水和饮用水中检测到了抗生素、抗惊厥抗抑郁药物、解热和非甾体消炎药、血脂调整剂、β-阻滞剂等环境药物的存在,其质量浓度一般为ng·L-1水平。该类污染物的化学性质较为稳定,传统生物处理工艺[6]及常规给水处理工艺(包括混凝、沉淀、砂滤等)对其去除效果较差[7-9];加氯等氧化工艺对环境药物有一定的降解作用,但易产生消毒副产物[10];膜技术、高级氧化以及活性炭吸附能有效或高效去除环境药物[11]。由于活性炭的强吸附性能和环境药物的疏水性作用,环境药物能够被有效吸附去除,且不产生副产物[12-13]。磺胺甲噁唑(SMZ)作为一种重要的磺胺类医药化合物,是日常生活中最常用的一类抗生素[14],在水环境中检出频率很高[2,4,7],并且有研究者提出磺胺甲噁唑(SMZ)可以作为评估污水处理和给水处理水质质量的指示性痕量污染物[15]。笔者针对目前广泛存在的水环境中抗生素等环境药物的残留问题,以商品活性炭为载体,分别制得负载锰氧化物MnOx和FeOx的活性炭,探讨了其对磺胺甲噁唑(SMZ)的吸附及解吸特性。
1 实验部分
1.1 材料
磺胺甲噁唑(SMZ)购于sigma公司。乙腈、甲酸为色谱纯;乙醇、硝酸铁、高锰酸钾盐酸、氢氧化钠和碳酸氢钠均为分析纯;煤质颗粒活性炭(8~20目)购自上海活性炭厂。实验用水为Milli-Q超纯水仪制备。
将煤质颗粒活性炭置于0.01mol/L的HNO3溶液中浸洗12~15h,抽滤后用去离子水洗涤,再用去离子水煮沸2~3h后漂洗至pH值为中性,在110℃下烘干备用[16],记为AC-0。将5gAC-0加入到15mL的1g/L的Fe(NO3)3·9H2O溶液中,搅拌均匀后室温下放置24h,然后在60℃水浴中熟化12h,用去离子水反复洗涤产物,室温下真空干燥24h备用[17],记为 AC-Fe。将5克 AC-0加入到40mL的0.02mol/L的KMnO4溶液中,搅拌均匀后沸腾回流30min,冷却后将活性炭分离出来,用去离子水洗至无MnO2的颜色为止,然后在105℃干燥至恒重备用[18],记为AC-Mn。
1.2 实验方法
SMZ的HPLC仪器测定条件为:Agilent 1200型高效液相色谱仪,配置DAD(G1315D)紫外检测器和LC 3D化学工作站。色谱操作条件为[19]∶CNWSIL C18色谱柱(250mm×4.6mm,5μm);流动相A为乙腈,流动相B为水(含0.1%甲酸),等度条件为A:B=30∶70;流动相流速为1.0mL/min,柱温30℃,紫外检测波长为265nm;该色谱条件下SMZ保留时间为10.5min。
目标污染物SMZ在3种活性炭上的吸附动力学、吸附等温线以及解吸行为由序批式实验确定。吸附动力学实验:将AC-0、AC-Fe和AC-Mn各1g分别置于含250mL浓度为30mg/L的SMZ溶液的锥形瓶中,溶液初始pH值为7.0±0.1,在25℃恒温下于150r·min避光振荡,每隔一定时间取样测定SMZ浓度。吸附等温线实验:SMZ的初始浓度范围为0~50mg/L,初始pH值为7.0±0.1,在25℃恒温下于150r/min避光振荡24h,测定溶液中SMZ的残留浓度。解吸实验:将吸附等温线实验后的吸附剂在室温下真空干燥24h后,加入10mL用于测定SMZ浓度的HPLC流动相(A∶B=30∶70),超声萃取10min后0.22μm有机膜过滤,测定滤液中SMZ的浓度。
2 结果与讨论
2.1 改性炭的表征
改性炭的比表面积和孔容由比表测定仪测定,结果列于表1。由表1可知,改性炭AC-Fe、AC-Mn的比表面积和平均孔容随活性炭负载金属氧化物含量的增加而减少。铁、锰氧化物的存在并未堵塞活性炭的孔隙,对平均孔径影响不大,其存在造成了改性炭材料比表面积和平均孔容的下降,但下降幅度不大。
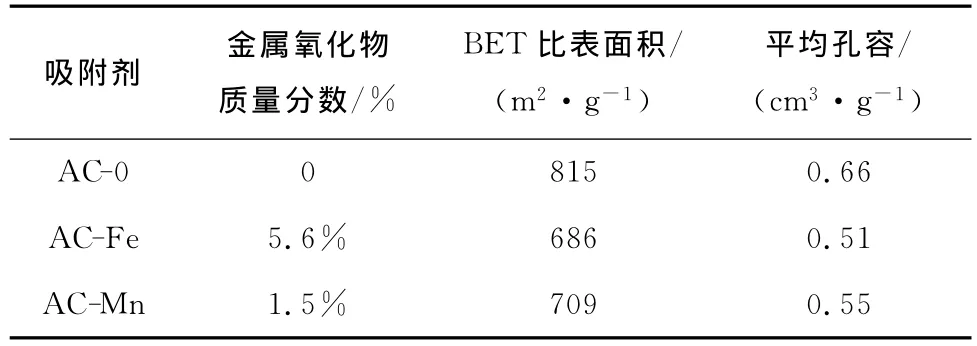
表1 改性炭的BET比表面积和平均孔容
采用Nicolet 5700智能傅里叶红外光谱仪对活性炭和改性炭进行400~4000cm-1范围的红外光谱扫描,图1为AC-0、AC-Fe和AC-Mn的红外谱图。由谱图分析可知,3种活性炭表面有丰富的含氧官能团,1515cm-1处有C== O键的吸收峰,962cm-1处有C—O键伸缩振动吸收峰,3400cm-1和1600cm-1附近出现—OH吸收峰,表明是以物理吸附水形式存在于材料中的羟基。而AC-Fe在1380cm-1处出现—OH吸收峰,则是以化学吸附水的形式存在于材料中的羟基,1114cm-1、1050cm-1和974cm-1处的吸收峰对应为Fe—O键,说明活性炭上负载的铁氧化物为水合氧化铁。AC-Mn的红外谱图中,775cm-1、518cm-1和467cm-1处的吸收峰对应为二氧化锰的Mn—O键特征吸收峰,两种改性炭在各自的Fe—O键、Mn—O键特种吸收峰强度较低是因为样品负载的金属氧化物质量百分比较低。

图1 AC-0、AC-Fe和 AC-Mn的IR谱图
2.2 吸附性能
通过吸附前后溶液中SMZ的浓度之差计算得到SMZ在活性炭上的吸附量,同时采用不同动力学方程和等温吸附方程进行拟合,结果如图2、图3所示。
2.2.1 吸附动力学
为确定 AC-0、AC-Fe和 AC-Mn吸附去除水中SMZ的速率,进行了动力学实验。结果如图2所示:初始阶段,SMZ在AC-0、AC-Fe和 AC-Mn上的吸附比较迅速,8h的吸附量分别是平衡吸附量的98.5%、93.5%和95.8%;8h后吸附很缓慢。这表明与原活性炭相比,改性炭对SMZ的吸附速率并没有多大变化。基于动力学结果,在其他序批式实验中,24h混合可以使吸附反应充分到达平衡。

图2 活性炭和改性炭吸附去除水中SMZ的动力学
采用拟一级和拟二级动力学模型拟合3种活性炭对SMZ的吸附速率曲线,AC-0、AC-Fe和 AC-Mn在相同条件下的吸附动力学模型的各参数见表2,两个动力学模型分别线性化为:
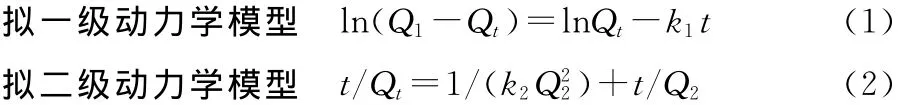
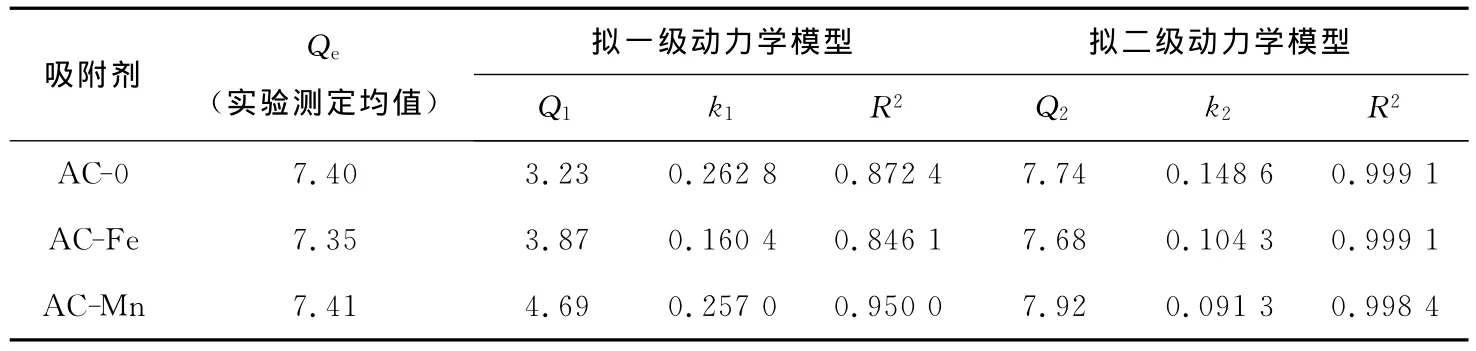
表2 吸附动力学模型的拟合参数
式(1)和(2)中,Qt(mg·g-1)表示t时刻吸附量,k1(min-1)和k2(g·mg-1·min-1)分别为拟一级和拟二级速率参数,Q1(mg·g-1)和Q2(mg·g-1)为平衡吸附量。
由表可见,3种活性炭的吸附动力学实验数据均与拟二级动力学模型拟合最优(R2>0.99),并且拟二级动力学模型计算所得平衡吸附量与实验测定值更为接近。一般拟一级动力学模型只能应用于吸附过程的初始阶段,而二级动力学模型假定限速步骤可能为化学吸附[20]。因此,可推测AC-0、AC-Fe和AC-Mn对SMZ的化学吸附是影响其吸附速度的重要因素之一。
2.2.2 吸附等温线
不同活性炭对SMZ的吸附等温线通常可用下列非线性等温吸附模型定量描述:

由式(3)可知,当1/n等于1时,方程为Langmuir模型;当Ce或klf趋近于0时,方程为Freundlich模型。式(3)~(5)中,Qe是吸附平衡时活性炭的吸附量(mg·g-1),Ce为液相平衡质量浓度(mg·L-1),Qm是SMZ以单分子层吸附时最大吸附量(mg·g-1);1/n为吸附指数,表征吸附等温线偏离线性吸附的程度以及吸附机理的差异;klf、kf和kl为吸附系数,代表吸附能力的大小。
用吸附等温线确定SMZ在 AC-0、AC-Fe和 AC-Mn上的吸附量,分别用Langmuir-Freundlich、Freundlich和Langmuir模型对实验数据进行拟合,结果如图3所示。通过拟合曲线计算可得相关等温吸附方程参数(见表3)。
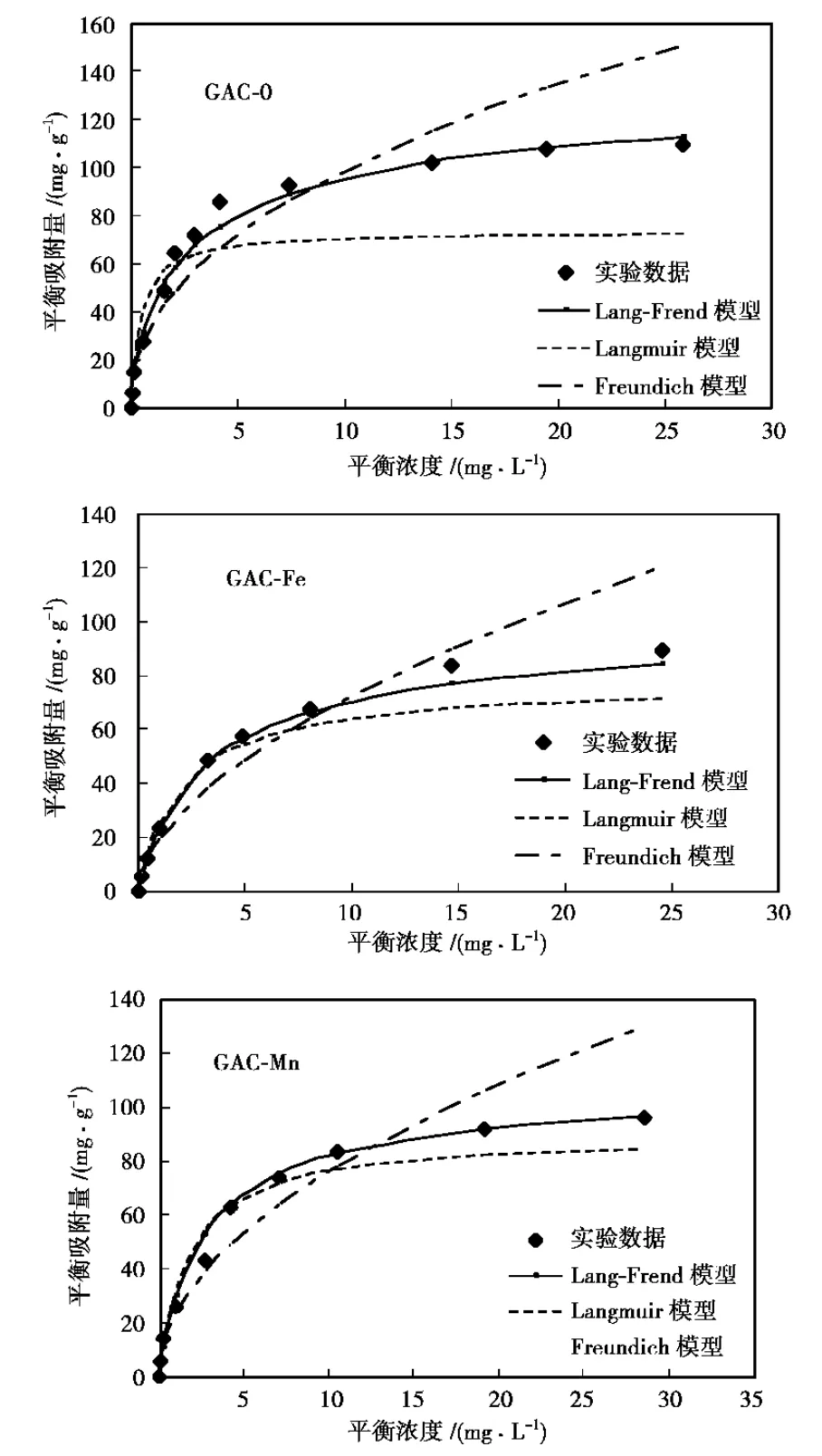
图3 SMZ在活性炭和改性炭上的吸附等温线
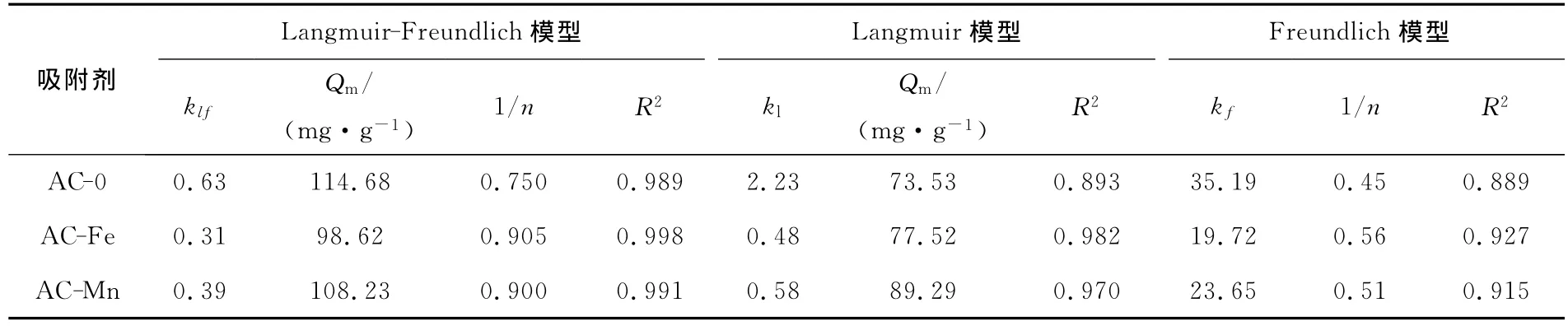
表3 吸附等温线模型的拟合参数
比较3种模型的拟合结果可知,单纯使用Freundlich模型对实验数据进行拟合时效果较差,这是因为Freundlich模型的应用范围广,对于多种吸附剂,在较宽的温度范围内都适用,但是该模型对吸附过程描述的准确性较差。Langmuir模型的拟合效果优于Freundlich模型,但在吸附质高浓度下与实验数据有一定偏差,这是因为吸附质分子浓度增大时,吸附剂表面上已吸附的分子间相互作用更加明显,因而需要进行修正。Langmuir-Freundlich模型在Langmuir模型的基础上,考虑吸附质分子之间的作用力,对吸附指数进行修正,经验证该模型与实验数据的吻合性最好,相关系数R2均大于0.985,优于其他两种模型拟合的结果。因此,认为SMZ在活性炭和改性炭上的吸附行为符合Langmuir-Freundlich模型。
拟合参数中3种活性炭的kl和kf值有偏差,说明3种活性炭对SMZ的吸附能力存在一定差异,SMZ在3种活性炭中kl和kf值的大小依次为:AC-0>AC-Mn>AC-Fe。由于溶液中固体表面吸附包括吸热和放热的物理化学过程,Langmuir等温吸附模型中的kl值是固体表面吸附溶质时与结合能有关的参数,由kl>0可以看出,活性炭和改性炭对SMZ的吸附为吸热过程。此外,SMZ在3种活性炭上的1/n均小于1,吸附的非线性说明在吸附过程中SMZ与活性炭之间还存在着其他的相互作用。例如,活性炭中的极性基团(酚羟基和羧基等)和三维孔隙能够与磺胺类药物SMZ通过氢键作用和范德华作用键合。Langmuir-Freundlich模型可以描述溶液中固体表面等温吸附的全部过程,其参数Qm能很好地预测SMZ的理论饱和吸附量。由Langmuir-Freundlich模型计算得到了SMZ在3种活性炭上的最大吸附量Qm,大小依次为:AC-0>AC-Mn>AC-Fe,其大小次序与kl和kf值的大小顺序一致。3种活性炭的Qm值的排序表明,活性炭负载金属氧化物以后吸附容量降低,这与改性炭比表面积和平均孔容的降低有关。但是,AC-Mn和AC-Fe的理论Qm值分别是 AC-0的94.4%和86.0%,而 AC-Mn和 AC-Fe中AC-0的质量分数分别为98%和94%,这表明改性炭的主体吸附部分——活性炭的吸附性能下降幅度不大,即金属氧化物的存在对活性炭的吸附行为影响甚微。
2.3 化学洗脱作用下活性炭的解吸
SMZ在活性炭上的吸附主要基于物理和化学吸附作用,同样地,如果采用一定量用于测定SMZ浓度的HPLC流动相使活性炭上的SMZ被洗脱下来,则能够达到解吸的目的。表4显示了化学洗脱作用下SMZ的解吸情况,图4为洗脱溶液的HPLC-DAD色谱图。

表4 活性炭和改性炭上SMZ解吸的效果
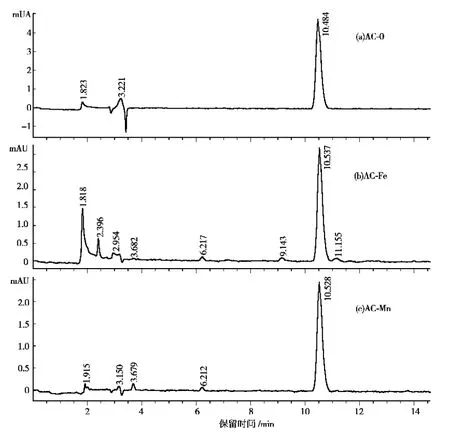
图4 活性炭和改性炭上SMZ及其产物的DAD色谱图
由表可知,SMZ的解吸效率随着活性炭和改性炭吸附量的增大而增大,其原因在于初始吸附的SMZ不仅在活性炭和改性炭表面结合较牢固,而且向内部迁移,因而不易被其他离子取代,而活性炭和改性炭表面被SMZ完全占据后,吸附作用愈来愈弱,结合不甚牢固,因此后吸附的SMZ容易被洗脱。同时流动相对AC-0上SMZ的解吸效果较好,在不同SMZ初始浓度下其解吸效率均高于AC-Fe和AC-Mn。一方面,由于改性炭上负载的MnOx和FeOx可能与SMZ发生表面络合作用,这就决定了其对SMZ的化学吸附能力增强,脱附自然比较困难;另一方面,锰氧化物是自然界中最为重要的非生物氧化剂[21-22],并且Fe(Ⅲ)和 Mn(Ⅳ)的氧化物能缓慢氧化降解水中的抗生素药物[23,24]。如图4所示,DAD色谱图(b)和(c)除了检测到SMZ(10.5min)外,还在2.4、3.7、6.2、9.1和11.2min等处出峰。可推测吸附到改性炭MnOx和FeOx表面的SMZ与之形成表面络合物,然后在表面络合物结构内发生电子转移传递过程,进行氧化还原反应,部分SMZ被氧化降解。
3 结 论
1)铁、锰氧化物的存在对活性炭的比表面积和平均孔容影响较小,制备的改性炭仍具有很大的比表面和孔容,金属氧化物的存在对活性炭吸附水中SMZ的性能影响甚微。SMZ在AC-0、AC-Fe和AC-Mn上的吸附动力学符合拟二级动力学方程,Freundlich、Langmuir和 Langmuir-Freundlich吸附等温模型均可拟合3种活性炭对SMZ的吸附,其中Langmuir-Freundlich等温吸附模型拟合最优。
2)与 AC-Fe和 AC-Mn相比,AC-0上吸附的SMZ更容易解吸。改性炭负载的金属氧化物可能与SMZ发生表面络合作用,这有助于增强改性炭对SMZ的化学吸附。此外,改性炭中的MnOx和FeOx可以有效促进吸附到其表面的残留抗生素类药物SMZ的降解消除过程,克服了活性炭仅能对SMZ起单一吸附作用的缺点。
[1]Jones O A,Lester J N,Voulvoulis N.Pharmaceuticals:a threat to drinking water?[J]Trends in Bioteachnology,2005,23(4):163-167.
[2]Mompelat S,Bot B L,Thomas O.Occurrence and fate of pharmaceutical products and by-products,from resource to drinking water[J].Environment International,2009,35(5):803-814.
[3]Maria H F,Maria T G,Francesc V.Occurrence and removal of pharmaceuticals and hormones through drinking water treatment[J].Water Research,2011,45(3):1432-1442.
[4]Wang C,Shi H L,Adams C D,et al.Investigation of pharmaceuticals in Missouri natural and drinking water using high performance liquid chromatography-tandem mass spectrometry[J].Water Research.2011,45(4):1818-1828.
[5]Yi R H,Wang Q J,Mo C H,et al.Determination of four fluoroquinolone antibiotics in tap water in Guangzhou and Macao [J]. Environmental Pollution,2010,158 (7):2350-2358.
[6]Heberer T.Tracking persistent pharmaceutical residues from municipal sewage to drinking water[J].Journal of Hydrology,2002,266(3/4):175-189.
[7]Stackelberg P E,Furlong E T,Meyer M T,et al.Persistence of pharmaceutical compounds and other organic wastewater contaminants in a conventional drinking-water-treatment plant[J].Science of the Total Environment,2004,3291(1/2/3):99-113.
[8]Stackelberg P E,Gibs J,Furlong E T,et al.Efficiency of conventional drinking-water-treatment processes in removal of pharmaceuticals and other organic compounds[J].Science of the Total Environment,2007,377(2/3):255-272.
[9]Adams C,Wang Y,Loftin K,et al.Removal of antibiotics from surface and distilled water in conventional water treatment processes[J].Journal of Environmental Engineering,2002,128(3):253-260.
[10]Shen R Q,Andrews S A.Demonstration of 20pharmaceuticals and personal care products(PPCPs)as nitrosamine precursors during chloramine disinfection[J].Water Research.2011,45(2):944-952.
[11]Homem V,Santos L.Degradation and removal methods of antibiotics from aqueous matrices:a review [J].Journal of Environmental Management,2011,92(10):2304-2347.
[12]Snyder S A,Adham S,Redding A M,et a1.Role of membranes and activated carbon in the removal of endocrine disruptors and pharmaceuticals[J].Desalination,2007,202(1/2/3):156-181.
[13]Kim S H,Shon H K,Ngo H H,et al.Adsorption characteristics of antibiotics trimethoprim on powered and granular activated carbon [J].Journal of Industrial and Engineering Chemistry,2010,16(3):344-349.
[14]Yangali-Quintanilla V,Sadmani A,McConville M,et al.Rejection of pharmaceutically active compounds and endocrine disrupting compounds by clean and fouled nanofiltration membranes[J].Water Research,2009,43(9):2349-2362.
[15]Dickenson E R V,Snyder S A,Sedlak D L,et al,Indicator compounds for assessment of wastewater effluent contributions to flow and water quality [J].Water Research,45(3):1199-1212.
[16]谢明,徐炎华.载铁活性炭对水中草甘膦吸附性能研究[J].中国环境科学,2011,31(2):239-244.XIE Ming,XU Yanhua.Glyphosate adsorption by ferric supported active carbon[J].China Environmental Science,2011,21(2):239-244.
[17]Jang M,Chen W,Cannon F S.Preloading hydrous ferric oxide into granular activated carbon for arsenic removal[J].Environmental Science & Technology,2008,42 (9):3369-3374.
[18]赵梅青,马予川,张立艳,等.高锰酸钾改性对活性炭吸附Cr(Ⅲ)的影响[J].中国给水排水,2010,26(13):71-73,77.ZHAO Meiqing,MA Yuchuan,ZHANG Liyan,et al.Effect of modification of activated carbon with KMnO4on Cr(Ⅲ)adsorption[J].China Water & Wastewater,201026(13):71-73,77.
[19]Ma M,Cheng Y,Xu Z,et al.Evaluation of polyamidoamine(PAMAM)dendrimers as drug carriers of anti-bacterial drugs using sulfamethoxazole(SMZ)as a model drug[J].European Journal of Medicinal Chemistry,2007,42(1):93-98.
[20]Kumar Y P,King P,Prasad V S.Equilibrium and kinetic studies for the biosorption system of copper(II)ion from aqueous solution using Tectona grandis L.f.leaves powder[J].Journal of Hazardous Materials,2006,137(2):1211-1217.
[21]Risser J A,Bailey G W.Spectroscopic study of surface redox reactions with manganese oxides[J].Soil Science Society of America Journal,1992,56:82-88.
[22]Zhang H,Huang C H.Oxidative transformation of triclosan and chlorophene by manganese oxides [J].Environmental Science & Technology,2003,37(11):2421-2430.
[23]Feitosa-Felizzola J, Hanna K, Chiron S. Adsorption and transformation of selected human-used macrolide antibacterial agents with iron(III)and manganese(IV)oxides [J].Environmental Pollution,2009,157(4):1317-1322.
[24]Zhang H,Huang C H.Reactivity and transformation of antibacterial N-oxides in the presence of manganese oxide[J].Environmental Science & Technology,2005,39(2):593-601.
