N(2羧酸基)2芳氧基烟酰胺的合成研究
2012-11-10胡景城周梦成刘永鹏左双全龚银香长江大学化学与环境工程学院湖北荆州434023
胡景城,周梦成,刘永鹏,叶 茂,左双全,杨 惠, 龚银香(长江大学化学与环境工程学院,湖北 荆州 434023)

胡景城,周梦成,刘永鹏,叶 茂,左双全,杨 惠, 龚银香(长江大学化学与环境工程学院,湖北 荆州 434023)
采用活性基团拼接的方法,首先由3-氰基-2-氯吡啶经醚化和水解合成了中间体芳氧基烟酸,再由芳氧基烟酸经酰氯化和酯化,再与氨基酸作用,得到3种未见文献报道的芳氧烟酰胺类化合物。采用红外光谱和核磁共振氢谱表征了目标化合物的结构,同时对中间体芳氧基烟酸及目标化合物的合成条件进行了探讨。
芳氧基烟酸; 氨基酸; 酰胺; 合成
酰胺类除草剂是一类具有多作用靶点性质的农用化学品,在现代农田化学除草剂中占重要地位[1-4]。氨基酸结构及其衍生物具有很好的生物活性[5],在绿色农药创新中有着重要的作用,已成为新农药研究的热点[6]。为了寻找具有新颖结构的新农药候选品种,笔者采用活性基团拼接的方法[7-8],用3-氰基-2-氯吡啶合成出相应的芳氧烟酸,再将芳氧烟酸与一系列氨基酸作用,得到3个未见文献报道的含氨基酸结构的芳氧烟酰胺类化合物。其合成路线如图1所示。

图1 合成路线
1 试验部分
1)仪器与试剂 美国Brucker AV 300型核磁共振仪,TMS为内标, CDCl3为溶剂;美国NICOLET6700FTIR锗镜面红外光谱仪;WRS-1A数字熔点仪(温度计未校正) ;3氰基-2-氯吡啶(工业品,购自青州市奥星化工有限公司,未纯化); NaH(60%); 其他所用药品均为分析纯。
2)芳氧烟酸的合成 在N2保护的条件下,在三口烧瓶中加入40ml DMF和2.04g(60%,0.051mol)的NaH,搅拌成均相。再分2次加入4.48ml(0.051mol)的邻甲酚,有气泡生成,搅拌均匀后再加入7.0g 0.051mol的3-氰基-2-氯吡啶,在90~100℃反应4h。停止反应,冷却后加入200ml水,有大量灰色絮状固体生成。抽滤,水洗。滤饼放入100ml 烧瓶中,加稀盐酸调节pH值至3~4,加热回流3h,得絮状粗产品。用乙醇重结晶得纯品Ⅰ1,熔点183~ 184℃。
用类似的方法制备其他芳氧烟酸Ⅰ2和Ⅰ3,其熔点分别为202~204℃和155~157℃。
3)芳氧烟酸的酰氯化和酯化 将0.05mol芳氧基烟酸置于圆底烧瓶中,加入30ml 二氯亚砜,电磁搅拌回流3~4h,减压蒸出过量的二氯亚砜,所得产物用二氯甲烷溶解转移到50ml圆底烧瓶中,再加入10ml(过量)无水乙醇,加热回流30min,用吸收装置吸收反应产生的HCl气体。产品转移到分液漏斗中,待用。
4)氨基酸的碱化 将0.05mol氨基酸置于圆底烧瓶中,加入6ml二氯甲烷,再加入10ml 0.01mol NaOH溶液,搅拌0.5h,待用。
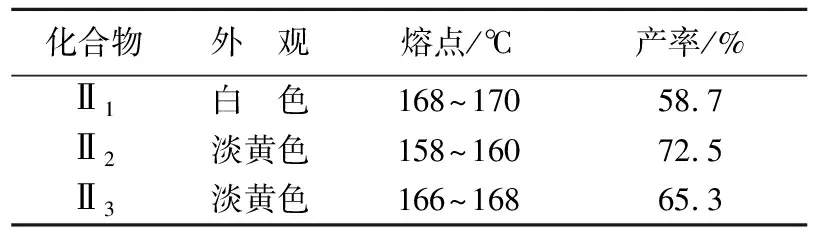
表1 目标化合物的物理常数
5)目标化合物的合成 将分液漏斗中的酯缓慢滴加到装有碱化的氨基酸的圆底烧瓶中,室温下搅拌0.5h,再升温至90℃,加热回流1h。停止反应,冷却,分液得水层,再酸化,抽滤,水洗得粗产品。用乙醇重结晶,得芳氧烟酰胺纯品。目标化合物溶于乙醇、DMF及NaOH溶液之中。目标化合物的物理性质见表1。
2 结果与讨论


表2 目标化合物的IR测试数据

表3 目标化合物的1HNMR数据
在1HNMR谱图中,酰胺 NH的化学位移值位于6.3~6.7之间。由于环上氮原子和羧基的强吸电子作用,吡啶环上各氢原子的共振吸收位于低场。连有氮原子和羧基的亚甲基因为诱导效应的影响,其氢原子的共振吸收向低场移动。而羧基结构中的活泼氢在1HNMR谱图中未见明显吸收峰,这可能是因为有形成分子内氢键的倾向而使氢原子位置不确定的缘故。这种情况与文献[9]报道的一致。
2)关于中间体芳氧烟酸的制备 笔者曾经参照文献[10-11] ,以2-氯烟酸和苯酚为原料,在碱性条件下直接合成芳氧烟酸。但该反应中因羧基负离子吸电子能力不强,在吡啶环上进行亲核取代反应较困难,不仅要求反应温度高,反应时间长,且反应产率非常低。以3-氰-2-氯吡啶为反应底物,通过NaH碱化酚后反应,首先制得2-芳氧基-3-氰吡啶,再经水解制得芳氧烟酸。由于—CN的吸电子能力较强,芳氧基引入吡啶环较容易,这样,尽管多了水解步骤,但实际上反应时间缩短,反应产率也大大提高了。
3)关于目标化合物的制备 将芳氧烟酸酯化的目的是为了提高酰胺化反应的选择性。若直接用酰氯与碱化氨基酸作用,则因为酰氯过于活泼而可能发生水解等副反应。将酰氯酯化后,因酯的反应活性差,此时只有进攻能力强的氨基可顺利反应,从而减少副反应发生的几率。
[1] Frank J V,Thomas A W,Elizabeth A W, et al. Benzopyranopyridine derivatives.1.aminoalkyl derinatives of the azaxanthenes as bronchodilating agents[J].Journal of Medicinal Chemistry ,1975,18(1):1-8.
[2]Goro A, Gerald B, Edward L M.Nitroheterocyclic antimicrobial agents.Ⅱ.5-Nitro-1, 3, 4-thiadiazole-2-carboxaldehyde derivatives[J].Journal of Medicinal Chemistry, 1970, 13(5):1015-1017.
[3]宋新建,谭小红,汪焱钢.5-吡啶基-2-芳酰胺基-1,3,4-噻而唑的合成及生物活性[J].华中师范大学学报(自然科学版),2005,39(3):340-342.
[4]王子云,张正文,陈传兵,等.N-[(2-羧基-1,3,4-噻二唑)-5-基]-N’-芳酰基硫脲的合成与表征[J].华中师范大学学报(自然科学版),2006,40(1):52-54.
[5]马大为.氨基酸衍生物的反应、合成和生物活性的研究[J].有机化学,2001,21(11):842-849.
[6]王正刚.含硫氨基酸衍生物的研究进展[J].氨基酸和生物资源,2001,23(1):38-41.
[7]李志芬,张敏,崔丽英,等.含吡啶环的[1,3,4] 噁二唑类化合物的合成及表征[J]. 有机化学,2008,28(3):479-483.
[8]Cordia A, Lacoste J M, Duhaul T J, et al. Synthesis of 1,2-diacyl-3-nicotinoyl glycerol derivatives and evaluation of their acute effects on plasma lipids in the rat[J]. Arzeim ittel for Schung ,1995, 45(9):997-1001.
[9]杨亚军,马康,刘军,等.2-呋喃甲酰基甲基丙氨酸的合成[J]. 化学试剂,2011,33(4): 297-298.
[10] Fredric J. Vinick, Nicholas A. Saccomano,et al.Nicotinamide Ethers: Novel Inhibitors of Calcium-Independent Phosphodiesterase and [3H] Rolipram Binding[J]. Med Chem,1991, 34: 86-89.
[11]顾群,张晓进.吡啶酰胺类除草剂——吡氟酰草胺[J].现代农药,2010,9(1):42-45.
[编辑] 洪云飞
10.3969/j.issn.1673-1409(N).2012.04.004
O626.5
A
1673-1409(2012)04-N011-02
2012-02-03
湖北省教育厅重点项目(B200612010);国家大学生创新性实验项目(091048916;101048920)。
胡景城(1989-),男,2008年大学入学,现主要从事应用化学方面的学习。
龚银香(1965-),男,1986年大学毕业,硕士,教授,现主要从事精细化学品合成方面的教学与研究工作;E-mail:gongyinxiang@sohu.com。
