四丁基溴化铵水合物储存氢气的研究
2012-11-09谢应明龚金明刘道平祁影霞
谢应明,龚金明,汤 涛,刘道平,刘 妮,祁影霞
(上海理工大学 能源与动力工程学院,上海 200093)
研究与开发
四丁基溴化铵水合物储存氢气的研究
谢应明,龚金明,汤 涛,刘道平,刘 妮,祁影霞
(上海理工大学 能源与动力工程学院,上海 200093)
利用高压搅拌式水合物实验装置,进行了四丁基溴化铵(TBAB)水合物储氢的研究。在恒容条件下,考察了水浴温度、初始压力对水合物储氢特性的影响,并比较了 TBAB 水合物和四氢呋喃(THF)水合物的储氢性能。实验结果表明,在初始压力 7.2 MPa、x(TBAB)=0.6% 的条件下, 水浴温度越低,生成水合物的诱导时间越短,储氢密度越大,水浴温度为 0.5 ℃ 时储氢密度最大(为0.095%);在水浴温度 0.5 ℃、x(TBAB)=0.6% 的条件下,初始压力越大,生成水合物的诱导时间越短,储氢密度越大,在初始压力为 8.4 MPa 时储氢密度最大(为0.109%);在水浴温度为 0.5℃、初始压力 7.2 MPa 的条件下,THF 水合物的储氢密度仅为 0.014%,远低于 TBAB 水合物的储氢密度(0.095%),TBAB 水合物的储氢性能更好。
四丁基溴化铵水合物;储氢;四氢呋喃
氢能作为一种清洁的新型能源,具有如下优点:氢气燃烧释能后的产物是水,无任何污染;氢气的来源广泛,既可以来自化石燃料转换,也可以来自由太阳能或风能分解水,是可再生能源;氢气具有很高的燃烧热值,燃烧1 kg 氢气相当于 3 kg 汽油或 4.5 kg 焦炭完全燃烧所释放的热量[1]。
目前,储氢技术是氢能发展的主要瓶颈。由于传统的高压气态储氢、低温液态储氢难以满足使用要求[2],人们研究了多种新型储氢方法,其中水合物储氢作为一种非常有前景的新型储氢方法,得到了广泛的重视和研究[3-9]。但由于采用水合物储氢的技术还只是处于起步的研究阶段,不同的研究结果有很大的差异,目前水合物储氢密度还达不到实用的标准,所以有必要进一步开展水合物储氢的研究[10]。
本工作利用自行设计的高压搅拌式水合物实验装置,在定容条件下考察了初始压力、水浴温度对四丁基溴化铵(TBAB)水合物储氢的影响,并与四氢呋喃(THF)水合物的储氢性能进行了对比。
1 实验部分
1.1 实验装置
高压搅拌式水合物的实验装置见图1。装置主要由反应釜、活塞容器、手动泵、水浴和气瓶等组成。反应釜材质为 316L不锈钢,有效容积为502.4 mL,设计最高工作压力 60 MPa,工作温度-20~30 ℃。反应釜内置温度、压力传感器,分别测量水合物生成过程中温度、压力的变化,温度和压力信号由 Agilent 34970A 数据采集仪采集,并记录在计算机中。
氢气:纯度不小于 99.999%,上海伟创标准气体有限公司;TBAB:纯度不小于 99.0%,江苏永华精细化学品有限公司;THF:纯度不小于 99.0%,宜兴市达华化工有限公司;二次蒸馏水:自制。
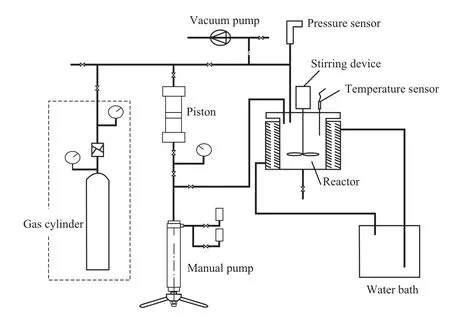
图 1 高压搅拌式水合物的实验装置Fig.1 The high pressure stirring experimental apparatus for the hydrogen hydrates.
1.2 实验方法
依据 TBAB - H2- H2O 及 THF -H2- H2O 系统的相平衡条件,在水浴温度 0. 5~ 1.5 ℃、初始压力6.0 ~ 8.4 MPa 的条件下,考察了水浴温度、初始压力对水合物储氢特性的影响。实验步骤为:(1)清洗反应釜,然后注入 270 mL 的 TBAB 溶液或 THF溶液;(2)抽真空;(3)开启数据采集系统,记录反应釜内的温度、压力;(4)充入氢气,同时开启恒温水浴和压力调节阀,设定水浴温度和初始压力;(5)记录反应过程中反应釜内的温度、压力的变化;(6)反应釜内的温度、压力恒定后停止采集数据,实验结束。
1.3 储氢密度的计算方法
水合物储氢密度以氢气在水合物中的质量分数(w)计:

式中,n1,n2分别为反应前后氢气的物质的量,mol;M为氢气的摩尔质量,取值 2.018 g/mol,m为生成的水合物的质量,g。
通过测量水合物生成前后反应釜中氢气的压力,由式(2)分别求出n1和n2。

式中,p为氢气的压力,MPa;V为反应釜体积,L;T为温度,K ;z为气体压缩因子;R为气体常数,J /(mol ·K)。
2 结果与讨论
2.1 水浴温度对 TBAB 水合物储氢特性的影响
水浴温度对 TBAB 水合物储氢特性的影响见图 2。由图 2 可见,当水浴温度为 1.5 ℃ 时,反应釜温度在整个实验过程中一直处于 1.5 ℃ 左右,变化很小,温度曲线趋于一条直线;当水浴温度为1.0 ℃时,反应釜温度在达到 1.0 ℃ 后,大约在 825 min时出现了上升的现象,并且这种现象在水浴温度为 0.5 ℃ 时表现得更为明显,只是出现的时间(水合物生成的诱导时间)提前到了 400 min。这是因为水合物的生成过程是一个放热过程,放出的热量会导致反应釜温度上升。当水浴温度为 1.5 ℃时,反应釜温度几乎没变化,说明生成的水合物很少或没有水合物生成,原因可能是过冷度不够大,水合物生长推动力较小,所以生成的水合物很少或没有生成水合物。随着水浴温度的降低,过冷度增大,水合物生长的推动力增大,此时有相对较多的水合物生成,水合反应放出的热量不能及时的通过水浴带走,因此出现了温度突然上升的现象。过冷度越大,水合物生成的诱导时间越短,生长速率也越快。
由图 2 还可见,当反应釜温度达到水浴温度后,由于发生水合反应,反应釜内的压降随水浴温度的降低而增大,即水浴温度越低,水合反应消耗的氢气越多,储氢密度越大。
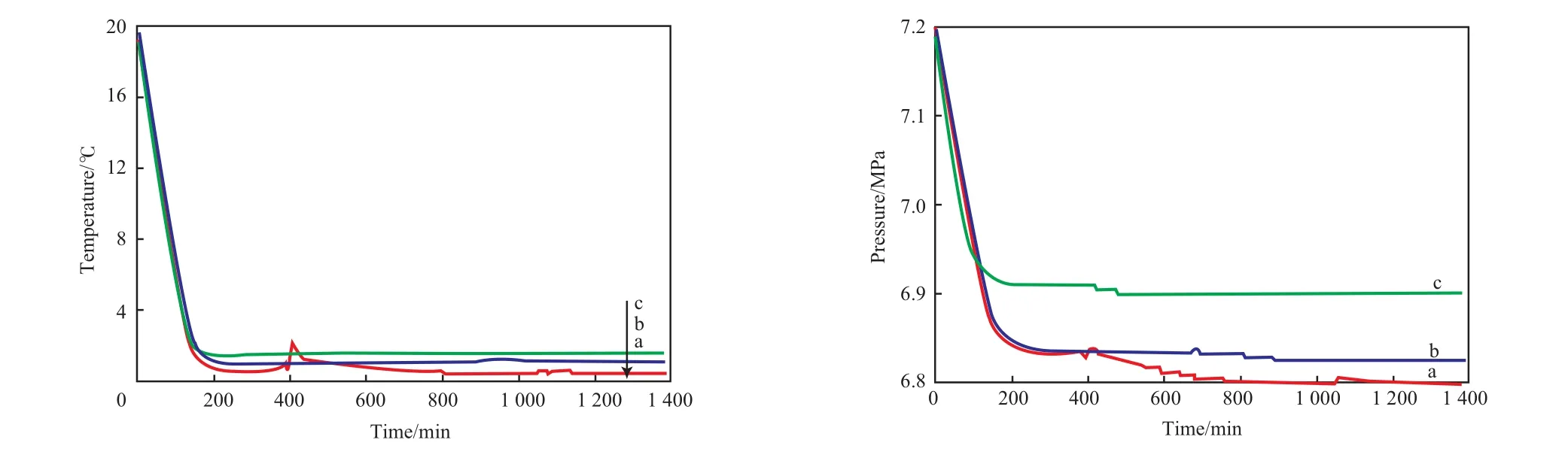
图 2 水浴温度对 TBAB 水合物储氢特性的影响Fig.2 The effects of the water bath temperature on the hydrogen storage with TBAB hydrate.
TBAB 水合物储氢的实验结果见表 1。由表 1可见,水浴温度越低,TBAB 水合物的储氢密度越大。这是因为过冷度越大,水合物生长推动力越大,水合物越容易生成,且生成量也越大[11]。
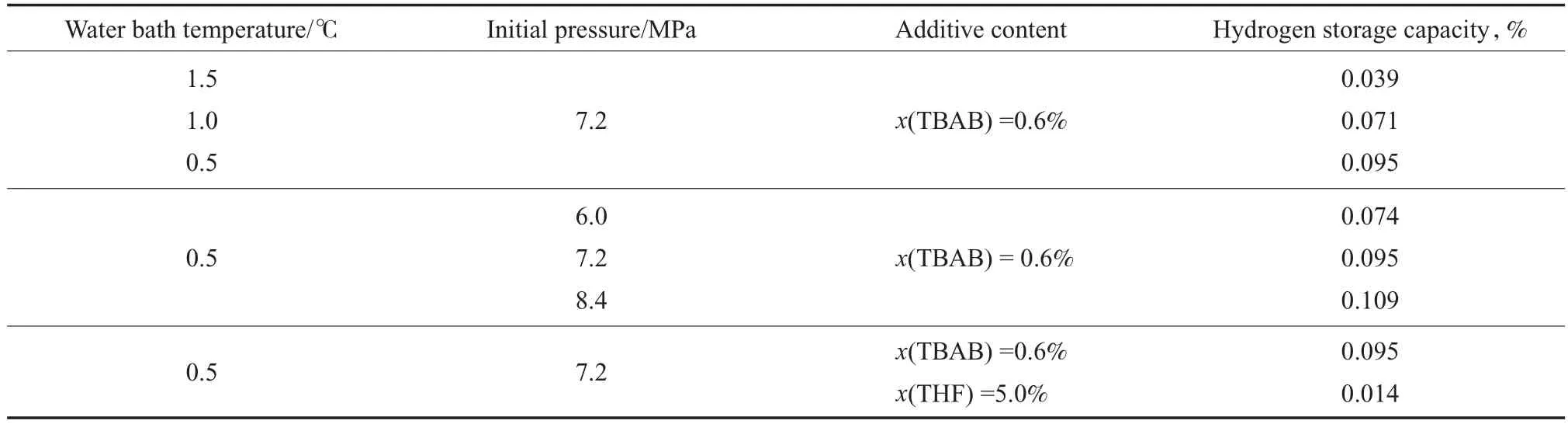
表 1 TBAB和THF水合物储氢的实验结果Table 1 The experimental results of the hydrogen storage with the TBAB and THF hydrates
2.2 初始压力对 TBAB 水合物储氢特性的影响
初始压力对 TBAB 水合物储氢特性的影响见图 3。由图 3 可见,随初始压力的提高,水合物生成的诱导时间缩短,压降也逐渐增大。这说明随初始压力的提高,水合反应愈发明显,不仅诱导时间缩短,水合物储氢密度也明显增大。由表 1 可见,随初始压力的提高,水合物的储氢密度增大。这是因为水合物的生成过程是一个边成核边生长的过程,成核和生长都需要大量的气体参与,而气体压力越高,单位体积内气体分子就越多,特别是气液界面处具有较大过饱合度的气体;而由于吸附作用,气液界面气体含量高有利于分子簇的生长[11]。所以初始压力越高,水合物生成速率越快,生成量也越大。
2.3 TBAB 水合物与 THF 水合物储氢特性的比较
氢气与纯水在 -23 ℃ 和 200 MPa 的条件下才能形成氢气水合物,所以在高于 0 ℃、低于10 MPa的条件下形成氢气水合物,就需要在水中加入辅助剂。辅助剂(THF或TBAB)分子进入水合物的大笼中,起到稳定水合物结构的作用,氢气分子则填充在水合物的小笼中,这大大降低了氢气水合物的相平衡条件,在高于 0 ℃、低于 10 MPa 的条件下,可以形成含辅助剂的水合物[12-15],从而使氢气储存在水合物中。
TBAB 水合物与 THF 水合物的储氢特性的比较见图 4。由图 4 可见,THF 水合物生成的诱导时间约为 590 min,TBAB 水合物生成的诱导时间约为 400 min;THF 水合物生成后的压降约为 0.3 MPa,TBAB 水合物生成后的压降约为 0.4 MPa。由表 1 可见,TBAB 水合物的储氢密度为 0.095%,THF水合物的储氢密度为 0.014%。因此,在同样的水浴温度、初始压力条件下,与 THF 水合物相比,TBAB水合物的生成速率更快,储氢密度更大。
图 3 初始压力对 TBAB 水合物储氢特性的影响Fig.3 The effects of initial pressure on the hydrogen storage with TBAB hydrate.
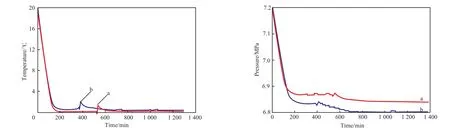
图 4 TBAB 水合物与 THF 水合物储氢特性的比较Fig.4 The comparison between hydrogen storages with TBAB hydrate and THF hydrate.
3 结论
(1)在初始压力 7.2 MPa、x(TBAB)=0.6% 的条件下,水浴温度越低,生成水合物的诱导时间越短,水合物生成速率越快,储氢密度也越大。在水浴温度为 0.5 ℃ 时,储氢密度最大,为 0.095%。
(2)在水浴温度 0.5 ℃、x(TBAB)=0.6% 的条件下,初始压力越高,生成水合物的诱导时间越短,水合物生成速率越快,储氢密度也越大。在初始压力为 8.4 MPa 时,储氢密度最大,为 0.109%。
(3)在水浴温度 0.5 ℃、初始压力 7.2 MPa 的条件下,生成 THF 水合物的的诱导时间约为 590 min ,其储氢密度为 0.014%,生成 TBAB 水合物的诱导时间约为 400 min,其储氢密度为 0.095%;与THF 水合物相比,TBAB 水合物的生成速率更快,储氢密度更大;TBAB 水合物比 THF 水合物的储氢性能更好。
[1]毛宗强. 氢能——21 世纪的绿色能源 [M].北京:化学工业出版社,2005:1 - 18.
[2]丁福臣,易玉峰.制氢储氢技术 [M].北京:化学工业出版社,2006:1243 - 2471.
[3]Strobel T A,Koh C A,Sloan E D. Hydrogen Storage Properties of Clathrate Hydrate Materials [J].Fluid Phase Equil,2007,261(1/2): 382 - 389.
[4]Ogata K ,Tsuda T,Amano S,et al. Hydrogen Storage in Trimethylamine Hydrate:Thermodynamic Stability and Hydrogen Storage Capacity of Hydrogen+Trimethylamine Mixed Semi-Clathrate Hydrate [J].Chem Eng Sci,2010,65(5):1616 -1620.
[5]Belosludov V R,Subbotin O S,Belosludov R V,et al. Thermodynamics and Hydrogen Storage Ability of Binary Hydrogen +Help Gas Clathrate Hydrate [J].Int J Nanosci,2008,8(1/2):57 - 63.
[6]Nakayama T,Tomura S,Ozaki M,et al. Engineering Investigation of Hydrogen Storage in the Form of Clathrate Hydrates:Conceptual Design of Hydrate Production Plants [J].Energy Fuels,2010,24(4):2576 - 2588.
[7]Chattaraj P K,Bandaru S,Mondal S. Hydrogen Storage in Clathrate Hydrates[J].J Phys Chem A,2011,115( 2):187 - 193.
[8]Hu Yanhang,Ruckenstein E. Clathrate Hydrogen Hydrate:A Promising Material for Hydrogen Storage [J].Angew Chem,Int Ed,2006,45(13): 2011 - 2013.
[9]邓灿,梁德青,李栋梁. 环戊烷-氢气水合物形成过程研究[J]. 石油化工,2009,38(9):951 - 956.
[10]谢应明,龚金明,刘道平,等. 一种新型储氢方法:水合物储氢的研究概况与发展方向[J].化工进展,2010,29(5):101 - 106.
[11]孙长宇,陈光进,郭天民. 水合物成核动力学研究现状 [J].石油学报,2008,22(4):82 - 86.
[12]Zhong Y,Rogers R E. Surfactant Effects on Gas Hydrate Formation [J].Chem Eng Sci,2000,55(19):4175 - 4187.
[13]Ogata K,Hashimoto S,Sugahara T,et al. Storage Capacity of Hydrogen in Tetrahydrofuran Hydrate [J].Chem Eng Sci,2008,63(23):5714 - 5718.
[14]Strobel T A,Taylor C J,Hester K C,et al. Molecular Hydrogen Storage in Binary THF-H2Clathrate Hydrates [J].J Phys Chem B,2006,110(34):17121 - 17125.
[15]Chapoy A,Anderson R,Tohidi B. Low-Pressure Molecular Hydrogen Storage in Semi-Clathrate Hydrates of Quaternary Ammonium Compounds [J].J Am Chem Soc,2007,129(4):746 - 747.
Hydrogen Storage withtetra-Butyl Ammonium Bromide Hydrate
Xie Yingming,Gong Jinming,Tang Tao,Liu Daoping,Liu Ni,Qi Yingxia
(School of Energy and Power Engineering,University of Shanghai for Science and Technology,Shanghai 200093,China)
The characteristic oftetra-butyl ammonium bromide(TBAB) hydrates for hydrogen storage was studied using experimental apparatus with high pressure stirring. The effects of water bath temperature and initial pressure on the hydrogen storage under the condition of constant volume were discussed. The characteristic of TBAB hydrates was compared with that of tetrahydrofuran(THF)hydrates. The results showed that under the initial pressure of 7.2 MPa and the TBAB solution mole fraction of 0.6%,low temperature could lead to short hydrate formation time and large hydrogen storage capacity,the largest hydrogen storage capacity was 0.095% at the water bath temperature 0.5 ℃. Under the water bath temperature of 0.5 ℃ and the TBAB solution mole fraction of 0.6%,high initial pressure could lead to short hydrate formation time and large hydrogen storage capacity,the largest hydrogen storage capacity was 0.109% at the initial pressure 8.4 MPa. Under the water bath temperature of 0.5 ℃ and the initial pressure of 7.2 MPa,the hydrogen storage capacity of THF hydrates was 0.014%,smaller than that of TBAB hydrates(0.095%).
tetra-butyl ammonium bromide hydrate;hydrogen storage;tetrahydrofuran
1000-8144(2012)01-0022-05
TQ 517
A
2011 - 08 - 05;[修改稿日期]2011 - 09 - 20。
谢应明(1976 —),男,湖北省应城市人,博士,副教授,电话 021 - 55273584,电邮 xymbox@163.com。
国家自然科学基金项目(50806050);上海市重点学科建设项目(S30503)。
(编辑 李治泉)
