新法合成绿色化工原料碳酸二甲酯—新课标高中化学内容扩展
2012-11-08朱鹏琼王明召
朱鹏琼 王明召
新法合成绿色化工原料碳酸二甲酯—新课标高中化学内容扩展
朱鹏琼 王明召
碳酸二甲酯(DMC)是合成食品添加剂、药物中间体、表面活性剂等物质的常用原料,本身无毒无害,是一种绿色化工原料。生产DMC的传统工艺是使光气和甲醇反应(如图1所示)。该工艺复杂,操作周期长,大量的副产物HCl会腐蚀设备,更重要的是原料光气有剧毒,所以现在发达国家已禁止使用[1]。目前国内外的研究热点集中在酯交换法和甲醇氧化羰基化法上。
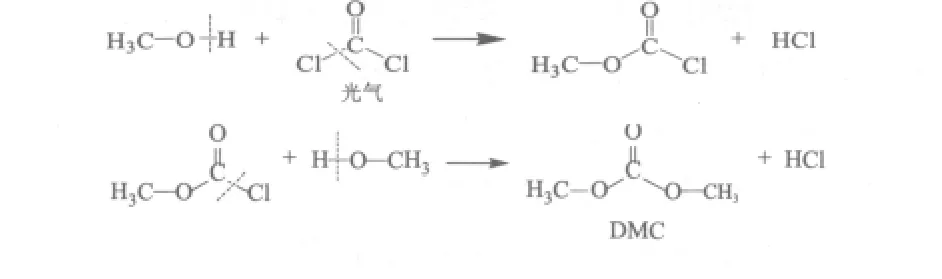
图1 DMC的传统合成原理
一、酯交换法
该法以环氧乙(丙)烷以及CO2为原料。反应首先生成碳酸乙(丙)烯酯(称为环加成反应),再由碳酸乙(丙)烯酯与甲醇交换合成DMC,同时生成乙(丙)二醇[2]。以环氧丙烷为例,反应方程式如图2所示。
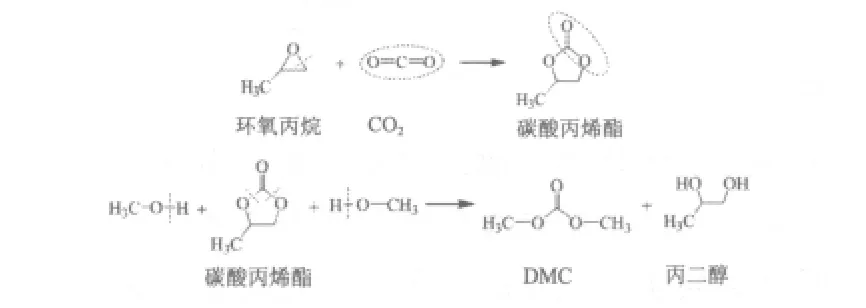
图2 环氧丙烷酯交换法合成DMC
这两步反应具体是怎样进行的?在此列举一个描述第一步环加成反应途径的例子[2](如图3所示)。这个过程使用了Cr配合物做催化剂,通过配位催化过程来加快反应。首先,催化剂分别与两种反应物结合,使它们活化,再与环氧化合物结合形成中间体a(步骤①),并在助催化剂的帮助下与CO2结合形成中间体b(步骤②)。接着,中间体b中带负电荷的O攻击中间体a的环氧化合物中空间阻碍最小的碳原子,形成二聚体c(步骤③)。由于该二聚体不稳定,分子内成环状碳酸酯(目标产物),得到中间体d(步骤④)。最后,目标产物从中间体d上离去,得到产物,完成催化过程。催化剂继续结合两种反应物,重新形成中间体a和b,催化过程继续进行。
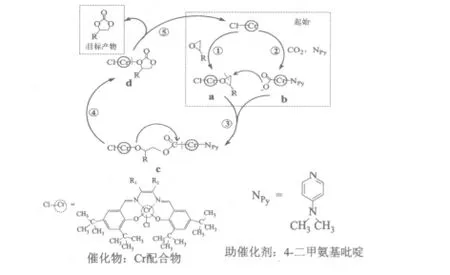
图3 金属配合物催化合成环状碳酸酯的可能反应途径
再列举一个描述第二步酯交换反应[3]的例子,实际途径如图4所示,这个过程使用CaO作为催化剂,在它的表面发生催化反应。(1)甲醇在CaO表面发生吸附而被活化,它的O―H键断裂,在CaO表面形成烷氧基负离子和H+(a,步骤①)。(2)这种烷氧基负离子与环状碳酸酯反应,使酯的一条C―O键断裂,形成中间体b(步骤②)。紧邻的烷氧基负离子与环状碳酸酯的另一条C―O键作用,使其断裂,生成中间体c和目标产物DMC(步骤③)。(3)中间体c中两个氧负离子分别夺取相邻的H+,生成副产物,副产物从CaO表面脱离,完成催化过程。
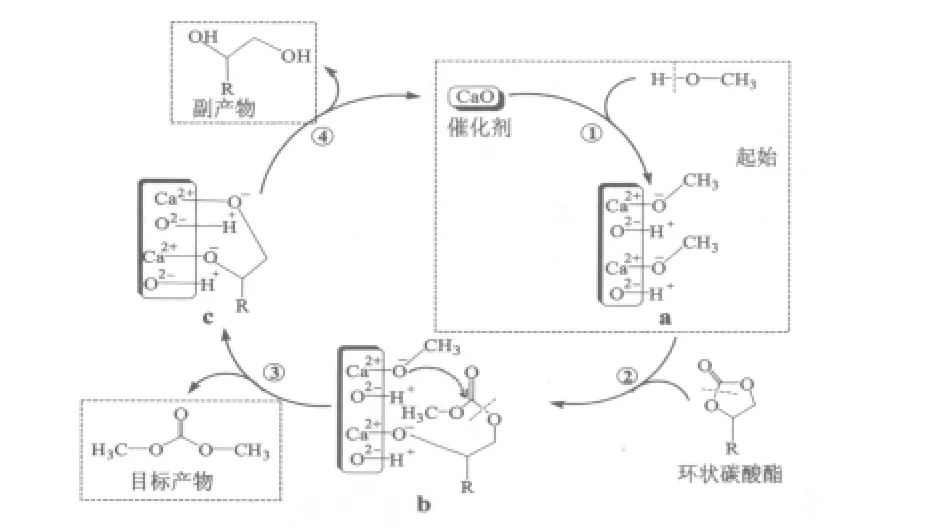
图4 CaO催化酯交换反应的可能途径
该法收率高,腐蚀性低,不产生有毒有害物质,反应条件温和,易于工业化生产。但是,反应工艺复杂且副产物处理烦琐,同时两步反应采用不同催化剂,这造成能耗大、成本高[1],因此只适于小规模生产。
二、甲醇氧化羰化合成法
该法目前在国外得到普遍运用[4],它以CH3OH,CO和O2为原料,也需借助催化剂,合成反应可表示如下:
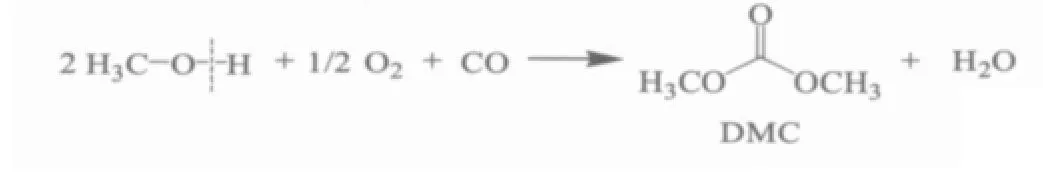

表1 反应的热力学数据
1.液相泥浆工艺
在该工艺的反应过程中,反应物呈泥浆状,所以称为液相泥浆法。该工艺常分为两步:第一步,将甲醇和粉状固体CuCl催化剂加入到高压反应釜中,加热搅拌,混合均匀并成浆。第二步,通入CO和O2,即可通过氧化羰基化反应生成碳酸二甲酯。催化剂CuCl对反应设备有强腐蚀作用,所以反应器内壁必须衬有搪瓷等防腐材料。由于CuCl在反应体系中溶解性差,必须保持它的高浓度才能保证反应速率,实际用量为1~2 mol•L-1,同时甲醇和CO需过量,而O2则需低于4%,以免发生爆炸。这是一个气体物质减少的反应,所以增大压强有助于提高反应物的转化率。这也是一个大量放热的反应,所以反应在低温下较为有利。但是从动力学角度考虑,温度升高通常使反应速率加快,所以需要适当升温。举一个实例,使用浓度为1.68 mol•L-1的CuCl催化剂,控制反应温度为94 ℃,压强为2.0 MPa,O2的转化率可达77%[7]。
该法的主要缺点是,甲醇电离产生的H+会使催化剂中的Cl-逐渐转化为HCl,从而造成催化剂失活,并会严重腐蚀设备。此外,CuCl催化剂和反应中生成的中间体Cu(OCH3)Cl在甲醇中都难以溶解,这也是反应较慢的一个原因[4]。
2.气相间接工艺
该法的特殊之处在于使用NO作循环介质,反应原理如图5所示。NO先与甲醇和O2反应生成中间体亚硝酸酯(过程放热),该中间体再与CO反应生成产物DMC(为速率控制步骤),NO复原。常用负载在活性炭上的Pd-Cu,Pd-Bi等双金属催化剂来催化反应,转化率很高,产物具有高纯度。例如,当催化剂为PdCl2-CuCl2/C时,在反应温度100 ℃,压强0.1 MPa的条件下,CO的转化率高达96%[8]。

图5 气相间接法的反应原理
该工艺采用两步反应,避免了甲醇-水-DMC之间形成共沸物而难以分离。由于水和催化剂不直接接触,避免了水对催化剂性能的影响,这有助于保持催化剂的活性。该法的主要缺点是:第一步反应在极短时间内大量放热,因此必须及时疏散热量,并将反应气的组成控制在爆炸极限之内。此外,反应中引入了剧毒的NO,必须对它回收,这已经成为一个十分关键的技术[9]。
[1] 王翔,刘定华,刘晓勤.酯交换法合成碳酸二甲酯催化剂及反应机理的研究进展[J].石油化工,2009,38(12):1346-1352.
[2] Paddock R L , Nguyen S T. Chemical CO2Fixation: Cr(Ⅲ) Salen Complexes as Highly Eff cient Catalysts for the Coupling of CO2and Epoxides [J]. J Am Chem Soc, 2001, 123(46): 11498-11499.
[3] 魏彤,王谋华,魏伟,孙予罕,钟炳.氧化钙室温催化碳酸丙烯酯和甲醇的酯交换合成碳酸二甲酯[J].催化学报,2003,24(1):52-56.
[4] 任军,李忠,周媛,邢燕玲,谢克昌.甲醇液相氧化羰基化合成碳酸二甲酯催化剂的研究进展[J].化工进展,2007,26(11):1569-1573.
[5] 姚允斌,解涛,高英敏.物理化学手册[M].上海:上海科学技术出版社,1985.
[6] 赵天生,韩怡卓,孙予罕.甲醇和CO2合成碳酸二甲酯体系的热力学分析[J].天然气化工,1998,23(5):52-55.
[7] Romano U, Tesel R, Mauri M M, Rebora P. Synthesis of dimethyl carbonate from methanol, carbon monoxide, and oxygen catalyzed by copper compounds [J]. Ind Eng Chem Prod Res Dev, 1980, 19(3): 396-403.
[8] UBE Industries, Process for preparing diester of carbonic acid:EP, 5162563[P].1992.
[9] 任军,李忠,周媛,孟凡会,谢克昌.甲醇气相氧化羰基化合成碳酸二甲酯研究[J].化工进展,2007,26(9):1246-1252.
2011-08-22
朱鹏琼,在读硕士研究生。王明召,博士,副教授。
北京师范大学化学学院。
国家级精品课程建设项目,北京市精品课程建设项目,国家级化学实验教学团队建设项目,教育部实验室共建项目,北京市教育委员会共建项目。
