红茂草生物碱提取工艺优选及色谱分析
2012-10-25王廷璞刘小东袁毅君
王廷璞,李 强,刘小东,袁毅君
(1.天水师范学院生命科学与化学学院,甘肃天水 741001;
2.上海海洋大学水产种质资源发掘与利用教育部重点实验室,上海 201306;
3.华中科技大学中英HUST-RRes基因工程与基因组学联合实验室,湖北武汉 430074)
红茂草生物碱提取工艺优选及色谱分析
王廷璞1,李 强2,刘小东3,袁毅君1
(1.天水师范学院生命科学与化学学院,甘肃天水 741001;
2.上海海洋大学水产种质资源发掘与利用教育部重点实验室,上海 201306;
3.华中科技大学中英HUST-RRes基因工程与基因组学联合实验室,湖北武汉 430074)
目地:优选红茂草生物碱提取与干燥工艺,对提取物进行分析鉴定。方法:优选提取方法,利用L9(34)正交实验优选红茂草生物碱的提取影响因子,高效液相色谱层析分离鉴定主要成分,用真空冷冻干燥技术进行干燥保存。结果:提取方式优选超声波提取法,L9(34)正交实验得液料比30∶1、pH7、乙醇体积分数75%、温度80℃为最佳的提取条件,平均得率可达4.215%,平均回收率和RSD分别为99.57%、0.68%,稳定性良好。异紫堇碱与原阿片碱含量显著高于其他生物碱。结论:超声波提取、真空冷冻干燥工艺适合于红茂草生物碱的提取,异紫堇碱和原阿片碱的高效液相色谱鉴定可用于红茂草生物碱制剂质量控制的指标。
红茂草,生物碱,色谱分析
红茂草(Dicranostigma leptopodum Maxim.),又名秃疮花、秃子花、勒马回(陕西),二年生或多年生草本,为罂粟科秃疮花属植物。主要分布在我国甘肃、陕西、河南、山西、青海、四川、云南、西藏等省区的低山丘陵地带。在民间的红茂草根或全草可入药,有清热解毒、消肿止痛、杀虫等功效。主治扁桃体炎、牙痛、喉咙痛、淋巴结核,外用于秃疮、疮疖疥癣、痈疽等症[1]。红茂草生物碱是从红茂草全草中分离提取的有效成分,为多种喹啉类或异喹啉类生物碱;主要成分为紫堇碱、异紫堇碱、原阿片碱、异紫堇啡碱、木兰碱5种生物碱,具有明显的镇痛、镇静、解除平滑肌痉挛等作用。近年来,研究发现其在抑菌、抗病毒、肝组织损伤保护和免疫调节等方面具有明显的效果,且安全无毒副作用。研究结果证明,红茂草是一种亟待开发的新药物资源,具有广阔的开发应用前景和巨大的社会经济效益。生物碱具有明显的生物学活性和药理学活性,是红茂草中的主要有效成分,其含量高低直接影响到药材的质量与疗效。国内对红茂草进行了大量研究[2-4],但对于红茂草生物碱提取工艺、冷冻工艺[5]与高效液相色谱分离检验却鲜有报道。故笔者希望能够通过此实验找到一种快速、灵敏、高效的提取与检测红茂草生物碱的方法,为工业化生产提供理论参考。
1 材料与方法
1.1 材料与仪器
原阿片碱标准品 Shanghai Tautd Biotech Co.,Ltd.,(China)公司,批号:E-0411,CASBO-86-9,规格:10mg;异紫堇碱标准品 ABCR Gmbh&Co.KG im Schlehert公司,批号:166401,规格:10mg;乙腈、三乙胺 色谱纯;红茂草生物碱对照品 由袁毅君教授提供,天水师范学院细胞工程室制备、保存,含量20mg/m L;其他试剂 均为分析纯;红茂草全草 甘肃省天水市规范化批量种植,阴干,制成粉末。
Agilent 1100 series高效液相色谱系统 安捷伦科技公司;紫外-可见分光光度计 日本;超声波裂解仪 昆山市超声仪器有限公司;旋转蒸发器 上海青浦沪西仪器厂;真空冷冻干燥机 德国。
1.2 实验方法
1.2.1 标准曲线的制备 准确称取生物碱对照品4mg于离心管中,加去离子水4m L制成浓度1mg/m L的对照液。测定时加去离子水稀释至浓度分别为0.01、0.02、0.03、0.04、0.05、0.06mg/m L。以去离子水为空白对照,在210nm波长处测吸光度得回归方程A=28.65x+0.0246,R2=0.9981,结果表明总生物碱在0~0.06mg/m L范围内,呈良好的线性关系。
1.2.2 提取方法选择 分别采用超声波提取法、冷浸提取法、索氏提取法[6]按如下过程操作:红茂草全草粉末10g→按1∶15加去离子水浸泡→分别于超声波裂解仪(60℃、1h)、冷浸(过夜)、索氏回流(8次)处理→经高速离心(3500r/min)10min得上清液→取上清加95%乙醇至原溶液酒精度达80%→静置过夜,常温高速离心(3500r/min)10min,取上清液→50℃旋转蒸发回收乙醇并浓缩至20mL→浓缩液-75℃冷冻过夜→真空冷冻干燥(-62℃,0.011MPa)24h得红茂草生物碱制品,称重→取各制品分别4mg溶于4mL去离子水中,6倍稀释→过微孔滤膜 (0.22μm)→得吸光度A→将所测得A值代入标准曲线回归方程,计算生物总碱含量→得生物总碱最佳提取方式。
1.2.3 影响因素的选择 分别选取超声时间、液料比、pH、乙醇体积分数、超声温度五因素进行单因素实验,操作方法同1.2.2。
得率(%)=制品中粗生物总碱提取质量(m1)/红茂草质量(m2)×100
1.2.4 正交实验设计 根据有关文献资料和预实验[7],结合单因素对红茂草生物总碱得率的影响分析,选择液料比、pH、乙醇体积分数、温度4因素为指标进行L9(34)正交实验,方法同1.2.2。通过正交实验确定红茂草生物总碱的最佳提取工艺。正交实验设计见表1。

表1 正交实验因素水平表Table 1 Factors and levels in orthogonal array design
1.2.5 重现性实验 取同一批红茂草粉末6份,按正交优选的最佳提取条件进行重复性实验三次,测定吸光度A值,计算含量,从而得到平均得率。在上述最佳提取条件下做重现性实验,计算生物碱平均得率为4.215%。
1.2.6 加样回收率实验 取同一批已知含量(质量分数4.212%)的红茂草真空冷冻产物6份,分别加入红茂草对照品溶液适量,按正交最佳提取条件提取,测定吸光度A值,计算含量,得平均回收率与RSD。
1.2.7 数据处理 运用Origin 75软件设计单因素考察图;利用SPSS 11.5软件对正交实验进行设计及其数据分析。
1.3 异紫堇碱与原阿片碱的含量测定
1.3.1 色谱检测波长的选择 将异紫堇碱对照品配制成浓度为2μg/m L,以去离子水作为对照,利用UV-2450紫外-可见分光光度计在190~500nm波长范围内扫描,即得异紫堇碱对照品的最大吸收波长;原阿片碱的最大吸收波长参考制品厂所提供以及相关文献[8]。
1.3.2 标准品与供试品溶液的制备 分别取所购原阿片碱标准品与异紫堇碱标准品各10mg,加入0.22μm的微孔滤膜过滤的去离子水10m L,充分摇匀溶解配制成1mg/m L的标准母液,备用。
取各组分供试品50mg,加入50m L去离子水于50m L容量瓶中定容至刻度,充分摇匀溶解,配制成1mg/m L的供试液,先用滤纸过滤,再用0.2μm微孔滤膜过滤,即得供试液样品。
1.3.3 色谱条件 异紫堇碱色谱条件:Zorbax eclipse XDB C8(150mm×4.6mm i.d);流动相[9]:乙腈∶0.03mol/L NaH2PO4=26∶74;流速:1.0m L/m in;检测波长:220nm;柱温:30℃。
原阿片碱色谱条件:Zorbax ec:lipse XDB C8(150mm×4.6mm i.d);流动相[10]:乙腈∶三乙胺-冰醋酸=18∶82(8m L三乙胺,50m L冰醋酸);检测波长:285nm;柱温:25℃。
1.3.4 线性关系考察 原阿片碱标准曲线的制备:精密量取原阿片碱母液分别稀释配制成浓度为0.00125、0.0025、0.01、0.02、0.03、0.055mg/m L的溶液,20μL进样,测定获取峰面积积分值作为纵坐标,同时以标准品质量浓度为横坐标,得原阿片碱线性回归方程。
异紫堇碱标准曲线的制备:方法同原阿片碱标准曲线的制备,得异紫堇碱线性回归方程。
2 结果与分析
2.1 提取方法对总生物碱得率的影响
多重比较结果表明,分别利用超声提取法、冷浸提取法、索氏提取法提取红茂草中的生物总碱,超声提取法对红茂草中总生物碱的提取的影响效果显著高于索氏提取法与冷浸提取法(p<0.05);冷浸提取法对红茂草中生物总碱提取的影响效果极显著于索氏提取法(p<0.01);而超声波提取法所用提取时间相对较少,操作简单,综合考虑,提取方式优选超声波提取法。
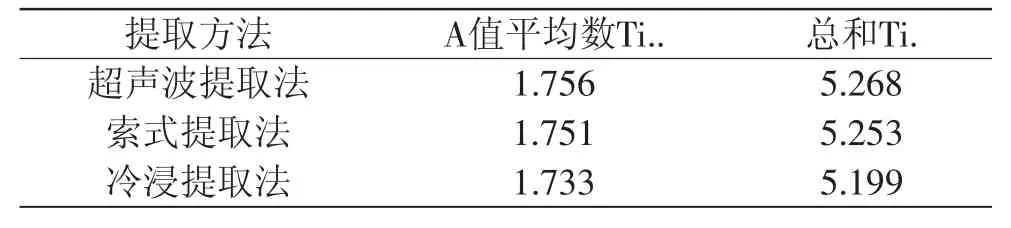
表2 不同提取方式对红茂草生物总碱提取效果比较Table 2 Differentextractionmethods on comparison of alkaloids’extraction
2.2 不同因素对生物总碱得率的影响
2.2.1 不同超声时间对红茂草生物总碱的得率的影响 由图1可知,不同超声时间下红茂草中生物总碱得率以0.5h最高,显著高于其他组别(p<0.05),1h与1.5h次之。多重比较结果表明,1h超声对红茂草中总生物碱得率极显著高于1.5h的得率(p<0.01)。

图1 不同超声时间对红茂草生物总碱的得率的影响Fig.1 Effectof differentultrasonic time on the Dicranostigma leptopodum alkaloids’extraction ratio
2.2.2 不同液料比对红茂草生物总碱的得率的影响
由图2可知,实验组液料比为30∶1时所提物中生物总碱的含量最高,料液比小于30∶1时,生物碱的得率随液料比的增加而增加,因为随着液料比的增加,细胞内外的浓度差逐渐变大,内扩散速度也增加,因此越有利于生物总碱的溶出。但是当液料比大于50∶1后,由于提取生物总碱时加入的溶剂量过大以至溶液被稀释程度增大,此时生物总碱的得率逐渐降低。多重比较结果表明,液料比为20∶1、30∶1、40∶1(mg/m L)时对红茂草生物碱得率相互之间差异显著(p<0.05)。

图2 不同液料比对红茂草生物总碱的得率的影响Fig.2 Effectof different liquid ratio on the Dicranostigma leptopodum alkaloids’extraction ratio
2.2.3 不同pH对红茂草生物总碱的得率的影响 由图3可知,不同pH对提取红茂草中生物总碱的影响当pH 8时最大,对应得率最高。当pH<8时,由于酸碱中和反应的影响,提取生物总碱的得率并不高;当pH>8时,可以发现生物碱的得率开始减少,说明pH对红茂草中总生物碱的影响已不再显著。多重比较结果表明,pH 7对红茂草中总生物碱得率的影响效果差异显著于pH 6、pH 8的组份(p<0.05),pH 8组份得率显著高于pH6的(p<0.05)。

图3 不同pH对红茂草生物总碱的得率的影响Fig.3 Effectof different pH on the Dicranostigma leptopodum alkaloids’extraction ratio
2.2.4 不同乙醇体积分数对红茂草生物总碱的得率
由图4可知,当乙醇体积分数为75%时,所对应的红茂草生物总碱得率最大,即其含量最高。当乙醇体积分数小于75%时,随着乙醇体积分数的不断增加,其对应的生物总碱的得率不断增加,即红茂草中生物总碱含量不断增加,但当乙醇体积分数大于75%时,其对应的生物总碱的含量随着乙醇体积分数的不断增加,呈现出相对减小的趋势,原因可能是随着乙醇体积分数不断增大,使得所得滤液中溶入的杂质物质的增多造成的。多重比较结果表明,乙醇体积分数75%的红茂草生物碱得率显著高于乙醇体积分数65%、85%的组别(p<0.05)。
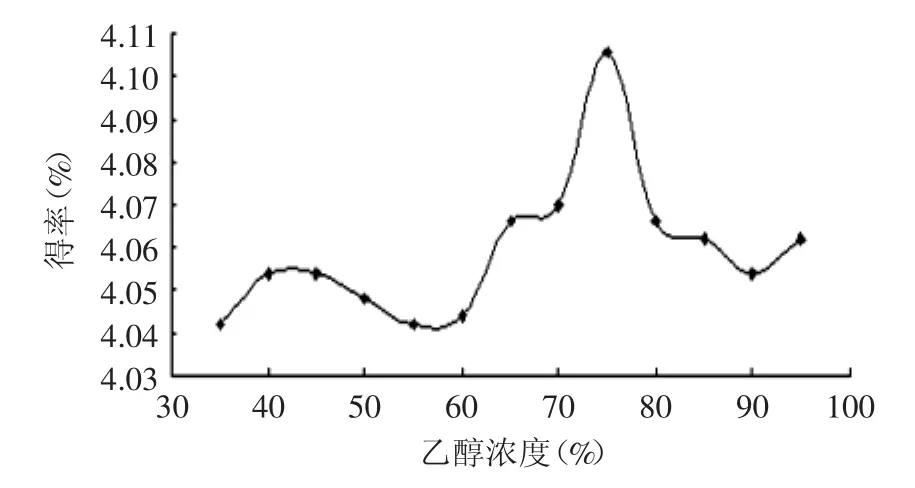
图4 不同乙醇体积分数对红茂草生物总碱的得率的影响Fig.4 Effect of differentethanol concentration on the Dicranostigma leptopodum alkaloids’extraction ratio
2.2.5 不同温度对红茂草中生物总碱的得率的影响由图5可知,温度对红茂草中生物总碱得率的影响表现为温度越高,得率相应越高,但考虑到实际生产的需要,以80℃为标准。多重比较结果表明,温度60、70、80℃对红茂草中总生物碱得率彼此间差异均显著(p<0.05)。
2.3 正交实验结果与分析

图5 不同温度对红茂草中生物总碱的得率的影响Fig.5 Effect of different temperatures on the Dicranostigma leptopodum alkaloids’extraction ratio
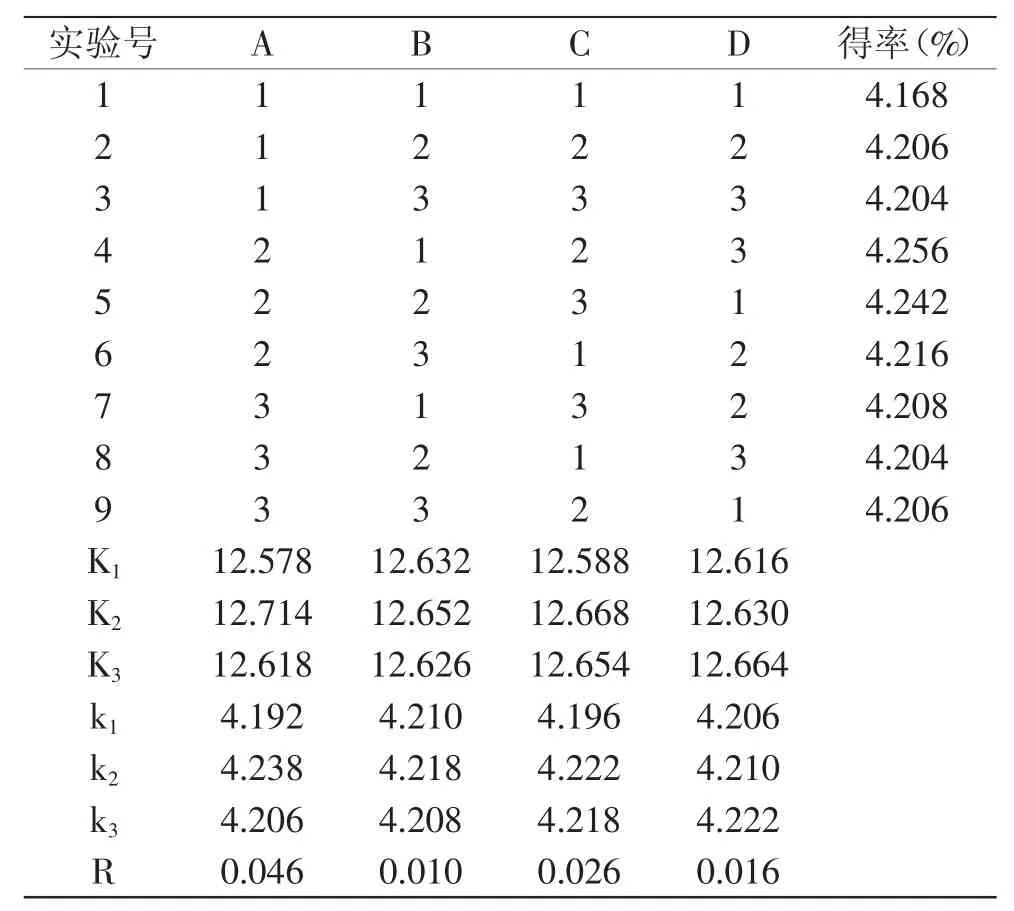
表3 结果与分析Table 3 Results and analysis
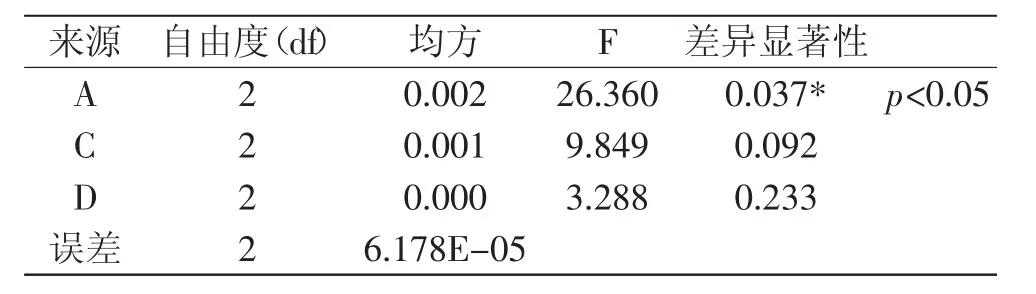
表4 方差分析Table 4 Analysis of variance
B因素(即pH)对红茂草中生物总碱提取的影响效果不显著,因此将B因素作为方差分析时的误差列。由表3可知,影响超声波提取红茂草生物总碱得率的影响因素依次为:液料比>乙醇体积分数>温度>pH。A因素(即液料比)对红茂草中生物总碱提取的影响显著强于其他因素,为正交实验提取红茂草中生物总碱的最主要因素。综合考虑,红茂草生物总碱最佳的提取条件为A2B1C2D3,即液料比30∶1、pH 7、乙醇体积分数75%、温度80℃。
2.4 加样回收率实验
根据有关标准[11]可知,平均回收率在95%~105%之间为回收率良好,RSD(相对标准偏差)<3%时,测定结果精密度良好,本实验红茂草生物总碱平均回收率与RSD分别为99.57%和0.68%,结果表明本实验优化提取方法准确度良好,专属性强,精密度良好。
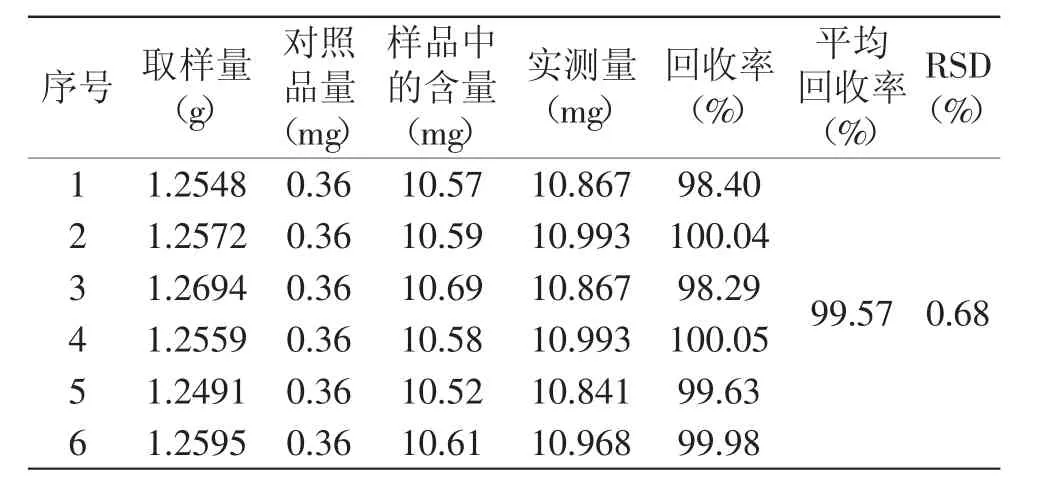
表5 回收率测定表(n=6)Table 5 Table of recovery rate(n=6)
2.5 异紫堇碱与原阿片碱的含量测定结果与分析
2.5.1 色谱检测波长的选择结果与分析 扫描图谱显示,异紫堇碱在220nm波长处有最大吸收,其吸收值为0.238;原阿片碱最大吸收波长选择285nm检测。

图6 异紫堇碱的最大吸收波长Fig.6 Maximum absorption wavelength of isocorydine
2.5.2 线性关系考察 原阿片碱线性回归方程为A=14453x-17.966,R2=0.9906。结果表明,红茂草样品生物总碱中原阿片碱的质量浓度在0.00125~0.055mg·m L-1的范围内具有良好的线性关系;异紫堇碱线性回归方程为A=112649x-7.9518,R2=0.9944。结果表明,红茂草样品生物总碱中异紫堇碱的质量浓度在0.002~0.025mg·m L-1的范围内具有良好的线性关系。
2.5.3 样品的鉴定结果与分析 图HPLC结果分析表明,异紫堇碱标品(浓度为0.1mg/m L)的保留时间为5.410m in(图A),吸收峰面积为10631.7,红茂草生物总碱样品在5.443m in有明显吸收峰(图B),吸收峰面积为1632.1。因此可知,样品中异紫堇碱含量为15.35%;同理,原阿片碱标品(浓度为0.1mg/m L)的保留时间13.386m in(图C),吸收峰面积为1610,红茂草生物总碱样品在13.373m in(图D)也出现显著特异峰,吸收峰面积为91.7。因此可知,样品中原阿片碱的含量为5.70%。但同时在HPLC过程中可以看出在保留时间2.940m in与2.111m in左右,样品中有明显高的不明吸收峰,有待进一步深入探究。
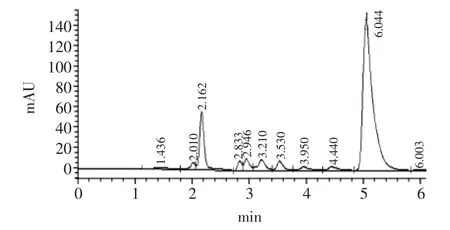
图7 对照品HPLCFig.7 HPLC of reference substance
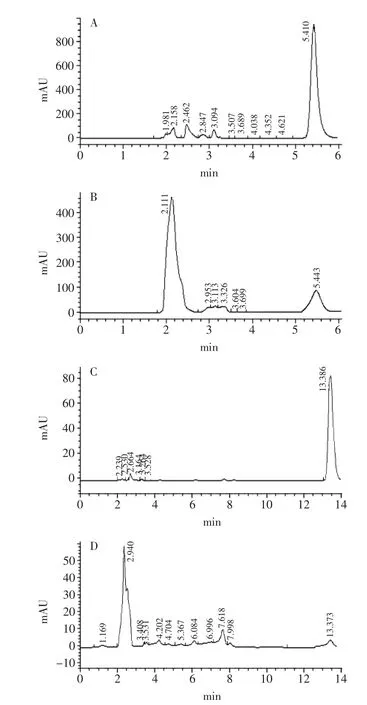
图8 异紫堇碱标准品HPLC(A)、正交实验所得异紫堇碱样品HPLC(B)、原阿片碱标准品HPLC(C)、正交实验所得原阿片碱样品HPLC(D)Fig.8 HPLC of standard isocorydine(A),sample of isocorydine from orthogonal experiment(B),HPLC of original protopine(C),sample of original protopine from orthogonal experiment(D)
3 结论
3.1 传统方法提取工艺繁杂、耗时、得率低、重现性差。本实验着手于提取工艺优化与主要成分的鉴定,正交实验所得结果提取得率高、重现性好,工艺稳定简便,很适合工业化生产。平均得率可达4.215%,平均加样回收率为99.57%,RSD为0.68%。
3.2 高效液相色谱法测定红茂草总生物碱中异紫堇碱与原阿片碱含量,专属性强、结果明显、准确可靠、实用性强、分离度良好、稳定、操作简便,可以作为中药红茂草中异紫堇碱与原阿片碱的鉴定方法。
[1]南京中医药大学.中药大词典[M].上海:上海科技出版社,2006.
[2]赵强,王廷璞,余四九,等.红茂草生物碱抑菌活性的测定[J].中国兽医科学,2008(12):18.
[3]巩江,骆蓉芳,倪士峰,等.珍稀中药秃疮花属植物药学研究概况[J].西北药学杂志,2010,25(2):153-155.
[4]陈正山,王勤,王廷璞,等.秃疮花注射液对小鼠腹腔巨噬细胞免疫功能的影响[J].上海免疫学杂志,2001(4):216-218.
[5]郭树国,王丽艳,李成华.黄瓜真空冷冻干燥工艺参数优化[J].食品研究与开发,2012,33(1):232-234.
[6]赵颖,刘琪,王萌,等.宝兴鼠尾草的有效成分提取及含量测定[J].浙江大学学报:农业与生命科学版,2012,33(3):293-298.
[7]杨金华,王登斌,陈小明.首乌藤中大黄素的提取工艺研究[J].中草药,2011,42(10):2017-2019.
[8]沈燕,韩超,夏碧琪.高效液相色谱法测定夏天无中4种生物碱的含量[J].中国中药杂志,2011,36(15):2110-2112.
[9]梁妍,郝小燕,朱杰,等.天参益智胶囊的质量标准研究[J].中成药,2008,30(5):11-13.
[10]潘成学,刘伟,申小静.HPLC测定夏天无胶囊中原阿片碱的含量[J].郑州大学学报:医学版,2005,40(4):721-722.
[11]国家药典委员会.中国药典[M].北京:中国医药科技出版社,2010.
Extraction methods and chromatographic analysis of Dicranostigma leptopodum alkaloids
WANG Ting-pu1,LIQiang2,LIU Xiao-dong3,YUAN Yi-jun1
(1.College of Life Science and Chemistry,Tianshui Normal University,Tianshui741001,China;
2.Key Laboratory of Exploration and Utilization of Aquatic Genetic Resources,Ministry of Education,ShanghaiOcean University,Shanghai201306,China;
3.China-UK HUST-RRes Genetics Engineering and Genomics Joint Laboratory,Huazhong University of Science and Technology,Wuhan 430074,China)
Ob jective:To get the alkaloids’op tim ization of p rocess of Dicranostigma lep topodum,detach and identify the extracts and d ry storage.Methods:First the methods of extrac ting were choosen,then impact fac tors were selected by the L9(34)orthogonal experiment,which was combined w ith high performance liquid chromatog raphy,and the vacuum freeze-d rying technology was used to store.Results:The op timal extraction means was ultrasonic wave extraction,and L9(34)orthogonal best extraction cond itions was liquid ratio 30∶1,pH7,75%ethanol volume frac tion and temperature 80℃.The average yield was 4.215%.The average recovery and RSD were 99.57%and 0.68%,with good stability.The content of p rotopine and Isocoryd ine were higher than other alkaloids.Conc lusion:The technology of ultrasonic wave extraction,vacuum freeze-d rying and HPLC were app lied to extract,d ry and separating inspection.The result was suitab le for its extraction and identification.
Dicranostigma lep topodum;alkaloids;chromatog raphic analysis
TS297
A
1002-0306(2012)22-0051-05
2012-06-13
王廷璞(1965-),男,研究员,主要从事分子生物学研究。
甘肃省中医药管理局基金项目(GZK-2010-20);2009年出国留学人员基金。
