窄分子量分布壳聚糖的制备工艺研究
2012-10-25李星科夏文水
李星科,纵 伟,夏文水
(1.郑州轻工业学院食品与生物工程系,河南郑州 450002;2.江南大学食品学院,江苏无锡 214122)
窄分子量分布壳聚糖的制备工艺研究
李星科1,纵 伟1,夏文水2,*
(1.郑州轻工业学院食品与生物工程系,河南郑州 450002;2.江南大学食品学院,江苏无锡 214122)
研究了超声波法制备窄分子量分布壳聚糖的制备工艺,在单因素实验的基础上,根据旋转组合设计原理,研究温度、壳聚糖浓度、乙酸浓度三个影响因素对超声波处理后壳聚糖分子量分布指数的影响,并建立了回归数学模型,通过实验结果进行方差分析及对数学模型进行优化得到了窄分子量分布的壳聚糖的制备条件。结果表明,最佳工艺参数为:温度24℃、乙酸浓度0.27mol/L,壳聚糖浓度根据实际需要定为1%,经过超声波处理后壳聚糖分子量分布指数从11.51降到了4.25。
壳聚糖,超声波处理,分子量分布指数,优化
分子量分布是指高聚物中各种不同的分子量组分在总量中所占的分量,一般用分子量分布指数表示,重均分子量与数均分子量的比值(Mw/Mn),比值愈大说明分子量分布愈宽。分子量分布直接影响着高聚物的物理化学性质以及其加工性能等[1]。壳聚糖是自然界唯一的碱性多糖,具有生物相容性、可降解性、无毒性及多种对人体有益的功能活性,日益受到人们的关注和青睐,在食品、化工、纺织、医药、环保等领域都有着广泛的用途[2]。壳聚糖属于高聚物,自然界中天然存在的壳聚糖分子量一般也在几万至上百万不等,经过化学方法提取出来的壳聚糖的分子量一般分布很宽[3]。Mette H Ottsy等用凝胶过滤色谱法对壳聚糖进行分级[4],这种方法得到的多糖纯度较高,但该技术过程较为繁琐、处理量太小难以实现工业化应用。非对称场流分离技术(AFFFF)是一个全新的技术,能快速而有效分离和准确表征不同的粒子和高聚物,Mao Shirui和Augsten Christian利用非对称场流分离技术对壳聚糖进行了分离,但是该技术也存在处理量太小的问题,适合于分离和测定大分子化合物、胶体和颗粒样品[5-6]。据报道超声波处理可以降低壳聚糖的分子量分布指数,而且处理过程中壳聚糖的氨基含量不会发生改变[7-10]。因此本文采用超声波处理壳聚糖,并系统研究关键因素对超声波处理后壳聚糖分子量分布指数的影响,以确定超声波法制备窄分子量分布壳聚糖的最佳工艺。
1 材料与方法
1.1 材料与设备
壳聚糖(重均分子量58万,分子量分布指数11.52,脱乙酰度86.1%,实验室自测) 由南通双林生物制品有限责任公司提供;冰乙酸、氨水等 均为分析纯。
Y88-II超声波细胞破碎仪 中国宁波新芝生物科技股份有限公司;CHRIST冻干机 德国Martin Christ GmbH;DELTA-320-S pH计 梅特勒-托利多仪器上海有限公司;Waters600高效液相色谱仪 包括2410示差折光检测器、Empower工作站、ultrahydrogel 2000和ultrahydrogel 250色谱分离柱。
1.2 实验方法
1.2.1 超声波处理壳聚糖 将一定量的壳聚糖溶解于酸溶液中配制成壳聚糖溶液,冰箱中放置过夜,于一定温度下间歇式超声波处理后,用稀氨水溶液调节溶液的pH至8~8.5,收集沉淀,用蒸馏水反复洗涤至中性,冷冻干燥即得到样品。
1.2.2 单因素实验设计 当超声波细胞破碎仪的功率为150W,超声时间为60min时,研究壳聚糖浓度(0.5%、1.0%、1.5%、2%)、酸的种类(相同浓度的乙酸、盐酸、乳酸溶液)、乙酸浓度(0.1、0.2、0.5、1mol/L)、温度(10、30、50℃)、溶液pH(3.9、4.4、4.9、5.4、5.9)等因素对超声波处理后壳聚糖分子量分布指数的影响。
当超声波细胞破碎仪的功率为150W、壳聚糖浓度为1.0%、乙酸浓度为0.2mol/L、温度为30℃时,研究不同的超声时间对壳聚糖分子量分布指数的影响。
1.2.3 旋转正交实验设计 在单因素实验的基础上,采用三因素二次通用旋转实验设计,研究温度、壳聚糖的浓度、乙酸浓度3个因素对超声波处理后的壳聚糖分子量分布指数的影响。其中超声波细胞破碎仪的功率为150W,超声时间为60min。因素水平编码如表1所示。

表1 三因素二次通用旋转设计因素水平编码表Table 1 Factors and levels coding of three factors quadratic rotation design
1.2.4 壳聚糖分子量分布的测定 在Waters600高效液相色谱仪(2410示差折光检测器、Empower工作站)上,用ultrahydrogel 2000和ultrahydrogel 250作为色谱分离柱,进行分子量分布测定,用Empower工作站进行数据采集和分析,标准样品为已知分子量的水溶性右旋糖苷(2000000、133800、41100、21400、4600、2500),以0.2mol/L CH3COOH/0.15mol/L CH3COONH4缓冲溶液为流动相,流速为0.9mL/min,柱温30℃。
分子量分布指数=重均分子量(Mw)/数均分子量(Mn)
1.2.5 壳聚糖脱乙酰度(DD)的测定 DD的测定参见文献[10]。
1.2.6 数据分析与作图 采用SASV8软件进行统计分析,orign8.0软件作图。
2 结果与讨论
2.1 单因素实验
2.1.1 壳聚糖浓度的影响 当超声波细胞破碎仪的功率为150W、乙酸浓度为0.2mol/L、温度为30℃、超声时间为30min时,研究不同的壳聚糖浓度对超声处理后的壳聚糖分子量分布指数的影响。如图1所示,在壳聚糖浓度0.5%~2.0%的范围内,随着壳聚糖浓度的增大,壳聚糖的分子量分布指数增大,说明壳聚糖浓度对超声波处理后壳聚糖的分子量分布有一定的影响。
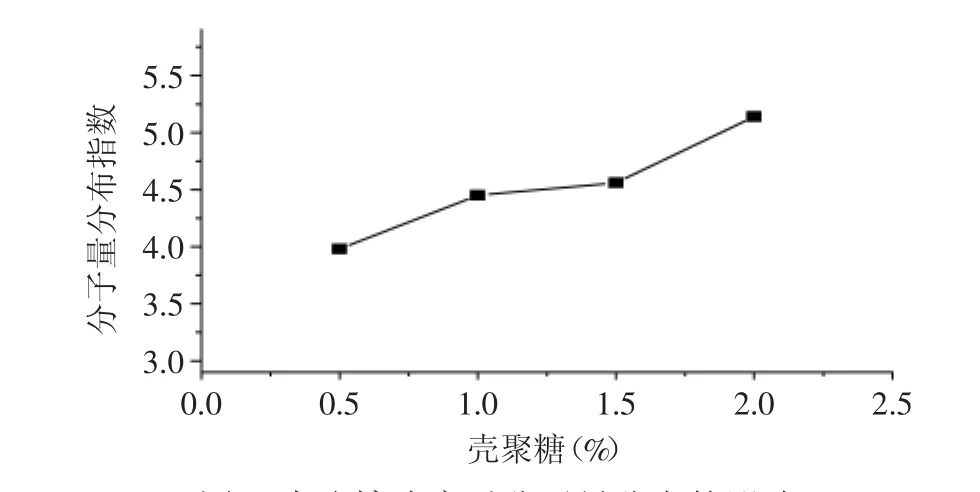
图1壳聚糖浓度对分子量分布的影响Fig.1 Effect of chitosan concentration on molecular weight distribution
2.1.2 酸的种类的影响 将壳聚糖分别溶解在相同浓度的乳酸、乙酸和盐酸溶液,当超声波细胞破碎仪的功率为150W、壳聚糖浓度为1%、酸浓度为0.2mol/L、温度为30℃、超声时间为30min时,研究酸的种类对超声波处理后的壳聚糖分子量分布的影响。如图2所示,经超声波处理的壳聚糖的分子量分布指数三者没有显著差别,说明酸的种类对超声波处理后壳聚糖的分子量分布没有显著影响。
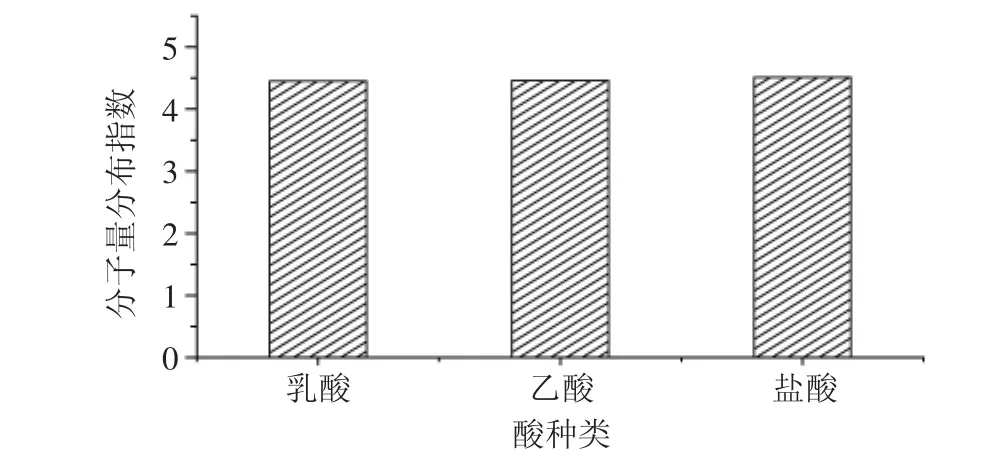
图2 酸种类对分子量分布的影响Fig.2 Effect of acid species on molecular weight distribution
2.1.3 乙酸浓度的影响 当超声波细胞破碎仪的功率为150W、壳聚糖浓度为1%、温度为30℃、超声时间为30min时,研究乙酸浓度对超声波处理的壳聚糖的分子量分布指数的影响。如图3所示,在0.1~1mol/L的范围内,随着乙酸浓度的提高,超声波处理的壳聚糖的分子量分布指数先减小后增大,在浓度0.2mol/L时达到最低,但浓度大于0.5mol/L时,乙酸浓度对处理后的分子量分布指数影响不大,说明乙酸浓度对超声波处理后壳聚糖的分子量分布有一定的影响。

图3 乙酸浓度对分子量分布的影响Fig.3 Effect of acetic acid concentration on molecular weight distribution
2.1.4 超声时间的影响 当超声波细胞破碎仪的功率为150W、壳聚糖浓度为1%、乙酸浓度为0.2mol/L、温度为30℃时,研究超声时间对超声波处理的壳聚糖的分子量分布指数的影响。如图4所示,在0~90min内,随着时间的延长,超声波处理后的壳聚糖的分子量分布指数呈下降趋势,在0~60min内下降比较快,在60~ 90min内下降比较缓慢,说明处理时间对分子量分布指数有显著影响。
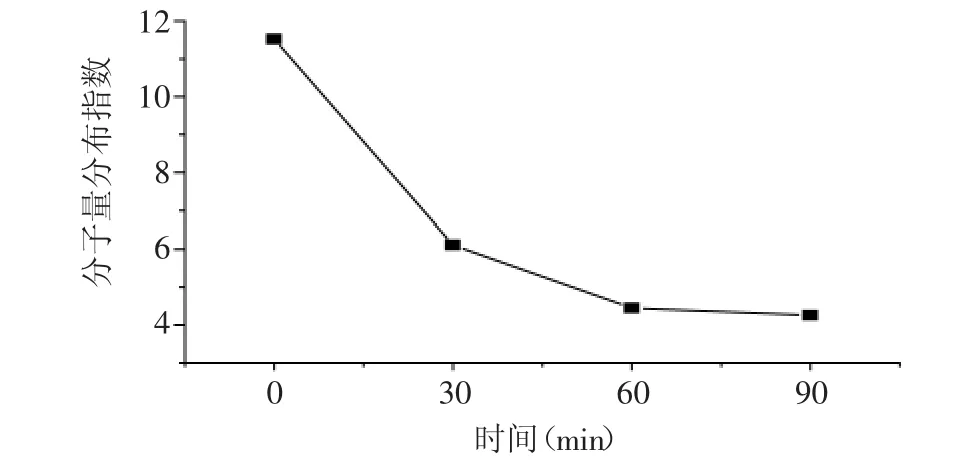
图4 超声时间对分子量分布的影响Fig.4 Effect of ultrasonic time on molecular weight distribution
2.1.5 温度的影响 当超声波细胞破碎仪的功率为150W、壳聚糖浓度为1%、酸浓度为0.2mol/L、超声时间为30min时,研究温度对超声波处理的壳聚糖的分子量分布指数的影响。如图5所示,在选择的10、30、50℃三个温度范围内,随着温度的升高,超声波处理后的壳聚糖的分子量分布指数先减小后增大,在30℃条件下处理壳聚糖得到的分子量分布最窄,说明温度对超声波处理后壳聚糖的分子量分布有一定的影响。
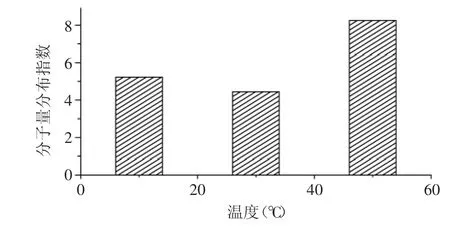
图5 温度对分子量分布的影响Fig.5 Effect of temperature on molecular weight distribution
2.1.6 pH的影响 当超声波细胞破碎仪的功率为150W、壳聚糖浓度为1%、酸浓度为0.2mol/L、温度为30℃、超声时间为30min时,研究溶液的pH对超声波处理后壳聚糖的分子量分布指数的影响。如图6所示,在3.9~5.9的范围内,随着壳聚糖溶液pH的升高,超声波处理后的壳聚糖的分子量分布指数先增大后减小,在pH4.4时达到最大值。而在pH4.4、4.9、5.4、5.9的条件下,超声波处理后的壳聚糖的分子量分布指数都比壳聚糖溶解于单一的乙酸溶液后的pH3.9都大,说明pH对超声波处理后壳聚糖的分子量分布没有积极的影响。
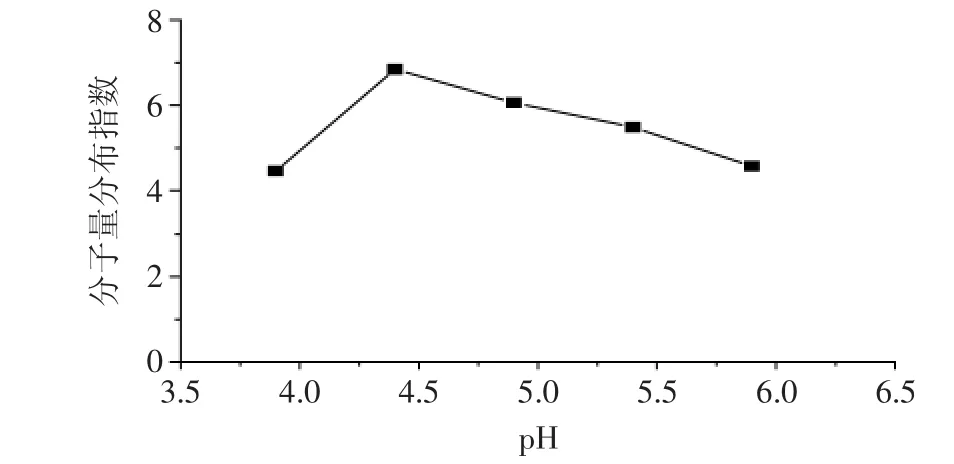
图6 pH对分子量分布的影响Fig.6 Effect of pH on molecular weight distribution
从单因素实验可以得出,壳聚糖浓度、乙酸浓度和温度对超声波降解后的壳聚糖的分子量分布指数影响较大,因此选择这三个因素建立旋转组合设计,系统研究关键因素对超声波处理后壳聚糖分子量分布指数的影响,并确定超声波法制备窄分子量分布壳聚糖的最佳工艺。
2.2 三因素二次通用旋转实验的结果分析
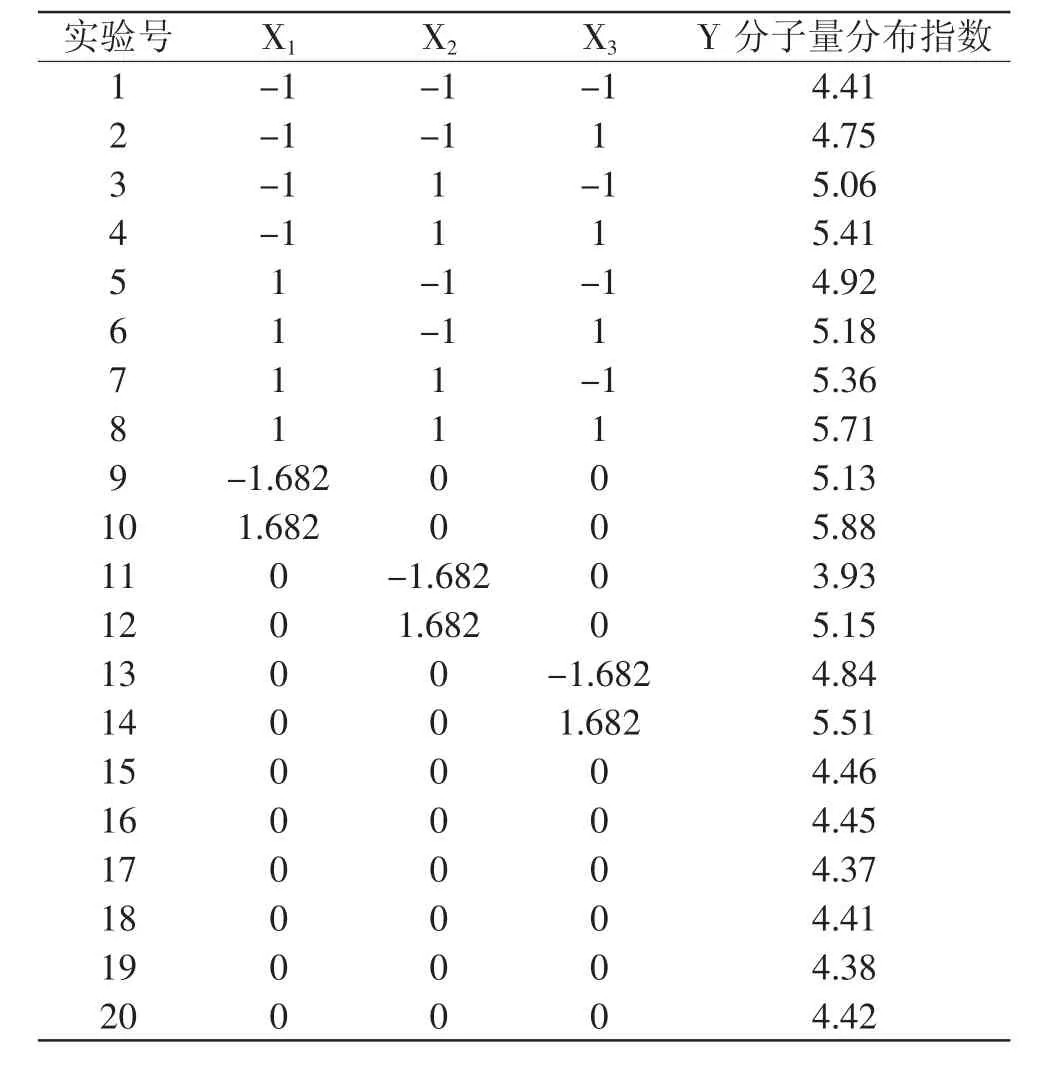
表2 三因素二次通用旋转设计及结果Table 2 Three elements quadratic current revolving design and results
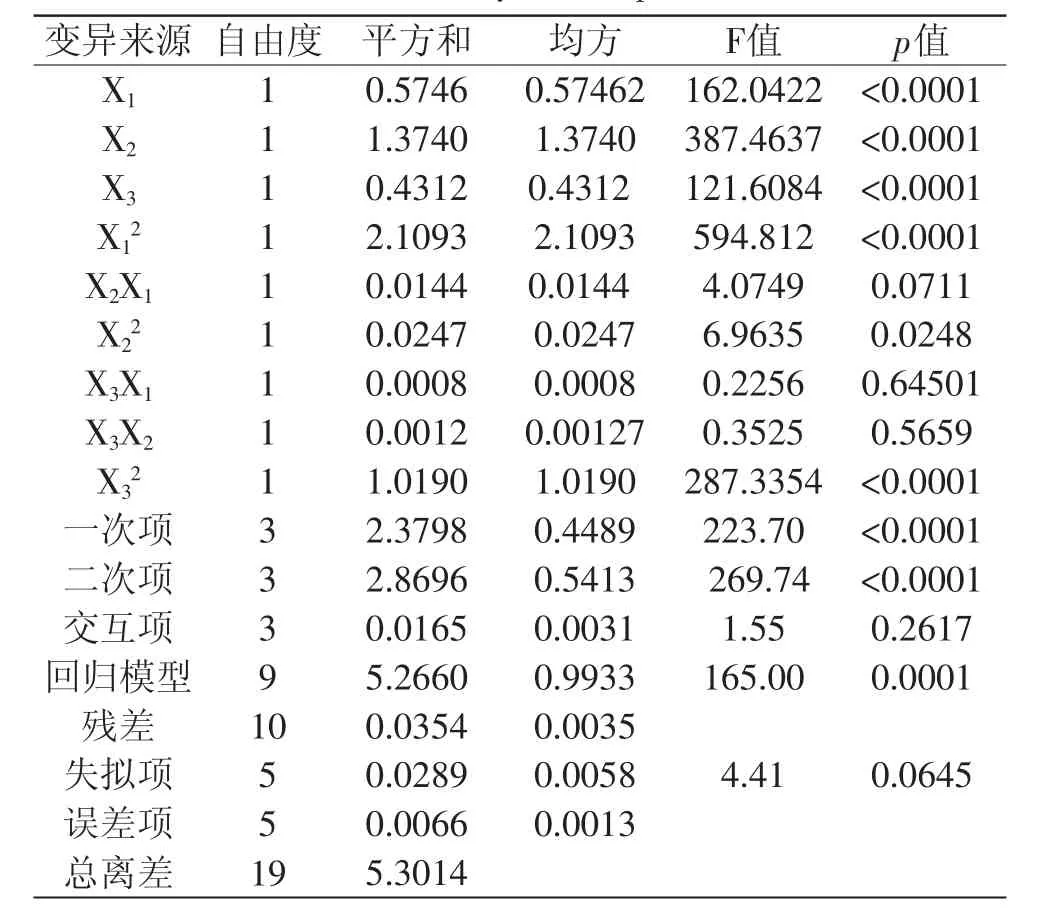
表3 实验结果的方差分析Table 3 Variance analysis of experimental results
2.2.1 回归分析及回归模型的建立 对实验所得的结果采用SAS软件RSREG过程进行多元回归分析,表3为实验结果的方差分析表。由表3可知,该回归模型的F值为165,大于在0.01水平上的F值,而失拟项的F值为4.41,小于在0.05水平上的F值,说明模型拟合结果较好;此外由表3可知,回归方程的一次项均差异极显著(p<0.0001),说明各个单因素都对分子量分布值有极显著影响;二次项中X1、X3对分子量分布值有极显著影响,而X2对分子量分布值有显著影响,说明三因素对分子量分布值的影响并不是简单的线性关系,但是因素之间的交互作用对分子量分布值的影响不显著[11-12]。
以分子量分布指数为Y值,得出与三种实验因素的编码值为自变量的回归方程。一次回归模型和二次回归模型的F值都可以说明模型方程差异极显著;回归方程的决定系数R2=0.9933,失拟项分析表明,该回归方程无失拟因素存在,回归模型与实测值能较好地拟合,因此可以用该模型分析各工艺参数对分子量分布指数的影响。由该回归方程偏回归系数绝对值的大小,可以得到各因素影响程度从大到小依次排列为壳聚糖的浓度、温度和乙酸浓度。
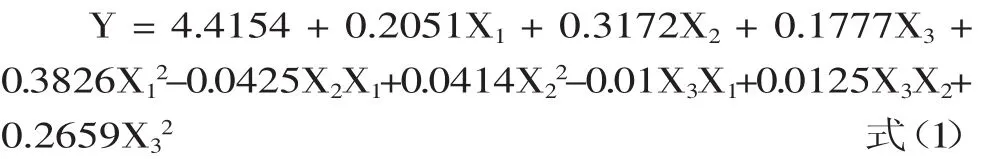
2.2.2 单因素效应分析 在单因子效应分析中,采用降维分析,将其它的因素固定在零水平,可分别得到各个单因素对应的回归方程,从此可以表述单因素变动时对分子量分布指数的影响,3个单因子效应方程如下,根据以上式(1)作图,可以得到单因子效应曲线图7。
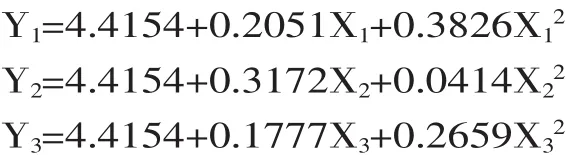
目前研究认为,超声波处理大分子物质的主要机理是机械性断键作用以及自由基的氧化还原反应,部分学者认为机械效应所作用的位点靠近最大分子的中心[13-16]。因此经过超声波处理后,大分子的壳聚糖变成小分子的壳聚糖,壳聚糖的平均分子量降低,而小分子的壳聚糖变化不大,分子量分布指数也减小。李瑾等研究证明随反应时间的延长,分子量大的壳聚糖更容易受到降解,其降解速率和降解速率常数降低较快,而分子量小的壳聚糖具有较低的降解速率和降解速率常数,随时间变化不明显[17]。
2.2.2.1 温度的效应分析 随着温度的升高,壳聚糖的分子量分布指数先减小后增大,这与单因素实验结果相一致。当温度的实验水平为-0.2680时,即温度为26.8℃时,分子量分布指数最小。当温度开始升高时,壳聚糖分子热运动加剧,快速变化的机械运动足以引起大分子的壳聚糖分子中共价键的断裂,而导致壳聚糖的降解,分子量分布指数的降低;同时温度升高,溶剂蒸气压随着增大,样品溶液内部的气体流失,超声空化作用产生的空泡爆裂强度较低,所释放出的能量也就较低,产生的自由基也少,因此由自由基氧化还原反应引起的壳聚糖的降解速率降低,分子量分布指数升高。从图7可以看出,在温度低于26.8℃时,分子量分布指数随温度的升高而降低趋势并不明显,而当温度高于26.8℃时,超声降解作用随着温度的升高而升高的趋势非常显著。这也说明了,壳聚糖的降解是机械效应与自由基的氧化还原反应的共同作用的结果。
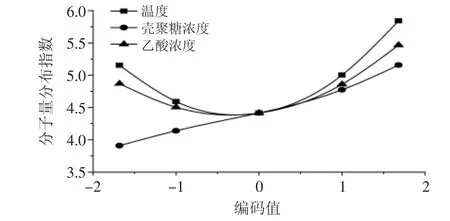
图7 单因子效应曲线Fig.7 Single factor utility curves
2.2.2.2 壳聚糖浓度的效应分析 浓度对分子量分布指数的影响接近线性关系,从图7可以看出,分子量分布指数随着体系中壳聚糖浓度的增大而增大。这与Chen Rong Huei等的研究结果一致[7]。壳聚糖溶液浓度较大时,在相同的超声功率下,分子链所接受的切点少,分子量变化幅度小,而浓度低时分子链所接受的切点多,分子量下降幅度大,壳聚糖降解速度快。同时壳聚糖浓度低时,溶液粘度也低,有利于空化泡的发生,从而使降解反应容易进行。
2.2.2.3 乙酸浓度的效应分析 乙酸浓度分子量分布指数的影响是二次关系,从图7可以看出,随着乙酸浓度的增加,壳聚糖的分子量分布指数是先减小后增大,这与单因素实验结果相一致。当乙酸浓度的实验水平为-0.3341时,即乙酸浓度为0.26mol/L时,分子量分布指数最小。Trzcinski等用低功率超声发生器降解壳聚糖时发现,动力学降解速率参数k随着乙酸浓度的增加而增加,表明超声能够加速壳聚糖酸性水解[15]。因为酸性水解是无规律的,因此这也说明了随着乙酸浓度的增加,分子量分布指数升高的原因。
将各模型分别固定2个因素于0水平,可以得到剩下1个因素与分子量分布指数的一元降维的回归模型,得到单因子边际效应方程。单因子边际效应方程反映了分子量分布指数随不同因子编码值的变化速率。单因子效应方程如下:


图8 边际效应曲线Fig.8 Marginal utility curves
根据单因子边际效应方程可以作出单因子边际效应曲线。由图8可知,随着因素水平的提高,X1、X2、X3的边际得率都呈上升趋势。3条单因子边际效应曲线中,超声温度对应的斜率最大,其次是乙酸浓度,最小的是壳聚糖浓度对应的斜率,这说明壳聚糖浓度的变化对分子量分布的边际得率的影响较其他两个因素稳定。当X1、X3的水平分别取-0.2680、-0.3341时,X1、X3的边际得率均为0,此时无减小效应,2个因素在该水平对应的分子量分布指数达到最小值,继续提高因素水平,边际得率为正值,分子量分布指数开始增大。
2.3 最佳工艺参数的确定及回归模型的验证

表4 回归模型验证和结果比较Table 4 Validation of regression model and result comparison
由SAS软件RSREG过程结果可知,当温度、乙酸浓度分别为24℃、0.27mol/L(相当于1.6%)时,壳聚糖浓度是越小越好,此时能取得分子量分布指数的最小值。壳聚糖浓度很低,每次的处理量太小,在实际操作中选择壳聚糖浓度为1%左右较适宜。理论值与实际值经验证误差为1.7%,所以该模型较好地反映了各因素对分子量分布指数的影响。如图9所示,经过超声波处理后壳聚糖分子量分布变窄了,分子量分布指数从11.51降到了4.25。
超声波处理后的壳聚糖的脱乙酰度基本没有改变,这与王伟、Baxter等人的研究结果一致[9,14],这表明超声波作用于壳聚糖时,对壳聚糖分子内存在的四种不同的糖苷键连接方式不存在特异性识别能力,所以不会选择性地切断壳聚糖分子的糖苷键,使得降解产物的脱乙酰度与壳聚糖原料相比没有改变。
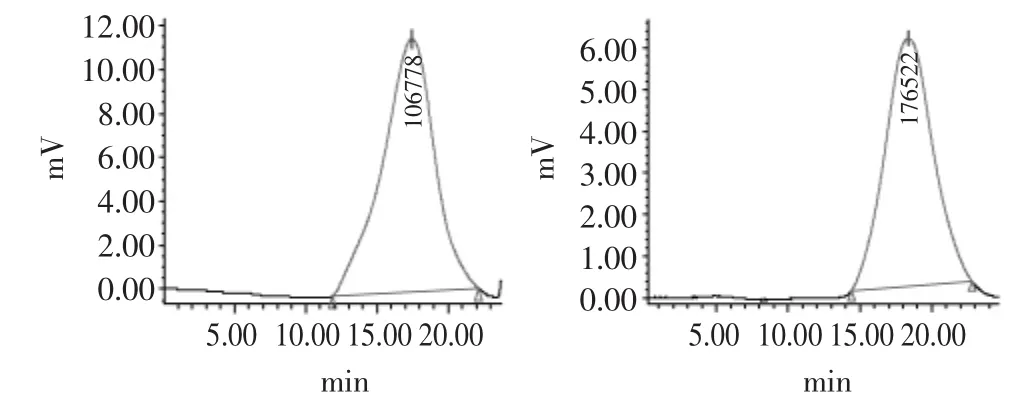
图9 壳聚糖的分子量分布Fig.9 Molecular weight distribution of chitosan
3 结论
对超声波处理后壳聚糖分子量分布指数的影响因素由大到小依次顺序是壳聚糖浓度、温度、乙酸浓度。采用三因素二次通用旋转设计,建立了温度、壳聚糖浓度和乙酸浓度3个因素对应的分子量分布指数的数学模型,实现了对工艺的优化,得出最佳工艺参数:温度为24℃、乙酸浓度为0.27mol/L、壳聚糖浓度根据实际需要定为1%,各个因素对分子量分布指数的影响由大到小依次顺序是壳聚糖浓度、温度、乙酸浓度。经过化学方法提取出来的壳聚糖一般分子量分布很宽,但是经过超声波处理后分子量分布变窄了,分子量分布系数从11.51降到了4.25。
[1]杨玉良,胡汉杰.高分子物理[M].北京:化学工业出版社,2001.
[2]夏文水.壳聚糖的生理活性及其在保健食品中的应用[J].中国食品学报,2003,3(1):77-81.
[3]蒋挺大.壳聚糖[M].第二版.北京:化学工业出版社,2006.
[4]Ottsy MH,Vaurn KM,Christensen BE.Preparative and analytical size-exclusion chromatography ofchitosans[J]. Carhohyhale Polymer1996,31:253-261.
[5]Mao Shirui,Augsten C,Mader K.Characterization of chitosan and its derivatives using asymmetricalflow field-flowfractionation:A comparison with traditional methods[J].Journal of Pharmaceutical and Biomedical Analysis 2007,45:736-741.
[6]Augsten C,Mader K.Characterizing molar mass distributions and molecule structures of different chitosans using asymmetrical flow field-flow fractionation combined with multi-angle light scattering[J].International Journal of Pharmaceutics 2008,351:23-30.
[7]Li CY,Chen CH,Yeh AI,et al.Preliminary study on the degradation kinetics of agarose and carrageenans by ultrasound [J].Food Hydrocolloids,1999,13(6):477-481.
[8]Kuijpers MWA,Kemmere MF,Keurentjes JTF.Calorimetric study of the energy efficiency for ultrasound-induced radical formation[J].Ultrasonic,2002,40:675-678
[9]王伟,秦汶.脱乙酰基甲壳素的超声波降解[J].化学通报,1989(9):44-46.
[10]Chen RH,Chang JR,Shyur JS.Effects of ultrasonic conditions and storage in acidic solutions on changes in molecular weight and polydispersity of treated chitosan[J].Carbohydrate Research,1997,299:287-294.
[11]赵思明.食品科学与工程中的计算机应用[M].北京:化学工业出版社,2005.
[12]潘丽军,陈锦权.实验设计与数据处理[M].南京:东南大学出版社,2008.
[13]Martijin WAK,Iedema PD,Kemmere MF,et al.The mechanism of cavitation-induced polymer scission experimental and computational verification[J].Polymer,2004,45:6461-6467.
[14]Baxter S,Zivanovic S,Weiss J.Molecular weight and degree of acetylation of high-intensity ultrasonicated chitosan[J].Food Hydrocolloids,2005,19(5):821-830.
[15]Trzcinski S,Staszewska DU.Kinetics of ultrasonic degradation and polymerization degree distribution of sonochemically degraded chitosan[J].Carbohydrate polymers,2004,56(4):189-198.
[16]Czecowska-Biskup R,Rokita B,Lotfy S,et al.Degradation of chitosan and starch by 360-KHZ ultrasound[J].Carbohydrate polymers,2005,60(2):175-184.
[17]李瑾,杜予民,姚评佳,等.壳聚糖超声可控降解及降解动力学研究[J].高分子学报,2007(5):401-406.
Study on preparing technique of chitosan with narrow molecular weight distribution
LI Xing-ke1,ZONG Wei1,XIA Wen-shui2,*
(1.Department of Food&Biological Engineering,Zhengzhou University of Light Industry,Zhengzhou 450002,China;2.School of Food Science and Technology,Jiangnan University,Wuxi 214122,China)
Preparing technique of chitosan with narrow molecular weight distribution through ultrasonic processed was investigated.According to the rotary unitized design principles,the influence of temperature and the concentration of chitosan and acetic acid on the polydispersity of chitosan after ultrasonic process were studied and the mathematical model was established based on the basis of single factor experiments.The preparation conditions of chitosan with narrow polydispersity were obtained by variance analysis and the optimization of mathematical model.Results showed that the optimum conditions of ultrasonic process were that the temperature of 24℃,the concentration of acetic acid of 0.27mol/L and the concentration of chitosan of 1%according to the actual situation.The polydispersity of chitosan decreased from 11.51 to 4.25 after ultrasonic processed.
chitosan;ultrasonic process;polydispersity;optimization
TS201.1
B
1002-0306(2012)14-0255-05
2011-11-29 *通讯联系人
李星科(1981-),男,讲师,博士,研究方向:多糖化学。
国家863计划项目(2007AA100401);重点实验室目标导向项目(SKLF-MB-200805);江苏省科技成果转化项目(BA2009082)。
