由环己烯经甲酸环己酯制备环己醇催化反应研究
2012-10-13杜文明王延吉
杜文明,薛 伟,李 芳,王延吉
(河北工业大学 绿色化工与高效节能河北省重点实验室,天津 300130)
环己醇是一种重要的化工中间体,广泛应用于有机化工工业、涂料和纺织工业等领域,主要用于生产己二酸、己二胺、环己酮、己内酰胺等,是酰胺类产品不可缺少的中间产品;也可用作肥皂的稳定剂,制造消毒药皂和去垢乳剂,用作橡胶、树脂、硝基纤维、金属皂、油类、酯类、醚类的溶剂,涂料的掺合剂,皮革的脱脂剂、脱膜剂、干洗剂、擦亮剂等.
生产环己醇的方法主要有:环己烷氧化法[1]、苯酚加氢法[2]与环己烯水合法[3-6].目前工业上生产环己醇主要采用环己烷氧化法,但该工艺中采用的氧化剂是空气,易与原料形成爆炸混合物,存在安全隐患,此外还有选择性差、能耗高等缺点[7-8];苯酚加氢工艺中原料苯酚的价格较高,且需要消耗大量氢气和能量,因此该工艺在应用上受到限制;环己烯水合制备环己醇是一个原子经济反应,选择性高,副产物少,是非常有前途的环己醇生产方法.1998年,日本旭化成公司将该工艺工业化.国内的神马集团、石焦集团等均引进了该工艺进行环己醇的生产.但环己烯水合反应受化学平衡的限制,平衡转化率较低,并且两种反应物的互溶能力极差,大大限制了该反应的进行.在旭化成工艺中,环己醇单程收率仅为10.8%.因此,开发具有高活性的双亲性催化剂以及新的环己烯水合工艺成为该工艺改进的关键问题.
Steyer等[9-11]研究了由环己烯间接水合制环己醇的催化反应过程.他们利用环己烯与甲酸反应生成甲酸环己酯,然后再将甲酸环己酯水解得到环己醇.该工艺克服了环己烯直接水合反应的热力学限制.经过模拟,Steyer等认为可以将环己烯接近100%的转化为环己醇.但该工艺使用了两个塔式反应器,并且使用离子交换树脂催化剂,存在设备投资大、操作复杂、催化剂寿命短等缺点.
本文以HZSM-5分子筛为催化剂,在间歇釜式反应器内,对由环己烯经甲酸环己酯间接水合制备环己醇催化反应进行了研究.分别考察了环己烯与甲酸酯化反应和甲酸环己酯水解反应的影响因素,优化了反应条件;考察了由环己烯经甲酸环己酯“一锅法”制备环己醇催化反应,在优化条件下,环己醇收率可达40%,远高于环己烯直接水合反应.
1 实验部分
1.1 环己烯与甲酸酯化反应
将一定量的环己烯、甲酸和HZSM-5催化剂置入反应釜中,密封后用N2气置换体系中的空气,搅拌同时升温至设定温度.反应一定时间后停止加热,并用冰水浴冷却反应釜至室温,泄压.过滤除去反应体系中的催化剂,并取上层油相进行色谱分析.
1.2 甲酸环己酯水解反应
将一定量的甲酸环己酯、去离子水和HZSM-5催化剂置入反应釜中,密封后用N2气置换体系中的空气,搅拌同时升温至设定温度.反应一定时间后停止加热,并用冰水浴冷却反应釜至室温,泄压.过滤除去反应体系中的催化剂,并取上层油相进行色谱分析.
1.3 由环己烯经甲酸环己酯“一锅法”制备环己醇
将一定量的环己烯、甲酸和HZSM-5催化剂置入反应釜中,用N2气置换体系中的空气后密封,搅拌同时升温至设定温度.反应一定时间后,用SSI II型泵向釜中打入一定量的去离子水,在设定的温度下继续反应一定的时间.反应结束后,用冰水浴冷却反应釜至室温,泄压.过滤除去反应体系中的催化剂,并取上层油相进行色谱分析.
1.4 产物分析
使用北京北分瑞利分析仪器有限公司生产的SP-3420型气相色谱对产物进行定性定量分析.色谱条件如下:SE-54毛细管柱(30 m×0.25mm),程序升温,初始温度80℃,升温速率10℃ m in1至280℃,保持20min;氢火焰离子检测器(FID),检测器温度280℃;汽化室温度280℃;载气+补充气流速30m L min1;进样量分流比1/20.
1.5 NH3-程序升温脱附(NH3-TPD)
采用美国M icromeriticsAutochem II-2920化学吸附仪进行催化剂的NH3-TPD表征.首先在500℃、He气氛进行表面净化,然后在110℃吸附探针分子NH3;用He气吹扫除去物理吸附的NH3,然后以10℃/min速率升温至500℃,用TCD检测脱附下来的NH3.
2 结果与讨论
由环己烯经甲酸环己酯制备环己醇主要涉及两个反应,一是环己烯与甲酸的酯化反应,二是甲酸环己酯的水解反应.对两反应进行了热力学分析,结果如图1所示.由图中数据可知,环己烯与甲酸的酯化为放热反应,低温有利于甲酸环己酯的生成;而甲酸环己酯水解为吸热反应,温度越高,越有利于其分解生成环己醇.此外,二反应的平衡常数远大于环己烯直接水合反应[6],说明由环己烯经甲酸环己酯制备环己醇在热力学上是有利的.只要开发出适宜的催化剂,就可以得到较高收率的环己醇.
为了得到最优的结果,分别对两个反应的影响因素进行了考察.
2.1 环己烯与甲酸酯化反应用催化剂筛选
Steyer[10]与Saha等[12]采用酸性离子交换树脂催化环己烯与甲酸的酯化反应,在一定的条件下,甲酸环己酯收率达到60%左右.但树脂存在耐高温性能差、易溶胀以及成本较高等缺点,从而限制了其工业应用.
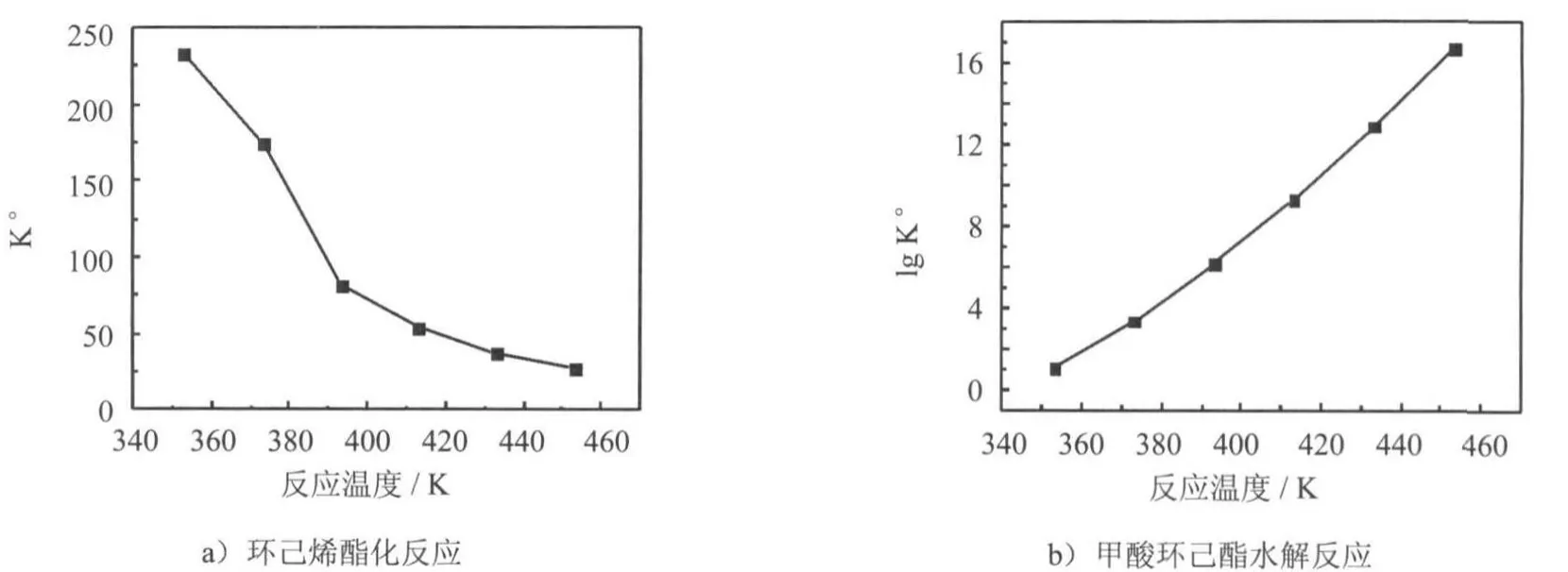
图1 温度对平衡常数K°的影响Fig.1 Effectof temperatureon theequilibrium constantK°
本文首先对环己烯与甲酸酯化反应用催化剂进行了筛选,选取常见的酸性分子筛HZSM-5、H进行考察,并采用一种酸性离子交换树脂D072H作为参比.在一定条件下考察了上述催化剂对该反应的催化性能,结果如表1所示.

表1 环己烯与甲酸酯化反应用催化剂筛选Tab.1 Catalyst screen for esterification of cyclohexenew ith form ic acid
由表1中数据可知,在给定条件下HZSM-5的催化性能最好,甲酸环己酯收率和选择性均为最高.由于HZSM-5分子筛具有十元环孔道结构(孔道直径为0.53~0.56 nm),与环己烯和甲酸环己酯的分子直径大小相当,因此具有较好的择形选择性,主要生成甲酸环己酯.
2.2 HZSM-5催化环己烯与甲酸酯化反应研究
2.2.1 反应温度的影响
环己烯与甲酸酯化反应是可逆放热反应,反应温度是重要的影响因素.反应温度过高,则平衡对逆反应有利;温度太低,则反应速率慢.因此,选择适当的反应温度非常重要.考察了反应温度对HZSM-5催化环己烯酯化反应的影响,结果如图2所示.由图可知,随着温度的升高,反应速率逐渐加快,甲酸环己酯收率逐渐增加;当反应温度为140℃时,甲酸环己酯收率为60.0%,选择性为97.6%.温度继续升高,副反应发生的可能性增加,并且化学平衡向甲酸环己酯分解的方向移动,因此甲酸环己酯选择性和收率均下降.
2.2.2 反应时间的影响
考察了反应时间对环己烯酯化反应的影响,结果如图3所示.由图3可知,甲酸环己酯选择性较高(约95%),但随反应时间的增加,变化并不明显;而其收率则随着反应时间的延长迅速增加,当反应时间为1 h时,甲酸环己酯收率为60.0%.继续延长反应时间,其收率变化不大.说明该反应速率较快,很快达到平衡.
2.2.3 HZSM-5用量的影响
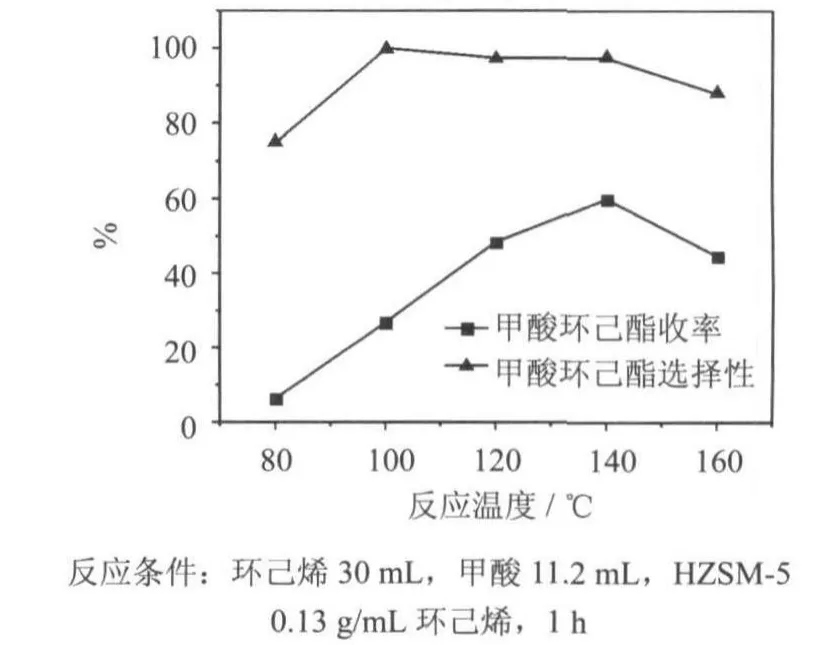
图2 反应温度对环己烯酯化反应的影响Fig.2 Effectof temperatureon esteri fication of cyclohexene with form ic acid
考察了HZSM-5用量对环己烯酯化反应的影响,结果如图4所示.由图可知,随着HZSM-5用量的增加,甲酸环己酯收率和选择性均逐渐增加.当HZSM-5用量为0.13 g/m L环己烯时,甲酸环己酯选择性为97.6%,收率为60.0%.继续增加催化剂用量,二者均略有下降.

图3 反应时间对环己烯酯化反应的影响Fig.3 Effectof reaction timeon esterification of cyclohexene with form icacid

图4 HZSM-5用量对环己烯酯化反应的影响Fig.4 EffectofHZSM-5amountonesteri fication of cyclohexene with formic acid
2.3 HZSM-5催化甲酸环己酯水解制备环己醇
对于甲酸环己酯的水解反应,目前尚未发现有直接的文献报道.Steyer等[11]曾在文献中提到了该过程,但并未给出详细的研究结果.通常,酯水解反应是碱或者酸催化反应.因此,本文选择固体酸HZSM-5分子筛作为催化剂,考察甲酸环己酯的水解反应.
2.3.1 反应温度对甲酸环己酯水解反应的影响
考察了反应温度对甲酸环己酯水解反应的影响,结果如图5所示.由图5可知,生成环己醇的选择性接近100%,并且随温度的变化较小.而环己醇收率则随温度的升高而增加,当温度为90℃时,环己醇收率为88.2%.继续升高温度,环己醇收率反而下降.
2.3.2 反应时间对甲酸环己酯水解反应的影响
考察了反应时间对甲酸环己酯水解反应的影响,结果如图6所示.由图可知,随着反应时间的增加,环己醇收率呈上升趋势.当反应时间为6 h时,环己醇收率为88.2%;继续延长时间,环己醇收率变化不大.环己醇选择性受反应时间的影响较小,均接近100%,说明该反应副产物很少.
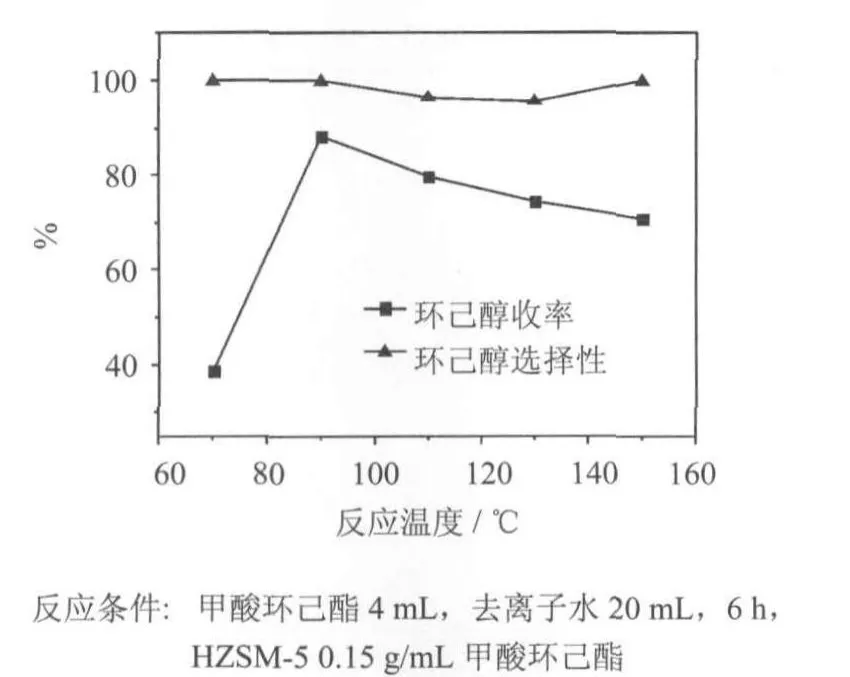
图5 反应温度对甲酸环己酯水解的影响Fig.5 Effectof reaction tem peratureon hydrolysis of cyclohexyl formate

图6 反应时间对甲酸环己酯水解的影响Fig.6 Effectof reaction timeonhydrolysisofcyclohexyl formate
2.3.3 HZSM-5用量对甲酸环己酯水解反应的影响
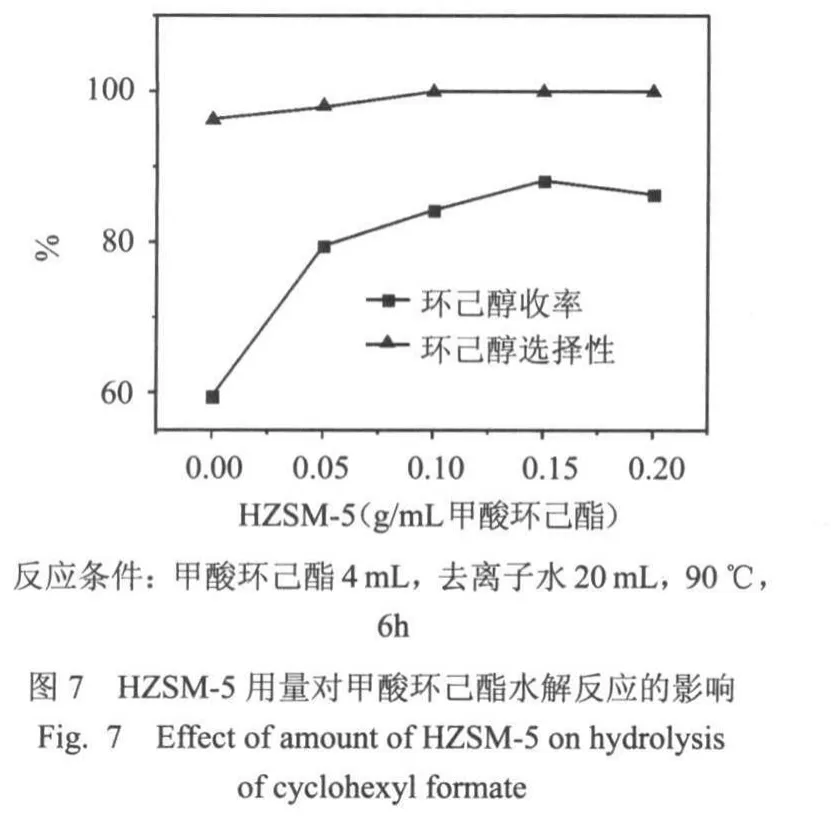
考察了HZSM-5用量对甲酸环己酯水解反应的影响,结果如图7所示.由图可知,随着HZSM-5用量的增加,环己醇收率逐渐升高.当HZSM-5用量为0.15 g/m L甲酸环己酯时,环己醇收率最高为88.2%.环己醇选择性接近100%,且受HZSM-5用量的影响不明显.
2.3.4 水用量对甲酸环己酯水解反应的影响
由于甲酸环己酯水解为可逆反应,水作为反应原料,量越大越有利于反应向正方向进行.考察了水用量对甲酸环己酯水解反应的影响,结果如图8所示.由图可知,随着水用量的增加,环己醇收率呈上升趋势.当水用量超过10m L/m L甲酸环己酯时,其上升趋势变缓.这是由于水用量过大时,降低了甲酸环己酯的浓度,从而使反应速率变慢.水用量对环己醇选择性的影响较小,其数值均接近100%,几乎无副反应发生.

2.4 由环己烯经甲酸环己酯“一锅法”制备环己醇
由前述研究可知,环己烯酯化反应和甲酸环己酯水解反应的收率均较高,可望利用该方法获得较环己烯直接水合反应更高的环己醇收率.但经甲酸环己酯的方法为两步反应,相对于原有的环己烯直接水合工艺,在资源利用率、能耗上处于不利的地位.考虑到两反应的反应条件接近,并使用相同的催化剂,本文试图采用“一锅法”操作方式,实现由环己烯经甲酸环己酯直接制备环己醇.并且,由于甲酸环己酯水解反应的平衡常数较大,在“一锅法”操作时,甲酸环己酯的转化可以促进环己烯的酯化反应.
考察了由环己烯经甲酸环己酯“一锅法”制备环己醇催化反应,结果如表2所示.
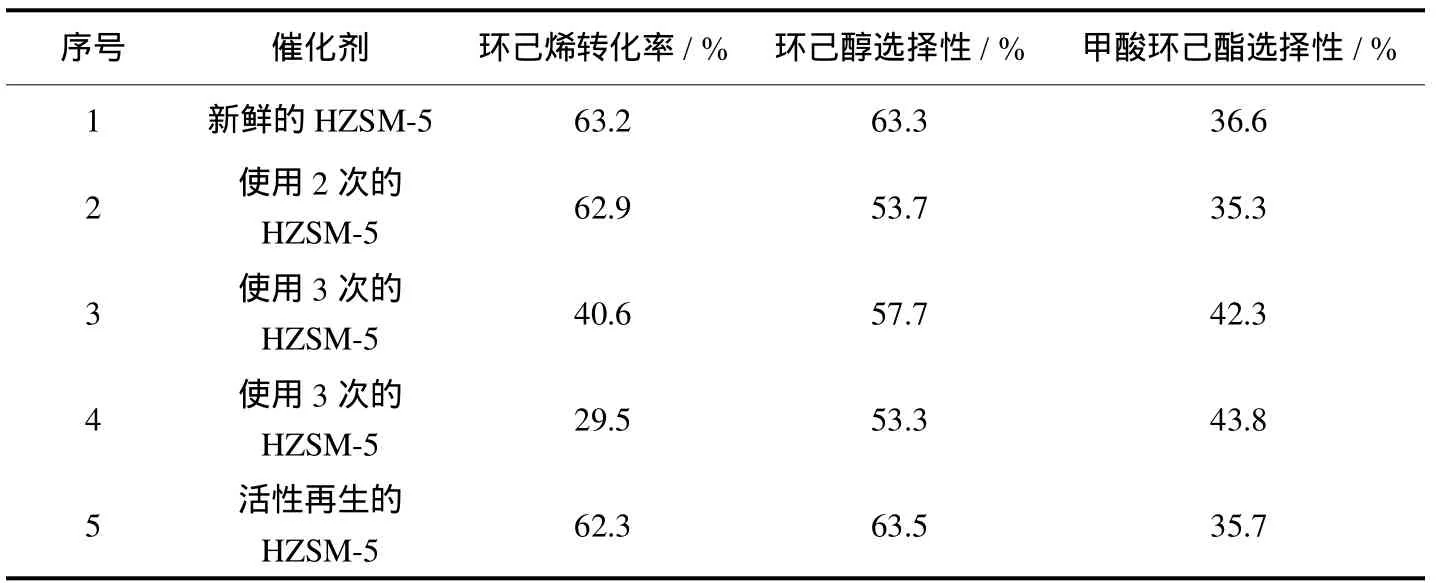
表2 由环己烯经甲酸环己酯“一锅法”制备环己醇Tab.2 One-pot synthesisof cyclohexanol from cyclohexene via cyclohexyl formate
由于水对环己烯酯化反应有阻碍作用,因此采用动态操作,控制水的加入时间.当环己烯与甲酸进行酯化反应一定时间后,再利用高压计量泵将水加入反应釜内.由表2中实验1可知,在所选条件下,环己醇收率可达40.0%,远高于环己烯直接水合反应.并且反应产物中的甲酸环己酯经分离、提纯后还可再水解得到环己醇.
2.5 催化剂失活与再生
考察了“一锅法”制备环己醇反应用催化剂HZSM-5的寿命.将使用过的催化剂经洗涤、干燥后重新用于该反应,结果如表2中实验2~4所示.随着催化剂使用次数的增加,环己醇收率下降趋势明显,但选择性变化不大;并且催化剂颜色由白色逐渐变为棕色.推测部分有机物吸附在催化剂表面,不能通过洗涤除去,从而覆盖了部分表面酸中心,使其活性降低.为了使催化剂活性再生,将使用4次的催化剂在550℃空气气氛中焙烧再生,然后重新用于催化该反应,结果见表2中实验5.由活性评价结果可知,再生后催化剂恢复了活性,并且环己醇选择性略有增加.
对使用前后及再生的HZSM-5进行NH3-TPD表征,结果如图9所示.由图可知,在新鲜 HZSM-5、使用4次后失活及再生催化剂表面均有NH3脱附温度180~200℃和380~400℃2种酸中心.但是,与新鲜催化剂相比,失活催化剂及再生催化剂表面酸中心强度有所降低,且酸量也略有减少,但后两者表面酸中心强度和酸量十分接近.这与表2中活性评价结果并不一致.由于催化剂样品进行NH3-TPD表征时,首先需要在高温He气中进行表面净化处理.因此推测流动的He气将吸附在失活催化剂表面的有机物带走,使酸中心重新暴露出来,从而与再生催化剂的NH3-TPD表征结果接近.

3 结论
1)考察了环己烯与甲酸酯化反应的影响因素,优化了反应条件,产物甲酸环己酯收率最高为60.0%,选择性97.6%;考察了甲酸环己酯水解反应的影响因素,在较优条件下,环己醇收率为88%,选择性接近100%.
2)考察了由环己烯经甲酸环己酯“一锅法”制备环己醇催化反应,环己醇收率最高可达40%,远高于环己烯直接水合反应.所用HZSM-5催化剂的活性随着使用次数的增加而逐渐降低,其失活是由于有机物覆盖了表面部分酸中心而导致.将失活催化剂在550℃空气中焙烧,可使其再生.
[1]Suresh A K,SridharT,PotterOE.Mass transferand solubility inautocatalyticoxidationofcyclohexane[J].AIChEJournal,1988,34(1):55-68.
[2]项益智,李小年.苯酚液相原位加氢合成环己酮和环己醇 [J].化工学报,2007,58(12):3041-3045.
[3]Hiroshi F,FujinaoM,Masao K.Preparation of cycloalkanols by catalytic hydration of cycloalkenes:Jpn Kokai Tokkyo Koho,JP 02040334 [P].1990-02-09.
[4]庞小英,姚志龙.环己烯水合制环己醇研究进展 [J].工业催化,2010,18(Z1):114-119.
[5]吴济民,戴新民,陈聚良,等.环己烯水合反应生成环己醇工艺条件的优化 [J].化工进展,2003,22(11):1222-1224.
[6]刘媛.苯选择加氢和环己烯水合催化反应过程研究 [D].天津:河北工业大学,2007.
[7]张丽芳,陈赤阳,项志军.环己烷氧化制备环己酮和环己醇工艺研究进展 [J].北京石油化工学院学报,2004,12(2):39-42.
[8]郭志武,靳海波,佟泽民.环己酮、环己醇制备技术进展 [J].化工进展,2006,25(8):852-859.
[9]Steyer F,Sundmacher K.VLE and LLE data set for the systemcyclohexane + cyclohexene + water + cyclohexanol + formic acid + formic acid cyclohexyl ester [J].J Chem Eng Data,2005,50(4):1277-1282.
[10]Steyer F,Sundmacher K.Cyclohexanol production via esterification of cyclohexene with formic acid and subsequent hydration of the esters reaction kinetics [J].Ind Eng Chem Res,2007,46(4):1099-1104.
[11]Steyer F,Freund H,Sundmacher K.A novel reactive distillation process for the indirect hydration of cyclohexene to cyclohexanol using a reactive entrainer [J].Ind Eng Chem Res,2008,47(23):9581-9587.
[12]Saha B,SharmaM M.Esterification of form ic acid,acrylic acid andmethacrylic acid w ith cyclohexene in batch and distillation column reactors:ion-exchange resinsas catalysts[J].Reactiveand Functional Polymers,1996,28(3):263-278.
