C-MSnO3(M=Ca, Sr, Ba)纳米复合物的合成及其电化学性能
2012-09-26卢周广唐有根黄远提
胡 菁,卢周广,唐有根,黄远提
(中南大学 化学化工学院 有色金属资源化学教育部重点实验室,长沙 410083)
C-MSnO3(M=Ca, Sr, Ba)纳米复合物的合成及其电化学性能
胡 菁,卢周广,唐有根,黄远提
(中南大学 化学化工学院 有色金属资源化学教育部重点实验室,长沙 410083)
用直接沉淀法制备前躯体MSn(OH)6,把导电炭黑(Super-P)与前躯体一起球磨后煅烧,合成MSnO3(M=Ca,Sr,Ba),并系统研究其作为锂离子电池负极材料的电化学性能。用SEM和XRD表征产物的形貌和结构,用恒电流充放电和循环伏安测试产物的电化学性能。结果表明:CaSnO3、SrSnO3和BaSnO3的首次充电容量分别为624.9、383.8和330.1 mA·h/g;CaSnO3经过20次循环之后,在0.1C、0.5C、1C倍率下的充电容量分别为510、390和258 mA·h/g,而球磨CaSnO3相应地分别为413、297、183 mA·h/g。这说明加Super-P球磨的CaSnO3样品循环稳定性和高倍率性能均得到较大提高。
锂离子电池;负极;锡酸盐;复合氧化物;纳米材料
进入21世纪之后,人类面临的两大挑战——能源危机和环境问题变得更加严峻,而交通运输作为化石燃料消耗和人为温室气体排放的主要方面,使得发展“绿色交通”变得刻不容缓。零排放、无污染的电动汽车有着广阔的发展前景,而电动车的核心在于作为动力的电池[1−2]。锂离子电池由于具有工作电压高、比容量高、充放电循环性能好、应用温度范围宽、自放电率低、可快速充电、无记忆效应和对环境危害小等其他可充电二次电池无法比拟的优点[3−4],因此成为动力电源和便携电源的首选。负极材料是电池的重要组成部分,是提高电池性能的关键之一。
目前,广泛应用的商业负极材料为炭材料其理论容量较低(仅为372 mA·h/g),且炭电极的工作电位和锂的相近,过充时可能析出锂枝晶,以致造成短路,存在安全隐患;此外,其与有机溶剂相容性差,易发生溶剂共插入现象,从而降低插锂性能[5]。1997年,日本富士胶片公司首先报道了作为锂离子电池负极材料用的无定型锡基复合氧化物,锡基氧化物具有高比容量(SnO理论比容量为875 mA·h/g,SnO2的理论比容量为782 mA·h/g)[6]、价格便宜、合成容易、环境友好等特点,吸引了研究者的广泛关注。虽然作为锂电池负极材料,锡基氧化物工作电压较高(MSnO3类材料氧化还原电位大约为0.1~0.6 V),和常规的正极材料配合,电池能量密度降低,不利于应用。但从另一面来说,正因为其具有比石墨高的工作电压,可以有效避免过充时金属锂析出造成短路的问题。因此,锡基氧化物另一个缺点是充放电过程中体积变化很大,引起活性物质的粉化和团聚,导致循环性能较差,且首次不可逆容量较大[7]。大量研究表明,在氧化锡中复合一些金属或非金属氧化物以及导电碳等可有效缓冲电化学反应过程中因体积膨胀引起的应力,从而降低材料的不可逆容量损失,大大提高材料的循环稳定性[8−9]。HOU等[10]用固相法合成反尖晶石结构的Zn2SnO4,经过50次充放电循环之后,充电比容量保持为689 mA·h/g。
最近,碱土金属锡酸盐MSnO3(M=Ca, Ba, Sr)作为一种新型锂离子电池负极材料吸引了研究者的广泛关注[9,11−14],但对于MSnO3(M=Ca, Ba, Sr)作为锂离子电池负极材料的系统研究还未见文献报道。本文作者用沉淀−球磨−热解法合成MSnO3(M=Ca, Sr, Ba)纳米复合氧化物,并系统研究其作为锂离子电池负极材料的电化学性能。
1 实验
1) 称取0.01 mol Na2SnO3(AP,天津)、0.011 mol MCl2(AP,天津)和0.1g PVP(AP,天津),分别溶于10 mL去离子水中;搅拌溶解之后,在磁力搅拌条件下把MCl2溶液缓慢滴加到Na2SnO3溶液中;滴加完之后,把PVP溶液加入混合溶液中,磁力搅拌20 min,超声波震荡5 min;然后减压抽滤,用去离子水多次洗涤,于70~90 ℃干燥6~10 h,得到前躯体MSn(OH)6。
2) 由于导电炭黑(Super-P)在乙醇中分散性较好,而MSnO3在水中分散性较好,因此,取乙醇和水作为混合溶剂更利于球磨过程中两种物质均匀混合。量取15 mL去离子水,再加入15 mL乙醇作为溶剂,称取产物质量换算为MSnO3质量的2/7的Super-P,和产物一起放入球磨罐中,搅拌均匀,球磨10 h;球磨后产物于70 ℃干燥10 h,干燥后于600 ℃氩气氛中煅烧3 h,得到黑色粉末状产物C-MSnO3。
3) 量取15 mL去离子水,再加入15 mL乙醇作为溶剂,直接加入CaSn(OH)6后球磨10 h,球磨产物于70 ℃干燥10 h,然后于600 ℃氩气氛中煅烧3 h,得到白色粉末状产物CaSnO3。
样品的物相采用日本JEOL公司的X射线衍射仪(D/ruax2550PC, JEOL, Japan;Cu Kα,λ=1.540 56 Å)分析,样品的表面形貌用日本电子的扫描电子显微镜(JSM−6360LV)进行表征。
按MSnO3-C和粘结剂PVDF质量比为9:1称取试剂量于玛瑙研钵中,研磨混合均匀后加入适量的NMP,研磨均匀后,把膏体均匀涂于铜箔上制成研究电极;按CaSnO3、Super-P和PVDF质量比为7:2:1称取试剂量于玛瑙研钵中,研磨混合均匀后加入适量的NMP,研磨均匀后,把膏体均匀涂于铜箔上制成研究电极。采用金属锂片做对电极,聚丙烯多孔膜做隔膜,1.0 mol/L LiPF6和EC+DMC (V(EC):V(DMC)=1:1)的混合溶液做电解液,在无水无氧操作箱(德国,MB-BL−1)中组装成2016型扣式电池。采用充放电测试仪(中国武汉,Land-CT 2001A)进行电池充放电测试,电压范围为1.5~0 V(vs Li+/Li);采用电化学工作站(中国上海,CHI660D)进行循环伏安测试,扫描速度为58 μV/s,电压范围为1.5~0V (vs Li+/Li)。
2 结果与讨论
2.1 样品的结构和形貌
图1所示为用沉淀−球磨−热解法合成的MSnO3(M=Ca, Sr, Ba)的XRD谱。由图1可以看出,所制备样品的主要衍射峰分别符合钙钛矿结构的CaSnO3(PDF: 31—0312)、SrSnO3(PDF: 22—1142)和BaSnO3(PDF: 15—0780),没有发现其它杂相峰,说明所合成的MSnO3均为纯相,且所添加的Super-P没有影响MSnO3(M=Ca, Sr, Ba)的晶相。BaSnO3是相对理想的钙钛矿结构,属立方晶系,CaSnO3与SrSnO3则由于八面体的倾斜而扭曲为正交晶系;BaSnO3的结构最稳定,因此要容易形成些。

图1 MSnO3(M=Ca, Sr, Ba)样品的XRD谱Fig. 1 XRD patterns of MSnO3(M=Ca, Sr, Ba) samples
图2所示为所制备样品的SEM像。CaSnO3样品为类球形的纳米颗粒,平均粒度大约为100 nm,但也有一些粒度约为1 μm的团聚体(见图2(a))。SrSnO3为纳米棒状颗粒,直径为30~50 nm,长度为2~5 μm(见图2(b))。对于BaSnO3样品,除了少部分为微米级片状晶体,大部分为粒度约为50 nm的均匀纳米颗粒,其中粒度很小(<20 nm)的颗粒为加入的导电炭黑(见图2(c))。由此可知,球磨使得导电炭黑非常均匀地分布于MSnO3中,由于Super-P可以有效抑制颗粒在煅烧过程中长大,且由于Super-P颗粒均匀地分布在MSnO3周围还可以提高产品的导电率,从而有利于提高产品的电化学性能。
2.2 材料的电化学性能
图3所示为MSnO3电极的首次充放电曲线图,放电电流密度为50 mA/g,电压范围为1.5~0.01 V。由图3可知,CaSnO3的初始放电容量为1 373.3 mA·h/g,初始充电容量为624.9 mA·h/g,不可逆容量损失(ICL)为54.5%;SrSnO3的初始放电容量为870.7 mA·h/g,初始充电容量为383.8 mA·h/g,ICL为42.4%;BaSnO3的初始放电容量为665.9 mA·h/g,初始充电容量为330.1 mA·h/g,ICL为62.1%。CaSnO3的初始放电容量高于理论值(1 089 mA·h/g),这主要内归因于Li与电解液反应形成固态电解质膜(SEI);SrSnO3和BaSnO3的初始放电容量略低于理论值,可能是由于活性物质未完全利用。MSnO3放电曲线主要有两个平台,第一个平台在0.7 V左右,CaSnO3的第二个平台开始于0.4 V左右,而BaSnO3与SrSnO3的第二个平台则开始于0.3 V左右。
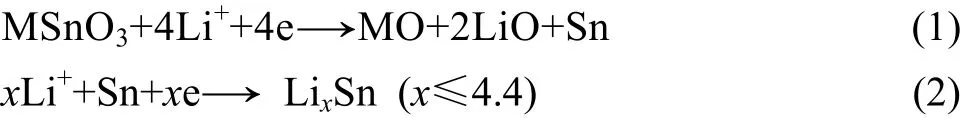

图3 MSnO3电极首次充放电曲线图.Fig. 3 Initial charge and discharge curves of MSnO3anode
图4所示为MSnO3的首次循环伏安图,扫描速度为58 μV/s,电压范围为1.5~0 V (vs Li+/Li)。CaSnO3的阴极扫描曲线显示在0.8-0.6V的有一个非常小的还原峰,然后在0.2V开始电流激增,出现一个还原尖峰,阳极扫描曲线在约0.7 V处有一个氧化宽峰,结合首次充放曲线(见图3),0.8~0.6 V处的小峰归因于CaSnO3形成金属Sn的反应,见方程(1)。0.2 V附近的还原尖峰对应合金Li4.4Sn的形成。氧化还原电对大约位于0.2 V/0.7 V,归因于可逆反应,见方程(2)。SrSnO3的循环伏安图与CaSnO3的曲线十分相似,表明两者具有相似的储锂机理。BaSnO3除了具有和CaSnO3、SrSnO3相似的氧化还原峰之外,还在约0.3 V出现了一个弱还原峰,而在约0.7 V的氧化宽峰则由3个弱峰组成。因此,BaSnO3还可能存在以下储锂机理,如方程(3)和(4)所示。这有可能是由于从Ca、Sr到Ba,电负性逐渐减小,因此Ba—O键较弱,容易断裂形成金属钡。
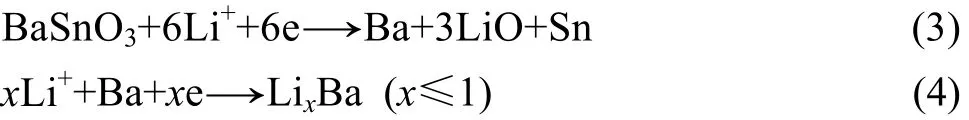
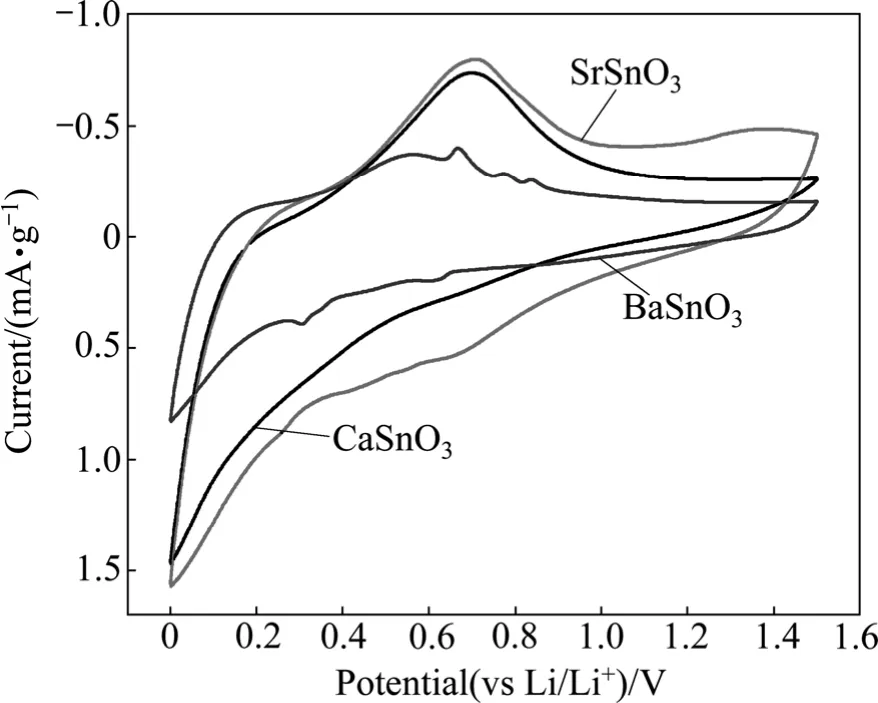
图4 MSnO3(M=Ca, Sr, Ba)电极的循环伏安曲线Fig. 4 Cyclic voltammogram curves of as-prepared MSnO3(M=Ca, Sr, Ba) anodes
图5所示为MSnO3前10次循环的比容量,除第一次充放电不可逆容量损失较大外,从第二个循环开始,库伦效率立刻提高到90%以上。首次充放电不可逆容量损失较大主要是由于反应(1)是不可逆的,SEI膜的形成也是不可逆容量损失的部分原因[15−17]。CaSnO3、SrSnO3和BaSnO3第10次循环的可逆容量分别为542.8、282.6和217.3 mA·h/g,分别约为其首次可逆容量的87%、74%和66%。可见,CaSnO3、SrSnO3和BaSnO3相比较,CaSnO3的可逆比容量最高,同时循环稳定性也最好。CaSnO3较于SrSnO3和BaSnO3更为廉价、环保,因此更具研究价值。
图6所示为加Super-P球磨的CaSnO3样品(图中显示为CaSnO3/C)和普通球磨CaSnO3样品在250 mA·h/g下放电前50次循环的充放电比容量和库伦效率。从图6可以看出,加Super-P球磨的CaSnO3放电时性能更为稳定,容量衰减较慢,50次循环后,充电容量为344.5 mA·h/g,保有率为79%,而普通球磨CaSnO3的容量为206 mA·h/g,保持率只有66%;加Super-P球磨的CaSnO3库伦效率较高,稳定在98%左右,而普通球磨的CaSnO3库伦效率则为94%左右;SHARMA等[15]用溶胶−凝胶法制备的CaSnO3在60 mA·h/g(0.12C)下充放45次后可逆容量稳定在350 mA·h/g。由此可见,添加Super-P球磨后,CaSnO3活性电极材料的稳定性得到明显提高。这归因于球磨过程有利于Super-P均匀分布于CaSnO3中,使得Super-P和活性材料充分接触,在大电流放电时可以起到缓解膨胀和抑制团聚的作用。
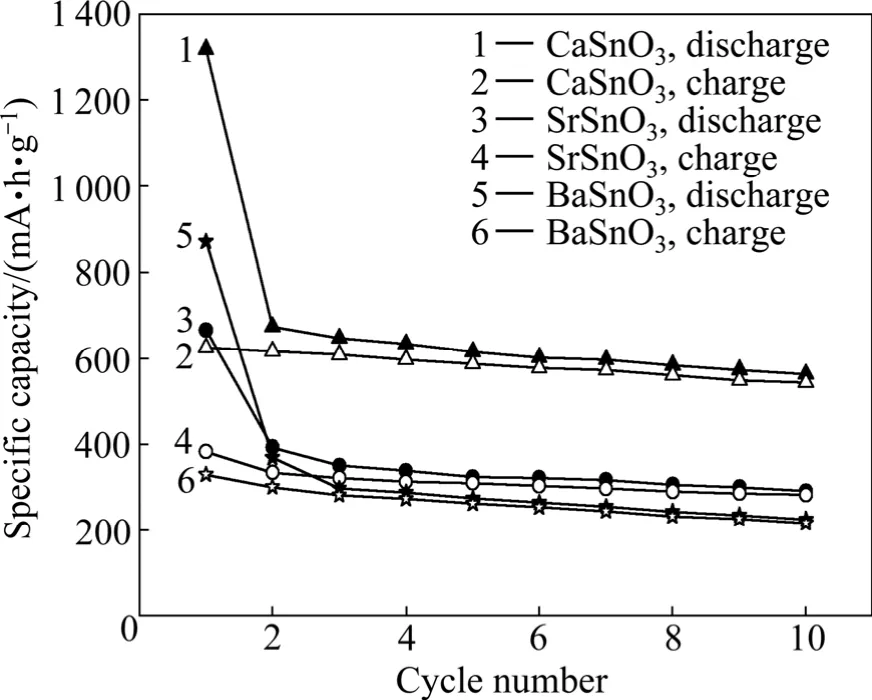
图5 MSnO3(M=Ca, Sr和Ba)在50 mA·h/g电流密度下前10次循环比容量和循环次数图Fig. 5 Specific capacity of MSnO3(M=Ca, Sr, and Ba) samples as function of cycle number during first ten cycles at current density of 50 mA·h/g

图6 加Super-P球磨CaSnO3/C样品和普通球磨CaSnO3样品在0.5C下的充放电循环性能Fig. 6 Charge and discharge cycling stability of CaSnO3/C sample ball milled with Super-P and traditional milled CaSnO3sample at 0.5C
高倍率充放电是衡量电极性能的重要指标。图7所示为添加Super-P球磨的CaSnO3样品和普通球磨CaSnO3样品在不同倍率下(0.1C、0.5C、1C)放电第20次循环的充放电曲线,从图7可以看出,加Super-P球磨的CaSnO3经过20次循环之后,0.1C、0.5C、1C的充电容量分别为510、390和258 mA·h/g,0.5C下的容量保有率为77%,1C下的容量保有率为51%;而普通球磨CaSnO3经过20次循环之后,0.1C、0.5C和1C下的充电容量分别为413、297和183 mA·h/g,0.5C的容量保有率为 72%,而1C下的容量保有率为44%。可见添加Super-P球磨后,样品的倍率性能得到有效提高,这是因为球磨过程中加入的Super-P在活性物质中均匀分布,起到了骨架支撑和提供电子通道的双重作用,有效解决了电极粉化和导电不良的问题,使得材料的电导率增加,使充放电过程中材料的极化变小,更有利于锂离子的传输。
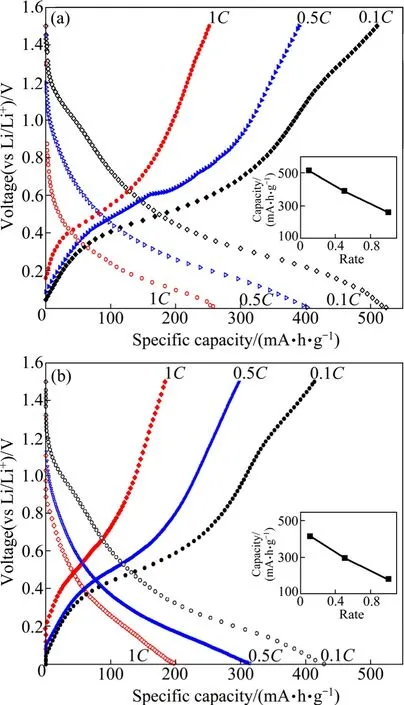
图7 加Super-P球磨和普通球磨制备的CaSnO3样品在不同电流倍率下第20次充放电循环曲线Fig. 7 20th charge and discharge cycling curves of CaSnO3samples prepared by ball-milled with Super-P (a) and traditional ball-milled method (b) at different current rates
3 结论
1) 采用直接沉淀法制备前躯体MSn(OH)6,并把通常作为导电剂的Super-P与前躯体一起球磨后煅烧,合成MSnO3(M=Ca,Sr,Ba),用作锂离子电池负极材料。
2) 通过SEM、XRD测试对合成的MSnO3(M=Ca,Sr,Ba)进行表征,发现该材料是钙钛矿型纳米材料。
3) 循环伏安测试和充放电性能测试表明CaSnO3、SrSnO3、BaSnO3具有相似而非完全一致的储锂机理。CaSnO3、SrSnO3、BaSnO3的充电容量分别达到624.9、383.8和330.1 mA·h/g。从性能、价格、环保等方面综合考虑,CaSnO3更具研究价值。
4) 与普通球磨的CaSnO3相经,加Super-P球磨的CaSnO3/C的循环稳定性得到明显提高,而且具有更加优异的高倍率性能。
REFERENCES
[1]LAM L T, LOUEY R. Development of ultra-battery for hybrid-electric vehicle applications [J]. Journal of Power Sources, 2006, 158: 1140−1148.
[2]戴德彬, 李中奇, 王彩霞. 电动车用超级蓄电池的研究[J]. 蓄电池, 2009, 46(2): 58−72. DAI De-bin, LI Zhong-qi, WANG Cai-xia. The research of super storage battery used in electric car [J]. Chinese Labat Man, 2009, 46(2): 58−72.
[3]郭炳煜, 徐 徽, 王先友, 肖立新. 锂离子电池[M]. 长沙: 中南大学出版社, 2002: 2. GUO Bing-yu, XU Wei, WANG Xian-you, XIAO Li-xin. Lithium ion battery [M]. Changsha: Central South University Press, 2002: 2.
[4]黄可龙, 王兆翔, 刘素琴. 锂离子电池原理与关键技术[M].北京: 化学工业出版社, 2008: 5. HUANG Ke-long, WANG Zhao-xiang, LIU Su-qin. The principle and key technology of lithium ion battery [M]. Beijing: Chemical Industry Press, 2008: 5.
[5]COURTNEY I A D, AHN J R. Electrochemical and in situ X-ray diffraction studies of the reaction of lithium with tin oxide composite [J]. Journal of the Electrochemical Society, 1997, 144(6): 2045−2052.
[6]IDOTA Y, KUBOT A, MATSUFUJI Y, MAEKAWA T. Tin-based amorphous oxide: A high-capacity lithium-ion-storage material [J]. Science, 1997, 276: 1395−1399.
[7]COURTNEY I A, MCKINNON W R, DAHN J R. On the aggregation of tin in SnO composite glasses caused by the reversible reaction with lithium [J]. Journal of The Electrochemical, 1999, 146(1): 59−68.
[8]CONNER P A, IRVINE J T S. Novel tin oxide spinel-based anodes for Li-ion batteries [J]. Journal of Power Sources, 2001, 97(8): 223−225.
[9]BELLIARD F, CONNOR P A, IRVINE J T S. Novel tin oxide-based anodes for Li-ion batteries [J]. Solid State Ionics, 2000, 135: 163−167.
[10]HOU X H, CHENG Q, BAI Y, ZHANG W F. Preparation and electro-chemical characterization of Zn2SnO4as anode materials for lithium ion batteries [J]. Solid State Ionics, 2010, 181: 631−634.
[11]雷钢铁, 高德淑, 李朝晖, 苏光耀. 锂离子电池锡基负极材料研究进展[J]. 材料导报, 2001, 15(7): 36−39. LEI Gang-tie, GAO De-shu, LI Chao-hui, SU Guang-yao. Progress in studies of Tin-based anode materials for lithium ion battery [J]. Materials Review, 2001, 15(7): 36−39.
[12]YUAN W S, TIAN Y W, LIU G Q. Synthesis and electrochemical properties of pure phase Zn2SnO4and composite Zn2SnO4/C [J]. Journal of Alloys and Compounds, 2010, 506(2): 683−687.
[13]MOHAMEDI M, LEE S J, TAKAHASHI D, NISHIZAWA M, ITOH T, UCHIDA I. Amorphous tin oxide films: Preparation and characterization as an anode active material for lithium ion batteries [J]. Electrochimica Acta, 2001, 46(8): 1161−1168.
[14]HU X Y, TANG Y W, XIAO T, JIAN J, JIA Z Y, LI D W, LI B H, LUO L J. Rapid synthesis of single-crystalline SrSn(OH)6nanowires and the performance of SrSnO3nanorods used as anode materials for Li-ion battery[J]. The Journal of Physical Chemistry C, 2010, 114(2): 947−952.
[15]SHARMA N, SHAJU K M, SUBBA R, CHOWDARI B V R. Sol-gel derived nano-crystalline CaSnO3as high capacity anode material for Li-ion batteries [J]. Electrochemistry Communications, 2002, 4(12): 947−952.
[16]SHARMA Y, SHARMA N, SUBBA R, CHOWDARI B V R. Studies on Nano-CaO·SnO2and Nano-CaSnO3as anodes for Li-ion batteries [J]. Chemistry of Materials, 2008, 20(21): 6829−6839.
[17]何则强, 熊利芝, 麻明友, 肖卓炳, 吴明显, 黄可龙. 新型锂离子电池CaSnO3负极材料的湿化学制备与电化学性能[J].无机化学学报, 2005, 21(9): 1311−1315. HE Ze-qiang, XIONG Li-zhi, MA Ming-you, XIAO Zhuo-bing, WU Ming-xian, HUANG Ke-long. Electrocchemical characterization of novel CaSnO3anode material for lithium ion batteries prepared by wet chemical route [J]. Chinese Journal of Inorganic Chemistry, 2005, 21(9): 1311−1315.
(编辑 何学锋)
Preparation of C-MSnO3(M = Ca, Sr, Ba) nanocomposites and its electrochemistry performances
HU Jing, LU Zhou-guang, TANG You-gen, HUANG Yuan-ti
(Key Laboratory of Resource Chemistry of Nonferrous Metals, Ministry of Education, School of Chemistry and Chemical Engineering, Central South University, Changsha 410083, China)
The precursors of MSn(OH)6(M=Ca, Sr, Ba) were prepared by direct precipitation method. After the precursors and Super-P were homogeneously mixed together by ball-milling, they were calcined to prepare the MSnO3(M = Ca,Sr, Ba) nanocomposites. The electrochemical properties of the products as anode materials for lithium-ion batteries were systematically investigated. SEM and XRD were taken to measure the morphologies and structures of the products. The electrochemical properties of the samples were examined by galvanostatic cycling and cyclic voltammetry. The results show that the first charge capacities of CaSnO3, SrSnO3and BaSnO3are 624.9, 383.8 and 330.1 mA·h/g, respectively. Particularly, for the CaSnO3sample, after 20 cycles, the remaining specific capacities are 510, 390 and 258 mA·h/g at 0.1C, 0.5Cand 1C, respectively. As a comparison, for the traditional ball-milling CaSnO3samples, the remaining specific capacities are only 413, 297, and 183 mA·h/g, respectively. The cycling stability and high rate capability of the CaSnO3sample are substantially improved after ball-milling with Super-P.
lithium ion batteries; anode; stannate; composite oxides; nanomaterial
TM912.9
A
国家自然科学基金资助项目(21001117),中南大学仪器共享开放基金资助项目
2011-03-01;
2011-08-31
卢周广,副教授,博士;电话:0731-88830886; E-mail: zglu@csu.edu.cn
1004-0609(2012)09-2614-06
