运用一元二次方程计算溶液的pH值
2012-09-25王亚玲苟如虎唐致卉刘伯渠卢新生
王亚玲,苟如虎,唐致卉,刘伯渠,卢新生
(甘肃民族师范学院 化学与生命科学系,甘肃 合作 747000)
0 引言
溶液pH值的计算是分析化学和无机化学重点难点之一[1-6],酸碱溶液中计算H+浓度是个复杂的问题,电荷平衡CBE是酸碱平衡处理的基本依据[2,6],是计算H+的关键。虽然不同条件下H+浓度的计算存在差异,但基本都可以按照这样的解题思路来求解,即利用CBE得到与H+浓度有关的表达式,用c、Ka、Kw等已知的浓度和常数等量替换式中除H+浓度以外的各项,将CBE处理为含H+浓度的一元二次方程,再根据具体条件和情况进行近似求解。为此,可把常见的十六种溶液pH值的计算归纳为一个一元二次方程进行求解。
1 原理推导(依据为质子平衡)


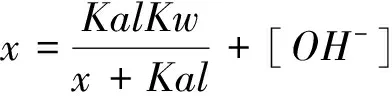
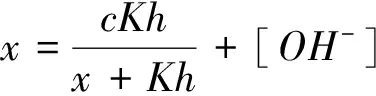
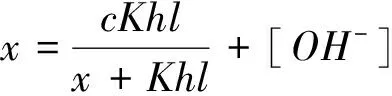


根据以上方法,还可得到二元强酸,一元弱酸和一元弱酸,一元弱碱和一元弱碱。
2 一元二次方程的归纳
对以上推理结果进行归纳分类,具体见下表1。

表1 一元二次方程中m和n取值一览表
3 公式的规律
认真分析表1,发现一元二次方程的m和n取值具有以下特点(见图1):
1)m的取值只看酸碱的强弱;n的取值要看酸碱强弱、几元弱酸碱、电离和溶液的组成;n中的K1和K2可以一样,C1和C2也可以一样。
2)强酸或强碱,不存在K,m里一定有C无K;弱酸或弱碱,一定存在K,m里一定有K无C;有弱有强,m里一定有K和C;弱弱混合,m为0。
3)一元强酸或强碱,不存在K,n里只有一项;一元弱酸或多元弱酸、一元弱碱或多元弱碱、一元弱酸强碱盐和一元弱碱强酸盐,只有K1,n里只有两项CK1+Kw;二元强酸,电离是1∶2的关系,n里有两项一样的2CKa和Kw;混合酸碱,有C1和C2,n里有三项C1K1+C2K2+Kw。
4)缓冲溶液的同离子效应不是H+和OH-,m和n里的C2是负值,其它反之。
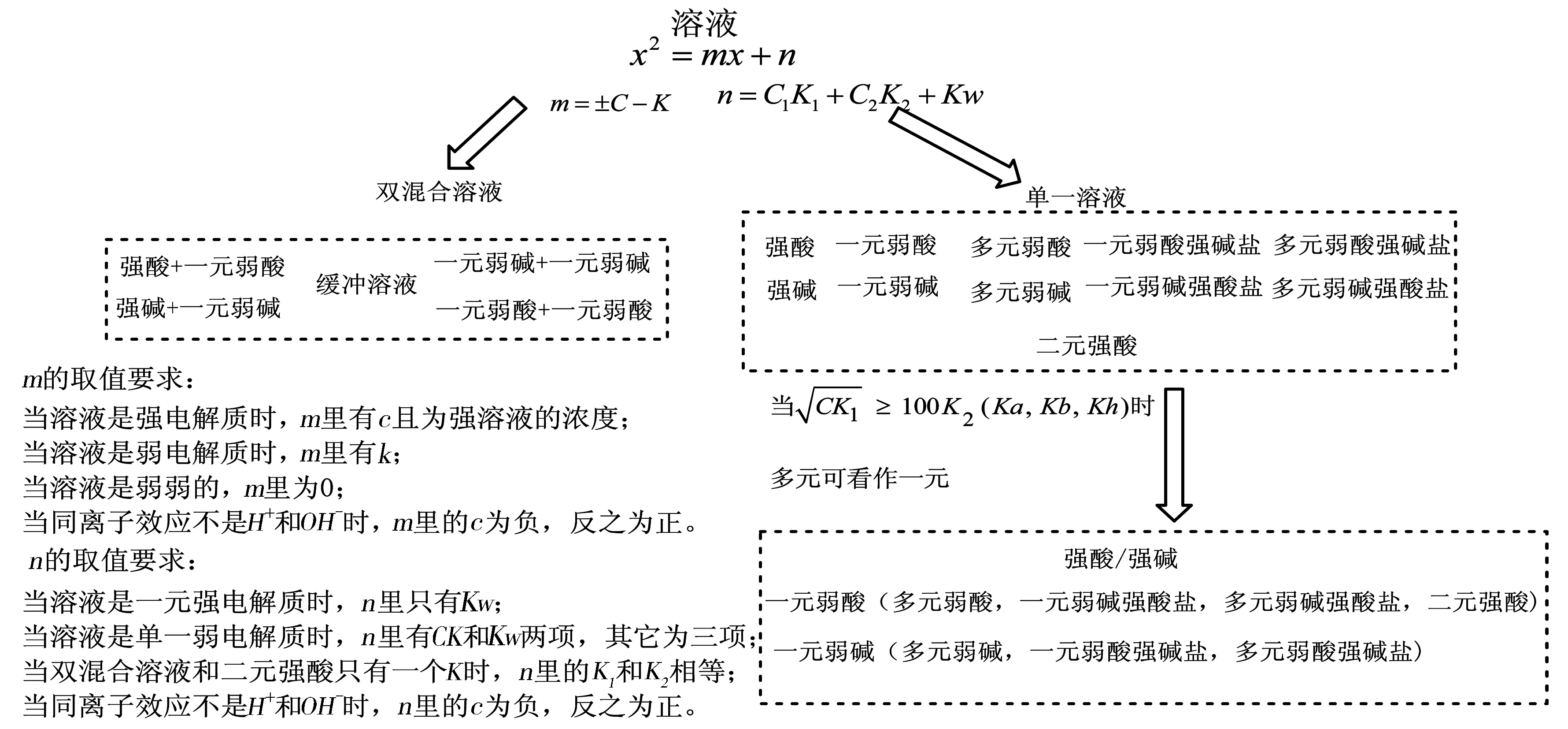
图1 一元二次方程的m和n的取值情况
4 公式的简化
简化的原则是抓住溶液中的主要平衡,舍去次要平衡,在近似处理中主要考虑三个方面因素的影响,即根据具体条件是否忽略水的离解对[H+]的影响,酸碱自身离解对平衡浓度c的影响以及在多元酸碱中是否忽略第二、第三级离解的影响而将它视为一元酸碱进行处理。具体计算过程中,如两项进行相加减,若其中一项与另一项相差1000倍,则可将较小的一项忽略,即A+B或A-B,若A与B相差3个数量级,则A+B或A-B≈A或B,这是进行近似计算的一般标准,计算结果的相对误差不大于5%[2,6],这与平衡常数测定的相对误差相当是比较符合实际情况的。
5 方法的应用
1)计算0.100mol·L-1H2SO4溶液的H+的浓度。已知Ka=0.012。
解:因为 1)H2SO4溶液是二元强酸,m里一定有C和K;
2)电离是1∶2的关系,n里有两项一样的2CKa和Kw,
2)计算0.10mol·L-1HF溶液的pH值。已知Ka=6.6×10-4。
解: 因为 1)HF溶液是一元弱酸,m里一定有K无C;
2)n里有CKa和Kw,
3)计算0.0001mol·L-1NH4Cl溶液的pH值。已知Ka=5.6×10-10。
解:因为1)NH4Cl溶液是一元强酸弱碱盐看作一元弱酸,m里一定有K无C;
2)n里有CKa和Kw,
6 方法评价
方法简单方便,把化学问题变成数学的一元二次方程的求解,讨论简单,易于记忆。
[参考文献]
[1] 无机化学教研室.无机化学[M].北京:高等教育出版社,1992:82-107.
[2] 华中师范大学.分析化学[M].北京:高等教育出版社,1986:190-218.
[3] 张淑民.基础无机化学[M].兰州:兰州大学出版社,1989:163-173.
[4] 高职高专化学教材编写组.无机化学[M].北京:高等教育出版社,2000:43-58.
[5] 吴英锦,王丽君,赵连俊.基础化学[M].北京:高等教育出版社,2006:66-71.
[6] 武汉大学.分析化学[M].北京:高等教育出版社,1995:44-77.
