5-氟尿嘧啶类脂囊泡药动学和组织分布研究
2012-09-25谌红丹
袁 悦,王 觅,2,谌红丹,车 鑫,赵 琨,王 晶
(1.沈阳药科大学药学院,辽宁沈阳110016;2.河北省中医院药剂科,河北石家庄500011)
5-氟尿嘧啶类脂囊泡药动学和组织分布研究
袁 悦1,王 觅1,2,谌红丹1,车 鑫1,赵 琨1,王 晶1
(1.沈阳药科大学药学院,辽宁沈阳110016;2.河北省中医院药剂科,河北石家庄500011)
用非离子表面活性剂制备5-氟尿嘧啶(5-Fu)囊泡,并对其进行了小鼠体内药动学和组织分布的研究.采用薄膜分散法制备5-Fu的类脂囊泡,以5-Fu水溶液为对照,尾静脉注射自制5-Fu囊泡和5-Fu水溶液,利用高效液相色谱法检测血浆和各组织中的5-Fu浓度,利用统计学方法计算了5-Fu在小鼠体内的药动学参数及小鼠的组织分布参数.与注射水溶液组相比,5-Fu囊泡组MRT值延长,AUC0~t值增加.组织分布结果显示:5-Fu囊泡在肝、肾中AUC值显著增加;5-Fu囊泡明显延长了5-Fu在体内的作用时间,比普通水溶液具有一定的缓释和提高生物利用度的作用.
5-氟尿嘧啶;类脂囊泡;药物动力学;组织分布
非离子表面活性剂囊泡(non-ionic surfactant vesicles,niosomes)是由合成的非离子表面活性剂与胆固醇形成的一种单室或多室具有封闭双层结构的有序组织聚集体,简称类脂囊泡[1].
近年来,随着新型药物传递系统的研究与应用,发现利用非离子表面活性剂囊泡包裹药物可以减少药物在达到有效部位前被破坏[2]、延长药物的半衰期[3],从而延长药物的作用时间以及降低药物毒副作用,改变药物在体内的分布,达到被动靶向作用等[4].与脂质体相比,非离子表面活性剂囊泡的载体材料不含磷脂,避免了磷脂的氧化降解,使工艺简化、成本降低,是一种极有希望的新型药物载体.近年来,囊泡包封技术已经成为化学、药学和生命科学研究领域中的热点课题之一.
5-Fu是临床常用的一种注射用抗代谢类抗肿瘤药物,抗瘤谱较广,但静脉给药后血中半衰期短,消除极快,需静脉持续给药,并且由于5-Fu静脉给药后对机体正常组织和病理部位无选择性,有严重的骨髓抑制和胃肠道反应的毒副作用等问题,因此临床应用受到限制[5].我们选用适宜的非离子表面活性剂将其制成非离子表面活性剂囊泡[6],进行静脉注射,希望能够延长其体内循环时间,增加药物的疗效.
本文制备了5-Fu囊泡,并研究其在小鼠体内的药动学及组织分布,考察其制成囊泡制剂后对小鼠体内行为的影响.
1 实验部分
1.1 仪器和材料
仪器:LC-10AT高效液相色谱仪(日本岛津株式会社),SPD-10A检测器(日本岛津株式会社),Easy3000色谱工作站(杭州普惠科技有限公司);MD200-2电子分析天平(奥豪斯国际贸易有限公司);TDL80-213型高速离心机(上海安亭科学仪器厂);XW-80A旋涡混合器(上海精科实业有限公司);79HW-1恒温磁力搅拌器(江苏金坛荣华仪器制造有限公司).
材料:5-Fu(上海邦成有限公司);Span20表面活性剂(国药集团化学试剂有限公司);胆固醇(天津市博迪化工有限公司);阿昔洛韦(郑州旭诚贸易有限公司);乙酸乙酯(山东禹王实业有限公司);甲醇(山东禹王实业有限公司).
1.2 实验方法
1.2.1 色谱条件
色谱条件:色谱柱为Agilent ODS C18柱(250mm×4.6mm,5μm);流动相为V(甲醇)∶V(水)=10∶90;流速为0.6mL/min;波长为267nm;柱温为25℃.
1.2.2 溶液的配置
标准储备液:精密称取160.0mg 5-Fu对照品,置于100mL容量瓶中,加适量水,超声溶解,用蒸馏水稀释至刻度,摇匀,得到质量浓度为1600μg/mL的储备液.分别精密吸取上述储备液0.1,0.5,1.5,2.5,4,5,10和30mL置于50mL容量瓶中,用蒸馏水稀释定容,配成质量浓度为3.2,16.0,48.0,80.0,128,160,320和960μg/mL的系列标准溶液,备用.
内标溶液:精密称取40mg阿昔洛韦对照品,置于50mL容量瓶中,加适量蒸馏水,超声溶解,加水至刻度,摇匀,得质量浓度为800μg/mL的阿昔洛韦溶液,即为内标溶液.
1.2.3 生物药品处理方法
精确量取生物样品(血浆或组织匀浆液)100μL,加入10μL内标液(阿昔洛韦的质量浓度为800μg/mL),涡旋混合1min,再加入1.5mL乙酸乙酯,涡旋5min,10000r/min离心8min.移取上清,氮气吹干,加入100μL流动相复溶,进样.
1.2.4 标准曲线的制定
精密吸取生物样品(血浆或组织匀浆液)100μL置于具塞离心试管中,分别加入5-Fu系列标准溶液10μL,配制成相当于质量浓度为0.32,4.8,8.0,12.8,16.0,32.0和96.0μg/mL的血液样品和质量浓度依次为0.32,1.6,4.8,8.0,12.8,16.0,32.0μg/mL的组织样品,加入内标溶液(质量浓度为800μg/mL阿昔洛韦溶液)10μL,按“1.2.1色谱条件”对生物样品进行处理,进样20μL,记录色谱图及峰面积,以A对C做线性回归.
1.2.5 回收率与精密度
取空白生物样品匀浆100μL,按“1.2.3标准曲线的制定”操作,配制低、中、高3个浓度(5-Fu血浆质量浓度分别为1.6,8.0和16μg/mL)的样品,每一浓度进行5个样本分析,连续测定3d,根据标准曲线,计算各样品的测得浓度,计算日内与日间精密度.
取100μL空白生物样品匀浆,按“1.2.3标准曲线的制定”操作,配制低、中、高3个浓度(5-Fu血浆质量浓度分别为1.6,8.0和16μg/mL)的样品,每一浓度5个样本进样分析,记录5-Fu的峰面积,并与配制相应浓度的5-Fu对照品溶液进样所得到的峰面积相比,计算提取回收率.
1.2.6 给药方案及样品采集
小鼠称重,5-Fu按25mg/kg剂量尾静脉注射对照溶液和制剂,每种剂型平行3组.分别在0,2,5,10,15,20,30,60,90,120,240min摘眼球取血,收集血液于肝素抗凝管中,10000r/min离心5min,取血浆备用.
其中取2,5,10,30,60,240min时间点小鼠心、肝、脾、肺、肾组织.置于生理盐水中,洗净,滤纸吸干,称重.按2mL/g组织加入生理盐水,制成组织匀浆.
2 结果与讨论
2.1 方法专属性
5-Fu的保留时间为7.121min,内标的保留时间为12.623min,分离度较佳且峰形良好.
2.2 标准曲线方程
相应的标准曲线方程如表1所示.结果表明在相应的浓度范围内,线性关系良好.

表1 各组织标准曲线方程
2.3 回收率及精密度
精密度和回收率结果如表2所示,结果表明,高、中、低3个浓度的日内与日间精密度及提取回收率结果均良好.

表2 各组织精密度及回收率结果
2.4 血药浓度和药动学参数测定
对小鼠尾静脉注射5-Fu水溶液和5-Fu类脂囊泡后,对血药浓度-时间数据进行处理,药时曲线如图1所示,药动学参数如表3所示.

图1 5-Fu 2种制剂药时曲线图

表3 体内药动学参数
药动学参数结果显示,5-Fu类脂囊泡和普通水溶液相比,AUC有明显的提高(P<0.05),半衰期也有一定的延长,说明类脂囊泡制剂相比于普通水溶液具有一定的缓释和提高生物利用度的作用.
各组织注射不同制剂后AUC结果见图2.由图2可知,5-Fu类脂囊泡在各组织中AUC相对于普通水溶液,药物在血浆、心、肝、脾、肾中的分布有一定的提高,尤其是在血浆、肝和肾中的提高是非常显著的,而在肺中的药物浓度却相对下降了.这可能是由于药物主要是通过肝肾代谢和排泄的,由于类脂囊泡的缓释作用,使得药物在体内滞留时间延长,从而使得药物在血浆、肝、肾中的浓度持续在一定的水平,表现为AUC显著增加.
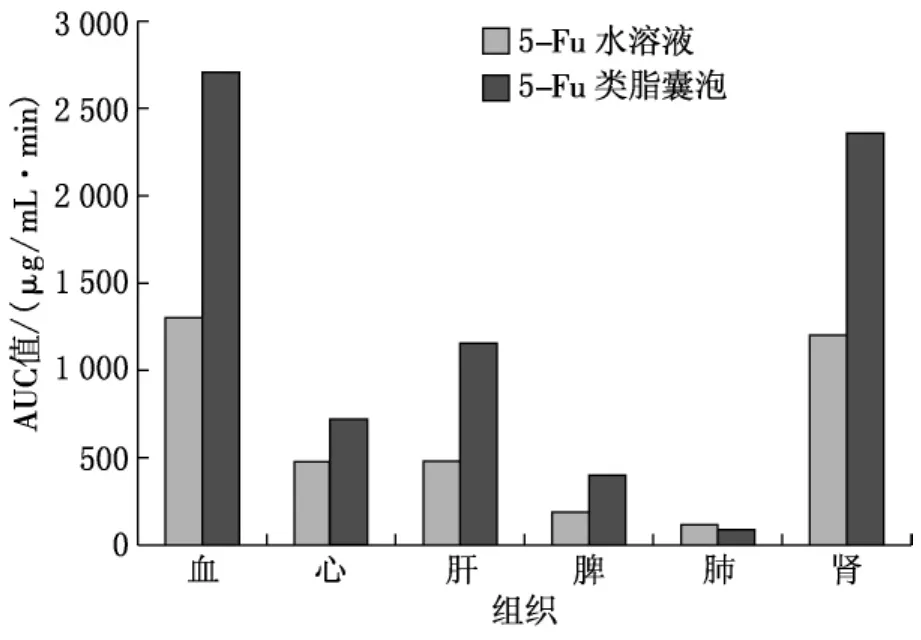
图2 不同制剂在不同组织中药物AUC结果
3 结论
本文以5-Fu水溶液为对照,考察了制备的5-Fu类脂囊泡通过尾静脉注射后在小鼠体内的药物动力学及组织分布结果.结果表明,制备的类脂囊泡具有一定的缓释和提高生物利用度的作用,从而可以实现降低制剂给药次数和药物毒副作用.
[1] HONG M,ZHU S,JIANG Y,et al.Efficient tumor targeting of hydroxycamptothecin loaded PEGylated niosomes modified transferrin[J].Journal of Control Release,2009,133:96-102.
[2] SANYOG JAIN,RAKESH KUMAR SHARMA,VYAS S P.Chitosan nanoparticles encapsulated vesicular systems for oral immunization:preparation,in vitro and in vivo characterization[J].Journal of Pharmacy &Pha2macology,2006,58(3):303-310.
[3] KHAKSA G,D SOUZA R,LEWIS S,UDUPA N.Pharmacokinetic study of niosome encapsulated insulin[J].Indian Journal of Experimental Biology,2000,38(9):901-905.
[4] DUFES CHRISTINE,GAILLARD FREDERIC,UCHEGBU IJEOMAF,et al.Glucose-targeted niosome deliver vasoactive intestinal peptide(VIP)to the brain[J].International Journal of Pharmaceutics,2004,285(1/2):77-85.
[5] FOURNIER E,PASSIRANI C,COLIN N,et al.Development of novel 5-Fu-loaded poly(methylidene malonate 2.1.2)-based microspheres for the treatment of brain cancers[J].Eur J Pharm Biopharm,2004,57(2):189-97.
[6] 袁悦,王红霞,刘岩,等.类脂囊泡作为5-氟尿嘧啶药物载体研究[J].分子科学学报,2010,26(6):420-423.
Abstract:To study the preparation of 5-flurouracil(5-Fu)noisomes and the pharmacokinetics and tissue distribution in mice.5-Fu noisomes were prepared using film dispersion method.5-Fu noisomes and 5-Fu solution were carried out in mice by caudal vein injection.5-Fu concentrations of plasma and various tissues were detected by HPLC methods.Statistical methods were used to calculate the parameters of pharmacokinetics and tissue distribution in mice.Compared to the group of 5-Fu solution,MRT and AUC0~tof 5-Fu niosomes both were increased.Compared with 5-Fu solution,5-Fu niosomes had a sustained release and a improved bioavailability.
Keywords:5-Fu;niosomes;pharmacokinetic;tissue distribution
(责任编辑:石绍庆)
Study on pharmacokinetic and tissue distribution in mice of 5-flurouracil niosomes
YUAN Yue1,WANG Mi1,2,CHEN Hong-dan1,CHE Xin1,ZHAO Kun1,WANG Jing1
(1.School of Pharmacy,Shenyang Pharmaceutical University,Shenyang 110016,China;2.Department of Pharmacy,Hebei Province Traditional Chinese Medicine Hospital,Shijiazhuang 500011,China)
O648[学科代码]150·30
A
2011-10-15
辽宁省博士启动基金资助项目(20081035);沈阳市科技局资助项目(1081231-1-00);辽宁省企业博士后项目(bsh2010042).
袁悦(1972—),女,博士,副教授,主要从事物理药学和药物新剂型研究;通讯作者:王晶(1963—),女,副教授,主要从事物理药学研究.
1000-1832(2012)02-0099-04
