卵巢卵泡膜细胞瘤的超声诊断
2012-09-18梁莹莹
梁莹莹 李 晶
卵巢卵泡膜细胞瘤是卵巢实性肿瘤中较常见的一种,属性索间质来源的良性肿瘤,占卵巢性索间质肿瘤的48%,约占全部卵巢肿瘤的0.5%~1.0%[1]。超声为诊断卵巢肿瘤的常规手段,但卵泡膜细胞瘤超声图像无特异表现,术前超声确诊困难。本研究通过回顾性分析30例卵泡膜细胞瘤患者的超声声像图、临床症状和病理改变,探讨卵泡膜细胞瘤的超声特征,以提高术前诊断准确率。
1 资料与方法
1.1 研究对象 1999-01~2011-09在广州市番禺区中心医院住院并经手术病理确诊的30例卵巢卵泡膜细胞瘤患者,年龄17~78岁,平均(48.36±13.65)岁;14例为绝经后妇女,15例为育龄妇女,1例为青春期女性;临床症状:绝经后阴道出血4例,月经失调2例,下腹痛6例(5例为蒂扭转引起,1例为肿物明显坏死引起),偶然发现或以盆腔包块就诊18例;10例合并子宫肌瘤,1例合并子宫腺肌瘤,2例合并子宫内膜样腺癌,4例合并子宫内膜息肉,2例合并畸胎瘤(2例均发生于对侧卵巢),1例合并浆液性囊腺瘤(发生于同侧卵巢),2例为乳腺癌术后。
30例患者中,14例盆腔积液深度<2cm,13例盆腹腔积液深度2~4cm(少量腹水),2例盆腹腔积液深度4~8cm(中量腹水),1例盆腹腔积液深度>8cm(大量腹水)。并发腹水的患者中,肿块最大径均>10cm。15例患者行癌抗原-125(CA125)、CA199、甲胎蛋白(AFP)及癌胚抗原(CEA)检查,5例CA125增高(222.0~999.1U/ml),肿块最大径均>10cm。
1.2 仪器与方法 使用GE Voluson 730、E8及Logic 8彩色多普勒超声诊断仪,经腹探头频率3~7MHz,经阴道探头频率5~7MHz.。经腹或经阴道超声检查子宫附件,测量肿块大小,观察肿块发生的部位、形态、边界、内部及后方回声特点,了解肿块血流情况,并测量血流阻力指数(RI)。
2 结果
2.1 病理结果 30例患者术后病理证实有31个肿块,单侧29例(左侧10例,右侧19例),双侧1例。病理诊断:卵泡膜细胞瘤29例(包括1例双侧卵巢卵泡膜细胞瘤),其中1例伴有广泛钙化、骨化,2例为伴有少量性索成分的卵泡细胞瘤;黄素化的卵泡膜细胞瘤1例。肿块大小不一,最大30cm×25cm×10cm,最小1.5cm×1.0cm×1.0cm。8例肿块形态呈不规则分叶状,2例呈肾形,20例呈类圆形或圆形。
2.2 超声表现 超声误诊4例,均误诊为子宫肌瘤。3例漏诊,肿块直径均<2cm,其中2例为子宫内膜癌,在手术切除卵巢后发现;1例为双侧病灶,超声仅发现一侧卵巢中较大的肿瘤,未发现另一侧卵巢中的小肿瘤。
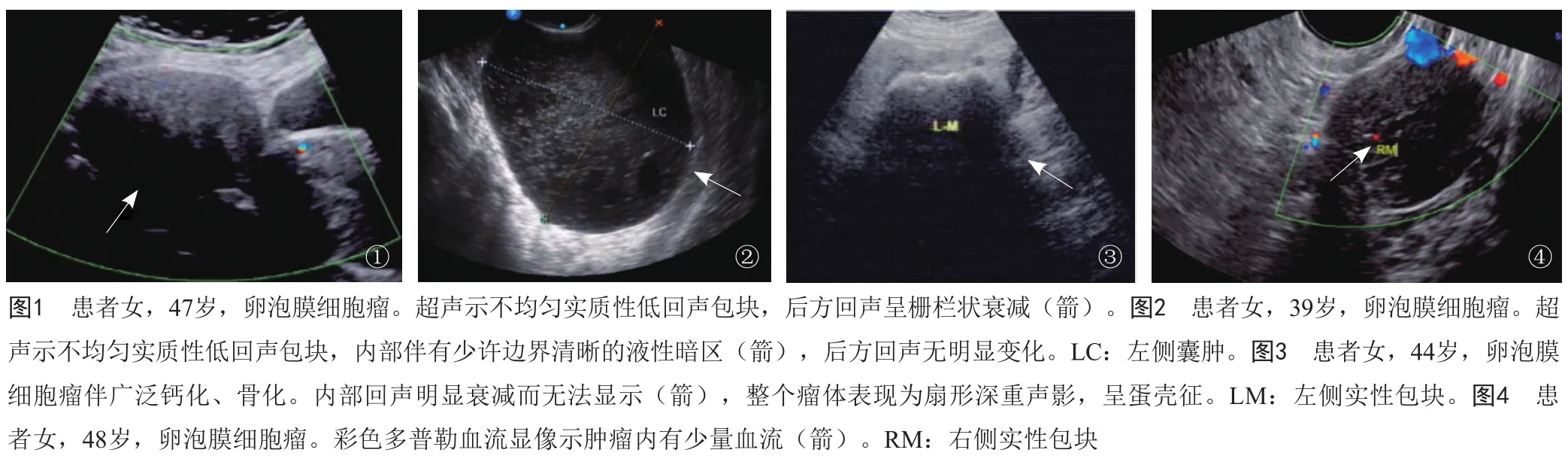
超声表现:①均匀或不均匀实质性低回声包块10例,内部伴或不伴有少许边界清晰的液性暗区,后方回声呈栅栏状衰减(图1)。②均匀或不均匀实质性低回声包块15例,内部伴或不伴有少许边界清晰的液性暗区,后方回声无明显变化(图2)。③内部回声明显衰减而无法显示,整个瘤体表现为扇形深重声影,呈蛋壳征1例(图3)。④以囊性为主的囊实性肿块2例,内呈实性条片状中低回声区及大片状液性暗区,可见粗细不一的光带,其中1例同侧卵巢合并浆液性囊腺瘤。15例血流评估[2]结果显示,5例无血流显示,8例少量血流显示(图4),1例中量血流显示(病理证实为黄素化的卵泡膜细胞瘤),1例丰富血流显示(病理证实为伴有少量性索成分的卵泡细胞瘤),RI 0.31~0.55。
3 讨论
3.1 病理特征 卵泡膜细胞瘤起源于卵巢间质的特殊间胚叶组织,向卵泡膜细胞分化,形成肿瘤,单侧多见,双侧少见。卵巢卵泡膜细胞瘤为实性肿物,常因囊性变、黏液性变等导致内部出现小囊性区,偶有囊性变显著者呈囊实性改变。镜下分为2种形态:①镜下见富含脂质的卵泡膜细胞及数量多少不等的成纤维细胞,并可伴有小灶性钙化,偶伴有广泛钙化、骨化。少数卵泡膜细胞瘤可有少量的性索成分,性索成分<10%,称为伴有少量性索成分的卵泡细胞瘤。②黄素化的卵泡膜细胞瘤,镜下见在纤维组织丰富的背景下散在成簇的、大的、嗜酸性富于脂质的卵泡膜细胞。
3.2 临床表现 卵泡膜细胞瘤多见于绝经前后妇女。临床多为偶然发现或以盆腔包块为临床表现。卵泡膜细胞瘤能分泌雌激素,引起相应临床症状[3],如生育期月经失调、绝经后阴道出血等;含性索间质成分时症状更加明显;也可分泌雄激素(常见于黄素化的卵泡膜细胞瘤)而产生男性化症状。部分患者因卵巢肿瘤蒂扭转突发下腹痛就诊。本组30例中,5例伴发卵巢肿瘤蒂扭转。卵泡膜细胞瘤肿瘤标志物检查无明显异常。当瘤体较大时,可出现腹水及CA125升高。卵泡膜细胞瘤本身并不产生腹水及CA125,而是增大的肿瘤刺激腹膜,继而产生腹水及CA125[4]。
3.3 超声表现 卵泡膜细胞瘤的病理特点决定了其超声特点以实性占位为主,内部呈低回声,实性区内可见小液性暗区[5]。含纤维组织多的肿物后方回声衰减明显,含卵泡膜细胞多、纤维组织少的肿物后方回声无明显变化。部分富含脂质的卵泡膜细胞瘤表现为内部均匀点状回声,甚至无回声。少数卵泡膜细胞瘤超声表现为以囊性为主的囊实性肿块,本组发现2例,其中1例卵泡膜细胞瘤囊性变,1例为实性卵泡膜细胞瘤合并浆液性囊腺瘤。本组发现1例广泛钙化、骨化的卵泡膜细胞瘤,其超声表现为内部回声明显衰减,无法显示。卵泡膜细胞瘤血供不丰富,彩色多普勒血流显像(CDFI)可在一部分肿瘤内部显示散在分布的较微弱的血流信号,记录到低阻血流频谱。本组15例患者行CDFI,仅1例检测到中量血流,病理结果为黄素化的卵泡膜细胞瘤;1例检测到丰富血流,病理结果为伴有少量性索成分的卵泡细胞瘤。
3.4 鉴别诊断 ①浆膜下子宫肌瘤:子宫肌瘤有假包膜,较大肌瘤内部呈漩涡状,CDFI可见肿块周边的环状或半环状血流,且肿块与子宫体有血流相连。而卵泡膜细胞瘤多呈均匀或不均匀低回声,CDFI未见明显血流或散在、不规则状血流;还可以通过解剖关系鉴别二者。②卵巢纤维瘤:由可产生胶原纤维的成纤维细胞构成,与卵泡膜细胞瘤同属卵泡膜瘤-纤维瘤组肿瘤[2]。由于胶原纤维含量不一,二者声像图具有差异,卵泡膜细胞瘤后方回声衰减程度较轻,纤维瘤则衰减更明显,实际操作时超声区别有一定困难。③卵巢良性Brenner瘤:典型的Brenner瘤体积较小,直径<2cm,由尿路上皮样细胞巢和纤维性间质组成,一般后者占优势,故超声声像图肿物常呈深重声影,导致瘤体侧壁、后壁边界显示不清。卵泡膜细胞瘤体积较大,多呈实性低回声。此外,部分富含脂质的卵泡膜细胞瘤表现为内部均匀点状回声,甚至呈无回声,超声应注意与卵巢囊肿鉴别[6]。
综上所述,卵巢卵泡膜细胞瘤术前超声定性诊断困难,与该病超声图像无特异性,操作者对该病认识较少有关[7]。超声图像以实性低回声为主,可伴或不伴小液性暗区,少部分呈以囊性为主的囊实性改变,血供不丰富。结合发病年龄、临床症状可提示诊断,避免漏诊绝经后卵巢小体积卵泡膜细胞瘤。
[1]陈忠年, 杜心谷, 刘伯宁. 妇产科病理学. 上海: 上海医科大学出版社, 1996: 221-223.
[2]Tavassoli FA, Devilee P. Pathology and genetics of tumours of the breast and female genital organs. Lyon: IARC Press,2003: 184-186.
[3]张惜阴.临床妇科肿瘤学.上海:上海医科大学出版社,1993: 214-216.
[4]Paladini D, Testa A, Van Holsbeke C, etal. Imaging in gynecological disease (5): clinical and ultrasound characteristics in fibroma and fibrothecoma of the ovary.Ultrasound Obstet Gynecol, 2009, 34(2): 188-195.
[5]来蕾, 许亮, 包凌云, 等. 卵巢卵泡膜细胞瘤的超声诊断分析. 医学影像学杂志, 2010, 20(1): 143-144.
[6]汪龙霞,王军燕,张晶. 卵巢卵泡膜瘤的超声表现分析.中国医学影像学杂志, 2003, 11(3): 181-182.
[7]张震,李雪丹,王学梅.卵巢卵泡膜细胞瘤超声表现的诊断价值探讨.中国医科大学学报, 2008, 37(6): 831-833.
