西洋参干预胰岛素抵抗大鼠活性部位的化学成分研究Ⅴ
2012-09-17李冀马育轩葛鹏玲杨炳友尚广巍
李冀,马育轩,葛鹏玲,杨炳友,尚广巍
(黑龙江中医药大学,黑龙江 哈尔滨 150040)
西洋参(Panax quinquefolium L.)为五加科多年生草本植物,又名花旗参,与人参(P.ginseng C.A May.)同科同属,根部入药,原产于美国和加拿大,近年在我国引种成功。其味甘,微苦而凉,入肺肾经,具补气养阴,生津止渴之功[1-2]。
本课题组早期实验证明,西洋参60%乙醇洗脱部位为干预胰岛素抵大鼠模型的活性部位[3-4]。本实验继续采用硅胶柱色谱及HPLC等分离技术与方法对该部位进行分离,得3个单体化合物,并对其化学结构作出鉴定,为进一步筛选其有效成分及探讨其作用机制奠定基础。
1 仪器与材料
超导核磁共振光谱仪采用Bruker-400型;TMS为内标,化学位移值以δ表示,重叠的信号用0表示,多重峰信号用m表示,偶合常数的单位均为Hz;半制备型色谱柱(Hypersil ODSⅡ(10μm,10mm ×250mm,大连依利特公司);制备型HPLC(Waters公司,Delta-600-2487型);ESI-MS(Finnigan MAT LCQ);分析型色谱柱(Hypersil ODSⅡ(5μm,4.6mm ×200mm,大连依利特公司);制备型色谱柱(Hypersil-ODSⅡ(10μm,20mm×300mm,大连依利特公司);满层色谱用硅胶板(Silica gel60F254)和反相板(Rp-18)(公国Merck公司);硅胶(青岛海洋化工厂、140~200目,200~300目);AB-8大孔吸附树脂(南开大学化工厂产品;化学试剂为分析纯(天津试剂一厂);柱色谱用反相ODS(ODS-AM,日本YMC公司);显色剂:10%的硫酸/乙醇溶液。
2 提取与分离
将西洋参的根部用70%EtOH回流提取后,回收EtOH,得到EtOH提取物。再将此提取物进行AB-8型大孔树脂柱色谱,依次分别用H2O、30%EtOH、60%EtOH、90%EtOH 洗脱,得到 XY -1、XY -2、XY -3 和XY-4四个部位。本课题组早期实验证明[2],XY-3部分为有效部位。继续采用硅胶柱色谱及HPLC等分离技术与方法对该部位进行分离,得到3个单体化合物,并对其化学结构进行鉴定。
3 鉴定
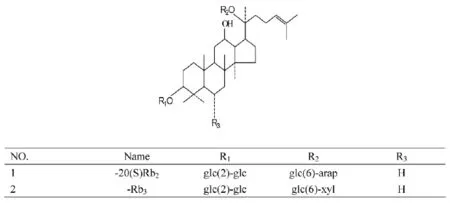
Fig.1 Structures of compounds 1,2
3.1 化合物1化学结构的鉴定
化合物1为白色无定形粉末(MeOH),Liebermann-Burchard和Molish反应均成阳性,化合物1的薄层水解后,经检识证明含阿拉伯糖和葡萄糖,因吡喃糖苷较呋喃糖苷难水解,提示C-20位连的两种糖中阿拉伯糖为吡喃型。化合物1的正性 ESI-MS在 m/z 1 101处可见[M+Na]+离子峰,表明化合物1的分子量为1 078。综合1H-NMR,13C-NMR谱等数据可推断出化合物1的分子式为C53H90O22,计算不饱和度为9,推断化合物1可能是三萜皂苷类。
化合物 1的1H -NMR(400MHZ,pyridine)谱,在高场区 δ0.78(3H,s)、δ0.93(3H,s)、δ0.95(3H,s)、δ1.09(3H,s)、δ1.26(3H,s)、δ1.58(3H,s)、δ1.62(3H,s)、δ1.64(3H,s)处可见8 个归属于皂苷元上的角甲基单峰信号。在低场区δ5.53处可以观察到烯氢质子的信号。在 δ4.92(1H,d,J=7.6Hz)、δ4.99(1H,d,J=7.2Hz)、δ5.13(1H,d,J=7.6Hz)、δ5.38(1H,d,J=7.6Hz)处分别出现4个归属于葡萄糖的端基质子信号。
结合化合物1的 DEPT、1H-1H COSY、HSQC和HMBC等波谱的综合解析,对化合物1的13C-NMR谱的全部碳信号(见Table1.1)进行了详细的解析和归属。将化合物1的13C-NMR谱数据与化学结构已知的化合物人参皂苷-20(S)Rb2相比较[5],两者基本一致。
综合各种分析结果,化合物1被鉴定为3-O-β-D-吡喃葡萄糖基-(1→2)-β-D-吡喃葡萄糖基-20-O-β-D吡喃阿拉伯糖基-(1→6)-β-D-吡喃葡萄糖基 -达玛 -24-烯 -3β,12β,20S-三醇[3-O-β-D-glucopyranosyl-(1→2)-β-D-glucopyranosyl-20-O-β-D-arab-inopyranosyl-(1→6)-β-D-glucopyranosyl-dammar-24-ene-3β,12β,20S -triol]。化学结构见 Fig.1 。
3.2 化合物2化学结构的鉴定
化合物2为白色无定形粉末(MeOH),Liebermann-Burchard和Molish反应均成阳性,化合物2的薄层水解后,经检识证明含D-葡萄糖和D-木糖。化合物2的正性 ESI-MS在 m/z 1 083.5处可见[M+Na]+离子峰,表明化合物2的分子量为1 060。综合1H-NMR,13C-NMR谱等数据可推断出化合物2的分子式为C53H88O21,计算不饱和度为10,推断化合物2可能是三萜皂苷类。
化合物 2的1H -NMR(400MHZ,pyridine)谱,在高场区 δ0.78(3H,s)、δ0.92(3H,s)、δ0.93(3H,s)、δ1.09(3H,s)、δ1.26(3H,s)、δ1.59(3H,s)、δ1.63(3H,s)、δ1.63(3H,s)处可见8 个归属于皂苷元上的角甲基单峰信号。在低场区δ5.52处可以观察到烯氢质子的信号。在 δ5.38(1H,d,J=7.6Hz)、δ5.13(1H,d,J=7.6Hz)、δ4.92(1H,d,J=7.6Hz)、δ4.70(1H,d,J=11.4Hz)处分别出现4个归属于葡萄糖的端基质子信号。
结合化合物2的 DEPT、1H-1H COSY、HSQC和HMBC等波谱的综合解析,对化合物2的13C-NMR谱的全部碳信号(见Table1.1)进行了详细的解析和归属。将化合物2的13C-NMR谱数据与化学结构已知的化合物人参皂苷-Rb3相比较[3],两者基本一致。
综合各种分析结果,化合物2被鉴定为3-O-β-D-吡喃葡萄糖基-(1→2)-β-D-吡喃葡萄糖基-20-O-β-吡喃木糖基-(1→6)-β-D-吡喃葡萄糖基 -达玛 -24-烯 -3β,12β,20S-三醇[3-O-β-D-glucopyranosyl-(1→2)-β-D-glucopyranosyl-20-O-β-D-glucopyra-nosyl-(1→6)-β-D -xylopyranosyl-dammara-24-ene-3β,12β,20S -triol]。化学结构见 Fig.1 。
3.3 化合物3化学结构的鉴定
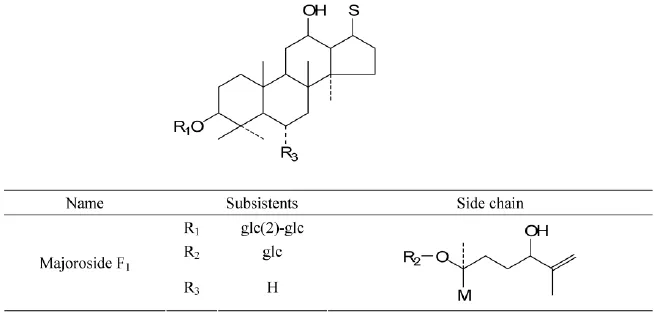
Fig.2 Structures of 3
化合物3为白色无定形粉末(MeOH),Liebermann-Burchard和Molish反应均成阳性,化合物3的薄层水解后,经检识证明含D-葡萄糖。化合物3的正性ESI-MS在m/z986处可见[M+Na]+离子峰,表明化合物3的分子量为963。综合1H-NMR,13C-NMR谱等数据可推断出化合物3的分子式为C48H83O19,计算不饱和度为8,推断化合物3可能是三萜皂苷类。
化合物 3的1H -NMR(400MHZ,pyridine)谱,在高场区 δ0.78(3H,s)、δ0.92(3H,s)、δ1.08(3H,s)、δ1.31(3H,s)、δ1.54(3H,s)、δ1.62(3H,s)、δ1.63(3H,s)处可见7个归属于皂苷元上的角甲基单峰信号。在低场区δ5.57处可以观察到烯氢质子的信号。在 δ4.93(1H,d,J=7.6Hz)、δ5.16(1H,d,J=7.6Hz)、δ5.39(1H,d,J=7.6Hz)处分别出现3个归属于葡萄糖的端基质子信号。
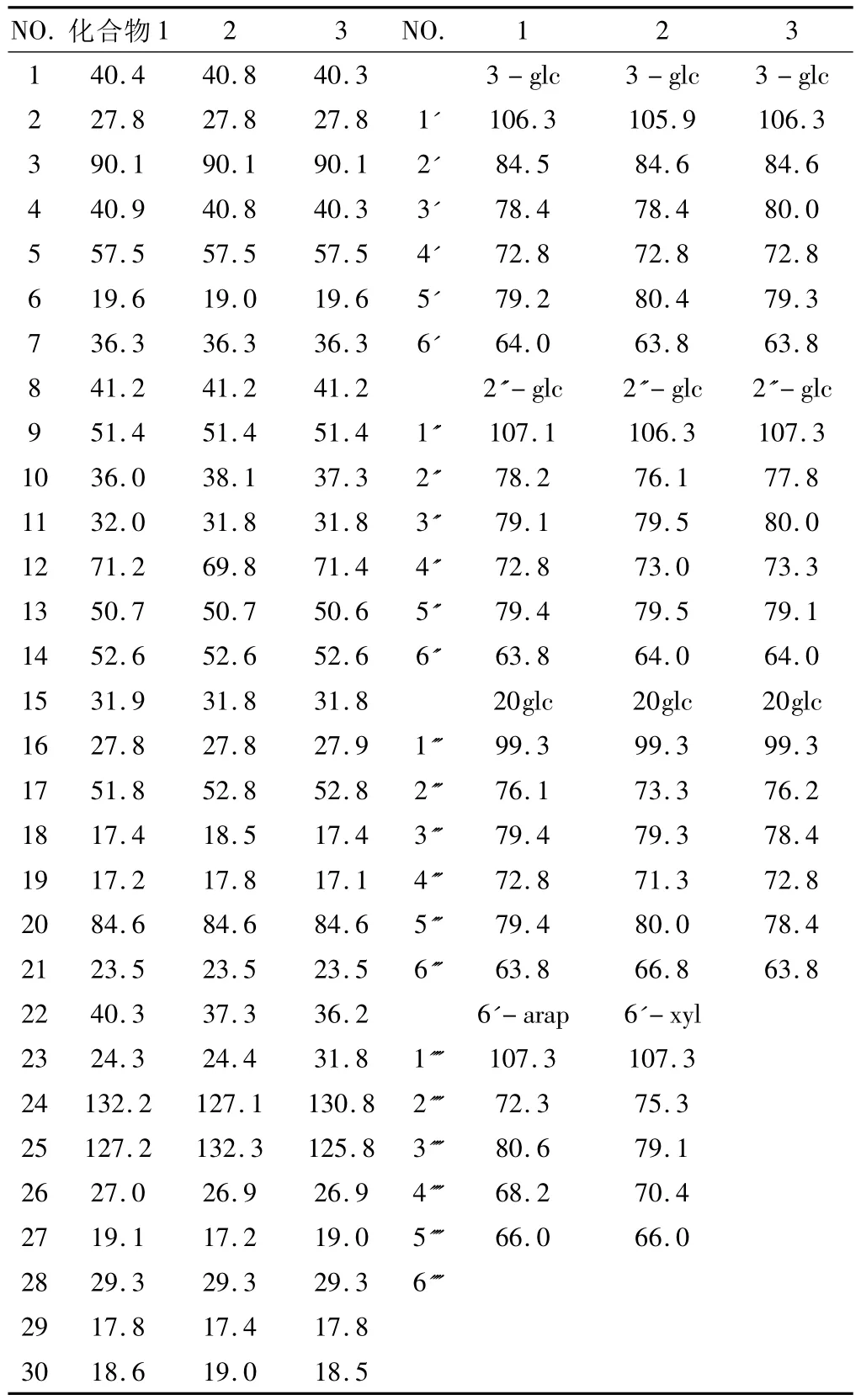
Tablel.1 13C - NMR data of 1,2,3(pyridine)
结合化合物3的 DEPT、1H-1H COSY、HSQC和HMBC等波谱的综合解析,对化合物3的13C-NMR谱的全部碳信号(见Table1.1)进行了详细的解析和归属。将化合物3的13C-NMR谱数据与化学结构已知的化合物Majoroside F1相比较[6],两者基本一致。
综合各种分析结果,化合物3被鉴定为达玛-25(26) - 烯 -3β,12β,20S,24ξ- 四醇(20-O - β -D -吡喃葡萄糖基)-3-O-β-D-吡喃葡萄糖基(1→2)-β-D-吡喃葡萄糖苷(dram-mar-25(26)-ene-3β,12β,20S,24ξ-ietraol-20-O - β -D -glucopyranosyl-(1→2)-β-gl-ucopyranoside)。化学结构见 Fig.2 。
[1] 李冀,马育轩,葛鹏玲,等.西洋参干预胰岛素抵抗大鼠活性部位的化学成分研究Ⅱ[J].中医药信息,2010,27(5):23 -26.
[2] 李冀,马育轩,葛鹏玲,等.西洋参干预胰岛素抵抗大鼠活性部位的化学成分研究[J].中医药学报,2009,37(6):68 -70.
[3] 李冀,盛波,葛鹏玲,等.西洋参不同洗脱部位对胰岛素抵抗大鼠脂代谢的影响[J].中医药信息,2008,25(3):13-14.
[4] 马育轩,葛鹏玲,杨炳友,等.西洋参干预胰岛素抵抗大鼠活性部位的化学成分研究Ⅳ[J].中医药学报,2011,39(1):74 -76.
[5] 王贵得,马兴元,绍春杰,等.国产西洋参叶化学陈分的研究—人参皂苷的分离鉴定[J].中成药,1994,41(2):33-34.
[6] Ping Zhao,Yu - Qing Liu,ChongRen Yang.Minor Dammarane Saponins from Panax notoginseng [J].Phytochemistry,1996,4(5):1419-1425.
