盐助溶燃烧法快速合成小粒径棒状氧化锌
2012-09-15李秀萍赵荣祥刘春生高霄汉冯锦烨
李秀萍, 赵荣祥, 刘春生, 高霄汉, 冯锦烨
(1.辽宁石油化工大学化学与材料科学学院,辽宁抚顺 113001;2.辽宁石油化工大学石油化工学院,辽宁抚顺 113001;3.中国石油抚顺石化分公司抚顺化工塑料厂,辽宁抚顺 113005)
盐助溶燃烧法快速合成小粒径棒状氧化锌
李秀萍1, 赵荣祥2, 刘春生1, 高霄汉1, 冯锦烨3
(1.辽宁石油化工大学化学与材料科学学院,辽宁抚顺 113001;2.辽宁石油化工大学石油化工学院,辽宁抚顺 113001;3.中国石油抚顺石化分公司抚顺化工塑料厂,辽宁抚顺 113005)
采用一种新型还原性的燃烧剂抗坏血酸与氧化性的六水合硝酸锌为原料,燃烧法合成乳白色棒状氧化锌,对燃烧剂的用量、是否煅烧和煅烧温度、是否加入助溶剂进行考察。结果表明,燃烧剂与六水合硝酸锌的物质的量之比为3∶1,六水合硝酸锌与助溶剂物质的量之比为1∶0.5,样品不经洗涤和煅烧,其纯度和结晶度较高。加入助溶剂样品更加蓬松,样品棒更短。样品经FTIR,XRD,UV-Vis,SEM表征,结果表明所制备的氧化锌在紫外和红外都有强吸收,粒径可达微米级,形貌为短的棒状。
燃烧法; 棒状; 氧化锌
近年来,各种形貌纳米氧化锌备受人们关注,原因在于其广泛的技术应用,例如在光电探测器、二极管、气体传感、光催化、太阳能电池等方面[1-5]。目前氧化锌的合成方法有两种途径:一是气相法[6-9],此方法温度高、产率低;二是液相法[10-11],尽管此方法产率有所提高,但是一般液相法合成时间都较长且经高温煅烧、洗涤等,浪费溶剂、污染环境。燃烧法制备氧化锌,产率高,样品质量轻,体积大。目前已有许多文献[12-15]采用燃烧法制备纳米氧化锌。
本文采用一种新型燃烧剂抗坏血酸作为还原剂和燃烧剂,硝酸锌作为氧化剂,通过控制燃烧剂的用量来制备一种纯度较高,结晶度较好,颜色可选择的纳米氧化锌,不经洗涤和煅烧就可得到纯的氧化锌。
1 实验部分
1.1 实验试剂与仪器
实验试剂:Zn(NO3)2·6H2O(沈阳市试剂二厂)、抗坏血酸(沈阳市试剂五厂)、氯化钠(沈阳新化试剂厂),以上试剂均为分析纯,水为二次去离子水。
实验仪器:氧化锌的晶相结构在日本理学的D/max-RB-12 k W转耙X射线衍射(XRD)仪进行测定,扫描范围为10°~80°,管电压30 k V,管电流15 m A,入射光波长为0.154 nm;用WQF-520傅立叶变换红外光谱(FT-IR)仪(北京瑞利分析仪器公司)对样品进行红外扫描,对样品的残留有机物和结合基团进行测定,KBr压片;用UV-VIS1100 Spectrophotometer(上海天美科学仪器有限公司)对制得氧化锌进行紫外波谱扫描表征;用LEO型扫描电子显微镜(SEM)对样品进行电镜扫描(德国LEO公司)。
1.2 氧化锌的制备及表征
按照一定的物质的量比称取适量的Zn(NO3)2·6H2O、抗坏血酸放进研钵中研磨均匀,然后将药品转移到大烧杯中加入少量的水使药品溶解。将烧杯放在加热套上开始加热,一段时间后烧杯中的水几乎蒸发完全。烧杯中所剩的溶液开始发泡,体积开始膨胀,当出现黑色固体物质时,继续加热反应,黑色固体物质开始发生缓慢的自蔓延燃烧反应,最终得粉状固体物质,将样品用蒸馏水洗涤3次,再用无水乙醇洗涤2次,放入干燥箱中干燥3~4 h,放入马福炉中煅烧3~4 h,冷却。取出样品研磨装袋,进行XRD,FT-IR,UV-VIS,SEM表征。
2 结果与讨论
2.1 燃烧剂用量考察
按表1物质的量比称取适量的Zn(NO3)2· 6H2O、抗坏血酸制备氧化锌进行燃烧剂用量考察,结果如图1所示。

Fig.1 Amount of burning agent effect on samples图1 燃烧剂用量对样品影响

表1 燃烧剂用量及样品颜色Table 1 Amount of burning agent and sample color

由图1可以看出,氧化锌的结晶度随着燃烧剂用量的增加变好,其燃烧反应方程式:当氧气的系数为0时,即φ=4/5,硝酸锌中的氧可完全与抗坏血酸反应而无需外界氧气的供给。通过对不同φ值理论燃烧火焰温度的热力学分析来确定实验中燃料与氧化剂的配比,进而研究不同配比下燃烧产物的性能变化。燃料不足时,由于硝酸锌没有得到充分燃烧所以生成的氧化锌为淡黄色,随着燃料的增加燃烧更充分样品逐渐变成白色。当燃料过剩时,表现出的自蔓延高温合成反应(SHS)特征为开始时是局部反应燃烧,然后以波动的形式自动燃烧并传播,直到全部反应完毕。这是因为当燃料过剩时,燃烧反应需要另外提供氧,从动力学来讲,氧是以扩散的方式进入反应区,这限制了反应速率,从而形成了SHS反应模型,使反应生成的氧化锌结晶度变好。因此,选择Zn(NO3)2·6H2O和抗坏血酸的物质的量比为1∶3。
2.2 助溶剂用量考察
由德拜-休克尔公式可知,强电解质可以增加物质的溶解性,由于燃烧法制备氧化锌时Zn(NO3)2·6 H2O和抗坏血酸中加入少量水会影响样品的溶解性,另外惰性助溶剂的加入,燃烧后迅速冷却结晶在样品的表面,阻止样品的长大,因此为提高反应物的溶解性可制备颗粒更小的氧化锌。所以实验对加入强电解质助溶剂进行考察。按表2物质的量比称取药品制备氧化锌进行助溶剂用量考察,结果如图2所示。

表2 助溶剂用量及样品颜色Table 2 Amount of cosolvent and sample color
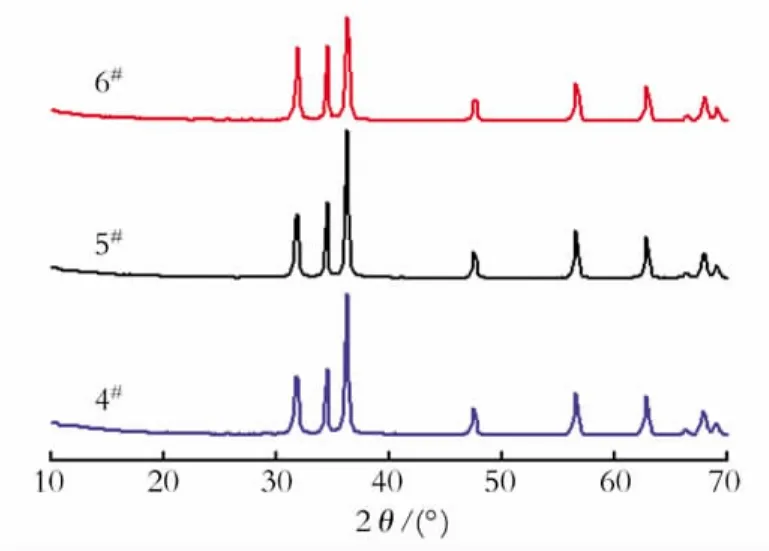
Fig.2 Amount of cosolvent efffect on samples图2 助溶剂用量对样品影响
从图2中可以看出,Zn(NO3)2·6H2O和助溶剂的物质的量比为1∶0.5时比未加入助溶剂的样品的结晶度有所改善,但是当Zn(NO3)2·6H2O与助溶剂的物质的量比为1∶1时结晶度变差,氧化锌的颜色稍变深由乳白色变为淡黄色。颜色变深会增强样品对光的吸收,影响样品的紫外屏蔽性能,助溶剂只能加入少量,Zn(NO3)2·6H2O与助溶剂物质的量比在1∶0.5以下。
2.3 煅烧温度考察
由于燃烧后的样品可能含有未燃烧净的硝酸锌或抗坏血酸以及其他杂质,所以对燃烧后制得的样品进行煅烧考察实验,实验结果如图3所示。

Fig.3 Calcination temperature effected on samples图3 煅烧温度对样品的影响
从图3中可以看出,煅烧温度对样品的晶化度影响不大,而且不经煅烧和洗涤的样品的晶化度和纯度与600,700℃的样品一样,所以实验以后制得的样品可以不经煅烧和洗涤,但本实验在此之后的样品也都经过洗涤和600℃煅烧。
2.4 氧化锌的SEM表征
在Zn(NO3)2·6H2O和抗坏血酸物质的量比为1∶3,煅烧温度为600℃下制备的纳米氧化锌进行电镜扫描,结果如图4所示。
由图4可知,氧化锌为棒状,由实验制的样品可知制备的氧化锌为乳白色和微黄色。a和b样品的分散性比c和d样品的分散性好,说明助溶剂的加入可以提高样品的分散性,在实验中加入助溶剂的样品在燃烧时有噼啪声和发生溅射。这是盐在加热时发生爆破同时带动样品溅射,使样品冷却更迅速,从而限制晶体继续长大,加入助溶剂所得样品更蓬松,棒更短。
2.5 氧化锌的红外和紫外谱图分析
实验对600℃煅烧样品进行红外和紫外光谱扫描,结果如图5,6所示。由图5可知,3 400 cm-1为氧化锌与水的羟基峰形成的化学键的伸缩振动,此峰在经过高温煅烧不会消失说明此吸收峰并不是氧化锌的表面吸附的水,而是水已经与氧化锌形成了化学键O—Zn—O—H—O。1 384,1 619 cm-1为O—C O的红外吸收峰,在1 700~1 800 cm-1未出现红外吸收峰说明氧化锌在经过燃烧之后并不吸附二氧化碳,而是表面的O—Zn—对O—C O形成O—Zn—O—C O键或者是O—Zn—O—C—O—在经高温加热也不会消失。说明此氧化锌在3 4 0 0 cm-1形成的O—Zn—O—H—O和1 3 8 4,1 619 cm-1形成的O—Zn—O—C O和O—Zn—O—C—O—化学键具有相当的稳定性。400 cm-1左右峰为氧化锌的吸收峰,由图5可以看出,氧化锌吸收峰在未加助溶剂时峰变得更加尖锐,加入助溶剂此峰变宽。煅烧前后氧化锌的红外峰吸收范围都是400~607 cm-1,未煅烧的氧化锌与煅烧的氧化锌红外谱图5基本一致,而且未煅烧的氧化锌红外吸收峰更强。说明未经煅烧的样品纯度较高,红外吸收效果好,加入盐助溶剂红外吸收范围更宽。由图6可以看出,氧化锌在375 nm处有强的紫外吸收峰,此吸收峰非常尖锐,加入盐助溶剂紫外吸收变强。说明用燃烧法加入助溶剂制备的氧化锌有较强的紫外吸收,可作为紫外屏蔽材料。这可能是由于加入盐助溶剂可改变样品在制备过程中的结晶度速率进而改变结晶度,从而提高紫外吸收。

Fig.4 Scanning electron microscopy of zinc oxide图4 氧化锌SEM扫描电镜
3 结束语
(1)燃烧法制备乳白色棒状纳米氧化锌Zn(NO3)2·6 H2O,NaCl,抗坏血酸物质的量比为1∶0.5∶3,不用煅烧,所制样品比较蓬松。
(2)燃烧法制备的氧化锌在3 400 cm-1有强吸收峰是由氧化锌吸附水而产生的。

Fig.5 Infrared absorption spectra图5 红外吸收光谱
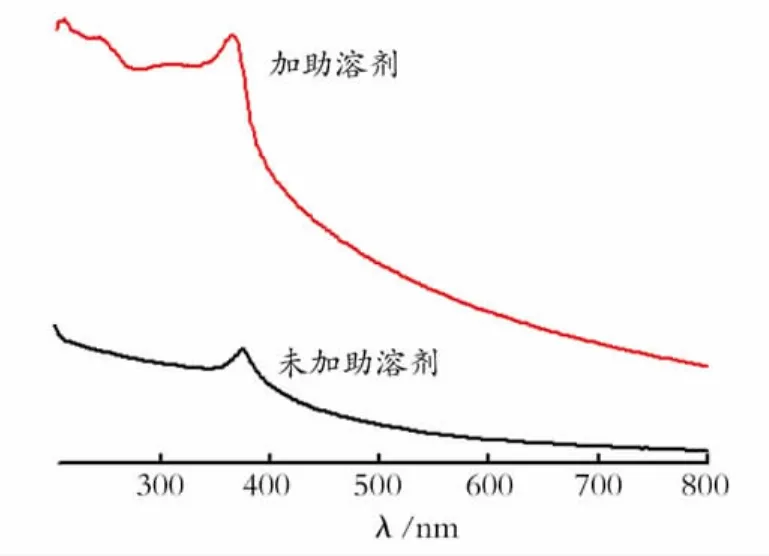
Fig.6 UV absorption spectra图6 紫外吸收光谱
[1] Lin C C,Lin W H,Li Y Y.Synthesis of ZnO nanowires and their applications as an ultraviolet photodetector[J].Nanosci nanotechno,2009,9(5):2813-2819.
[2] Zhou H,Fang G J,Yuan L Y,et al.Deep ultraviolet and near infrared photodiode based on n-ZnO/p-silicon nanowire heterojunction fabricated at low temperature[J].Appl.phys.lett.,2009,94:13503-13505.
[3] Karan S,Mallik B.Nanostructured organic-inorganic photodiodes with high rectification ratio[J].Nanotechnology,2008,19:495202-495207.
[4] Zimmler M A,Voss T,Ronning C,et al.Exciton-related electroluminescence from ZnO nanowire light-emitting Diodes[J].Appl.phys.lett.,2009,94:241120-241123.
[5] Cao P X,Ding Y,Wang Z L.Electronic transport in superlattice-structured ZnO nanohelix[J].Nano.lett.,2009,9(1):137-143.
[6] Li P G,Wang X,Tang W H.Facile synthesis of well-aligned ZnO nanowire arrays and their photoluminescence properties[J].J.alloys compo.,2009,476:744-748.
[7] Wu J J,Liu S C.Low-temperature growth of well-aligned ZnO nanorods by chemical vapor deposition[J].Adv.mater.,2002,14:215-218.
[8] Lao J Y,Wen J G,Ren Z F.Hierarchical ZnO nanostructures[J].Nano.lett.,2002,2:1287-1291.
[9] Li Y,Meng G W,Zhang L D,et al.Ordered semiconductor ZnO nanowire arrays and their photoluminescence properties[J].Appl.phys.lett.,2000,76:2011-2013.
[10] Gao X P,Zheng Z F,Zhu H Y,et al.Rotor-like ZnO by epitaxial growth under hydrothermal conditions[J].Chem.commun.,2004,12:1428-1429.
[11] Liu J,Guo C,Li C M,et al.Carbon-decorated ZnO Nanowire array:a novel platform for direct electrochemistry of enzymes and biosensing applications[J].Electrochem.commun.,2009,11:202-205.
[12] 牛俊粉,田贵山,魏春城,等.自蔓延燃烧法制备铁酸锌微粉[J].硅酸盐通报,2008,27(2):386-389.
[13] 吴佳卿,郑敏.燃烧合成法制备氮掺杂粉色氧化锌纳米晶[J].无机材料学报,2008,23(6):1277-1282.
[14] 周国华,廖世焱,万端极.燃烧法制备纳米Zn O及光催化降解甲基橙的研究[J].化学工程师,2009,170(11):15-19.
[15] 陈亮,宋武林,谢长生,等.熔融燃烧法制备四针状纳米氧化锌[J].功能材料,2007,38(3):495-498.
(Ed.:SGL,CP)
Salt Cosolvent-Combustion Rapidly Synthesized Small-Size Rod Zinc Oxide
LI Xiu-ping1,ZHAO Rong-xiang2,LIU Chun-sheng1,GAO Xiao-han1,FENG Jin-ye3
(1.School of Chemistry &Material,Liaoning Shihua University,Fushun Liaoning 113001,P.R.China;2.School of Petrochemical Engineering,Liaoning Shihua University,Fushun Liaoning 113001,P.R.China;3.CNPC Fushun Chemical Plastics Plant,Fushun Liaoning 113005,P.R.China)
1 June 2012;revised 25 June 2012;accepted 2 July 2012
With zinc nitrate as the oxidant and ascorbic acid as reducing agent and a new burners,combustion rapidly synthesized milky and rod zinc oxide.The burning agent dose,calcined or not,calcination temperature,adding cosolvent or not were inspected.The experiment show ratio of ascorbic acid and zinc nitrate is 3∶1,ratio of ascorbic acid and cosolvent is 1∶0.5.Product of combustion wasn't calcined and washed,which is high purity and good crystallinity.The samples more fluffy and shorter by adding cosolvent.The sample was characterized by FTIR,XRD,UV-Vis,SEM.Zinc oxide has strong absorption in UV-Vis and IR wave band,particles size is micron,morphology is short rod.
Combustion method;Rod;Zinc oxide
.Tel.:+86-13942361930;e-mail:zhaorongxiang@sina.com
TE65;O643.3
A
10.3969/j.issn.1006-396X.2012.05.005
1006-396X(2012)05-0018-04
