直接甲醇燃料电池用Co-N-C电催化剂的制备及性能*
2012-07-31杨伟陈胜洲董新法林维明
杨伟 陈胜洲 董新法 林维明,2
(1.华南理工大学化学与化工学院,广东广州510640;2.广州大学 化学化工学院,广东广州510006)
目前直接甲醇燃料电池(DMFC)的阴极催化剂主要使用铂或者铂基合金催化剂,由于铂资源匮乏,价格昂贵,造成了该类电池成本过高,严重阻碍了其商业化应用[1-3].同时甲醇渗透会导致阴极铂催化剂发生电氧化,产生“混合电位”,且甲醇氧化产生的毒性中间体易使催化剂中毒,严重影响电池的输出性能[4-5].因此开发高活性的耐甲醇非贵金属氧还原催化剂是目前DMFC研究的关键问题之一.
含氮碳材料负载过渡金属催化剂对氧还原反应具有较高活性,且对甲醇氧化呈惰性,近几年来成为DMFC 研究的热点[6].Ye 等[7]采用高温碳化含有Co、Fe等非贵金属盐的聚丙烯腈,制得具有高氧还原活性的含氮碳气凝胶负载非贵金属电催化剂.李旭光等[8]考察了甲醇对Pt/C和碳载四羧基酞菁钴(CoPcTc/C)催化氧还原性能的影响,发现800℃热处理的CoPcTc/C具有较高氧还原催化活性和耐甲醇能力.
含氮碳材料负载过渡金属催化剂具有取代Pt系催化剂作为DMFC催化剂的潜能,但其催化机理仍未有定论,很难确定影响催化剂活性的控制因素,然而碳化温度和氮含量是影响含氮碳材料负载过渡金属催化剂形成氧还原催化活性位的关键因素已经得到共识[9].文中以高含氮量的三聚氰胺甲醛树脂(MF)和硝酸钴为主要原料,在不同碳化温度下制备了含氮碳载钴(Co-N-C)氧还原电催化剂,并利用热重与傅里叶变换红外光谱(TG-FTIR)、X射线衍射分析(XRD)、元素分析等考察了不同碳化温度对电催化剂的氧还原催化活性的影响和电催化剂的耐醇性能.
1 实验部分
1.1 试剂和仪器
试剂:三聚氰胺甲醛树脂(工业级,98%,晋州市中兴化工有限公司);硝酸钴、甲醇、乙醇、异丙醇(分析纯,广州试剂厂);Nafion溶液(5%,分析纯,Fluka公司);高纯氧气、高纯氮气(纯度为99.999%,佛山梅塞尔气体有限公司).
仪器:美国 TA SDT Q600型热分析仪,美国PerkinElmer Spectrum 100型红外光谱仪,德国Elementar Vario EL III元素分析仪,北京普析XD-3型X射线衍射分析仪(北京普析通用仪器有限公司),美国TesSol Fideris燃料电池测试系统,上海辰华CHI760B型电化学测试系统,美国PINE MSR型旋转圆盘电极,DF 101S型恒温磁力搅拌器,DZF6051型真空干燥箱.
1.2 实验方法
称取计量比的硝酸钴与MF树脂(Co与C的质量比为5%)混合,加入适量水,在室温下搅拌30min,然后在35℃下真空干燥,将干燥后的样品在高温管式炉中 Ar气保护和不同温度(600、700、800、900℃)下碳化,制得含氮碳载钴电催化剂,分别标记为 Co-N-C-600、Co-N-C-700、Co-N-C-800、Co-N-C-900.
由热分析仪、傅里叶变换红外光谱仪组成红外-热分析联用仪,对样品的碳化过程进行表征.实验中同时记录样品的热重(TG)、微商热重(DTG)曲线和红外吸收光谱.实验中样品量为7 mg,升温范围为100~1000℃,升温速率为10℃/min,载气(Ar)流量为50mL/min.红外光谱仪气体传输线路及检测气室温度为240℃,扫描波数范围为4000~650cm-1.采用元素分析仪测试电催化剂中C、H、N元素的含量.
采用XD-3型X射线衍射仪分析电催化剂的晶相结构,Cu靶激发Kα辐射为射线源,管压为36kV,电流为20mA,扫描范围(2θ)为10°~90°,扫描速度为4(°)/min.
在25℃的0.5 mol/L H2SO4溶液或者含有0.2mol/L CH3OH 的 0.5 mol/L H2SO4溶液中对Co-N-C电催化剂进行氧还原活性测试.采用传统的三电极体系,以Pt片电极为对电极,饱和甘汞电极(SCE)为参比电极,负载Co-N-C电催化剂的玻碳电极(直径4mm)为工作电极.实验前分别依次使用1.0、0.3、0.05μm 氧化铝粉末对玻碳电极进行抛光,然后分别用乙醇和水进行超声清洗.称取1 mg Co-N-C电催化剂与1 mL异丙醇-Nafion混合溶液(异丙醇、水和 Nafion的体积分数分别为20%、73.75%和6.25%),配成1g/L 的悬浮液.超声分散30min,移取6μL悬浮液至电极表面,自然晾干制得工作电极.测试前向 H2SO4溶液中通高纯氧气10min.采用旋转圆盘电极进行测试,扫描电压为-0.2 ~0.8V(vs.SCE),扫描速率为10mV/s,转速为1500r/min.
采用Fideris燃料电池测试系统对催化剂进行DMFC单电池测试.膜电极(MEA)制备中,经过预处理的Nafion 117膜为质子交换膜,阳极催化剂为PtRu/C(Johnson Matthey,60%),PtRu 金属载量为4mg/cm2;阴极催化剂为自制催化剂,Co金属载量为10mg/cm2;阳极和阴极的几何面积为5cm2.MEA在0.5MPa和135℃下热压90s.
2 结果与讨论
2.1 Co-N-C 电催化剂的结构表征
2.1.1 TG-FTIR 分析
样品在Ar中升温速率为10℃/min的TG和DTG曲线见图1,不同碳化温度下分解产生的尾气的红外吸收光谱见图2.综合分析样品的热重曲线和红外光谱图,样品的热解失重过程可根据升温过程划分为3个阶段:(1)在300℃以下,主要为样品中水分和少量CO2的挥发,失重量较小;(2)在300~600℃之间,小分子基团如HCHO(特征峰为2960~2770、1800~1690cm-1)等受热挥发,部分有机基团在惰性气氛中受热剧烈分解,以CO2(特征峰为2380~2260cm-1)、CO(特征峰为 2190 ~2080 cm-1)、NH3(特征峰为1150 ~850cm-1)等形态随气流流失[10-11],3250cm-1处的吸收峰是分解产物Co-N-C的吸收峰,且该位置的吸收峰始终存在,此阶段为主要的失重阶段;(3)在600℃以上,此碳化过程中样品深层的挥发性物质向外层缓慢扩散,持续时间较长,尾气中只有少量CO2、CO出现,样品结构基本稳定,最后即可得到含氮的碳载钴电催化剂.
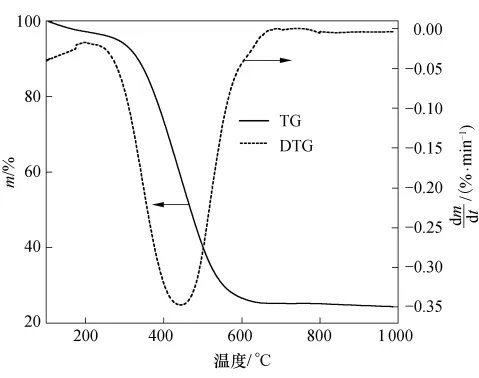
图1 样品在Ar(Ar流量为50 mL/min)中升温速率为10℃/min的TG和DTG曲线Fig.1 TG and DTG curves of sample at a heating rate of 10℃/min and Ar flow of 50mL/min

图2 Co-N-C电催化剂在不同碳化温度下分解产生的尾气的红外光谱图Fig.2 FTIR spectra of gases produced by Co-N-C electrocatalysts at different carbonization temperatures
2.1.2 元素分析
表1为 Co-N-C 电催化剂中 C、H、N、Co元素的含量,其中Co含量是由加入原料量和失重量计算得出.由表1可知,H、N元素的含量随碳化温度的升高而减小,C、Co元素的含量随温度升高而增加,超过700℃后各元素的含量趋于稳定.
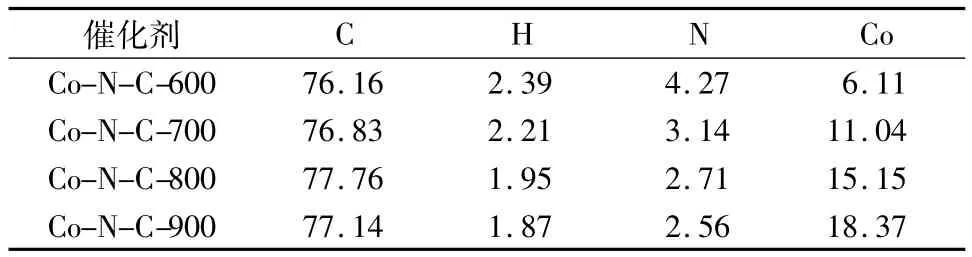
表1 Co-N-C电催化剂的元素含量Table 1 Element content of Co-N-C electro-catalysts %
2.1.3 X 射线衍射分析
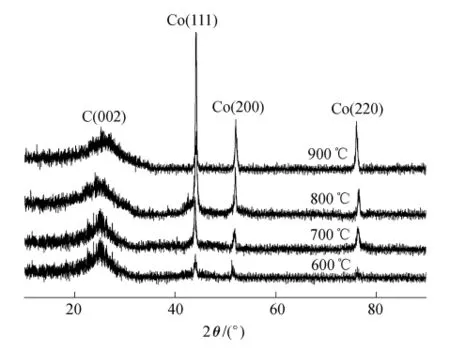
图3 不同碳化温度下制备的Co-N-C电催化剂的XRD谱图Fig.3 XRD patterns of Co-N-C electro-catalysts prepared at different carbonization temperatures
不同碳化温度下制备的Co-N-C电催化剂的XRD 谱图见图3,在 2θ为 44.6°、52.1°和 76.2°处出现的衍射峰分别对应于Co的(111)、(200)和(220)晶面衍射峰[12],与标准图谱(PDF 89 -4307)对照,结果表明热处理后的碳载体表面形成面心立方的晶态α-Co.从图3可知,碳化温度越高,Co的衍射峰峰宽越小,说明Co晶粒尺寸随碳化温度的升高逐渐变大[13].
2.2 碳化温度对Co-N-C电催化剂氧还原活性的影响

图4 不同催化剂在O2饱和的0.5mol/L H2SO4溶液或含有0.2mol/L CH3OH 的 0.5 mol/L H2SO4溶液中的极化曲线Fig.4 ORR curves of different catalysts in saturated oxygen 0.5mol/L H2SO4solution with or without 0.2mol/L CH3OH
不同催化剂在O2饱和的0.5mol/L H2SO4或含有0.2mol/L CH3OH 的 0.5mol/L H2SO4溶液中的极化(ORR)曲线见图4.从图4(a)可知:不同温度下制备的Co-N-C电催化剂的氧还原起始电位在0.5 V左右,与同载量的Pt/C催化剂的氧还原起始电位接近;Co-N-C电催化剂的氧还原起始电位随碳化温度升高出现负移;催化剂的极限电流大小顺序依次为Pt/C>Co-N-C-700 >Co-N-C-600 > Co-N-C-800 > Co-N- C-900,700℃下制备的Co-N-C电催化剂具有最大的极限电流.这是因为在500~700℃之间热处理的催化剂中[14-15],Co与 N 在碳载体表面上相结合,生成含有Co—N和Co—C结构的片段,其中部分片段为对氧还原反应具有催化活性的Co—N4结构.因此,700℃是MF树脂和硝酸钴制备Co-N-C电催化剂的最佳碳化温度.当热处理温度超该温度后,Co—N4结构中可能有一部分Co—N键断裂,形成大颗粒的无氧还原催化活性的Co金属原子簇,使氧还原催化活性降低[16],与XRD检测结果一致.
从图4(b)中可知,不同温度下制备的Co-N-C电催化剂在有CH3OH或无CH3OH的电解质溶液中的极化曲线基本无变化,说明Co-N-C电催化剂具有良好的耐醇性能;而Pt/C催化剂则在0.45 V处出现一个明显的CH3OH氧化峰,表明Pt/C催化剂的耐醇性能较差.

图5 阴极催化剂为Co-N-C-700的DMFC单电池性能Fig.5 Single cell performance of DMFC with Co-N-C-700 as the cathode electro-catalyst
2.3 Co-N-C 电催化剂的 DMFC 单电池性能测试
选取性能最佳的Co-N-C-700电催化剂作为阴极催化剂进行DMFC单电池测试,电流密度与放电电压和功率密度的关系曲线见图5.阳极催化剂为商用PtRu/C,PtRu金属载量为4 mg/cm2;阴极催化剂为 Co-N-C-700,Co 金属载量为 10 mg/cm2;处理后的 Nafion117膜为质子交换膜[17].电池运行条件:甲醇浓度为2mol/L,流速为1mL/min,氧气流速为100mL/min,温度为60℃.由图5可以知道,阴极催化剂为Co-N-C-700的DMFC 单电池电流密度为260mA/cm2时,出现最高功率密度为54.73mW/cm2、单电池放电电压为0.223 V,然后功率密度迅速减小,说明催化剂在电池运行条件下稳定性较差,有待进一步研究.
3 结语
采用MF树脂和硝酸钴在不同碳化温度下制备了一系列的氧还原电催化剂,并对其结构和性能进行了表征,结果发现:实验所制备的含氮碳载钴氧还原电催化剂都具有较好的氧还原电催化活性和抗甲醇性能,是一种有极大应用前景的DMFC阴极催化剂;碳化温度为700℃的催化剂具有最高的氧还原催化活性;当碳化温度超过700℃后,催化剂的氧还原活性随碳化温度升高而降低.有关含氮碳载钴电催化剂的稳定性有待进一步研究.
[1] Arico`A S,Srinivasan S,Antonucci V.DMFCs:from fundamental aspects to technology development[J].Fuel Cells,2001,1(2):133-161.
[2] Kundu A,Jang J H,Gil J H,et al.Micro-fuel cells-current development and applications [J].JournalofPower Sources,2007,170(1):67-78.
[3] 廖世军,谌敏.有机溶胶法制备Pt/C催化剂的影响因素[J].华南理工大学学报:自然科学版,2008,36(11):1-6.Liao Shi-jun,Chen Min.Factors to affect preparation of Pt/C catalyst via organic colloidal method [J].Journal of South China University of Technology:Natural Science Edition,2008,36(11):1-6.
[4] Han Jiahua,Liu Hongtan.Real time measurements of methanol crossover in a DMFC [J].Journal of Power Sources,2007,164(1):166-173.
[5] Xu Chao,Faghri Amir,Li Xianglin,et al.Methanol and water crossover in a passive liquid-feed direct methanol fuel cell[J].International Journal of Hydrogen Energy,2010,35(4):1769-1777.
[6] Bezerra Cicero W B,Zhang Lei,Lee Kunchan,et al.A review of Fe-N/C and Co-N/C catalysts for the oxygen reduction reaction [J].Electrochimica Acta,2008,53(15):4937-4951.
[7] Ye Siyu,Vijh Ashok K.Non-noble metal-carbonized aerogel composites as electrocatalysts for the oxygen reduction reaction [J].Electrochemistry Communications,2003,5(3):272-275.
[8] 李旭光,邢巍,陆天虹,等.直接甲醇燃料电池的耐甲醇阴极电催化剂炭载四羧基酞菁钴的研究[J].高等学校化学学报,2003,24(7):1246-1250.Li Xu-guang,Xing Wei,Lu Tian-hong,et al.Studies on methanol-tolerant cathode electrocatalysts cobalt tetracarboxylic phthalocyanine supported on carbon black(CoPcTc/C)in direct methanol fuel cell[J].Chemical Journal of Chinese Universities,2003,24(7):1246-1250.
[9] Bezerra Cicero W B,Zhang Lei,Liu Hansan,et al.A review of heat-treatment effects on activity and stability of PEM fuel cell catalysts for oxygen reduction reaction[J].Journal of Power Sources,2007,173(2):891-908.
[10] 连晨舟,吕子安,徐旭常.典型毒害气体的FTIR吸收光谱分析[J].中国环境监测,2004,20(2):17-20.Lian Chen-zhou,Lü Zi-an,Xu Xu-chang.FTIR spectroscopic analysis of the exit gas in industry[J].Environmental Monitoring in China,2004,20(2):17-20.
[11] Yang Jing-biao,Cai Ning-sheng.A TG-FTIR study on cata-lytic pyrolysis of coal[J].Journal of Fuel Chemistry and Technology,2006,34(6):650-654.
[12] Zhang Hui-juan,Yuan Xianxia,Wen Wen,et al.Electrochemical performance of a novel CoTETA/C catalyst for theoxygen reduction reaction [J].Electrochemistry Communications,2009,11(1):206-208.
[13] Yang Ruizhi,Stevens Krystal,Bonakdarpour Arman,et al.Dependence of the activity of sputtered Co-C-N oxygen reduction electrocatalysts on heat-treatment temperature[J].Journal of the Electrochemical Society,2007,154(9):B893-B901.
[14] Faubert G,Lalande G,Côté R,et al.Heat-treated iron and cobalt tetraphenylporphyrins adsorbed on carbon black:physical characterization and catalytic properties of these materials for the reduction of oxygen in polymer electrolyte fuel cells[J].Electrochimica Acta,1996,41(10):1689-1701.
[15] Bouwkamp-Wijnoltz A L,Visscher W,Van Veen J A R,et al.On active-site heterogeneity in pyrolyzed carbonsupported iron porphyrin catalysts for the electrochemical reduction of oxygen:an in situ mössbauer study [J].Journal of Physical Chemistry B,2002,106(50):12993-13001.
[16] Velázquez-Palenzuela Amado,Zhang Lei,WangLiucheng,et al.Fe-Nx/C electrocatalysts synthesized by pyrolysis of Fe(II)-2,3,5,6-tetra(2-pyridyl)pyrazine complex for PEM fuel cell oxygen reduction reaction[J].Electrochimica Acta,2011,56(13):4744-4752.
[17] Chen Shengzhou,Ye Fei,Lin Weiming.Effect of operating conditions on the performance of a direct methanol fuel cell with PtRuMo/CNTs as anode catalyst[J].International Journal of Hydrogen Energy,2010,35(15):8225-8233.
