微波加热高碳锰铁粉固相脱碳显微结构
2012-07-31李凯陈津池成忠刘科
李凯,陈津,池成忠,刘科
(1. 太原理工大学 材料科学与工程学院,山西 太原,030024;2. 湘潭市联智科技有限公司,湖南 湘潭,411101)
中低碳锰铁是生产铬锰系不锈钢等合金钢的基础原料,也是电焊条行业的重要原料[1-4]。随着铬锰系不锈钢等低碳合金钢的快速发展,中低碳锰铁的需求量明显增加,尤其对碳等杂质含量的要求越来越严格[5-6]。由于锰与氧的结合能较大,且锰的蒸气压相对较高,高碳锰铁液相脱碳时锰的损失比较严重[7-9]。高碳锰铁的固相脱碳能避免金属锰液的高温蒸发,日益受到冶金界的重视[10-11]。锰和碳可以形成多种碳化物,在高碳锰铁(含碳量为6%~8%)中,碳主要以锰铁复合碳化物(Fe,Mn)xCy的形式存在[12]。高碳锰铁的金相显微结构及碳化物形态关系到碳原子的固态扩散等固相脱碳的机理,高碳锰铁粉配加碳酸钙粉在微波场中进行固相脱碳可以实现深度脱碳,且残留的氧化钙又可辅助脱碳锰铁添加过程中钢水的脱硫脱磷作用。但是目前,对于这种脱碳物料的显微结构与物相组成以及不同脱碳温度下的氧化程度研究较少,所以了解这种高碱度脱碳物料的物相组成和显微结构对其合理使用十分必要。 本文作者主要研究微波加热高碳锰铁粉与碳酸钙粉混合物料固相脱碳后物料的物相组成及显微结构。对微波加热高碳锰铁粉固相脱碳后的物料分别进行碳含量测定、电子探针及 XRD分析,结合锰-碳相图,得出微波加热高碳锰铁粉固相脱碳后的物相组成、各物相形态特点与显微结构。
1 实验
实验材料为广西钦州某锰业公司生产的电炉高碳锰铁,其成分(质量分数)见表1。高碳锰铁粉由块状高碳锰铁经球磨机制成粒度小于0.3 mm的粗粉料,再经制粉机制成粒度小于0.074 mm的细粉料。碳酸钙粉为粒度小于0.045 mm的工业碳酸钙粉,其成分(质量分数)见表2。

表1 广西钦州电炉高碳锰铁化学成分Table 1 Chemical compositions of high-carbon ferromanganese produced in Qinzhou, Guangxi %

表2 实验用碳酸钙粉的主要化学成分Table 2 Main chemical composition of calcium carbonate %
实验所用的加热装置为自行研制的微波冶金加热炉,交流电工作电压为220 V,微波加热功率为10 kW;测定碳含量所用仪器为南京诺新分析仪器有限公司生产的NXQ-2D碳硫联测分析仪;背散射电子探针图像来于日本电子光学公司生产的 JXA-8800R电子探针分析仪;X线衍射图谱来于德国BRUKER/AXS公司生产的D8-ADVANCE型X线衍射仪。
微波加热实验物料由0.5 kg高碳锰铁粉和0.5 kg碳酸钙粉组成,坩锅由轻质耐火砖制成。将混合物料充分搅拌均匀后自然装入坩锅内,然后将坩埚放入微波冶金炉加热腔内,微波冶金另热炉结构示意图见图1。微波加热频率为2.450 GHz,在室内自然条件下选择合适的微波加热功率分别加热到900,1 000,1 100和1 200 ℃,并分别在其温度保温脱碳60 min,自然冷却后下料,微波加热混合料开温特性曲线见图2。

图1 微波冶金加热炉结构示意图Fig.1 Sketch of microwave metallurgical heating oven
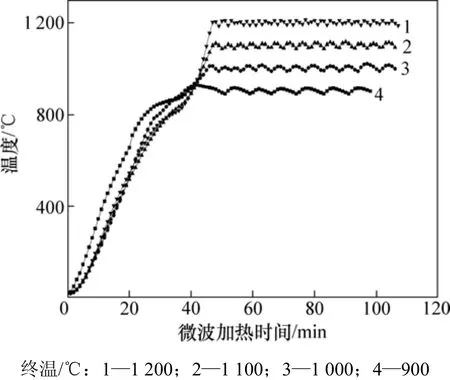
图2 微波加热高碳锰铁粉与碳酸钙粉混合物料升温特性曲线Fig.2 Heating curve of microwave heating high carbon ferromanganese materials mixed with calcium carbonate powder
测定不同脱碳温度下脱碳物料的碳含量,并取一部分脱碳物料分别外送进行电子探针分析和 XRD分析(Cu Kα)。
2 结果与分析
2.1 碳含量分析
由于脱碳过程中碳酸钙粉完全分解为 CaO和CO2,故脱碳后物料的碳含量(质量分数,下同)需换算成除CaO外锰铁的实际碳含量。

表3 混合物料在不同脱碳温度下的碳含量Table 3 Carbon content of mixed materials at different decarburization temperatures
由表3可以看出:微波加热到900 ℃保温脱碳60 min后,物料的实际碳含量为1.54 %,脱碳温度为1 000℃时,实际碳含量为1.13 %,脱碳物料的实际碳含量随脱碳温度的升高而降低,当脱碳温度在1 000 ℃以上时,脱碳程度受温度影响较小。虽然脱碳温度越高,碳含量越低,但是温度越高,金属锰、铁的氧化程度越高,将会出现高价金属氧化物和锰酸钙、硅酸钙等产物,而且较高脱碳温度下金属锰挥发损失增加,故需要进一步讨论微波加热高碳锰铁粉固相脱碳的最佳脱碳温度。
2.2 电子探针分析
对不同脱碳温度下的物料进行电子探针分析,得到各脱碳温度下物料的背散射电子图像及各分析点的成分分别如图3~6和表4~7所示。
由图3(a)可以看到:微波加热900 ℃脱碳温度下,生成的金属锰铁相和金属锰相呈星点状和蠕虫状零散分布在加热后的物料中。这是由于高碳锰铁粉颗粒具有良好的微波吸收性,在微波场中可以快速升温,有利于碳在金属锰铁中的扩散与还原,金属锰铁相首先在高碳锰铁粉颗粒中心附近生成,随着金属锰铁及金属锰的增加,局部有金属相的聚集现象。金属相周围为碳酸钙粉分解后的氧化钙,低碳锰铁碳化物与锰铁相存在包裹与镶嵌结构。
由图3(b)可以看到:球形层状结构,此结构为晶粒级的反应单元,最里层为还原出来的金属锰铁相,金属锰铁相外面环绕有断续环状的少量残余的游离碳及深黑色的颗粒间的空洞,最外层为包裹的少量球壳状氧化锰,球形层状结构周围为碳酸钙粉分解后生成的氧化钙。由表4结合图3可看出:微波加热900 ℃保温脱碳 60 min固相脱碳后物料的主要物相组成为金属锰铁、金属锰、氧化钙和低碳锰铁碳化物(见图3(a)),其中有少量的氧化锰和极少量的单质游离碳。

图3 微波加热900 ℃背散射电子图像Fig.3 Backscattered electron image of mixed materials heated at 900 ℃ by microwave

表4 图3(b)中分析点主要成分(质量分数)电子探针分析结果Table 4 Electron microprobe analysis results of points in Fig.3(b)

图4 微波加热1 000 ℃背散射电子图像Fig.4 Backscattered electron image of mixed materials heated at 1 000 ℃ by microwave

图5 微波加热1 100 ℃背散射电子图像Fig.5 Backscattered electron image of mixed materials heated at 1 100 ℃ by microwave

图6 微波加热1 200 ℃背散射电子图像Fig.6 Backscattered electron image of mixed materials heated at 1 200 ℃ by microwave
由图4(a)可以看到:微波加热1 000 ℃脱碳温度下,生成的金属锰铁相和金属锰相有明显的聚集现象,金属相的环边彼此相连成片,在随后保温的60 min里由于温度较高,还原出来的金属相逐渐氧化生成氧化锰;其间分布着氧化钙和低碳锰铁碳化物,还有反应颗粒间的空隙及少量残余的碳质。图4(b)则反映出与图3(b)类似的的球形层状结构,最里层为金属锰铁相与低碳锰铁碳化物的镶嵌结构,锰铁相表面氧化为少量MnFe2O4,其外面深黑色为物料空洞,再往外为环绕的氧化锰,球形层状结构周围为氧化钙。由表5结合图4可看出:微波加热1 000 ℃固相脱碳后的物料主要组成为金属锰铁、氧化钙和氧化锰,其中还有极少量的单质游离碳。
由图5(a)可以看到:微波加热1 100 ℃脱碳温度下,锰的氧化明显加剧,氧化产物由MnO变为Mn3O4;多数还原出来的金属锰铁相和金属锰相已被完全氧化,但是由于铁不如锰活泼且球形层状结构中心氧化性气体难以进入,还有少量金属铁未被氧化。锰铁氧化物周围为氧化钙和低碳锰铁碳化物,还有反应颗粒间的空隙,此时已看不到游离的单质碳。从图5(b)可以看到:球形层状结构最里层亮白色的金属锰铁相,该物相铁含量远远高于锰含量,实为固溶了少量金属锰的金属铁。往外为 Mn3O4与物料空洞,外层为Mn3O4。球形层状结构的表面为Mn3O4在微波场中高温下与CaO反应生成的CaMnO3,周围为氧化钙及部分由于硅钙反应生成的Ca2SiO4。由表6结合图5可看出:微波加热1100 ℃固相脱碳后的物料主要组成为Fe,CaO 和 Mn3O4,其中还有少量的 CaMnO3和Ca2SiO4。
由图6可以看到:微波加热到1 200 ℃后,球形层状结构消失,取而代之的是实心球形结构,中间有少量微小孔隙。这是由于高碳锰铁的熔化温度在1 070~1 260 ℃之间,保温时间内实际温度在1 200 ℃上下波动,高碳锰铁粉颗粒在一定时间内会变为锰铁小液滴,锰铁液滴内部比高碳锰铁粉颗粒内部致密,脱碳冷却后小液滴凝固为致密实心球形结构,外部氧化性气体只能氧化锰铁表面;微小孔隙为在液态凝固时反应生成的CO来不及完全逸出形成的。1 200 ℃脱碳温度下实际碳含量为0.94 %(见表3),此含碳量的锰室温下为碳在锰中的固溶体α-Mn。同样,α-Mn的最外层高温氧化生成Mn3O4,Mn3O4进一步与CaO反应生成CaMn2O4,且高温时球形结构周围CaO与SiO2反应生成Ca2SiO4。

表5 图4(b)分析点主要成分电子探针分析结果Table 5 Electron microprobe analysis results of points in Fig.4(b)

表6 图5(b)分析点主要成分电子探针分析结果Table 6 Electron microprobe analysis results of points in Fig. 5(b)

表7 图6(b)分析点主要成分电子探针分析结果Table 7 Electron microprobe analysis results of points in Fig.6(b)
2.3 XRD分析

图7 微波加热900 ℃ XRD衍射谱Fig.7 XRD pattern of mixed materials heated at 900 ℃ by microwave

图8 微波加热1 000 ℃ XRD衍射谱Fig.8 XRD pattern of mixed materials heated at 1 000 ℃ by microwave

图9 微波加热1 100 ℃ XRD衍射谱Fig.9 XRD pattern of mixed materials heated at 1 100 ℃ by microwave

图10 微波加热1 200 ℃ XRD衍射谱Fig.10 XRD pattern of mixed materials heated at 1 200 ℃ by microwave
XRD物相分析结果见图7~10。图7~10各衍射峰特性表明:高碳锰铁粉与碳酸钙粉混合物料经微波加热后的实际物相组成是比较复杂的,除了含有 Mn,Fe,FeMn3,FeMn4,CaO,Mn23C6和 Fe0.3Mn2.7C 等物相外,还存在少量Mn5C2,MnO和Mn3O4等物相。其中,CaO为碳酸钙粉分解后产物,900 ℃和1 000 ℃脱碳温度下产生金属锰、金属铁、锰铁合金及低碳锰铁碳化物,同时有少量MnO和Mn3O4,其中900 ℃时氧化程度最低,1 000 ℃时氧化物较多。1 100 ℃和1 200 ℃脱碳温度下,由于较高温度下金属锰、金属铁等氧化加剧,出现 Fe2O3和 MnO2等氧化物,同时出现硅酸钙和锰酸钙等杂质。
3 结论
(1)微波场中微波对物料进行选择性均匀体加热,物料整体同步升温,高碳锰铁粉颗粒具有良好的微波吸收性,可以快速升温,有利于碳在金属锰铁中的扩散与还原,金属锰铁和金属锰首先在高碳锰铁粉颗粒中心生成。
(2)微波场中高碳锰铁粉固相脱碳温度在900 ℃时的综合效果最好,实际碳含量可达1.54 %,脱碳物料的金属化率高且无锰酸钙、硅酸钙等杂质相产生,在此温度下金属锰的挥发损失也最低。
(3)微波场中高碳锰铁粉固相脱碳后脱碳物料的显微结构主要为包裹与镶嵌结构、球形层状结构和实心球形结构。
(4)经900 ℃固相脱碳后的物料主要物相组成为金属锰铁、金属锰、低碳锰铁碳化物与氧化钙,可以在铬锰系不锈钢等合金钢冶炼中作为合金添加剂与脱磷、脱硫剂使用。
[1]张泾生, 乐毅. 锰系铁合金产业的现状与展望[J]. 中国锰业,2006, 24(3): 1-5.ZHANG Jing-sheng, LE Yi. The current situation and prospect of ferro-alloy industry[J]. China’s Manganese Industry, 2006,24(3): 1-5.
[2]Sil’man G I. Alloys of the Fe-C-Mn system. Part 4. Special features of structure formation in manganese and high-manganese steels[J]. Metal Science and Heat Treatment,2006, 48: 1-2.
[3]Napara-Volgina S G, Maslyuk V A, Orlova L N. Economically alloyed manganese-containing powder structural steels.composition, preparation conditions, and properties[J]. Powder Metallurgy and Metal Ceramics, 2005, 44: 3-4.
[4]Srivastava A K, Karabi D. Microstructural characterization of hadfield austenitic manganese steel[J]. Journal of Materials Science, 2008, 43: 5654-5658.
[5]李辉, 储少军. 纯净锰铁生产工艺方案的实验研究[J]. 铁合金, 2004, 175(2): 1-4.LI Hui, CHU Shao-jun. Experimental study of the craft project of clean ferromanganese[J]. Ferro-Alloys, 2004, 175(2): 1-4.
[6]刘中柱, 蔡开科. 纯净钢生产技术[J]. 钢铁, 2000, 35(2):64-69.LIU Zhong-zhu, CAI Kai-ke. Purity steel production technology[J]. Iron and Steel, 2000, 35(2): 64-69.
[7]Nokhrina O I, Komshukov V P, Dmitrienko V I. Developing a technology for the direct alloying of steel with manganese in an electric-ARC-furnace[J]. Metallurgist, 2004, 48: 5-6.
[8]屠章云, 杭祖辉, 张玉林. 双联摇包工艺生产中碳锰铁试验[J]. 中国锰业, 2009, 27(1): 15-17.TU Zhang-yun, HANG Zu-hui, ZHANG Yu-lin. The technology of double-rocker in mid-carbon Mn-Ferro[J]. China’s Manganese Industry, 2009, 27(1): 15-17.
[9]张晓斌, 韩永光. 转炉生产中碳铬铁和中碳锰铁的技术研究与实践[J]. 铁合金, 2008(1): 15-19.ZHANG Xiao-bin, HAN Yong-guang. Producing medium carbon ferrochrome and medium carbon ferromanganese with converter[J]. Ferro-Alloys, 2008(1): 15-19.
[10]Bhonde P J, Angal R D. 高碳锰铁的固态脱碳[J]. 铁合金,1992(6): 51-55.Bhonde P J, Angal R D. Decarburization of high-carbon ferromanganese in solid state[J]. Ferro-Alloys, 1992(6): 51-55.
[11]梁敏, 陈津, 林万明, 等. 高碳锰铁粉固相脱碳热力学研究[J].铁合金, 2009, 204(1): 14-17.LIANG Min, CHEN Jin, LIN Wan-ming, et al. Thermodynamics study on solid phase decarbonization of high carbon ferromanganese powder[J]. Ferro-Alloys, 2009, 204(1): 14-17.
[12]Lis J, Lis A, Kolan C. Manganese partitioning in low carbon manganese steel during annealing[J]. Materials Characterization,2008, 59: 1021-1028.
