藤黄健骨片的临床应用评价
2012-07-30贡联兵冯常智解放军第305医院北京100017
贡联兵,冯常智(解放军第305医院,北京 100017)
藤黄健骨片上市已3年多,为了做好藤黄健骨片上市后再评价,我们收集了藤黄健骨片上市后国内相关文献,对藤黄健骨片的应用状况、有效性、安全性等进行分析评价。
1 概述
藤黄健骨片是长春中医学院名老中医刘伯龄教授的经验处方,主要成分:熟地黄、鹿衔草、骨碎补(烫)、肉苁蓉、淫羊藿、鸡血藤、莱菔子(炒)。上药经研粉,过筛,混匀,共压制成片包薄膜衣片。方中重用熟地黄,滋阴补血,益精填髓,大补肝肾之真阴,为君药;淫羊藿、肉苁蓉、骨碎补、鹿衔草辅助君药补益肝肾,强筋健骨,共为臣药;鸡血藤活血通络,补骨止痛,为佐药;莱菔子以防补而滋腻之弊,为使药。藤黄健骨片以中医“治骨先治肾”的理论为基础,功能补肾、活血、止痛,主要用于肥大性脊椎病、颈椎病、跟骨刺、增生性关节炎、大骨病。
2 藤黄健骨片的有效性
2.1 实验研究
湖南中医药研究院临床药理研究室[1]进行了藤黄健骨片对氢化可的松肾虚模型组[2]小鼠,去卵巢、地塞米松、维甲酸骨质疏松模型[3-5],血瘀模型组动物影响的研究及藤黄健骨片止痛、抗炎、活血试验的研究。结果显示藤黄健骨片能提高氢化可的松肾虚模型组小鼠的胸腺系数、睾丸重量、小鼠碳粒廓清K及校正指数α,改善去卵巢骨质疏松模型大鼠的一般症状和股骨病理症状,可以看出藤黄健骨片能提高模型大鼠的骨密度、组织含量及血清钙、降钙素、皮质酮、雌二醇含量,降低碱性磷酸酶活力。藤黄健骨片能改善地塞米松骨质疏松模型大鼠的一般症状和病理症状,提高股骨的最大弯曲力、抗弯强度与断裂挠度,升高血清钙、皮质酮、雌二醇,降低碱性磷酸酶,能提高维甲酸骨质疏松模型大鼠血清钙、磷、碱性磷酸酶,改善股骨骨小梁细小疏松、排列紊乱不规则的病理症状,见表1。藤黄健骨片对甲醛致小鼠疼痛的Ⅰ相反应和Ⅱ相反应均有一定的止痛作用。藤黄健骨片能抑制大鼠棉球肉芽组织增生,见表2、3。藤黄健骨片对肾虚、骨质疏松症模型动物的改善作用,以及止痛、抗炎等辅助作用,为其功能及其临床应用提供了一定的药理学依据。
2.2 临床评价
2.2.1 椎动脉型颈椎病:张波等[6]观察藤黄健骨片对椎动脉型颈椎病的疗效。对椎动脉型颈椎病63例患者给予藤黄健骨片口服进行治疗,用药3个月,观察患者眩晕程度、眩晕时间、眩晕频率、视物模糊、头痛及旋颈实验。结果显示藤黄健骨片能够明显改善患者头晕症状,从而达到对椎动脉型颈椎病的临床治疗作用。
2.2.2 膝关节骨性关节炎(肾虚血瘀型):湖南省中医药研究院附属医院、湖南中医药大学第一附属医院、湖南中医药大学第二附属医院3家医院门诊收治膝关节骨性关节炎患者共240例(每家医院各入组80例),按随机数字表法分为2组,治疗组120例,对照组120例。治疗组给予藤黄健骨片,1次3~6片,bid,4周为1个疗程;对照组给予西乐葆胶囊(辉瑞制药有限公司,规格:0.2 g/片),1 次 0.2 g,bid,餐后服用,4周为1个疗程。2组治疗1个疗程后膝关节WOMAC评分均较治疗前减少,差异有统计学意义(P<0.01,P<0.05);治疗组治疗后与对照组比较,在疼痛程度方面差异无统计学意义(P>0.05);2组综合疗效比较差异有统计学意义(P<0.01),治疗组优于对照组;治疗组患者均未出现不良反应;对照组有5例患者出现胃肠道不适,包括腹痛1例、腹泻1例、消化不良2例、胀气1例。结果显示藤黄健骨片治疗膝关节骨性关节炎肾虚血瘀证安全有效。
表1 藤黄健骨片对去卵巢骨质疏松模型大鼠骨密度的影响(±s)Tab 1Effect of Tenghuang Jiangu Tablets on bone mineral density in ovariectomized rats of osteoporosis model(±s)

表1 藤黄健骨片对去卵巢骨质疏松模型大鼠骨密度的影响(±s)Tab 1Effect of Tenghuang Jiangu Tablets on bone mineral density in ovariectomized rats of osteoporosis model(±s)
注:与空白组比较,*P<0.05,**P <0.01;与模型组比较,#P<0.05note:vs.blank control:*P <0.05,**P <0.01;vs.model group:#P <0.05
组别 剂量/g·kg-1 骨密度/g·cm-2 骨矿含量/g 组织含量/% 体重/g空白组(n=10) - 0.171 1±0.005 6 12.51±1.58 39.96±8.17 408.9±68.1模型组(n=9) - 0.164 0±0.005 5** 13.52±0.84 51.83±5.68** 466.9±34.1*依普黄酮组(n=10) 0.1 0.169 2±0.004 9# 12.99±1.11 45.72±8.67 456.6±32.9藤黄健骨片组(n=9) 1.2 0.166 0±0.005 8 12.91±1.27 50.08±6.79 453.3±42.6藤黄健骨片组(n=9) 2.4 0.167 2±0.004 9 12.90±1.14 46.07±12.68 431.6±35.5#藤黄健骨片组(n=10) 4.8 0.171 3±0.006 6# 12.86±1.02 46.83±4.99#451.9±37.0
表2 藤黄健骨片对大鼠足疼痛反应的影响(±s,n=10)Tab 2 Effect of Tenghuang Jiangu Tablets on the pain reaction of rats’foot(±s,n=10)
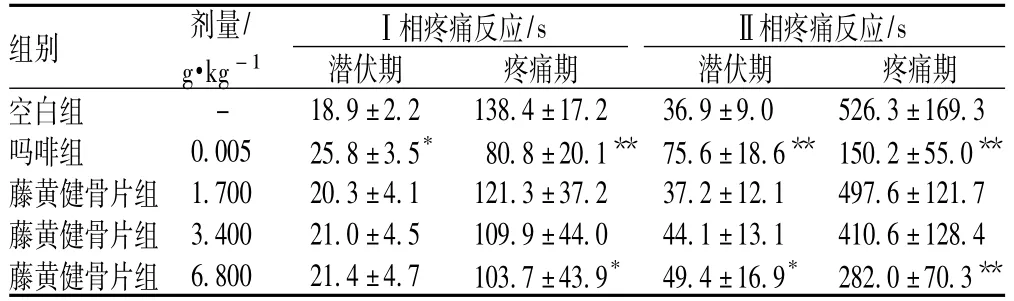
表2 藤黄健骨片对大鼠足疼痛反应的影响(±s,n=10)Tab 2 Effect of Tenghuang Jiangu Tablets on the pain reaction of rats’foot(±s,n=10)
注:与空白组比较,*P<0.05,**P <0.01note:vs.blank group:*P <0.05,**P <0.01
组别 剂量/g·kgⅠ相疼痛反应/s Ⅱ相疼痛反应/s潜伏期 疼痛期 潜伏期 疼痛期空白组-1- 18.9±2.2 138.4±17.2 36.9±9.0 526.3±169.3吗啡组 0.005 25.8±3.5* 80.8±20.1** 75.6±18.6** 150.2±55.0**藤黄健骨片组 1.700 20.3±4.1 121.3±37.2 37.2±12.1 497.6±121.7藤黄健骨片组 3.400 21.0±4.5 109.9±44.0 44.1±13.1 410.6±128.4藤黄健骨片组 6.800 21.4±4.7 103.7±43.9* 49.4±16.9* 282.0±70.3**
表3 藤黄健骨片对大鼠肉芽肿形成的影响(±s,n=10)Tab 3 Effect of Tenghuang Jiangu Tablets on granuloma formation of rats(±s,n=10)

表3 藤黄健骨片对大鼠肉芽肿形成的影响(±s,n=10)Tab 3 Effect of Tenghuang Jiangu Tablets on granuloma formation of rats(±s,n=10)
注:与空白组比较,*P<0.05note:vs.blank group:*P <0.05
组别 剂量/g·kg-1 棉球肉芽肿总重/mg 肉芽肿净重/mg空白组39.5±3.6 19.5±3.6布洛芬组 0.4 36.4±2.8* 16.4±2.8*藤黄健骨片组 1.7 37.3±2.2 17.3±2.2藤黄健骨片组 3.4 36.3±3.0* 16.3±3.0*藤黄健骨片组 6.8 35.6±3.6* 15.6±3.6-**
2.2.3 膝骨关节炎:张波等[7]观察藤黄健骨片口服联合玻璃酸钠(施沛特)关节注射对膝骨性关节炎的临床疗效。将151例膝骨性关节炎患者随机分为2组,对照组73例,给予玻璃酸钠关节腔内注射,1次1支,每周1次,5次为1个疗程;治疗组78例,在前述治疗的基础上加服藤黄健骨片,1次3片,1日2次。对照组73例,痊愈33例,有效率为89.04%;治疗组78例,痊愈50例,有效率为96.15%,2组比较差异有统计学意义(P<0.01)。结果显示玻璃酸钠和藤黄健骨片联合应用治疗骨性关节炎,标本兼治,疗效较好,值得临床推广应用。
3 藤黄健骨片的安全性
3.1 急性毒性试验
湖南省中医药研究院为观察藤黄健骨片的毒性[8],以最大浓度、最大体积给小鼠灌胃,均未出现动物死亡,得不出半数致死量(LD50)。24 h内间隔4 h连续给药3次,藤黄健骨片1日累计给药量(最大给药量)达171.6 g·kg-1(生药),按公斤体重折算相当于体重60 kg成人临床用量的794倍(按体表面积折算为体重70 kg成人临床用量的103倍),连续观察14 d,动物未见明显异常,亦无动物死亡,表明藤黄健骨片在推荐人用剂量范围内用药是安全的,见表4。

表4 藤黄健骨片急性毒性试验结果Tab 4 Result of acute toxicity test on Tenghuang Jiangu Tablets
3.2 长期毒性试验研究
用藤黄健骨片 2.6、6.4、12.9 g·kg-1(生药)3 个剂量连续灌胃大鼠6个月(24周),此时低、中、高剂量分别相当于60 kg成人临床剂量的12、30、60倍,结果给药第1期(12周)、给药第2期(12周)与空白组比较,高剂量组大鼠血液生化指标中门冬氨酸氨基转移酶、血糖有明显差异,恢复性观察期(即停药期4周)无明显差异;其他组指标和其他血液生化指标以及一般状况、体重增长、血液学、主要脏器系数、肉眼观察及镜下组织形态学观察均无明显差异或异常,表明藤黄健骨片高剂量时对大鼠的门冬氨酸氨基转移酶、血糖可能有一定的影响,停药恢复后无明显影响,认为是可逆性影响[9,10]。
4 讨论
从藤黄健骨片的组方可以看出,藤黄健骨片成分中并不含有毒性的中药材“藤黄”,急性毒性试验和长期毒性试验研究也已证明:藤黄健骨片是安全无毒的药物。藤黄健骨片这个药名在临床上容易造成误导,使之感觉该药毒性较大。藤黄健骨片以中医“治骨先治肾”的理论为基础,在治疗退行性骨关节疾病、脊椎退行性疾病引发的疼痛方面具有很好的疗效,可以用来替代需要长期服用某些缓解症状的非甾体抗炎药,又避免了可能会引起的胃肠道反应及肝肾损害等不良反应。经国内外相关文献检索,未发现藤黄健骨片应用后致不良反应报告。藤黄健骨片临床应用更适合脊髓型的颈椎病,治疗腰椎的椎管狭窄有优势,在骨质疏松方面应加强探索研究。藤黄健骨片二期临床重点应放在骨质疏松症和骨关节病上,增加对晨僵、疼痛的观察,治疗椎管狭窄是否有效要增加核磁诊断结果分析。应针对藤黄健骨片治疗骨关节疾病开展大样本、多中心的具有循证医学要求的药品上市后再评价。藤黄健骨片是由骨科专家的经验方研发出来的,是地标转国标的品种,目前经3千例患者临床应用,取得满意的效果,已普遍应用于骨科临床。
[1]王 冰,徐又佳,郝彦明,等.去卵巢和激素致骨质疏松模型中骨密度与血清指标的比较[J].苏州大学学报:医学版,2008,28(1):10-13.
[2]周成刚,周庆来,冯梅梅,等.正骨通痹丸对糖皮质激素致骨质疏松大鼠骨力学的影响[J].中国中医骨伤科杂志,2009,17(3):7-8.
[3]许 鹏,郭 雄,张银刚,等.维甲酸诱导骨质疏松模型大鼠的效果及机理[J].四川大学学报:医学版,2005,36(2):229-232.
[4]陈 旭,杨 勇,刘 慧,等.预先鞘内注射氯诺昔康对福尔马林致痛大鼠行为学及脊髓c-Fos蛋白表达的影响[J].四川大学学报:医学版,2008,39(1):89-93.
[5]贾经汉,邱新建,陈志坚.常用骨质疏松动物模型特点的综述[J].广西中医学院学报,2006,9(4):76-79.
[6]张 波,卢 敏,唐 盾.藤黄健骨片治疗椎动脉型颈椎病临床疗效观察[J].中国现代药物应用,2010,4(16):171-172.
[7]张 波,卢 敏,唐 盾.藤黄健骨片、玻璃酸钠联用与单用玻璃酸钠治疗骨性关节炎疗效比较[J].中国当代医药,2010,17(17):67-68.
[8]李仪奎.中药药理实验方法学[M].上海:上海科学技术出版社,1991.
[9]中药、天然药物长期毒性研究技术指导原则[S].指导原则编号:[Z]GPT3-1.
[10]蒋中仁,徐 薇,金 伟,等.SD大鼠血液学指标、血生化指标及脏体比正常值范围探讨[J].预防医学情报杂志,2011,27(10):789-791.
