制药企业浓缩倍数的研究及节水分析
2012-07-19李占强
杨 健,李占强
(河北省石家庄水文水资源勘测局,河北 石家庄050051)
1 引言
我国的水资源不足且用水效率不高,这要求企业把节约用水和提高水的重复利用率作为用水方向的重点。在制药企业中,循环水占的比重较大,随着生产规模的不断扩大,企业需要一个合理的循环水运行的浓缩倍数,既能最大限度地利用有限的水资源,使资源可持续发展,又能减低设备和投入的成本,达到合理的经济效益。
循环冷却水中,随着循环水在冷却塔中分的蒸发,使得水分中的盐分不断浓缩,盐度不断升高,为了不使水分的盐度过高,就必须排放一部分循环水,并补充一些低盐度的新水。新鲜水和循环水中的含盐分不同,比值就成为浓缩倍数(用K表示)。
数值上浓缩倍数用含盐量计算是比较麻烦的,同时因浓缩倍数提高之后有盐类的沉积,故用含盐量计算出的倍数也存在着误差。因此,一般用在水中比较稳定的离子来计算浓缩倍数。这种离子在浓缩过程中不受外界条件的影响,不分解、不沉淀而且投入的药剂中也不含有此离子。故通常选用Cl-、SiO2、K+等来计算,有时也可以采用好几种离子锁测定的浓缩倍数的平均值来作为倍数的基准。
2 浓缩倍数与水量的关系
循环水的盐度与补水量和排水量有关,根据循环水系统水量平衡和物料平衡可以得出浓缩倍数与补充水量和排污水量必定存在的一定的联系。
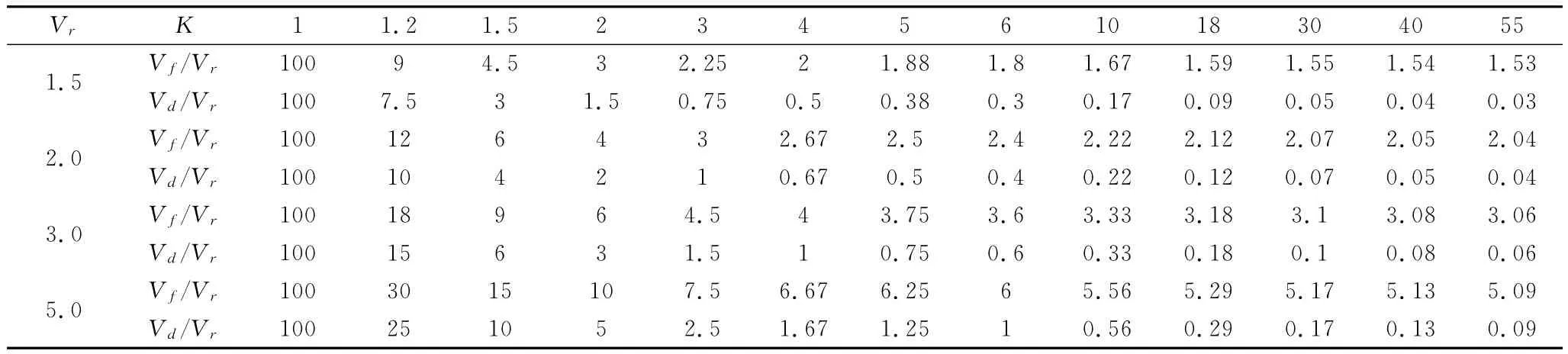
表1 浓缩倍数与补充水量和排污水量的关系
由表1可以看出,当浓缩倍数K等于1时,补水和排污水、循环水量是一样的,这实际上就是未做循环处理的直流直排水系统。当浓缩倍数K大于1时,随着K值的增大,排水和补水量逐渐减小,节水开始见到成效。但是当K大于6时,水量减小的速率减低,节水程度变小。浓缩倍数K受到排污水量的限制,不能无限的提高。当Vd/Vr=1.5%时,浓缩倍数最大不会超过2。在实际操作中,大幅度该表补水量和排污水量会使浓缩倍数K也随之变化。当K值不断增大时,循环水系统的正常运行的难度会增大。若操作时保持浓缩倍数不变,蒸发量增大时,要增大补充水量,还要保持水量平衡,就要增大排水量。因此,增加补水量和排污水量都要影响浓缩倍数的下降。
3 制药企业的用水现状及浓缩倍数分析
3.1 工艺水
企业的制药车间可通过纯化水设备,制造出来的纯化水供制作药品是药品的中间体使用,或是在制药工序中发酵、提炼、合成、稀释和反洗等工序都需要水的工艺水的使用。并产生一定量的废水外排到污水管网。
3.2 间接冷却水
主要用于企业的动力车间。通过水泵将水送至各个生产车间的冷冻机、空压机以及各种设备冷却,返回到循环水池通过冷却塔降温使水重复使用。
3.3 生活用水
生活用水主要包括办公楼、餐厅、车间洗浴、绿化以及消防和职工生活用水等。在这其中间接冷却水占的比重是最大的,一般可达到80%左右。因此这部分的用水相比之下更具有节水的潜力。循环水的利用率与浓缩倍数有着密切的联系。
某制药厂补水水质分析,pH 值7.6、总硬度250mg/L、氯化物31.5mg/L、硫酸盐67.5mg/L、矿化度457mg/L、氨氮<DL、亚硝酸盐氮0.004mg/L、硝酸盐氮1.91mg/L、高 锰 酸 钾 指 数 0.5mg/L、氟 化 物 0.73mg/L、总铅0.01mg/L。
公司循环水水质分析:pH值7.8、总硬度700mg/L、氯化物102mg/L、硫酸盐246mg/L、矿化度1 350mg/L、氨氮0.29mg/L、亚硝酸盐氮0.038mg/L、硝酸盐氮4.60mg/L、高锰酸钾指数7.2mg/L、氟化物1.07mg/L、溶解性铁0.06mg/L、总铅0.08mg/L,总汞0.0002mg/L、总砷0.0001mg/L。
根据以上的水质数据中前3项对比测算浓缩倍数的可以看出该企业循环冷却水浓缩倍率仍较低,现在企业循环水浓缩倍数保持在3.5左右,浓缩倍率从目前的3倍提高至5倍,每1万m3循环冷却水可减少补充新水约43m3,按照制药厂年间冷循环水量为1 108.5万m3计算,则年减少新水4.8万m3。这样可以一定程度上节省企业用水开支,达到节水的目的。
4 结语
在企业循环水的浓缩倍数处于比较低的运行状态下,提高浓缩倍数会使节水效果十分显著。但是当浓缩倍数处于比较高的水平时,再设法增加浓缩倍数,会使节水成效不明显,还增加了设备的运行风险。在现有医药行业的水处理情况下,还是将循环水的浓缩倍数控制在4.0~5.0之间,以保证设备的安全运行。减少蒸发损失也是提高节水效率的有效方法。在循环水在安全的浓缩倍数运行下,减少蒸发就是减少了新水的补充量。根据用水分析可以看出制药行业中工艺用水占其用水量的比重也比较大。制药企业中制作纯水的工艺废水可以用于循环水中这样对水质要求一般的设备中。医药工艺的污染较重的废水可以经过一定的环保处理,再重复利用到企业自身的循环冷却水中。这样可以充分利用水资源,提高浓缩倍数。
[1]常明旺.工业企业水平衡[M].北京:化学工业出版社,1998.
[2]李智慧.水平衡测试技术[M].太原:山西科学技术出版社,2008.
