超声场中钙基固体碱催化猪油制备生物柴油*
2012-06-25邹华生雷敏李剑
邹华生 雷敏 李剑
(华南理工大学化学与化工学院,广东广州510640)
化石能源的逐日减少以及开发和使用化石能源所造成的环境污染的逐年加剧,使得寻找可持续发展的绿色环保的新能源成为科学研究的热点.生物柴油因具有优良的燃烧性能和环保性能而受到广泛的重视[1-2].生物柴油是植物油和动物脂肪与甲醇或者乙醇进行酯交换反应得到的脂肪酸单酯,是一种可再生的环保型燃料[3-4].
我国具有巨大的猪油来源,生猪屠宰以及食品加工行业每年会产生大量的猪油.据统计,2007年我国猪板油产量在226万~283万吨,五花油产量在85万~113万吨,而且我国的猪肉和猪油产量还呈现出逐年上涨的趋势[5].猪油含有较高的饱和脂肪酸和胆固醇,长期食用容易引发高血压等疾病,因此猪油大量过剩.在生物柴油的生产中,原料成本占到了生产成本的75%以上[6].利用废弃猪油制备生物柴油有利于降低生产成本,提高市场竞争力,丰富生物柴油的原料来源.
当超声波作用于互不相溶的醇油体系时,其产生的空化作用会强烈地扰乱相界面并引起乳化,增强传质过程,加快反应速率[7-8].目前,对于酸值较高的原料油,为避免酯化过程中出现严重皂化,先以浓硫酸为催化剂对原料油进行预酯化处理,将酸值降到2mg KOH/g以下[9-10],再使用均相碱催化剂催化油脂与甲醇酯交换反应得到生物柴油.以均相碱为催化剂时,反应条件温和,反应速度快,转化率高,但存在着催化剂难于回收、产品需要洗涤、产生废液多、乳化严重等问题;而以固体碱为催化剂时,反应后催化剂易于分离和回收,且可重复利用,产品不需要水洗,减少了环境污染[11-13].
目前,国内外以动物脂肪为原料制备生物柴油的研究较少,以猪油为原料制备生物柴油更是鲜有报道.Dias等[14]以猪油为原料,采用两步法来制备生物柴油.该研究以机械搅拌的方式强化醇油两相混合,混合效率低,反应时间长.黄瑛等[15]使用Novozym435和Lipozyme TLIM两种脂肪酶来协同催化猪油酯化以制备生物柴油,甲酯收率达到了97.6%.但是该方法使用的酶用量较大且无法回收,生产成本高,反应时间长,催化效率低.
以猪油为原料生产生物柴油既利用了剩余猪油,又丰富了能源供给,经济可行,高效环保.文中将超声辐射的高效强化作用与固体碱催化剂的环保、可回收优点结合起来,采用两步法来制备生物柴油,系统地研究了超声功率、醇油摩尔比、温度、催化剂用量对预酯化反应和酯交换反应的影响,以探求最佳工艺条件;通过正交试验优化了固体碱催化剂的制备条件,评价了催化剂的重复使用性能.
1 材料与方法
1.1 原料试剂
实验所用猪油(酸值为13.82 mg KOH/g,皂化值为208.3mg KOH/g)由当地猪肉市场及餐饮行业收集的废弃余料加热炼制而成;甲醇、浓硫酸、氢氧化钾、醋酸钙均为分析纯,购于天津市化学试剂一厂;载体NaA,购于广州光义化工科技发展有限公司;参照标准(肉豆蔻酸甲酯、棕榈酸甲酯、棕榈油酸甲酯、硬脂酸甲酯、油酸甲酯、亚油酸甲酯和亚麻酸甲酯)和内标物(十三碳酸甲酯)均为色谱纯,购于Sigma公司.
1.2 浓硫酸催化预酯化
甲醇与100 g猪油按比例混合,在40 kHz超声波作用下水浴恒温至设定温度,以浓硫酸为催化剂进行预酯化反应.反应过程中每隔一段时间取样,水洗除去甲醇和催化剂,参照GB/T5530—2005测定样品的酸值.
1.3 固体CaO/NaA催化剂的制备
采用等体积浸渍法制备固体CaO/NaA催化剂.首先将载体NaA研磨至100目,然后将载体加入到不同质量分数的Ca(Ac)2溶液中,机械搅拌3h后陈化24h,在120℃下将溶液中的水分蒸干并于马弗炉中煅烧.
1.4 固体碱催化酯交换反应
在40kHz超声波作用下水浴恒温至设定温度,用一定量最佳条件下制备的固体碱催化剂催化预酯化后的猪油(100g)与甲醇进行酯交换反应.反应过程中每隔一段时间取样,静置分层,取上层酯层,水洗以除去甲醇和催化剂,用气相色谱仪(Agilent-6820)测定生物柴油的组成.采用内标法计算脂肪酸甲酯的含量.色谱分析条件:毛细管柱DB-1(30m×0.32mm×0.25μm),进样量为 1 μL,载气为 N2,载气流速为80mL/min,进样口温度为290℃,FID检测器,检测温度为300℃,柱箱初始温度为140℃,保持2min后以6℃/min的速度升温至220℃,保持1min后再以5℃/min的速度升温至270℃,保持10min.
参照GB/T17376—2008对猪油进行甲酯化处理,测得理论脂肪酸甲酯产量,计算猪油的甲酯转化率:

2 结果与讨论
2.1 超声功率对预酯化反应的影响
在醇油摩尔比为8∶1、反应温度为50℃、催化剂用量为2%(质量分数,下同)、超声频率为40kHz和不同功率的超声波作用下,猪油酸值随时间的变化如图1所示.当超声功率从30 W增大到150 W时,超声空化效应逐渐增强,空化泡的形成和破裂扰乱了醇油两相边界,强化了传质,增大了预酯化速率,猪油酸值迅速降低;当继续增大超声功率至180 W时,预酯化速率反而变小,反应平衡时猪油的酸值变大.这是因为过于剧烈的空化效应使反应体系中形成了大量的空化泡,减小了甲醇的有效浓度,降低了预酯化效果.因此,超声功率以150W为宜.
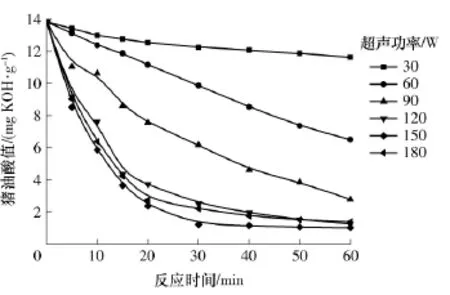
图1 超声功率对猪油酸值的影响Fig.1 Influence of ultrasonic power on acid value of lard
2.2 醇油摩尔比对预酯化反应的影响
在150W及40kHz的超声场、反应温度为50℃、催化剂用量为2%和不同醇油摩尔比作用下,猪油酸值随时间的变化如图2所示.由于适当增大醇油摩尔比可以促使预酯化反应平衡正向移动,增大预酯化速率,因此,随着醇油摩尔比从3∶1逐渐增大到8∶1,预酯化速率逐渐变大,反应平衡时猪油的酸值逐渐变小,再继续增大醇油摩尔比至10∶1,预酯化速率并没有显著变化.因此,醇油摩尔比以8∶1为宜.
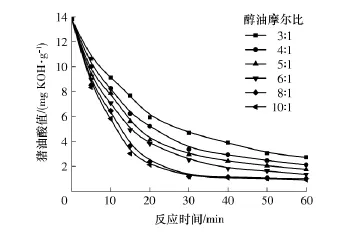
图2 醇油摩尔比对猪油酸值的影响Fig.2 Influence of molar ratios of methanol to oil on acid value of lard
2.3 反应温度对预酯化反应的影响
在150W及40kHz的超声场、醇油摩尔比为8∶1、催化剂用量为2%和不同温度下,猪油酸值随时间的变化如图3所示.随着温度从40℃升高到55℃,预酯化速率逐渐增大,反应平衡时猪油酸值变小,再继续升温到60℃,预酯化速率并没有显著变化,且当温度升高到65℃时,预酯化速率反而降低.这是因为温度已经达到甲醇的沸点,甲醇剧烈汽化,降低了甲醇的有效浓度.考虑到较高的温度会增加操作成本,温度为50℃时猪油的预酯化速率及反应平衡时猪油的酸值与55℃时相近,因此以50℃为最佳反应温度.

图3 反应温度对猪油酸值的影响Fig.3 Influence of reaction temperature on acid value of lard
2.4 催化剂用量对预酯化反应的影响
在150W及40kHz的超声场、醇油摩尔比为8∶1、反应温度为50℃和不同催化剂用量下,猪油酸值随时间的变化如图4所示.随着催化剂用量从0.5%增加到2.5%,预酯化速率逐渐增大,反应平衡时猪油酸值变小,再继续增大催化剂用量至3.0%,预酯化反应速率并没有显著变化,而且过量的催化剂还会使油脂脱水和炭化,影响反应的效果.因此,以2.5%为最佳催化剂用量.

图4 催化剂用量对猪油酸值的影响Fig.4 Influence of amounts of catalyst on acid value of lard
2.5 固体CaO/NaA催化剂制备条件的优化
当载体一定时,对影响固体催化剂活性的3个因素(负载量、焙烧温度、焙烧时间)进行正交试验.用不同条件下制备的催化剂催化预酯化后的猪油进行酯交换反应(超声功率为150W,频率为40kHz,醇油摩尔比为9∶1,温度为55℃,催化剂用量为4%,反应时间为90min),以甲酯转化率作为评价催化剂活性的指标.正交试验结果如表1所示,3个因素对催化剂活性的影响从大到小的顺序为:焙烧温度>负载量>焙烧时间,最优水平为:负载量为15%、焙烧温度为700℃、焙烧时间为6h.将最优条件下制备的固体催化剂用于后续的酯交换反应.
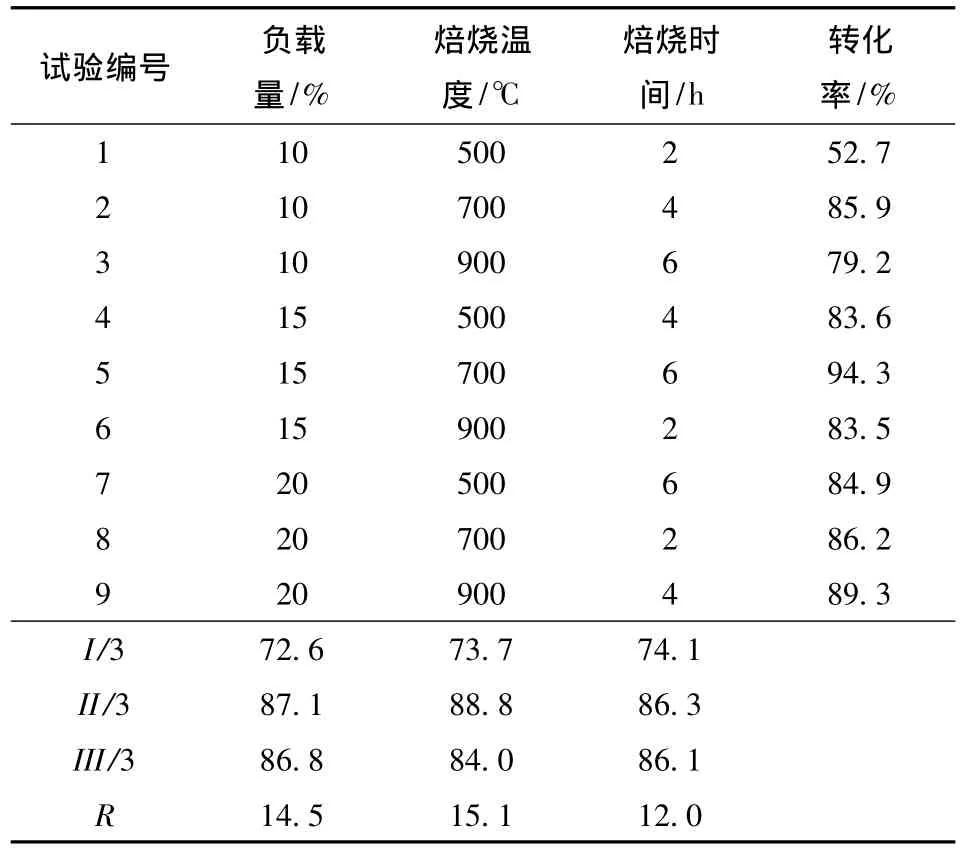
表1 正交试验结果1)Table 1 Results of orthogonal experiment
2.6 超声功率对甲酯转化率的影响
在醇油摩尔比为9∶1、温度为55℃、催化剂用量为4%、超声频率为40 kHz和不同功率的超声波作用下,甲酯转化率随时间的变化如图5所示.随着超声功率从30W逐渐增大到150 W,超声空化效应逐渐增强,超声空化作用及其产生的微射流使反应体系形成乳化,强化了传质,增大了酯化速率,甲酯转化率迅速增大,但空化效应产生的空化泡也会降低甲醇的有效浓度,进而降低酯化反应速率;当继续增大超声功率至180W时,甲酯转化率反而变小.因此以150W为最佳超声功率.
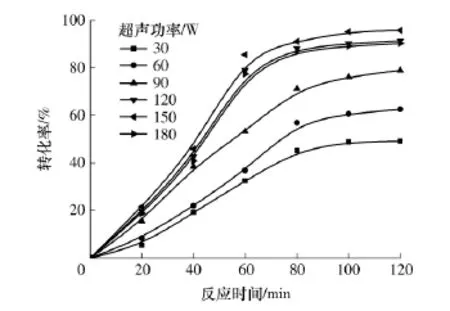
图5 超声功率对甲酯转化率的影响Fig.5 Influence of ultrasonic power on conversion of methyl esters
2.7 醇油摩尔比对甲酯转化率的影响
在150W及40kHz的超声场、反应温度为55℃、催化剂用量为4%和不同醇油摩尔比作用下,甲酯转化率随时间的变化如图6所示.当醇油摩尔比从3∶1逐渐增大到9∶1时,酯化反应速率逐渐增大,甲酯转化率先增大后趋于平缓.当醇油摩尔比超过9∶1时,再增大醇油摩尔比对甲酯转化率没有明显的影响.因此,选择最佳醇油摩尔比为9∶1.
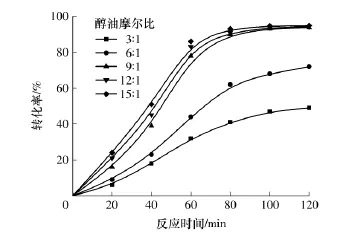
图6 醇油摩尔比对甲酯转化率的影响Fig.6 Influence of molar ratios of methanol to oil on conversion of methyl esters
2.8 反应温度对甲酯转化率的影响
在150W及40kHz的超声场、醇油摩尔比为9∶1、催化剂用量为4%和不同温度下,甲酯转化率随时间的变化如图7所示.随着温度从40℃升高到55℃,酯化反应速率和甲酯转化率逐渐增大;当继续升温到60℃时,甲酯转化率并没有显著变化;当温度升高到65℃时,甲酯转化率反而降低,这是因为甲醇沸腾时会剧烈汽化,降低了甲醇的有效浓度.因此,以55℃为最佳反应温度.
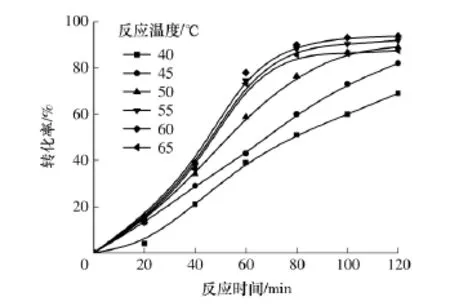
图7 反应温度对甲酯转化率的影响Fig.7 Influence of reaction temperature on conversion of methyl esters
2.9 催化剂用量对甲酯转化率的影响
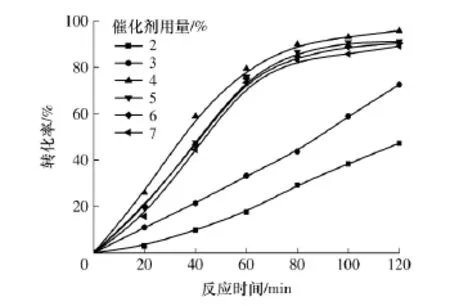
图8 催化剂用量对甲酯转化率的影响Fig.8 Influence of amounts of catalyst on conversion of methyl esters
在150W及40kHz的超声场、醇油摩尔比为9∶1、温度为55℃和不同催化剂用量下,甲酯转化率随时间的变化如图8所示.由于反应体系是非均相的,反应物与催化剂活性中心接触不充分,增加催化剂用量有利于增加酯化反应速率和甲酯转化率.随着催化剂用量从2%增加到4%,酯化反应速率和甲酯转化率逐渐增大;当继续增加催化剂用量时,甲酯转化率反而下降.这是由于甲醇呈极弱的酸性,在催化剂用量达到4%时,甲醇的离解趋于饱和,继续增加催化剂用量并不增加甲醇的离解度和催化剂与甲醇络合物的浓度,反而因催化剂用量过高而导致碱性中心过多,皂化增强.因此,以4%为最佳催化剂用量.在最佳条件下反应120min,甲酯的转化率达到了95.8%,与文献[12]相比,文中甲酯转化的反应时间大大缩短.
2.10 催化剂的可重复性
反应结束后,通过抽滤将催化剂和产物分离,在700℃下用马弗炉焙烧1 h后循环使用.在150 W及40kHz的超声场、醇油摩尔比为9∶1、反应温度为55℃、催化剂用量为4%、反应时间为90min的条件下,考察催化剂的重复使用性能,结果如图9所示.
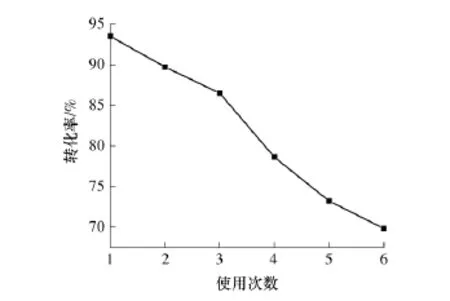
图9 催化剂的可重复性实验结果Fig.9 Experimental result of reusability of catalyst
随着催化剂使用次数的增加,甲酯转化率逐渐降低,在第4次重复使用后,甲酯转化率降低到80%左右,表明文中制备的催化剂的重复使用性能和催化剂活性高于文献[10]中的CaO/MgO/Fe3O4催化剂.催化剂重复使用活性出现衰减,主要是由于多次使用后,载体与活性组分的相互作用减弱,部分活性组分从载体上脱落,溶解于反应体系,导致活性组分流失.另外,预酯化后猪油中残留的游离脂肪酸也会与部分活性组分发生反应,生成脂肪酸钙,使催化剂活性降低.
3 结论
(1)对于初始酸值为13.82 mg KOH/g的猪油,其最佳预酯化条件为:超声功率为150 W,醇油摩尔比为8∶1,温度为50℃,催化剂用量为2.5%.在最佳条件下反应30 min后,猪油的酸值可降到2mg KOH/g以下.
(2)以NaA为载体,固体碱催化剂的最佳制备条件为:CaO负载量为15%,焙烧温度为700℃,焙烧时间为6h.
(3)CaO/NaA催化剂的成本低廉,制备工艺简单,容易再生,具有较高的催化活性.在150 W及40kHz的超声场中,用最佳条件下制备的固体碱催化剂催化预酯化后的猪油进行酯交换反应,在醇油摩尔比为9∶1、反应温度为55℃、催化剂用量为4%的条件下反应120 min,甲酯转化率达到了95.8%.催化剂重复使用3次后仍然具有较高的活性.
[1]Fazal M A,Haseeb A S M A,Masjuki H H.Biodiesel feasibility study:an evaluation of material compatibilityerformance;emission and engine durability [J].Renewable and Sustainable Energy Reviews,2011,15(2):1314-1324.
[2]Yusuf N N A N,Kamarudin S K,Yaakub Z.Overview on the current trends in biodiesel production [J].Energy Conversion and Management,2011,52(7):2741-2751.
[3]Gerhard Knothe.Biodiesel and renewable diesel:a comparison [J].Progress in Energy and Combustion Science,2010,36(3):364-373.
[4]Rashid U,Anwar F.Production of biodiesel through optimized alkaline catalyzed transesterification of rapeseed oil[J].Fuel,2008,87(3):265-273.
[5]张东明,吴潇,马美湖.猪膘脂肪液化利用研究进展[J].肉类研究,2009(5):75-83.Zhang Dong-ming,Wu Xiao,Ma Mei-hu.Research progress of utilization and liquefaction of lard [J].Meat Study,2009(5):75-83.
[6]Meng X,Yang J M,Xu X,et al.Biodiesel production from oleaginous microorganisms[J].Renewable Energy,2009,34(1):1-5.
[7]Stavarache C,Vinatoru M,Maeda Y.Ultrasonic versus silent methylation of vegetable oils[J].Ultrasonics Sonochemistry,2006,13(5):401-407.
[8]Zou H S,Lei M.Optimum process and kinetic study of jatropha curcas oil pre-esterification in ultrasonical field[J].Journal of the Taiwan Institute of Chemical Engineers,doi:10.1016/j.jtice.2012.02.013.
[9]Marchetti J M,Errazu A F.Esterification of free fatty acids using sulfuric acid as catalyst in the presence of tri-[J].Biomass ,2008,32(9):892-895.
[10]Berrios M,Siles J,Martín M A,et al.A kinetic study of the esterification of free fatty acids(FFA)in sunflower oil[J].Fuel,2007,86(15):2383-2388.
[11]Lam Man Kee,Lee Keat Teong,Mohamed Abdul Rahman.Homogeneous,heterogeneous and enzymatic catalysis for transesterification of high free fatty acid oil(waste cooking oil)to biodiesel:a review [J].Biotechnology Advances,2010,28(4):500-518.
[12]陈英,陈东,谢颖,等.用于生物柴油清洁生产的磁性固体催化剂 CaO/MgO/Fe3O4[J].燃料化学学报,2010,38(4):415-421.Chen Ying,Chen Dong,Xie Ying,et al.A magnetic solid catalyst of CaO/MgO/Fe3O4for production of clean biodiesel[J].Journal of Fuel Chemistry and Technology,2010,38(4):415-421.
[13]邹华生,李剑,陈文标.超声辅助固体碱催化酯交换制备生物柴油[J].华南理工大学学报:自然科学版,2011,39(11):6-11.Zou Hua-sheng,Li Jian,Chen Wen-biao.Ultrasonic-enhanced preparation of biodiesel via transesterification catalyzed by solid base[J].Journal of South China University of Technology:Natural Science Edition,2011,39(11):6-11.
[14]Dias Joana M,Alvim-Ferraz Maria C,Almeida Manuel F.Production of biodiesel from acid waste lard [J].Bioresource Technology,2009,100(24):6355-6361.
[15]黄瑛,高欢,郑海,等.脂肪酶协同催化猪油合成生物柴油工艺研究 [J].中国生物工程杂志,2008,28(1):30-35.Huang Ying,Gao Huan,Zheng Hai,et al.Immobilized lipases cooperates to catalyze transesterification reaction of lard [J].China Biotechnology,2008,28(1):30-35.
