纳米石墨化碳在锂离子电池中的应用进展
2012-06-01黄佳琦张强金涌魏飞
黄佳琦,张强,金涌,魏飞
(清华大学化学工程系,绿色反应工程与工艺北京市重点实验室,北京 100084)
随着人类社会对移动能源和清洁发展要求的不断提高,电化学储能受到人们越来越多的重视,自20世纪90年代日本科学家将石墨结构负极材料引入锂离子电池获得广泛工业应用以来,锂离子电池已成为最重要的二次电池。短短20年时间,其应用已渗透到从计算机、照相机、手机到电动汽车等人们生活的方方面面[1-2]。这些应用需求也对锂离子电池的性能提出越来越高的要求,其中对个人电子设备移动电源来说要求电池更小、更薄,甚至具有柔性,而对于动力电池系统来说则要求电池具有更高的能量和功率密度。锂离子电池系统依靠锂离子在正极和负极之间迁移进行能量的储存和释放:充电时,锂离子从正极材料脱嵌并嵌入负极材料中,使负极处于富锂状态;放电时则从负极材料脱嵌并嵌入正极材料中,使正极材料处于富锂状态。该储锂机制要求电极材料具有诸如高化学稳定性、高导电性、高力学稳定性等特点。如何优化电极材料,使其体现更优的电化学储能性质,甚至使电池具有可弯折等新功能是锂离子电池进一步发展的一个重要方向[3]。
炭材料在锂离子电池中一直被广泛使用。例如,带来了锂电池商业化革命、解决了金属锂电池安全问题的石墨插层技术及中间相炭微球负极材料[4];高性能导电材料气相生长碳纤维(VGCF)[5];碳包覆磷酸铁锂正极材料等[6]均在锂离子电池系统中起着重要作用。近年来,随着纳米技术的发展,纳米石墨化碳也加入到炭材料大家族中,以碳纳米管及石墨烯为代表的纳米石墨化碳具有纳米尺度上的低维度特性,同时sp2骨架结构也使其具有优异的电学及力学性能[7-8],为构建高性能锂离子电池电极材料提供了丰富的空间。
碳纳米管从结构上可以认为是石墨层沿着一定矢量方向卷曲闭合形成的管状结构。碳纳米管的sp2杂化结构以及高的长径比为其带来了一系列优异性能。力学性能方面,σ键是自然界中最强的化学键,而碳纳米管全部由C—C之间通过sp2杂化形成的σ键构成,在轴向方向上具有极强的力学性质。结构完美的碳纳米管杨氏模量达到TPa量级,断裂强度可达上百GPa,优于目前使用的凯芙拉等高强度纤维[12]。由于其纳米结构,可使其在伸长17%的条件下不断裂,从而使其在使用过程中有很好的柔性[13],改善电池充放电过程中因体积变化所带来的结构破坏及导电性劣化。电学性能方面,单壁碳纳米管随螺旋度的变化可呈金属性或半导体性,多壁碳纳米管均为金属性。金属性碳纳米管呈现良好的导电性,其电导率可高达106S/cm。室温下,石墨的面内电阻率约0.4 μΩ· m,采用单壁碳纳米管管束或多壁碳纳米管测得的电阻率与0.4 μΩ·m相当或更低[14],在纳米级尺度下,其电导率及最大电流密度优于同尺寸的金属纳米线[15]。同时,由于纳米石墨化碳导电过程中不存在金属导电的离子迁移问题,使小尺度下电池的导电可靠性更好。另外,碳纳米管具有极高的导热率。据分子动力学模拟预测,单壁碳纳米管的c轴方向导热率可达6600 W/(m·K)以上[16],实测值略低于理论预测,实测的单根多壁碳纳米管热导率达到3000 W/(m·K)[17],是导热率最高的金属银的6倍以上,这一性质对于大功率充放电过程中强放热的导出十分重要。
基于碳纳米管及石墨烯本身的石墨化碳结构,使其具有的高化学稳定性、高机械强度与柔性、高导电、高导热性质等,不仅可直接用作锂离子电池负极材料,容量可突破石墨的理论容量372 mA·h/g[18];另一方面,纳米石墨化碳结构也可与其它高容量电极材料复合获得以高导电性纳米石墨化碳为导电、强度骨架的高性能复合电极材料,从而克服活性材料低电导率、充放电过程中易粉化等缺点。本文从纳米石墨化碳在上述综合性能上的优势入手,分别从其在负极材料及正极材料中的应用两方面分析了其在锂离子电池体系中的应用现状及发展前景。
1 纳米石墨化碳在锂电池负极中的应用
以sp2形式杂化的碳材料在锂离子电池负极材料中应用广泛,包括具有石墨层状结构的活性材料中间相炭微球等。而纳米石墨化碳除具有相似的碳原子排布形式外,其独特的低维度纳米结构使其具有相比传统石墨结构碳材料更突出的特征,既可以直接作为高容量锂电池负极材料[19],也可充当骨架材料与硅基、锡基、金属氧化物基活性材料复合,以克服该类材料充放电过程中体积变化率大及电导率低的问题,获得高性能复合负极材料。
1.1 纳米石墨化碳直接用于负极活性材料
目前商用的锂离子电池负极材料主要是石墨结构的碳材料。石墨层内的碳原子通过碳-碳键相连,而石墨层间通过范德华力相互作用,由于其两个方向作用力存在显著差异,在锂离子电池充放电过程中,锂离子可以通过可逆的嵌入/脱嵌在石墨层间插层,从而实现能量的储存和释放。锂离子的嵌入会阻止锂离子在相邻的碳六元环嵌入,故体相石墨材料只能以6个碳原子储1个锂离子的比例储锂,相对应的理论容量为372 mA·h/g。而纳米石墨化碳材料直接用于负极活性材料时的储锂容量往往高于石墨的理论容量,这主要与纳米材料巨大的表面积带来的表面储锂以及材料缺陷带来的储锂能力相关。
1.1.1 碳纳米管直接用作负极活性材料
作为石墨的一种同素异形体,碳纳米管可以作为锂离子电池的负极材料使用。众多研究组采用单壁碳纳米管测得的储锂容量差异较大,可逆储锂容量多在石墨材料的1~2倍。对碳纳米管进行机械或化学处理可进一步提高其容量[20-21]。对多壁碳纳米管来说,有报道指出其初始嵌锂容量可达1000 mA·h/g左右,但首次库仑效率低于50%,可逆容量为447 mA·h/g[22]。采用化学处理或机械处理的方法可有效提高碳纳米管的可逆容量,一方面通过在碳纳米管表面引入缺陷可以增加缺陷处储锂的容量,另一方面化学或机械处理可将碳纳米管截短从而降低锂离子嵌入过程中的迁移距离,提高其储锂的效率[23]。通过元素掺杂等手段可改变石墨层的排布方式并引入缺陷,氮掺杂碳纳米管等材料在作为负极储锂材料方面也有巨大的应用潜能[24]。
值得指出的是,采用碳纳米管直接作为锂离子电池负极材料也存在不少显著的劣势,这些都与其结构密切相关。首先,采用碳纳米管作为负极材料具有较大且难以克服的首次不可逆容量。由于具有较大的比表面积,在首次循环过程中需要消耗大量锂离子形成固体电解质层,如何降低碳纳米管材料的比表面积使其作为电极材料得以使用是重要课题。另一方面,首次充电过程中也有锂离子不可逆地嵌入碳纳米管中。相比中间相炭微球等商用负极材料,碳纳米管在首次不可逆容量方面存在显著的先天劣势。此外,碳纳米管负极也存在缺乏稳定电压平台的劣势。由于大量电子设备对稳定的电源压力提出较高要求,这一特性也会影响碳纳米管真正替代目前商用的石墨类电极材料。尽管如此,我们仍须看到碳纳米管的研究历史仅有20年,在碳纳米管结构的精确控制方面仍缺乏手段[25]。随着碳纳米管制备技术的进一步提升,仍有望针对负极材料结构要求实现碳纳米管负极材料的可控制备。如能实现对碳纳米管管壁数、管径以及表面缺陷的精确控制和批量制备,碳纳米管仍有望作为一种高容量储锂负极材料得到应用。1.1.2 石墨烯直接用作负极活性材料
在大量招生后,高职院校护理教育不仅会受到生源质量不佳的困扰,还会受自身经济实力以及师资力量的限制,使得护理专业教学中出现教学质量不佳、师资力量不足、班级规模过大以及学生护理能力培养不足等问题。这些问题的存在导致学生在医院临床护理中表现不佳,无法满足国家护理行业发展的需求。
理想石墨烯材料具有单层的石墨结构,锂离子的插入过程中能同时在石墨烯片层双侧进行。故石墨烯可与锂离子形成Li2C6的结构,理论容量为传统石墨类材料的2倍,达到744 mA·h/g。与此同时,石墨烯片层边缘以及石墨烯之间相互搭接形成的皱褶状空隙结构也贡献了大量的可逆储锂容量[26-27],如图1所示(锂离子在两种情况下的间距均为0.435 nm)。石墨烯材料储锂的具体嵌入/脱嵌机制仍未彻底得到解释,相关的储能机制研究仍需进一步开展。
在石墨烯储锂的实验研究方面,有研究组采用化学还原氧化石墨烯(rGO)为原料,获得了540 mA·h/g的储锂容量。由于在液相化学还原的过程中石墨烯部分恢复堆叠状态从而导致其容量下降,设法缓解石墨烯在还原过程中的堆叠现象可显著提高其容量和稳定性,故而以碳纳米管和C60与石墨烯材料复合可将其储锂容量分别提高至730 mA·h/g及784 mA·h/g[28]。为简化电极材料制备过程,也可将氧化石墨组装成膜后进行化学还原,并将该石墨烯膜直接用作电池负极材料[29-30],但石墨烯还原时紧密堆叠限制了锂离子在负极材料中有效的迁移,使该膜电极在高充放电电流下容量性能表现不佳。相比液相的化学还原过程,热还原法获得的石墨烯材料具有更丰富的孔道结构以及更优的储锂容量。通过氧化石墨的热还原获得的材料具有1233 mA·h/g的初始容量以及672 mA·h/g的可逆容量[31],通过在氮气环境下进行石墨烯的热还原获得了1264 mA·h/g的初始容量,且在40个循环后仍能保持848 mA·h/g的容量[31]。另一方面,采用石墨烯/碳纳米管杂合物作为锂离子电池负极材料时,这类二维/三维杂合物结构为电极材料提供了丰富的孔道结构,具有650 mA·h/g左右的可逆容量和较优的循环稳定性,同时改善了材料的大电流充放电性能[32]。

图1 锂离子在传统石墨材料和单层石墨烯材料的插层情况Fig. 1 Schematic illustration of the intercalation of lithium ions into graphite materials and the adsorption on both sides of the graphene sheets
与碳纳米管类似,由于其纳米尺度二维结构特点以及大量缺陷、边缘结构的存在,石墨烯材料具有远高于石墨的理论储锂容量,但其巨大的比表面积及缺陷结构带来的储锂死区也使其首次循环效率较低;同时,其充放电曲线缺乏电压平台,不利于其在实际电池系统中的应用。在目前的制备水平下,通过对氧化石墨还原所获得的还原氧化石墨烯结构中氧等杂元素含量偏高也可能导致石墨烯负极材料在长循环过程中稳定性不足。随着制备技术的发展,通过控制石墨烯片层间的间距,避免固体电介质层的形成大量消耗锂离子,并合理平衡缺陷结构储锂与“死锂”的产生可能是石墨烯材料进一步向实用化材料发展的方向之一。
1.2 纳米石墨化碳复合材料用于负极材料
除石墨化碳材料之外,硅基材料、金属氧化物等也有望成为锂离子电池的负极材料。这些材料主要通过合金的形式储存锂离子,具有远高于石墨类材料的理论容量[33],见表1。但另一方面,通过合金形式与锂离子的结合也导致此类材料在充放电过程中会产生巨大的体积变化,会很快导致材料的粉化从而失去储锂能力[34]。同时,硅材料、金属氧化物等往往导电性不佳,这也限制其作为负极材料得到应用。将纳米石墨化碳材料与此类高容量锂电池负极材料复合,可利用纳米石墨化碳构建高效的导电网络以提高负极材料的整体导电性,同时依靠其力学性质一定程度上克服活性材料粉化的问题是目前研究的热点之一。需要指出的是,纳米石墨化碳相比气相生长碳纤维等传统导电添加材料具有更大的比表面积,在首次循环过程中会消耗大量锂离子,如何克服这一缺点仍是该类高性能材料商用化的关键之一。
1.2.1 纳米石墨化碳-硅基复合材料
硅是一类重要的锂离子电池负极材料,作为一种储量十分丰富的材料,其可以以合金的形式与锂离子形成Li4.4Si,从而具有高达4200 mA·h/g的理论容量;同时,硅材料也具有较低的放电电位,有利于构建新型高能量锂离子电池。然而,硅材料在充放电过程中与锂离子形成合金的过程中体积变化可达400%,导致硅基材料在数个循环后迅速粉化失效[27]。解决这一问题的主要途径是实现硅材料本身的纳米化[37],以及通过硅与纳米碳材料复合结构获得稳定性更高的材料[38-39]。纳米石墨化碳材料的引入不仅能通过碳材料的强度和韧性抑制硅材料的粉化,也可以利用其本身导电性构建高效导电网络,提升复合材料的储锂性能。

表1 不同负极材料本征性质比较[23,35-36]Table 1 Comparison of the intrinsic properties of various anode materials[23,35-36]
为验证碳纳米管对硅负极材料的改性作用,早期的研究主要采用机械混合的方法获得碳纳米管/硅复合材料[40-41]。例如,采用球磨[42]的方法实现碳纳米管与硅的复合,对其电化学性能的测试表明:未添加碳纳米管的硅电极材料的首次嵌锂容量超过3000 mA·h/g,但其可逆容量仅仅为300 mA·h/g左右,且经过10个循环就丧失储锂能力;而多壁碳纳米管/硅复合电极的首次库仑效率可达80%左右,经过50个循环的充放电仍能保持1200 mA·h/g以上的容量。除硅颗粒和碳纳米管机械混合外,利用硅和碳纳米管可以通过化学气相沉积的方法获得的原理,也可制备两者的复合材料。如图2所示,采用浮游催化法制备碳纳米管阵列,随后利用硅烷进行硅颗粒的沉积,获得的材料具有2000 mA·h/g以上稳定的可逆储锂容量[43]。通过在不锈钢片上生长10μm左右的短碳纳米管阵列,并以硅烷化学气相沉积的方式在管径5 nm的碳纳米管上负载尺寸10 nm左右的硅颗粒实现了复合电极的制备[44]。该杂化结构中的硅颗粒的纳米级尺寸以及短碳纳米管阵列带来的电子和离子通道使其具有较高的容量,在1.3 C充放电电流下达3000 mA·h/g;同时,该材料也体现出优良的高功率性能,在5 C及15 C的充放电电流条件下仍能获得1900 mA·h/g及760 mA·h/g的容量。采用类似的沉积方法,Evanoff等[45]获得了厚度达到1 mm的碳纳米管阵列/硅复合电极,并具有3000 mA·h/g以上的容量;Cui等[39]也在碳纳米管海绵上制备了高容量复合电极材料。

图2 碳纳米管阵列/硅纳米颗粒复合电极材料结构及电化学性能Fig. 2 The structure and electrochemical performance of silicon/carbon nanotube hybrid materials
二维石墨烯材料也是进行硅负极改性的重要骨架材料。通过氧化石墨或石墨烯的溶液进行硅/石墨烯复合材料的制备是一种高效的方法。Tao等[46]对比了硅纳米颗粒、rGO膜以及硅纳米颗粒/rGO复合膜3种材料作为锂离子电池负极的性能,在充放电电流为50 mA/g的情况下,30个循环内,硅纳米颗粒的放电容量从1250 mA·h/g降低至250 mA·h/g左右;rGO膜的放电容量稳定在500 mA·h/g左右,但是首次库仑效率仅有27%,而硅纳米颗粒/rGO膜复合电极材料的容量稳定在1000 mA·h/g左右,呈现较高的容量及循环稳定性。采用更小粒度的硅纳米颗粒(20~25 nm)制备硅/rGO膜材料时[47],硅纳米颗粒镶嵌在石墨烯层间避免了氧化石墨还原时发生堆叠;另一方面,这类三明治结构同时为硅纳米颗粒提供了良好的导电网络,同时对避免纳米颗粒的聚并以及充放电过程中的粉化具有重要作用。该电极材料在50次循环后仍具有2200 mA·h/g以上的容量,300次循环后容量仍在1300 mA·h/g以上。通过在GO表面进行硝酸处理引入一定的缺陷也可以有效提高硅/rGO膜复合材料的电极性能[48],通过在石墨层面内引入缺陷可提高锂离子扩散效率,从而大幅提高电极材料的大电流充放电性能。在1 C充放电电流下,该电极材料在150次循环后仍具有2500 mA·h/g以上的容量。利用石墨烯材料还可构建多层核壳状电极材料:通过化学气相沉积的方法,以硅烷为原料,高温下实现了石墨烯表面硅薄膜的沉积,然后通过在丙烯环境下热处理实现了石墨烯@硅@碳层结构的制备[49]。在该材料中,石墨烯作为骨架结构提供了一定的强度,而层间的空隙也为硅充放电过程中体积变化提供了充分的空间。该材料在1400 mA/g的充放电电流下脱锂容量达到1000 mA·h/g以上,并且在150个循环内未见显著衰减,如图3所示。
1.2.2 纳米石墨化碳-金属氧化物复合物
除了硅材料以外,大量的金属氧化物也具有较高的储锂容量,可作为负极材料使用,包括SnO2、TiO2、Co3O4、MnO2、Fe3O4等。与硅材料类似,高容量的金属氧化物负极材料的应用也受到低电导率以及充放电过程显著的体积效应的影响[50]。纳米石墨化碳可以在纳米尺度上实现其与金属氧化物的复合,从而克服其导电性差的缺点,降低充放电过程中极化的现象;另一方面也为金属氧化物颗粒提供了力学骨架,避免粉化带来的容量衰减。
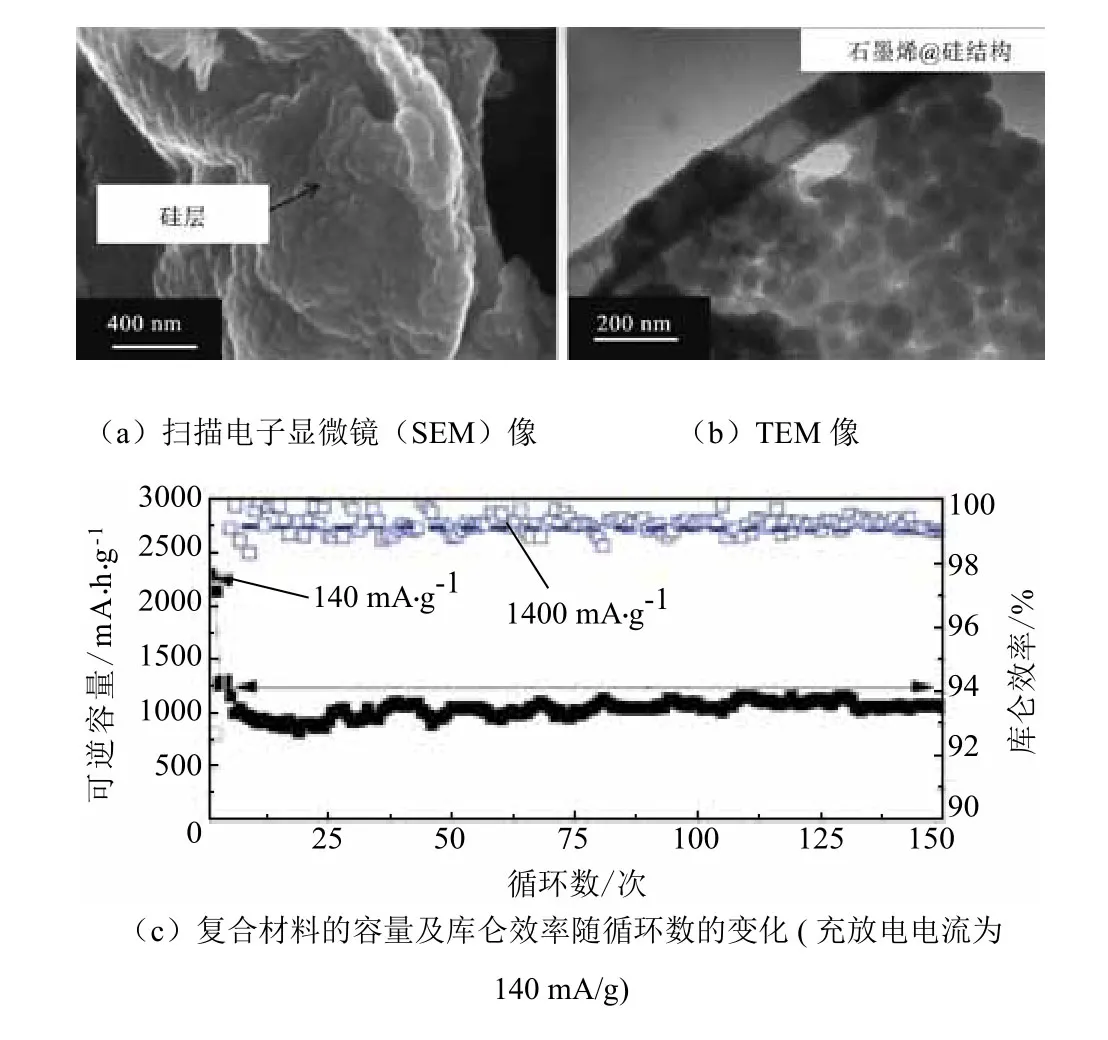
图3 石墨烯@纳米硅薄膜复合材料的结构及电化学性能Fig. 3 The structure and electrochemical performance of C-Si-graphene materials
金属氧化物/碳纳米管复合物可通过球磨[51]、水热[52]、电镀[53]等过程制备。碳纳米管对电极材料的增强作用可大幅提高金属氧化物活性材料的电化学性能。利用水热的方法制备FeOOH纳米棒并与单壁碳纳米管混合抽滤并进行煅烧可获得Fe3O4/单壁碳纳米管复合电极材料。单壁碳纳米管在电极材料中起到导电和力学骨架作用,使纳米尺度Fe3O4活性材料同时获得高容量和高稳定性。该复合材料在1 C充放电电流下,50个循环内容量保持在1000 mA·h/g以上,且未见明显衰减,容量和稳定性均优于Fe3O4颗粒/炭黑复合电极材料[54]。通过在碳纳米管纸上直接滴加水热获得的TiO2颗粒溶液,制得TiO2/碳纳米管复合电极。平均粒径在4.5 nm左右的TiO2颗粒负载在碳纳米管表面,使其同时具有高容量、高倍率性能及高稳定性特点[55]。需要指出的是,金属氧化物/碳纳米管复合物的微观结构对其电化学性能具有显著影响。以MnO2/碳纳米管复合电极材料为例,Yang等[56]采用水热的方式在碳纳米管表面负载了MnO2,并获得了210 mA·h/g左右的可逆充放电容量。通过改变复合物中MnO2材料的形态,可在无序碳纳米管表面通过水热的方式负载片状的MnO2,大幅提高了MnO2/碳纳米管复合材料的性能,获得800 mA·h/g左右的可逆容量[57]。通过进一步优化复合材料的结构,Reddy研究组[58]以阳极氧化铝为模板,通过模板法获得了CNT@MnO2同轴纳米管阵列的结构,如图4所示。该结构通过碳纳米管阵列形态避免了电极内大量接触电阻产生,提高了导电率;具有均匀孔道,提高了锂离子扩散效率;通过MnO2的均匀负载提高了活性材料的利用率。这些特征使该材料获得了1000 mA·h/g以上的可逆容量。
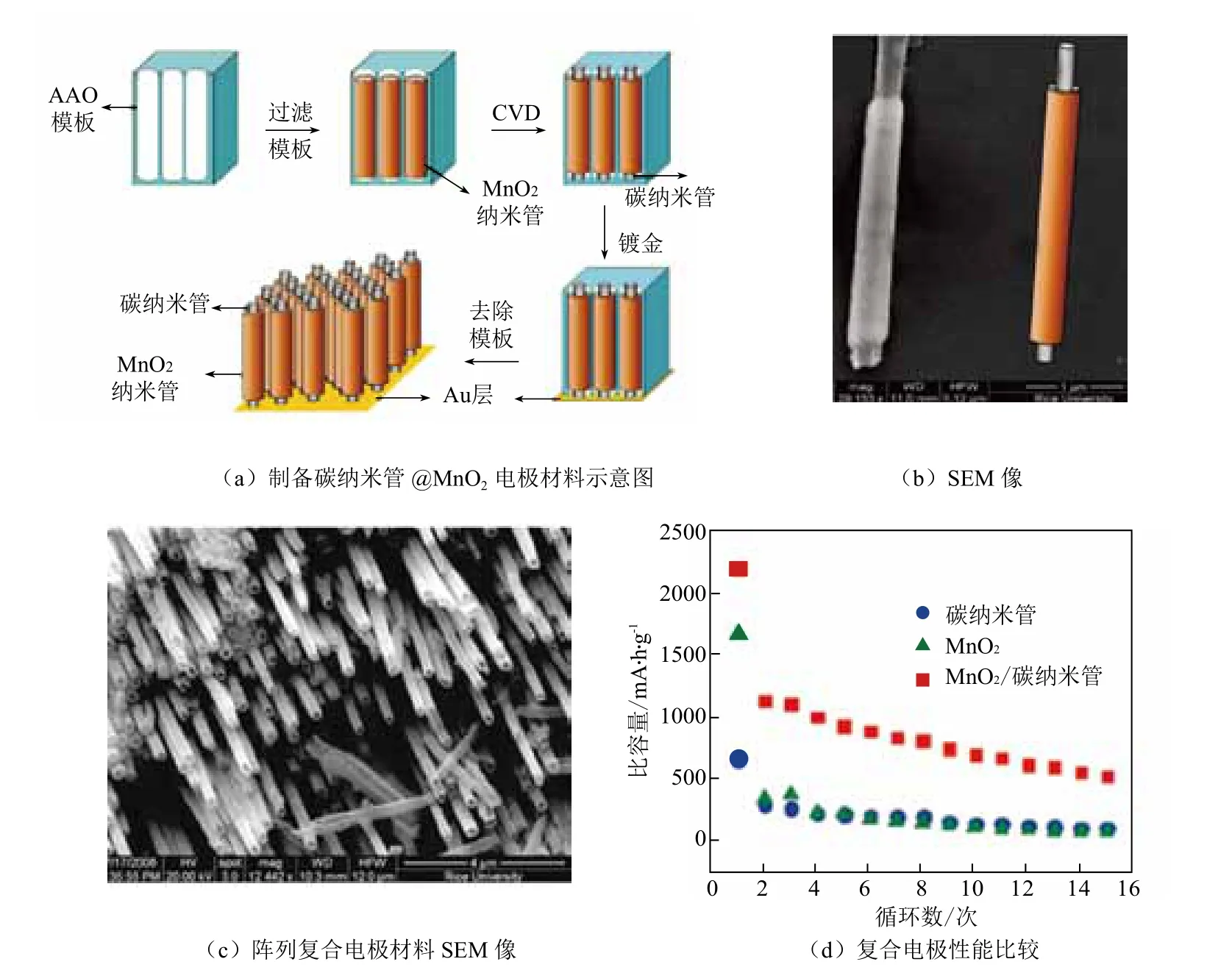
图4 碳纳米管@MnO2同轴复合电极材料结构及其电化学性能Fig. 4 The structure and electrochemical performance of MnO2/CNT hybrid coaxial nanotube arrays
石墨烯材料与金属氧化物也可形成结构丰富的复合电极材料。Honma等[59]将rGO与水解获得的SnO2颗粒在乙二醇溶液中混合,使其自组装形成SnO2/rGO复合物。在充放电过程中,氧化锡和石墨烯材料均可储锂;同时,石墨烯三维网络结构不仅提高了电极材料的整体导电性,也为SnO2充放电提供了形变的空间,使其在近300%的充放电体积变化率下仍能避免粉化,保持其储锂活性。与纯SnO2颗粒或石墨烯、石墨材料相比,SnO2/rGO复合物体现出更高的容量(810 mA·h/g)以及更高的循环稳定性(30个循环后容量保留率70%);此外,在SnO2/石墨烯复合材料的制备过程中,复合与还原过程的先后顺序也会对复合材料的电化学性能产生影响[60]。利用石墨烯的二维片状结构,也可以构造金属氧化物@石墨烯的核壳结构以获得高性能电极材料。例如,可利用静电相互作用力进行石墨烯-纳米颗粒组装,即通过溶液中氧化石墨烯带负电荷的特性,采用氨丙基三甲氧基硅烷对金属氧化物纳米颗粒进行修饰,使其表面带有正电荷;在静电力作用下,两者自组装形成氧化石墨烯包覆的纳米金属氧化物颗粒结构;通过随后进行的化学还原即可获得金属氧化物颗粒@石墨烯的核壳结构[61],如图5所示。此类结构能抑制活性纳米颗粒的聚并,抑制纳米颗粒体积变化带来的粉化等效应,同时也在电极材料中构建了一个导电网络。以Co3O4为例,通过此方法获得的Co3O4@石墨烯材料具有1100 mA·h/g以上的可逆储锂容量,在130个循环后仍具有1000 mA·h/g以上的容量,具有较优的循环稳定性。石墨烯包覆的Fe3O4纳米颗粒在作为锂离子电池负极材料时也呈现更优的性能,在低电流密度(35 mA/g)下可逆容量达到1026 mA·h/g,在高电流密度(700 mA/g)下仍具有580 mA·h/g的容量[62]。

图5 构建纳米金属氧化物颗粒@石墨烯结构的方法示意图Fig. 5 Schematic showing the fabrication of grapheneencapsulated metal oxide
大部分高容量负极材料均存在导电性较低及充放电过程体积变化率过大等问题,而纳米石墨化碳的低维度结构特点、极高的导电率以及优异的力学性质可以大幅改善复合负极材料的电化学性能;同时,具有较高比表面积的纳米石墨化碳在负极材料中的添加也会增加负极材料的不可逆容量。如何通过结构的设计和制备技术的发展制备具有低比表面积网络结构的纳米石墨化碳是解决这一问题的核心之一,进一步发展纳米石墨化碳的多级结构控制技术及工程化放大技术是重要的科学与工程问题。
2 纳米石墨化碳在正极材料中的应用
纳米石墨化碳在正极材料中起到的主要作用是作为力学增强及导电添加剂,以提高其功率及循环性。通常加入的较为常用的导电剂为导电炭黑,从导电网络结构角度分析,高长径比的一维碳纳米管及二维石墨烯可在低添加量下形成渗流网络,使电极材料具有较高的导电性,同时其力学性能也可以在一定程度上避免活性材料从集流体剥离带来的容量衰减。研究表明[23],纳米石墨化碳在钴酸锂、锰酸锂、磷酸铁锂等正极材料中均可起到提高电极性能的作用。以磷酸铁锂正极材料为例,磷酸铁锂是目前常用的锂离子电池正极材料之一,具有良好的循环稳定性和较高的理论储锂容量,而磷酸铁锂材料作为正极材料主要的劣势之一就是其极低的本征电子导电率(10-9S/cm)[63]。通过与导电性良好的纳米石墨化碳复合可以有效利用碳材料构建导电网络,从而获得高性能复合电极材料。
通过磷酸铁锂可实现电极材料性能的提升。通过对磷酸铁锂和石墨烯材料进行共沉淀,Ding等[65]获得了两者的复合材料。尽管其中石墨烯的含量仅为1.5%,但复合材料仍在0.2 C和10 C的电流密度下具有高达160 mA·h/g和109 mA·h/g的容量。通过在磷酸铁锂水热制备过程中原位加入石墨烯可在石墨烯表面实现磷酸铁锂纳米颗粒的生长,在复合物中石墨烯含量8%的情况下,可将放电容量在0.1 C下自120 mA·h/g提高至160 mA·h/g[66]。通过形成磷酸铁锂颗粒的石墨烯包覆结构,同样也可以显著提升电极材料的电化学性能。Zhou等[64]通过喷雾干燥的方法,获得微米级别的磷酸铁锂/石墨烯复合物颗粒。该颗粒中,石墨烯材料均匀地包覆在磷酸铁锂纳米颗粒表面,并在磷酸铁锂颗粒间形成了三维导电网络,使该正极材料具有优良的循环稳定性和高功率性能,如图6所示,该材料在20 C充电、60 C放电的情况下仍具有70 mA·h/g的容量,体现出较优的高功率性能;同时,该材料在10 C充电、20 C放电的情况下,1000次循环仅有5%的容量衰减,稳定性方面的表现也可圈可点,这与颗粒内部石墨烯包覆带来的导电性及力学稳定性的提高是密不可分的。

图6 磷酸铁锂石墨烯复合电极材料制备过程示意图及材料结构Fig. 6 The synthesis process and the structures of microscale structure of LiFePO4/graphene composite
碳纳米管可用以取代正极材料中导电炭黑等导电添加剂,更高效地实现导电网络的构建。通过对比炭黑和碳纳米管在磷酸铁锂正极材料中的应用,有数据显示[67]采用多壁碳纳米管替代导电炭黑可提高电池的初始容量(146~155 mA·h/g),提高电池的循环稳定性(50个循环后容量保持率从90%提高至95%),并降低电池体系的阻抗。利用纳米聚团流化床技术大批量生产的多壁碳纳米管,Cnano公司等将其分散成N-甲基吡咯烷酮及水相单分散的CNTs浆液,与锂电池的多种正极材料混合,制成了碳纳米管复合正极材料,使正极材料的容量、循环稳定性、功率密度等与导电炭黑、气相生长碳纤维等导电添加剂相比均有大幅度提高。采用碳纳米管导电剂不仅可将导电剂添加量降低至0.6%,同时依靠碳纳米管的高导热性,电池在高功率工况下的升温也大大减少。目前该技术已在动力电池、消费类电子产品的电池中得到大规模应用。
碳纳米管还能与正极材料LiCoO2复合实现柔性电极材料的开发[68](图7),将超顺排碳纳米管与正极材料颗粒复合成膜,可利用碳纳米管之间的搭接获得自支撑的碳纳米管膜复合电极。使用此类碳纳米管复合电极可以简化电极制备流程,避免集流体和黏结剂等的使用,从而进一步提高电极材料中活性物质的含量,有利于高能量密度电极材料的开发。同时,长碳纳米管所构成的高效导电网络大幅提高了电极材料的导电性(比炭黑导电添加剂提高3个数量级),使其在高充放电电流下仍能保持高容量。碳纳米管膜电极优良的柔性特征以及力学强度也为柔性电池的开发提供了可能。V2O5等正极材料也可以通过水热的方式与碳纳米管复合并形成柔性电极[69]。
3 结 语
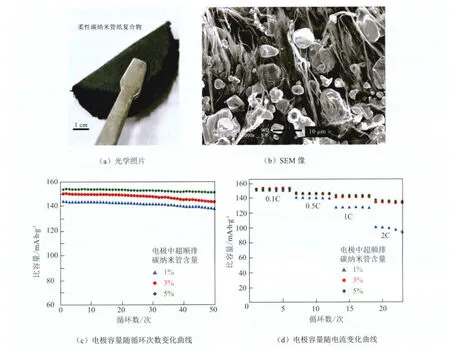
图7 柔性碳纳米管纸/LiCoO2复合电极结构及电化学性能Fig. 7 The structure and electrochemical performance of LiCoO2-super aligned CNT composite
具有石墨结构的炭材料在自20世纪90年代锂离子电池正式商业化以来,以其高电化学稳定性、导电性、力学性能等对其安全性及循环性提高起到了重要的作用,使锂离子电池技术在电池容量性能、功率性能、安全性、工业规模等方面都得到了长足的发展。随着近年来人们对高性能个人电子设备及电动汽车等设备的电源系统的要求不断提高,锂离子电池包括电极材料在内的各个组成部分仍需要不断优化、改良。同时,近20年来,纳米石墨结构碳(包括一维的碳纳米管及石墨烯等)无论在其概念、结构表征到制备应用等方面,在纳米领域均得到了长足的进步,其在电极材料的优化中可承担多种角色:①纳米石墨化碳具有与石墨材料类似的层状结构,可实现较高的储锂容量;②纳米石墨化碳具有优良的导电性能,可在电极材料中构建高效导电网络;③纳米石墨化碳的力学性质可使其用作电极材料的骨架结构,克服体积效应等带来的结构改变和容量衰减;④纳米石墨化碳材料甚至可以利用本身的低维度特征构建柔性自支持结构,为构建柔性电池等多功能电池带来可能。利用以上特点,已有众多研究组开发了基于纳米石墨化碳的高性能锂离子电池电极材料,在许多方面大大超越了现有电极材料的性能级别,有望大幅推进锂离子电池性能的提高。
与此同时,也需要注意到纳米石墨化碳电极材料的开发仍不完善,在许多方面仍存在一些显著的缺陷。例如,纳米材料本身就具有低密度的特点,具有大量孔道结构的纳米石墨化碳材料大幅提升了活性材料与电解液的接触面积,从而使其具有单位质量下极高的容量和功率密度,但此类杂合物在使用过程中往往会遇到低体积性能的困扰;纳米石墨化碳具有极高的比表面积,作为锂离子电池电极材料尤其是负极材料时会消耗大量锂离子,从而降低电池系统的总体性能;纳米石墨化碳材料与活性物质之间的组装方式和调控手段仍有限,难以实现结构精确控制的自组装过程等。随着对纳米石墨化碳研究的不断深入,其在锂离子电池中的应用仍具有广阔的空间。例如,通过进一步了解纳米石墨化碳的储锂机制,可控制备出具有合理结构的碳材料,在利用缺陷、边缘等储锂位点的同时控制不可逆储锂容量,有望实现高容量电极材料的制备。通过对纳米石墨化碳复合材料制备手段的开发,实现纳米尺度上活性材料分散性的精确控制,更好地结合骨架碳材料与高容量活性材料的优势,有望进一步提升高容量复合电极材料的制备水平。基于各向异性纳米石墨化碳之间通过非共价键连接时会带来较大的电阻及热阻,并影响其力学性能的问题,如何通过共价键连接实现三维多级结构纳米石墨化碳的构建,在科学及工程上仍是待攻克的前沿问题,相信随着纳米石墨化碳材料科学的不断发展,此类共价连接的纳米石墨化碳三维结构的可控制备将会得到解决,其在锂离子电池电极材料中的应用空间也将得到进一步拓展。由此可见,以目前石墨化碳在锂离子电池中的应用为基础,进一步开展机理研究和过程研究将对新一代高能量、高功率锂离子电池的开发具有重要推动作用。
[1]Armand M, Tarascon J M. Building better batteries[J].Nature,2008, 451(7179):652-657.
[2]Tarascon J M, Armand M. Issues and challenges facing rechargeable lithium batteries[J].Nature, 2001, 414(6861):359-367.
[3]Nishide H, Oyaizu K. Materials science—Toward flexible batteries[J].Science, 2008, 319(5864):737-738.
[4]稻垣道夫, 康飞宇. 炭材料科学与工程:从基础到应用[M]. 北京:清华大学出版社, 2006.
[5]Endo M, Kim Y A, Hayashi T, et al. Vapor-grown carbon fibers(VGCFs): Basic properties and their battery applications [J].Carbon, 2001, 39(9):1287-1297.
[6]Doeff M M, Hu Y Q, McLarnon F, et al. Effect of surface carbon structure on the electrochemical performance of LiFePO4[J].Electrochemical and Solid State Letters, 2003, 6(10):A207-209.
[7]Rao C N, Sood A K, Subrahmanyam K S, et al. Graphene:The new two-dimensional nanomaterial[J].Angewandte Chemie International Edition, 2009, 48(42):7752-7777.
[8]Dai H J. Carbon nanotubes: Opportunities and challenges[J].Surface Science, 2002, 500(1-3):218-241.
[9]Lee C, Wei X D, Kysar J W, et al. Measurement of the elastic properties and intrinsic strength of monolayer graphene[J].Science,2008, 321(5887):385-388.
[10]Balandin A A, Ghosh S, Bao W Z, et al. Superior thermal conductivity of single-layer graphene[J].Nano Letters, 2008, 8(3):902-907.
[11]Chen J H, Jang C, Xiao S D, et al. Intrinsic and extrinsic performance limits of graphene devices on SiO2[J].Nature Nanotechnology, 2008, 3(4):206-209.
[12]Terrones M. Science and technology of the twenty-first century:Synthesis, properties and applications of carbon nanotubes[J].Annual Review of Materials Research, 2003, 33:419-501.
[13]Zhang R, Wen Q, Qian W, et al. Superstrong ultralong carbon nanotubes for mechanical energy storage[J].Advanced Materials,2011, 23(30):3387-3391.
[14]Soh H T, Quate C F, Morpurgo A F, et al. Integrated nanotube circuits:Controlled growth and ohmic contacting of single-walled carbon nanotubes[J].Applied Physics Letters, 1999, 75(5):627-629.
[15]Kreupl F, Graham A P, Duesberg G, et al. Carbon nanotubes in interconnect applications[J].Microelectronic Engineering, 2002, 64(1):399-408.
[16]Berber S, Kwon Y K, Tomanek D. Unusually high thermal conductivity of carbon nanotubes[J].Physical Review Letters, 2000,84(20):4613-4616.
[17]Arenal R, Stephan O,Kociak M, et al. Electron energy loss spectroscopy measurement of the optical gaps on individual boron nitride single-walled and multiwalled nanotubes[J].Physical Review Letters, 2005, 95(12):127601.
[18]Kaskhedikar N A,Maier J. Lithium storage in carbon nanostructures[J].Advanced Materials, 2009, 21(25-26):2664-2680.
[19]Casas C, Li W. A review of application of carbon nanotubes for lithium ion battery anode material[J].Journal of Power Sources,2012, 208:74-85.
[20]Shimoda H, Gao B, Tang X, et al. Lithium intercalation into opened single-wall carbon nanotubes: Storage capacity and electronic properties[J].Physical Review Letters, 2001, 88(1):015502.
[21]Gao B, Bower C, Lorentzen J D, et al. Enhanced saturation lithium composition in ball-milled single-walled carbon nanotubes[J].Chemical Physics Letters, 2000, 327(1):69-75.
[22]Frackowiak E, Gautier S, Gaucher H, et al. Electrochemical storage of lithium in multiwalled carbon nanotubes[J].Carbon,1999, 37(1):61-69.
[23]Liu X M, Huang Z D, Oh S W, et al. Carbon nanotube (CNT)-based composites as electrode material for rechargeable Li-ion batteries:A review[J].Composites Science and Technology, 2012, 72(2):121-144.
[24]Shin W H, Jeong H M, Kim B G, et al. Nitrogen-doped multiwall carbon nanotubes for lithium storage with extremely high capacity[J].Nano Letters, 2012, 12(5):2283-2288.
[25]Zhang Q,Huang J Q, Zhao M Q, et al. Carbon nanotube mass production: Principles and processes[J].Chem. Sus. Chem. 2011, 4(7):864-889.
[26]Liu Y H, Xue J S, Zheng T, et al. Mechanism of lithium insertion in hard carbons prepared by pyrolysis of epoxy resins[J].Carbon,1996, 34(2):193-200.
[27]Zheng T, Xing W, Dahn J. Carbons prepared from coals for anodes of lithium-ion cells[J].Carbon, 1996, 34(12):1501-1507.
[28]Yoo E,Kim J, Hosono E, et al. Large reversible Li storage of graphene nanosheet families for use in rechargeable lithium ion batteries[J].Nano Letters, 2008, 8(8):2277-2282.
[29]Wang C, Li D, Too C O, et al. Electrochemical properties of graphene paper electrodes used in lithium batteries[J].Chemistry ofMaterials, 2009, 21(13):2604-2606.
[30]Abouimrane A, Compton O C, Amine K, et al. Non-annealed graphene paper as a binder-free anode for lithium-ion batteries[J].Journal of Physical Chemistry, 2010, 114(29):12800-12804.
[31]Guo P, Song H, Chen X. Electrochemical performance of graphene nanosheets as anode material for lithium-ion batteries[J].Electrochemistry Communications, 2009, 11(6):1320-1324.
[32]Fan Z J, Yan J, Wei T, et al. Nanographene-constructed carbon nanofibers grown on graphene sheets by chemical vapor deposition:High-performance anode materials for lithium ion batteries[J].ACS Nano, 2011, 5(4):2787-2794.
[33]Park C M, Kim J H, Kim H, et al. Li-alloy based anode materials for Li secondary batteries[J].Chemical Society Reviews, 2010, 39(8):3115-3141.
[34]Kasavajjula U, Wang C, Appleby A J. Nano- and bulk-silicon-based insertion anodes for lithium-ion secondary cells[J].Journal of Power Sources, 2007, 163(2):1003-1039.
[35]Su L, Jing Y, Zhou Z. Li ion battery materials with core-shell nanostructures[J].Nanoscale, 2011, 3(10):3967-3983.
[36]Zhang W J. A review of the electrochemical performance of alloy anodes for lithium-ion batteries[J].Journal of Power Sources, 2011,196(1):13-24.
[37]Chan C K, Peng H, Liu G, et al. High-performance lithium battery anodes using silicon nanowires[J].Nature Nanotechnology, 2008, 3(1):31-35.
[38]Cui L F, Hu L, Choi J W, et al. Light-weight free-standing carbon nanotube-silicon films for anodes of lithium ion batteries[J].ACS Nano, 2010, 4(7):3671-3678.
[39]Cui L F, Yang Y, Hsu C M, et al. Carbon-silicon core-shell nanowires as high capacity electrode for lithium ion batteries[J].Nano Letters, 2009, 9(9):3370-3374.
[40]Zhou Z, Xu Y, Hojamberdiev M, et al. Enhanced cycling performance of silicon/disordered carbon/carbon nanotubes composite for lithium ion batteries[J].Journal of Alloys and Compounds, 2010,507(1):309-311.
[41]Zhang Y, Zhang X G, Zhang H L, et al. Composite anode material of silicon/graphite/carbon nanotubes for Li-ion batteries[J].Electrochimica Acta, 2006, 51(23):4994-5000.
[42]Eom J Y, Park J W, Kwon H S, et al. Electrochemical insertion of lithium into multiwalled carbon nanotube/silicon composites produced by ballmilling[J].Journal of the Electrochemical Society, 2006, 153(9):A1678.
[43]Wang W, Kumta P N. Nanostructured hybrid silicon/carbon nanotube heterostructures: Reversible high-capacity lithium-ion anodes[J].ACS Nano, 2010, 4(4):2233-2241.
[44]Gohier A, Laik B, Kim K H, et al. High-rate capability silicon decorated vertically aligned carbon nanotubes for Li-ion batteries[J].Advanced Materials, 2012, 24(19):2592-2597.
[45]Evanoff K, Khan J, Balandin A A, et al. Towards ultrathick battery electrodes: Aligned carbon nanotube-enabled architecture[J].Advanced Materials, 2012, 24(4):533-539.
[46]Tao H C, Fan L Z, Mei Y, et al. Self-supporting Si/reduced graphene oxide nanocomposite films as anode for lithium ion batteries[J].Electrochemistry Communications, 2011, 13(12):1332-1335.
[47]Lee J K, Smith K B, Hayner C M, et al. Silicon nanoparticlesgraphene paper composites for Li ion battery anodes[J].Chemical Communications, 2010, 46(12):2025-2027.
[48]Zhao X, Hayner C M, Kung M C, et al. In-plane vacancyenabled high-power Si-graphene composite electrode for lithium-ion batteries[J].Advanced Energy Materials, 2011, 1(6):1079-1084.
[49]Evanoff K, Magasinski A, Yang J, et al. Nanosilicon-coated graphene granules as anodes for Li-ion batteries[J].Advanced Energy Materials, 2011, 1(4):495-498.
[50]Huang J Y, Zhong L, Wang C M, et al. In situ observation of the electrochemical lithiation of a single SnO2nanowire electrode[J].Science, 2010, 330(6010):1515-1520.
[51]Huang H, Zhang W, Gan X, et al. Electrochemical investigation of TiO2/carbon nanotubes nanocomposite as anode materials for lithiumion batteries[J].Materials Letters, 2007, 61(1):296-299.
[52]Zhang H X, Feng C, Zhai Y C, et al. Cross-stacked carbon nanotube sheets uniformly loaded with SnO2nanoparticles:A novel binder-free and high-capacity anode material for lithium-ion batteries[J].Advanced Materials, 2009, 21(22):2299-2304.
[53]Zhang H, Cao G, Wang Z, et al. Growth of manganese oxide nanoflowers on vertically-aligned carbon nanotube arrays for high-rate electrochemical capacitive energy storage[J].Nano Letters, 2008, 8(9):2664-2668.
[54]Ban C, Wu Z, Gillaspie D T, et al. Nanostructured Fe3O4/SWNT electrode: Binder-free and high-rate li-ion anode[J].Advanced Materials, 2010, 22(20):E145-149.
[55]Chen Z, Zhang D, Wang X, et al. High-performance energystorage architectures from carbon nanotubes and nanocrystal building blocks[J].Advanced Materials, 2012, 24(15):2030-2036.
[56]Yue H,Huang X, Yang Y. Preparation and electrochemical performance of manganese oxide/carbon nanotubes composite as a cathode for rechargeable lithium battery with high power density[J].Materials Letters, 2008, 62(19):3388-3390.
[57]Xia H,Lai M, Lu L. Nanoflaky MnO2/carbon nanotube nanocomposites as anode materials for lithium-ion batteries[J].Journal of Materials Chemistry, 2010, 20(33):6896-6902.
[58]Reddy A L, Shaijumon M M, Gowda S R, et al. Coaxial MnO2/carbon nanotube array electrodes for high-performance lithium batteries[J].Nano Letters, 2009, 9(3):1002-1006.
[59]Paek S M, Yoo E J, Honma I. Enhanced cyclic performance and lithium storage capacity of SnO2/graphene nanoporous electrodes with three-dimensionally delaminated flexible structure[J].Nano Letters,2008, 9(1):72-75.
[60]Chen C M, Zhang Q, Huang J Q, et al. Chemically derived graphene-metal oxide hybrids as electrodes for electrochemical energy storage:Pre-graphenization or post-graphenization[J].Journal of Materials Chemistry, 2012, 22(28):13947.
[61]Yang S, Feng X, Ivanovici S, et al. Fabrication of grapheneencapsulated oxide nanoparticles: Towards high-performance anode materials for lithium storage[J].Angewandte Chemie International Edition, 2010, 49(45):8408-8411.
[62]Zhou G M, Wang D W, Li F, et al. Graphene-wrapped Fe3O4anode material with improved reversible capacity and cyclic stability for lithium ion batteries[J].Chemistry of Materials, 2010, 22(18):5306-5313.
[63]Chung S Y, Bloking J T, Chiang Y M. Electronically conductive phospho-olivines as lithium storage electrodes[J].Nature Materials,2002, 1(2):123-128.
[64]Zhou X, Wang F, Zhu Y, et al. Graphene modified LiFePO4cathode materials for high power lithium ion batteries[J].Journal of Materials Chemistry, 2011, 21(10):3353-3358.
[65]Ding Y, Jiang Y, Xu F, et al. Preparation of nano-structured LiFePO4/graphene composites by co-precipitation method[J].Electrochemistry Communications, 2010, 12(1):10-13.
[66]Wang L, Wang H, Liu Z, et al. A facile method of preparing mixed conducting LiFePO4/graphene composites for lithium-ion batteries [J].Solid State Ionics, 2010, 181(37-38):1685-1689.
[67]Li X, Kang F, Bai X, et al. A novel network composite cathode of LiFePO4/multiwalled carbon nanotubes with high rate capability for lithium ion batteries[J].Electrochemistry Communications, 2007, 9(4):663-666.
[68]Luo S, Wang K, Wang J, et al. Binder-free LiCoO2/carbon nanotube cathodes for high-performance lithium ion batteries[J].Advanced Materials, 2012, 24(17):2294-2298.
[69]Jia X L, Chen Z, Suwarnasarn A, et al. High-performance flexible lithium-ion electrodes based on robust network architecture[J].Energy& Environmental Science, 2012, 5(5):6845.
