注射用脂溶性维生素(I)细菌内毒素检查法研究
2012-05-12潘卫松周永标张讷敏
潘卫松,肖 瑛,周永标,张讷敏
(1.广州市药品检验所,广东 广州 510610;2.暨南大学 药学院,广东 广州 510632;3.暨南大学 中药药效物质基础及创新药物研究广东省高校重点实验室,广东 广州 510632)
注射用脂溶性维生素(I)是由维生素A棕榈酸酯、维生素D2、E、K1等多种维生素成分制成的无菌冻干粉针,临床上用于各种内、外科手术、严重传染性疾病、昏迷等症的肠外维生素补充剂,是各种外科手术后必用的药物。我所承担了其国家评价性抽检的任务。其现行标准共有3个,分别为国家食品药品监督管理局标准(试行)YBH09722008,国家食品药品监督管理局标准(试行)YBH05222009,国家食品药品监督管理局标准YBH38402005,其中,前两个标准都是使用细菌内毒素检查法对热原进行控制,限度均为10EU/瓶,最后一个标准则采用了家兔热原检查法对热原进行控制。我们按2010年版《中国药典》(二部)“细菌内毒素检查法”对实施国家食品药品监督管理局标准YBH38402005的本品种进行了干扰试验,以考察对其进行细菌内毒素检查的可行性,并提出将其限度提高到5EU/瓶。现将结果报道如下。
1 仪器与试药
SUB14恒温水浴(英国GRANT公司);MSI旋涡混合器(广州IKA公司)。
细菌内毒素工作标准品(规格:每支160EU,批号:150601-201174;)及细菌内毒素检查用水(BET水,规格:每支50mL,批号:1105060)均购自中国药品生物制品检定所;鲎试剂(TAL)A(湛江安度斯生物有限公司,规格:每支0.1mL,批号:1105101,灵敏度:0.25EU·mL-1);TAL B(厦门市鲎试剂实验厂有限公司,规格:每支0.1mL,批号:110603,灵敏度:0.25EU·mL-1;TAL C(湛江安度斯生物有限公司,规格:每支0.1mL,批号:1103242,灵敏度:0.06EU·mL-1);TAL D(厦门市鲎试剂实验厂有限公司,规格:每支0.1mL,批号:100915,灵敏度:0.06EU·mL-1;注射用脂溶性维生素(I)(规格:复方制剂,批号:110102(II)206,110201(II)57,101201(II)52,10100704,10050694,101202(II)174,110101(II)41,10100787,110201(II)150,10100731,10030389,110401(II)83,110202(II)33,110203(II)89,110201(II)73)。
2 方法与结果
2.1 细菌内毒素限值的确定
根据药品使用说明书和规格,注射用脂溶性维生素(I)细菌内毒素限值拟定为5EU/瓶。
2.2 鲎试剂灵敏度复核试验
按照2010年版《中国药典》(二部)附录细菌内毒素检查法规定,进行鲎试剂的标示灵敏度(λ)复核。结果见表1。

表1 鲎试剂灵敏度复核试验结果
由表1可见,2批鲎试剂经用细菌内毒素工作标准品检查,λc均在0.5λ~2.0λ之间,结果均符合规定。
2.3 预干扰试验
注射用脂溶性维生素(I)有效稀释浓度(MVC)的计算:根据公式MVC=λ/L,其中L为注射用脂溶性维生素(I)的细菌内毒素限值5EU/瓶,每瓶先加入2mL BET检查用水,溶解充分后,其限度可认为2.5EU/mL,λ为鲎试剂标示灵敏度,目前市售鲎试剂灵敏度λ通常在0.25~0.03EU/mL,则注射用脂溶性维生素(I)的对应有效稀释倍数为:
C0.25=2.5/0.25=10倍;C0.125=2.5/0.125=20倍;C0.06=2.5/0.06=40倍;C0.03=2.5/0.03=80倍
预干扰试验:
将上述系列浓度溶液记为NPC。同时在上述NPC液中加入细菌内毒素标准溶液,使每一浓度的试验液中均含有2λ浓度的细菌内毒素,记此系列溶液为PPC。取两个不同厂家的鲎试剂,分别与上述PPC和NPC进行反应,每一浓度重复两管,并设阳性和阴性对照。
由预干扰试验结果可以初步了解:两个厂家的鲎试剂对注射用脂溶性维生素(I)的细菌内毒素的试验结果在进行40倍稀释后均无干扰。
2.4 正式干扰试验
为了最终确认注射用脂溶性维生素(I)是否存在干扰因素的影响,笔者进行了正式干扰试验。
正式干扰试验:
取脂溶性维生素(I),先每瓶用2mlBET水溶解,再以BET水溶解,使其最终干扰试验稀释倍数为40倍,按2010年版《中国药典》二部附录中的“细菌内毒素检查供试品干扰试验项”进行试验,结果见表2。
由表2可知,注射用脂溶性维生素(I)在进行40倍稀释后Es/Et均在0.5~2.0范围之内,确认在40倍及以上稀释倍数时无干扰影响。
2.5 样品细菌内毒素检查
按2010年版《中国药典》细菌内毒素检查法,使用2批不同厂家的鲎试剂分别对样品进行细菌内毒素检查,并同时设立样品的自身阳性对照品,结果见表3。
3 讨论
由干扰预试验结果可以初步发现注射用脂溶性维生素(I)在40倍以上稀释倍数对两个厂家生产的鲎试剂均无干扰作用。正式干扰试验样品进行40倍稀释且用两个厂家的鲎试剂结果Es/Et均在0.5~2.0范围之内,确认在40倍以上稀释倍数时无干扰影响。
限值定为5EU/瓶。注射用脂溶性维生素(I)可适用细菌内毒素检查法,鲎试剂灵敏度应使用0.06EU/mL。

表2 样品(40倍稀释)干扰试验结果

表3 样品细菌内毒素检查结果
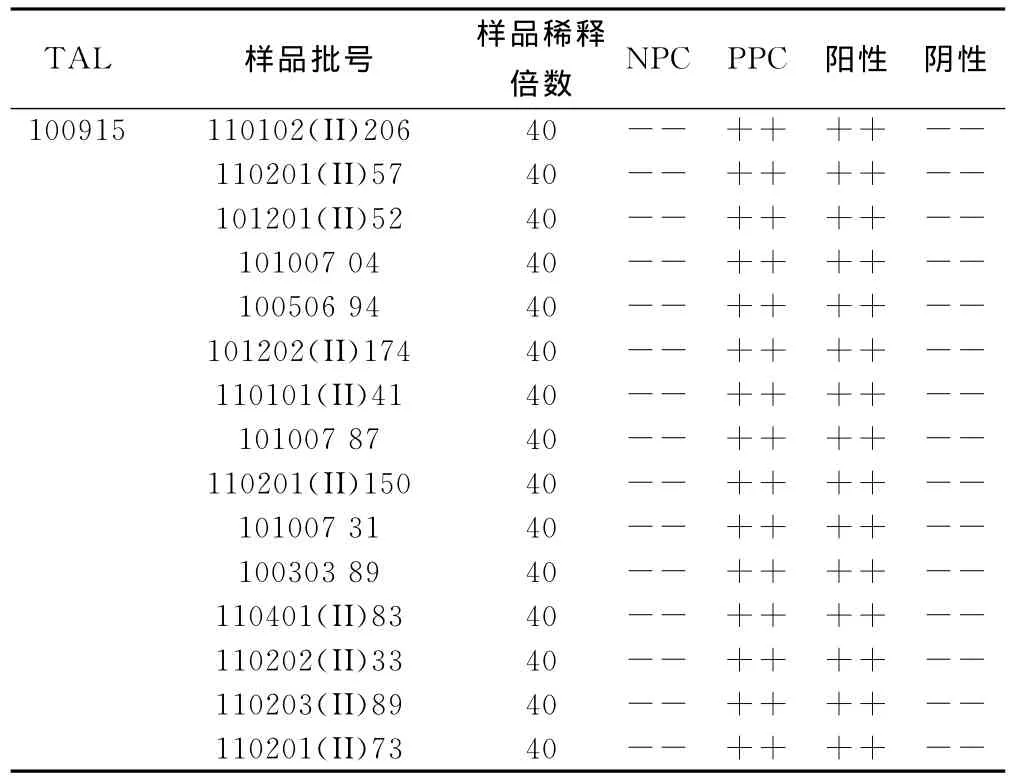
续表3
[1]国家药典委员会.中华人民共和国药典(二部)[S].2010.北京:中国医药科技出版社,2010:附录99.
[2]潘卫松,肖瑛.透明质酸钠注射液细菌内毒素检查法的研究[J].中国医药导报,2009,20(6):45-7.
[3]潘卫松,肖瑛,潘建明.荧光素钠注射液细菌内毒素检查法的研究[J].中国药房,2009,20(13):1010-12.
[4]江红,潘卫松,肖 瑛.对口岸药品检验所进口药品留样时间的思考[J].中国药事,2011,25(6):582-3.
