氨基酸型两性表面活性剂的合成进展
2012-05-07孔玉明任朝华刘国霖谭良柏
孔玉明,罗 跃,任朝华,刘国霖,谭良柏
(1.长江大学化学与环境工程学院,湖北 荆州 434023;2.长江大学石油工程学院,湖北 荆州 434023)
1 引言
随着科学技术的发展,表面活性剂新品种不断出现,研发高质量的多功能环境友好型表面活性剂已成为表面活性剂工业的主要方向。两性表面活性剂是指具有两个或多个官能团的表面活性剂,它在水溶液中能被电离,因介质的条件不同,可以呈现阴离子表面活性剂特性或阳离子表面活性剂特性[1]。近年来,氨基酸型两性表面活性剂以其安全性、温和性、生物降解性和优良的表面活性,受到人们的重视。此外,氨基酸型两性表面活性剂还具有一些独特的功能,其分子中包含氨基酸骨架,既有氨基又有羧基,可引入不同碳原子数目的酰基、烷氧基;其自身的烃基、氨基、羧基的数目也可不同。因此,氨基酸型两性表面活性剂的表面活性可从多方面得到调节,应用广泛[2]。
20世纪40年代氨基酸型两性表面活性剂在德国首次被商品化。我国目前对氨基酸型两性表面活性剂的报道很少,其产量只占两性表面活性剂总产量的2%左右[3]。因此,研究氨基酸型两性表面活性剂的合成方法十分重要。氨基酸本身就是两性物质,其分子中的阴离子为羧基、阳离子为铵盐,因而合成氨基酸型两性表面活性剂就是向氨基酸分子上引入疏水性的烃基,烃基既可引在N原子上也可引在C原子上。作者在此综述了氨基酸型两性表面活性剂的合成进展。
2 氨基酸型两性表面活性剂的合成
2.1 羧酸基氨基酸
2.1.1N-烷基-β-丙氨酸的合成
(1)丙烯酸甲酯法是最常用的N-烷基-β-丙氨酸化学合成方法,较为成熟,如美国General Mill公司的Deriphat系列产品就是由此方法制得[4]。反应式如下:

RNHCH2CH2COOCH3+NaOH
实验室研究中,采用C12~C18的脂肪胺与丙烯酸甲酯反应,然后将生成的产物放入烧杯后置于沸水水浴中,一边搅拌一边慢慢加入与脂肪胺摩尔数相同的氢氧化钠水溶液进行皂化反应得到产品。
(2)丙烯腈法是我国研究出的合成路线,也属于化学合成方法[5]。反应式如下:

RNHCH2CH2CN+NaOH+H2O
RNHCH2CH2COONa+HCl
此方法以廉价的丙烯腈代替价格较高的丙烯酸甲酯与脂肪胺作用,生产成本较低,国内外研究不多。赵晓东等[6]用丙烯腈法合成N-烷基-β-丙氨酸型表面活性剂,并对其起泡性能进行了研究。结果发现,其在pH=2~6.5范围内起泡性能较差,在pH>8时起泡能力强、稳定性好,受温度、体系氯化钠浓度和少量钙离子的影响较小[6,7]。
(3)其它方法合成N-烷基-β-丙氨酸。如丙烯酸法是脂肪胺与丙烯酸在浑浊溶液中进行加成反应;β-丙内酯法[8]是脂肪胺与β-丙内酯反应;胺类与醛类物质反应;脂肪胺与β-溴取代羧酸反应等[9]。这些方法文献报道较少,具体的工艺还需要进一步的研究。
2.1.2N-酰基氨基酸的合成
(1)化学合成法
化学合成法视原料不同而有不同的工艺路线,如脂肪酰氯与氨基酸反应工艺、脂肪酸酐与氨基酸盐的酰化反应工艺、脂肪腈水解酰化反应工艺、酰胺羰基化反应工艺、脂肪酸与氨基酸盐反应工艺等[10]。
目前工业应用得最多的N-酰基氨基酸制备方法是肖顿-鲍曼(Schotten-Baunmann)缩合法,也就是脂肪酰氯与氨基酸反应工艺,脂肪酰氯和氨基酸在碱性水溶液或其它有机溶剂中一次反应制得N-酰基氨基酸盐,然后经无机酸中和、分离,得到N-酰基氨基酸粗品,再加碱中和,得到较纯的N-酰基氨基酸盐[11]。
肖顿-鲍曼法工艺包含酰化、缩合、酸化、成盐4个步骤,反应式如下(RCOOH为长链脂肪酸,以肌氨酸为例):
酰化:

缩合:

酸化:
成盐:
肖顿-鲍曼工艺大都采用亲水性溶剂水-丙酮作为缩合反应的溶剂,丙酮自身的缩合反应会产生有臭味的物质,在后期分离中很难除尽。虽然此方法比较成熟,但成本仍较高,对环境也造成一定影响,还需要进一步改进。
脂肪酸酐与氨基酸盐的酰化反应工艺由Thomnas等在20世纪60年代提出,是在不断搅动的水溶液中,在酸酐的熔点之上(不超过100 ℃)进行酸酐与氨基酸盐的反应。该反应不需要催化剂,也不需要控制水量,但需要消耗大量的脂肪酸酐,导致成本高、分离困难,因此并未用于大规模工业生产[12]。反应式如下:

NaOOCCH2CH2NHOCCH2CH2COONa
脂肪腈水解酰化反应工艺在1955年提出,反应产率和选择性大于95%,但由于该法设备要求高,且反应过程中有剧毒物质HCN和NaCN产生,操作和管理必须十分严格,也未能实现工业化应用[12]。反应式如下:

酰胺羰基化反应工艺是Beller等提出的,该法产率可达90%以上,原料成本低,不使用酰氯又无副产物,避免了对环境的污染,但需在高压、CO存在下反应,对设备要求高,且催化剂羰基钴络合物[Co2(CO)8]活性不高,不易实现工业化[13]。反应式如下:
脂肪酸与氨基酸盐反应工艺是乌布赖等提出的,在170~190 ℃和氮气保护下,由脂肪酸与氨基酸钠反应直接得到产品。研究发现,脂肪酸与氨基酸钠按摩尔比1∶1反应时产率仅为50%~55%,延长反应时间,产率并未提高;但多加一倍量的氨基酸,反应8~10 h后转化率提高到85%~90%,若加入两倍量的氨基酸,反应3~5 h后转化率即提高到90%[14]。此方法不使用三氯化磷、亚硫酰氯或羧酸氯化物,是在高温下直接将N-酰基氨基酸的碱金属盐与脂肪酸反应,同时不断除去反应所产生的水,从而得到N-酰基氨基酸,其流程简单、环境友好,但产品分离困难、对设备要求高,且成本因氨基酸过量而大幅提高。从环保的角度考虑,这一工艺仍值得进一步深入研究和完善。
(2)酶合成法
与化学合成法相比,酶合成法具有很多优点:反应条件温和(T<70 ℃,pH=7.0左右),能耗低、不使用强酸性物质、安全性高、选择性好、产物易分离纯化、可避免有毒有害副产物的产生、固定化酶可以重复使用等。酶合成法合成氨基酸型两性表面活性剂研究始于20世纪80年代中期,目前仍处于研究阶段,未见相关的工业化报道。
NOVO-Nordisk首次选用Candidaantarctica脂肪酶(Novozyme 435)来催化脂肪酸与氨基之间的酰胺化反应[15]以合成N-酰基氨基酸型两性表面活性剂,但经改进后其产率仍然很低。Soo等[16]以酶催化法由棕榈油合成N-氨基酸型两性表面活性剂,分别对Lipozyme、Novozyme 435、AK脂肪酶、C.rugosa脂肪酶和蛋白酶胰岛素的催化效果进行了对比,结果发现Lipozyme的催化效果最佳。李祖义等[17]直接将固定化酶如Lipozyme和Novozyme应用于L-赖氨酸和长链脂肪酸或其甲酯的酰胺化反应,经过数天反应,产物的收率只有2%~4%。
2.2 磺基氨基酸
目前有关磺基氨基酸型两性表面活性剂的合成报道不多,主要采用烷基胺与价格昂贵、毒性大、易水解的卤代烷基磺酸盐、磺酸内酯等原料合成[18~20],存在成本高、条件苛刻、不易操作、环境污染严重等缺陷,从而大大制约了磺基氨基酸型两性表面活性剂的发展。
利用带有苯环或聚氧乙烯酚醚的卤代物与牛磺酸或甲基牛磺酸反应可制得磺基氨基酸型两性表面活性剂。反应式如下:
高碳脂肪胺与溴代乙基磺酸钠加热可制备N-烷基氨乙基磺酸钠[21]。反应式如下:

汤芝平等[22]以烷基胺、甲醛和无机磺化剂(NaHSO3或Na2SO3)为原料,先经两步合成出酸式产物,再由固相成盐反应得到磺基氨基酸型两性表面活性剂,此法原料易得、条件温和、操作简便,有一定的工业化参考价值。反应式如下:
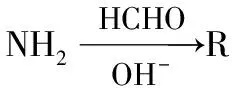

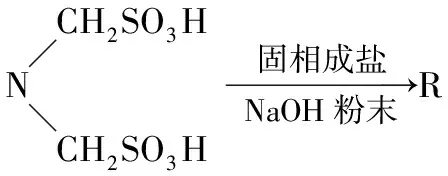
2.3 硫酸基氨基酸
硫酸基氨基酸型两性表面活性剂主要由含双键或羟基的脂肪胺进行硫酸化反应得到。反应式如下:
CH3(CH2)7CH=CH(CH2)7CONHCH2CH2NH2
2.4 磷酸基氨基酸
磷酸基氨基酸型两性表面活性剂主要是通过氧乙基桥接而成,尚处在实验室研究阶段[23]。
2.5 其它类型氨基酸
双子/孪子链型氨基酸表面活性剂的合成主要采用化学-酶合成法。有如下几种途径:一种是两种屏蔽性氨基酸衍生物与隔离链反应,最后引入两个疏水基,如Valivety等[24]首先利用Novozyme 435和Lipozyme脂肪酶催化合成相应的Bola两亲化合物,然后通过肖顿-鲍曼缩合反应合成双子/孪子链型氨基酸表面活性剂;另一种是氨基酸酰基化反应后得到的直链结构直接与具有不同功能的隔离链相连接,如Piera等[25]先采用鲜艳酰基氯化法制备精氨酸双子型表面活性剂直链结构,然后以其作为底物通过酶催化二聚反应得到精氨酸双子型表面活性剂。
3 结语
作为“工业味精”的氨基酸型两性表面活性剂,因在生产和生活领域中的独特功效,被认为是一种典型的品种多、用途广、需求量大的化工产品。其合成普遍采用的是化学合成方法,虽然相对比较成熟,但合成成本高,对环境也有一定的影响,还需进一步优化已有工艺、研发新工艺,以降低成本、消除环境污染。与此同时,酶合成法正在逐渐成熟,为实现酶合成法的工业化应用,必须解决酶的回收再利用以及酶活性的保持问题,同时深入研究反应条件,以提高产率。化学-酶合成方法是化学与酶两种方法的结合,不仅具有酶合成法的诸多优点,同时化学法的采用又在一定程度上解决了酶法产率低的问题,发展潜力很大。总之,在当前生物技术快速发展、社会追求可持续发展的大环境下,氨基酸型两性表面活性剂的合成必将朝着绿色化学的方法发展,酶法和化学-酶法有着广阔的发展应用前景。
参考文献:
[1] 穆瑞花,李仲谨,宋俊.两性表面活性剂在洗涤用品中的应用[J].中国洗涤用品工业,2006,(3):81-84.
[2] 李忠义,张淑绮.氨基酸系表面活性剂[J].辽宁化工,1990,(1):13-18.
[3] 方云.两性表面活性剂[M].北京:中国轻工业出版社,2001:15-17.
[4] Bluestein B R,Hilton C L.Amphoteric Surfactants[M].New York:Marcel Dekker Inc,1982:175-228.
[5] 田在龙.N-烷基-β-氨基丙酸型两性表面活性剂的研究[J].天然气化工,1991,13(2):4-7.
[6] 赵晓东,李巨峰,杨世光,等.N-烷基-β-氨基丙酸型两性表面活性剂的合成及其泡沫性能研究[J].日用化学工业,1998,12(6):9-13.
[7] 汪祖模,徐玉佩.两性表面活性剂[M].北京:中国轻工业出版社,1990:145-155.
[8] Rosen M J.Surfactants and Interfacial Phenomena(2 nd)[M].New York:John Wiley & Sons,1989:29-30.
[9] 兰云军,鲍利红.N-烷基-β-氨基丙酸的合成方法[J].皮革化工,2002,19(2):21-23.
[10] 陈丽,周美华.氨基酸型表面活性剂研究动态[J].精细与专用化学品,2004,12(19):7-11.
[11] 杨璐,高清来,李可彬.N-酰基氨基酸型表面活性剂合成及应用研究进展[J].化工技术与开发,2006,36(10):24-28.
[12] 陈燕妮,卢云,吴昊,等.N-酰基氨基酸系列表面活性剂的合成和应用[J].化学研究与应用,2001,13(2):192-195.
[13] 贝勒M.N-酰基-α-氨基酸衍生物的制备方法[P].CN 1 120 533A,1996-04-17.
[14] 乌布赖R P,高德特R P,乌德P D.碱金属氨基酸的制备[P].CN 961 945 613,1996-05-31.
[15] Godtfredsen S E,Bjoerkling F.Enzyme-catalyzed process for preparingN-acyl amino acids andN-acyl amino acid amides[P].WP 90/14 429,1990-11-29.
[16] Soo E L,Salleh A B,Basri M.Optimization of the enzyme-catalysed synthesis of amino acid-based surfactants from palm oil fractions[J].J Biosci Bioeng,2003,95(4):361-367.
[17] 李祖义,陈倩.酶法合成表面活性剂[J].工业微生物,2001,31(2):42-48.
[18] Klass D L.Preparation of quaternary ammonium betaine salts[P].USP 9 313 118,1964-04-28.
[19] Uirianu J Z.Alkali-resistant sulfobetaine amphoteric surfactant[P].JP 61 260 055,1986-11-18.
[20] Karaivanova M,Kodunova A,Pavlova S.Preparation of sodium salts ofN-sulfonic acids by sulfomethylation of nitro oligomers obtained from waste rubbers[J].Journal of Applied Polymer Science,2005,95(5):1002-1013.
[21] 郭秀兰,涂伟萍,何庭玉.两性表面活性剂的合成及其在化妆品中的应用[J].广西化工,2001,30(4):20-23.
[22] 汤芝平,薛永强,赵红,等.氨基磺酸系两性表面活性剂的一种新合成法[J].日用化学工业,2007,37(5):338-340.
[23] 徐亮,郭义,杨建洲.氨基酸型两性表面活性剂的合成及其在皮革工业中的应用[J].皮化材料,2006,(4):33-36.
[24] Valivety R,Gill I S,Vulfson E N.Application of enzymes to the synthesis of amino acid-based bola and gemini surfactants[J].Journal of Surfactants and Detergents,1998,1(2):177-185.
[25] Piera E,Infante M R,Clapés P.Chemo-enzymatic synthesis of arginine-based gemini surfactants[J].Biotechnology and Bioengineering,2000,70(3):323-331.
