间硝基苯胺水杨醛Schiff碱过渡金属配合物的合成及性质
2012-05-05陆兰青
李 艳,杨 剑,陆兰青,甘 红
(1.咸宁学院 化学与生命科学学院,湖北 咸宁 437000;2.襄州区第一中学,湖北 襄阳 441114;3.咸宁高中,湖北 咸宁 437000 ;4.白鹤中学,湖北 咸宁 437000)
Schiff碱是一类非常重要的含氮配体,具有一定的药理学和生理学活性[1~3]。由于Schiff碱在合成上具有很大的灵活性,与金属离子有很好的配位作用,使得Schiff碱及其配合物的研究十分广泛,特别是在其合成、结构与应用等方面都有引人注目的进展。在大量合成工作的基础上,人们发现许多以S、N或O、S、N为配位原子的配合物具有抗癌、抗病毒、杀菌等生物活性[4~6],近年来对这类化合物的研究已成为配位化学领域的热点。
荧光光谱是研究生物大分子与小分子、离子相互作用的重要手段。研究牛血清白蛋白(BSA)与小分子的作用,不仅可得到许多蛋白质的相关信息,且更易于了解有机小分子在生物体内的运输和分布情况,对于开发其在医药上的应用价值有非常重要的意义[7]。
作者在此合成了4种间硝基苯胺水杨醛Schiff碱过渡金属配合物,其结构经UV-Vis、IR、元素分析和摩尔电导率测定等表征,并研究了其光谱特征和抑菌活性。
1 实验
1.1 试剂和仪器
所用试剂均为国产(或进口)化学纯或分析纯。
U-2010型紫外分光光度计;F-4500型荧光分光光度计(带有恒温系统),日本日立;FTIR-8400S型傅立叶红外光谱仪,美国Perkin Elmer公司;PHS-25型酸度计;电导仪(CHI600C系列电化学分析仪/工作站),上海振华仪器公司;VarioEL Ⅲ型元素分析仪。
1.2 合成方法
1.2.1 合成路线(图1)

图1 配合物的合成路线
1.2.2 间硝基苯胺(Ⅰ)的制备
参照文献[8]制备。应用间二硝基苯在硫化钠、硫粉作用下得到黄色晶体间硝基苯胺,m.p.113~114 ℃(文献值[8]m.p.113~114 ℃)。
1.2.3 间硝基苯胺水杨醛Schiff碱(Ⅱ)的制备
于100 mL圆底烧瓶中加入0.6 g间硝基苯胺、8 mmol水杨醛、20 mL无水乙醇和8~10滴冰醋酸,低温加热回流3 h后,于回流冷凝管上端补加2 mmol水杨醛,继续回流3 h,冷却至室温,减压抽滤,即得到黄色针状固体间硝基苯胺水杨醛Schiff碱,产率70%。
1.2.4 配合物的制备
取间硝基苯胺水杨醛Schiff碱2.42 g加热溶于50 mL无水乙醇中,待其完全溶解后,缓慢滴加含有10 mmol Cu(NO3)2·3H2O的无水乙醇溶液,在65~70 ℃下搅拌回流3 h,再加入0.4 g NaOH,继续加热回流24 h,冷却、抽滤,得绿色固体间硝基苯胺水杨醛Schiff碱铜配合物,产率68%,m.p.300 ℃以上。
用相同的方法合成银、镍和锰的配合物。银配合物为灰色固体,产率69.5%;镍配合物为深棕色固体,产率66%;锰配合物为绿色固体,产率69.3%。
1.3 分析测试
1.3.1 配合物的元素分析、摩尔电导率
对各配合物进行元素分析测定。
将各配合物配成1.0×10-3mol·L-1的DMF溶液,于25 ℃测定摩尔电导率。
1.3.2 紫外可见吸收光谱
将配体及配合物配制成乙醇溶液,测试紫外可见吸收光谱。
1.3.3 红外光谱
将配体及配合物分别用KBr压片,在400~4000 cm-1范围内进行红外光谱分析。
1.3.4 荧光光谱
在2 cm的比色皿中加入2 mL 1×10-5mol·L-1的BSA溶液和不同量的各种配合物,得到各配合物与BSA之间不同物质的量之比的系列溶液。测定各溶液荧光光谱,选定激发和发射狭缝均为2.5 nm,激发波长为295 nm,绘制310~360 nm的荧光光谱。
1.3.5 抑菌实验
抑菌实验采用滤纸片法,实验菌株为金黄色葡萄球菌(S.aureus,革兰氏阳性菌)、大肠杆菌(E.coli,革兰氏阴性菌)、枯草芽孢杆菌(B.subtilis,革兰氏阳性菌)、绿脓杆菌(P.aeruginosa,革兰氏阴性菌)。稀释液为二甲亚砜,实验表明二甲亚砜对所选用的4种菌株无杀伤抑制作用。同时进行空白对照实验。
2 结果与讨论
2.1 元素分析、摩尔电导率和溶解性
配合物的元素分析和摩尔电导率见表1。

表1 配合物的元素分析和摩尔电导率
各配合物极易溶于DMSO、DMF,可溶于无水乙醇、甲醇、丙酮,但不溶于乙醚、石油醚。表1的摩尔电导率数值表明,各配合物均为非电解质。分别按化学式M(C13H9O3N2)2计算,其测定值与理论值基本相符。
2.2 紫外可见吸收光谱分析
配体(HL)和配合物(ML2)的紫外可见吸收光谱数据列于表2。

表2 配体和配合物的UV-Vis数据/nm
由表2可知,配体在紫外区222.0 nm、341.0 nm处出现2个吸收峰,分别归属为芳环、亚氨基的π-π*和n-π*跃迁产生的吸收峰;形成配合物后2个峰均发生位移,说明亚氨基上的氮原子与中心金属离子发生了配位作用。
2.3 红外光谱分析(表3)
由表3可知,配体在1641 cm-1处有强吸收峰,归属为C=N伸缩振动峰,铜、镍、锰、银配合物中νC=N振动峰出现在1633 cm-1、1618 cm-1、1630 cm-1、1609 cm-1处,都不同程度地向低频移动,这说明金属离子与C=N键上的N原子发生了配位作用;配体中O-H为酚羟基中的氢氧键,各配合物中O-H峰消失,说明H已经脱落,而O则参与了配位;配体在1247 cm-1处的峰归属为C-O伸缩振动峰,751 cm-1处的峰归属为C-H弯曲振动峰,而这些峰在相应的配合物中都发生了明显变化,这可能是因为金属离子与氧配位后,对C-O和C-H键的影响所致。
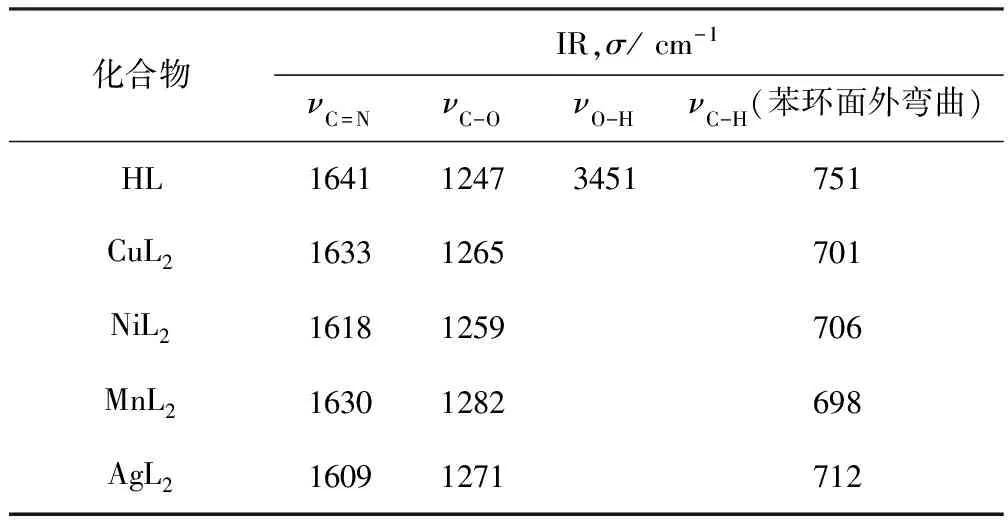
表3 配体和配合物的红外光谱数据
由元素分析、摩尔电导率、紫外可见吸收光谱和红外光谱推测出配合物的结构可能为ML2,如图2所示。
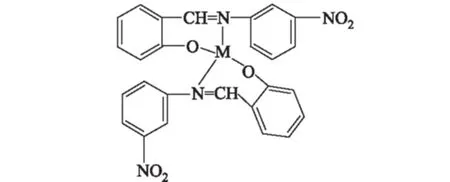
图2 配合物的结构
2.4 荧光光谱分析
各不同配比的配合物与BSA的混合溶液的荧光光谱如图3所示,图中从上至下配合物的浓度呈等差数列增大。

图3 配合物对BSA荧光光谱的影响
由图3可知,固定BSA的量,随着体系中配合物浓度的增大,BSA的内源荧光呈现有规律地猝灭。说明4种配合物在生物体内能和蛋白质相互作用,具有一定的药理价值。
2.5 抑菌活性
配体和配合物的抑菌活性如表4所示。
由表4可知,配合物对4种菌株均有不同程度的抑菌活性,其中对绿脓杆菌的抑菌性均较强。4种配合物的抑菌活性均大于配体的抑菌活性。

表4 配体及配合物的抑菌活性
3 结论
在非水溶剂中合成了间硝基苯胺水杨醛Schiff碱及其铜、镍、锰、银配合物。4种配合物都能强烈猝灭BSA的内源荧光,说明4种配合物在生物体内能和蛋白质相互作用,具有一定的药理价值。生物活性实验表明,配合物对金黄色葡萄球菌(S.aureus)、大肠杆菌(E.coli)、枯草芽孢杆菌(B.subtilis)、绿脓杆菌(P.aeruginosa)均有不同程度的抑菌作用,其中对绿脓杆菌的抑菌活性均较强。4种配合物的抑菌活性均大于配体的抑菌活性。
参考文献:
[1] 曹克广.2,3-二取代-4-(1H-1,2,4-三唑-1-基)-5-苯基氨基噻吩的合成及生物活性研究[J].有机化学,2003,24(3):1411-1415.
[2] 雷福厚,蓝虹云,朱广金,等.歧化松香希夫碱-铜配合物催化漆酚氧化聚合的研究[J].南京林业大学学报(自然科学版),2005,29(3):16-18.
[3] 石德清,陈琦,李中华.含氨基酸Schiff碱的5-氟尿嘧啶衍生物的合成及其抗肿瘤活性[J].有机化学,2005,25(5):549-553.
[4] 闭献树,毕小平,李廷盛.糠醛缩邻苯二胺双希夫碱配合物的合成、表征及抑菌活性[J].化工时刊,2000,14(4):22-24.
[5] Yong L,Huang G L,Lian B,et al.Synthesis of titanium(Ⅳ)complexes with Schiff bases ligand and their catalytic activities for polymerization of ethylene and etyrene[J].Chinese Journal of Chemistry,2001,19(4):429-432.
[6] 竹学友,俞志刚,刘洲亚,等.一种新型希夫碱及其铜配合物的合成与抑菌活性的研究[J].化学与生物工程,2008,25(4):43-46.
[7] 孙绍发,於敏敢,朱先军.光谱法研究一种咪唑啉酮类衍生物与牛血清白蛋白的相互作用[J].华中师范大学学报(自然科学版),2007,41(3):406-410.
[8] 李霁良.微量半微量型有机化学实验[M].北京:高等教育出版社,2003:177-178.
