纳米氧化镍制备及表征
2012-04-04王红涛张乐观贺茂云
王红涛,张乐观,贺茂云
(1.神马尼龙化工有限责任公司,河南平顶山467044;2.华中科技大学环境科学与工程学院)
纳米氧化镍制备及表征
王红涛1,张乐观2,贺茂云2
(1.神马尼龙化工有限责任公司,河南平顶山467044;2.华中科技大学环境科学与工程学院)
以六水硝酸镍和氨水为原料,采用配位均匀沉淀法制备了纳米氧化镍。探讨了制备条件对氧化镍前驱体产率和纳米氧化镍平均粒径的影响,得出最佳工艺条件:镍离子浓度为0.8 mol/L,反应物配比[n(氨水)/n(硝酸镍)]为3∶1,沉淀反应温度为80℃,反应时间为90 min,焙烧温度为400℃,焙烧时间为1 h。同时,利用X射线衍射(XRD)和透射电镜(TEM)等分析方法对产品组成和形貌进行了表征,结果显示,实验制得的氧化镍纳米晶属标准面心立方晶系结构,晶粒呈球形,平均粒径约为12 nm。
氧化镍;纳米颗粒;配位沉淀法;表征
NiO是一种具有较好催化性能的氧化催化剂,Ni2+具有3d轨道,对多电子氧具有择优吸附倾向,对其他还原气体也有活化作用并对还原气体的氧化起催化作用[1]。纳米NiO以其较大的表面积、短的晶内扩散通道、丰富的活性位、高的表面原子比及表面能、远高于传统催化剂的活性和选择性,在催化领域备受关注。尤其是近些年来,随着能源稀缺问题的日益加剧,生物质等可再生能源通过热分解技术被开发利用,在一定程度上替代了化石原料,NiO作为一种性价比极佳的催化剂大大提高了生物质气化和热解的产率和效率[2-3]。纳米NiO的合成方法有多种,通常采用固相反应法[4]、沉淀法[5-6]和溶胶-凝胶法[7-8]等。其中均匀沉淀法具有反应条件温和、工艺简单、原料成本低、容易洗涤、避免杂质共沉淀等优点。笔者以六水硝酸镍和氨水为原料,采用配位均匀沉淀法制备了粒度均匀、分散性好的纳米NiO。
1 实验部分
1.1 试剂与仪器
试剂:六水硝酸镍[Ni(NO3)2·6H2O]、氨水等均为分析纯;实验用水均为去离子水。
仪器:KSW型马弗炉,LD 4-2A型离心机,DF-101B型恒温加热磁力搅拌器;X′Pert PRO型X射线粉体衍射仪,Tecnai G2 20型透射电子显微镜。
1.2 纳米氧化镍的制备
向称量好的六水硝酸镍中加入一定量蒸馏水,在搅拌条件下加入一定量氨水,继续搅拌得到深蓝色镍氨配合物溶液。在搅拌条件下加热溶液,待反应液出现绿色浑浊物后冷却陈化2 h,然后离心分离,沉淀物用蒸馏水反复洗涤至洗涤液无色。沉淀于105℃干燥8 h,得浅绿色粉末状前驱物。将前驱物置于马弗炉中焙烧,即得纳米NiO粉末。
2 结果与讨论
2.1 镍离子浓度和反应物配比对前驱体产率的影响
固定条件:反应温度为 70℃、反应时间为90 min、反应物配比[n(氨水)/n(硝酸镍)]为4∶1,考察镍离子浓度对氧化镍前驱体产率的影响,结果见图1。从图1可以看出,随着镍离子浓度的增加,前驱体产率增大,但当镍离子浓度超过0.8 mol/L以后,前驱体产率的增加趋势变得非常缓慢。因此选择镍离子浓度为0.8 mol/L。
固定条件:反应温度为 70℃、反应时间为90 min、镍离子浓度为0.8 mol/L,考察反应物配比对氧化镍前驱体产率的影响,结果见图2。从图2可以看出,随着反应物配比的逐渐增加,前驱体产率明显提高。这可能是因为,氨水与硝酸镍物质的量比越大,溶液碱性越强,生成的沉淀物的量也相应增多,产率也随即逐渐增大。因此选择反应物配比为3∶1。
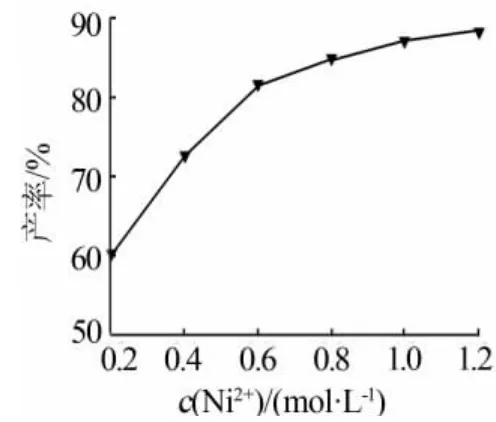
图1 镍离子浓度对氧化镍前驱体产率的影响
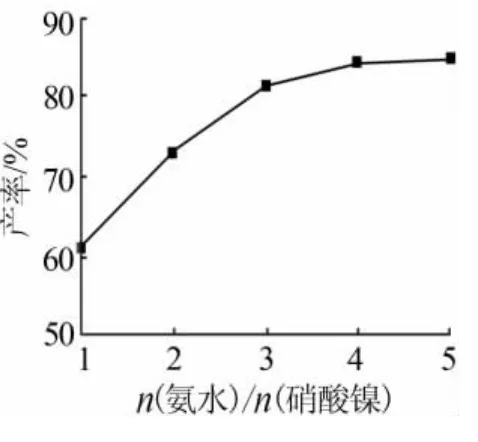
图2 反应物配比对氧化镍 前驱体产率的影响
2.2 反应温度对前驱体产率和氧化镍粒径的影响
固定条件:反应时间为90 min、反应物配比为3∶1、镍离子浓度为0.8 mol/L,焙烧温度400℃,焙烧时间1 h,考察反应温度对氧化镍前驱体产率和氧化镍平均粒径的影响,结果见图3。从图3可知:随着反应温度的升高,前驱体产率和氧化镍粒径均不断增加,反应温度对氧化镍粒径的影响较大。当温度达到80℃时,产率随温度变化己趋于平缓,此时平均粒径也较细小。反应温度对于配合物的分解反应速度影响较大,从而强烈影响到沉淀的生成速率和沉淀剂的过饱和比值。反应温度越低,配合物的分解速度越慢,生成沉淀的绝对晶核数目少,由这些少量的晶核逐渐生长成的晶粒大,使得产品粒径分布变宽,且沉淀的析出产率低,所以反应温度不宜过低。而温度太高,溶液中离子运动速率较低温时快得多,晶粒生长快,使颗粒尺寸有所增大。实验确定反应温度为80℃。
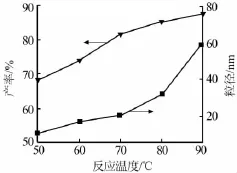
图3 反应温度对氧化镍前驱体产率和氧化镍平均粒径的影响
2.3 反应时间对前驱体产率和氧化镍粒径的影响
固定条件:反应温度为80℃、反应物配比为3∶1、镍离子浓度为0.8 mol/L,焙烧温度为400℃,焙烧时间为1 h,考察反应时间对前驱体产率和氧化镍纳米晶粒径的影响,如图4所示。由图4可知,在开始的90 min内,随着时间的增加产率逐渐增加。这是由于随着时间的增加,氨水分解速度随之增大,水解程度增加,消耗较多的Ni2+,生成的沉淀也增加,所以产率增加。但是,当反应时间达到90 min以后,产率随时间的变化很小。由图4还可以看出,反应时间过长会导致产物粒子不断长大,造成粒径分布宽化;反应时间太短,虽然产品粒度较小,但产率极低。综合考虑,选择反应时间为90 min。

图4 反应时间对氧化镍前驱体产率和平均粒径的影响
2.4 焙烧温度和焙烧时间对氧化镍粒径的影响
固定条件:反应温度为80℃,反应时间为90min,镍离子浓度为0.8 mol/L,反应物配比为3∶1,焙烧时间为1 h,考察焙烧温度对氧化镍粒径的影响。结果表明,在400、500、600、700℃焙烧所得氧化镍粒径(将所得产品进行XRD分析,并根据Scherrer公式估算其粒径)分别为11.7、26.8、41.4、63.2 nm。焙烧温度升高,产品粒径变大。这是由于,随着热处理温度的升高,处于高度无序状态的表面在粒子整体中所占的比例减小,晶型更加完整,晶粒增大表明粒子的粒径变大。从外观看,随着焙烧温度的升高,NiO晶粒长大,NiO粉体的颜色亦由深黑色逐渐变成略带灰黑色最后变为浅灰色。实验选择焙烧温度为400℃。
固定焙烧温度为400℃,考察焙烧时间对氧化镍产品粒径的影响。结果表明,1、2、3、4 h焙烧所得产品粒径分别为11.7、36.1、72.2、84.3 nm。随着焙烧时间的延长,晶粒尺寸逐渐增大。选择焙烧时间为1h。
2.5 产品XRD分析和TEM分析
图5为最佳条件制备的纳米NiO样品XRD谱图。由图5可以看出,产物在36.9[对应(111)晶面]、43.0(200)、62.6(220)、74.9(311)、78.7°(222)处出现特征衍射峰,峰位置均与JCPDS标准衍射卡NO.47-1049上的衍射数据相吻合,说明产物为标准面心立方晶系NiO,而且产物的衍射峰无杂峰出现,纯度较高。根据Scherrer公式计算出产物平均粒径为12 nm。
图6为在最佳条件下制备的氧化镍TEM照片。从图6可以看出,NiO晶粒呈球形,有轻微团聚现象,粒径在10~15 nm,这与Scherrer公式计算的结果基本一致。
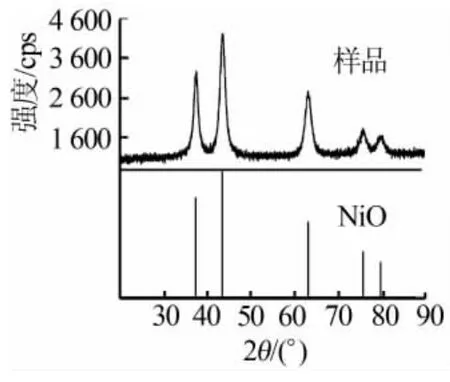
图5 制得的纳米氧化镍XRD谱图

图6 制得的纳米氧化镍TEM照片
3 结论
采用配位均匀沉淀法制备了分散性较好、纯度高的纳米氧化镍。最佳条件:沉淀反应温度为80℃,反应时间为90 min,氨水与硝酸镍物质的量比为3∶1,镍离子浓度为0.8 mol/L,焙烧温度为400℃,焙烧时间为1 h。在此条件下制得的产品收率高且粒径较小,属标准面心立方晶系,平均粒径约为12 nm。
[1] Xing Wei,Li Feng,Yan Zifeng,et al.Synthesis and electrochemical properties of mesoporous nickel oxide[J].J.Power Sources,2004,134(2):324-330.
[2] 夏熙,魏莹.纳米级β-Ni(OH)2的制备和放电性能[J].无机材料学报,1998,13(5):674-678.
[3] Han X J,Xie X M,Xu C Q,et al.Morphology and electrochemical performance of nano-scale nickel hydroxide prepared by supersonic coordination precipitation method[J].Opt.Mater.,2003,23(1/2):465-470.
[4] 周立群,杨念华,周丽荣,等.纳米氧化镍的固相合成[J].应用化学,2006,23(6):682-684.
[5] Wu Lili,Wu Youshi,Wei Huiying,et al.Synthesis and characteristics of NiO nanowire by a solution method[J].Mater.Lett.,2004,58(21):2700-2703.
[6] 李国军,任瑞铭,黄校先,等.纳米晶氧化镍的制备及表征[J].无机化学学报,2004,20(3):287-292.
[7] 景茂祥,沈湘黔,沈裕军.柠檬酸盐凝胶法制备纳米氧化镍的研究[J].无机材料学报,2004,19(2):289-295.
[8] Yang Qing,Sha Jian,Ma Xiangyang,et al.Synthesis of NiO nanowiresbyasol-gelprocess[J].Mater.Lett.,2005,59(13):1967-1970.
联系方式:pheric@yeah.net
Preparation and characterization of nano-sized nickel oxide
Wang Hongtao1,Zhang Leguan2,He Maoyun2
(1.Shenma Nylon Chemical Co.,Ltd.,Pingdingshan 467044,China;2.School of Environmental Science&Engineering,Huazhong University of Science and Technology)
Nano-sized NiO was prepared by coordination homogeneous precipitation method using ammonia water and Ni(NO3)2·6H2O as raw materials.Influences of various processing parameters in preparation process on the yield of precursor and on mean particle diameter of nano-sized NiO were investigated.Optimum conditions for preparing nano-sized NiO were as follows:nickel ion concentration was 0.8 mol/L,amount-of-substance ratio of ammonia water to nickel nitrate hexahydrate was 3∶1,temperature of precipitation reaction was 80℃,reaction time was 90 min,calcination temperature was 400℃,and calcination time was 1 h.XRD and TEM etc.were used to characterize crystalline structure and morphology of the product.Results indicated that nano-sized NiO prepared under the optimum conditions had a fine crystal phase of standard face-centered cubic lattice structure with a mean particle diameter of about 12 nm.Shape of nano-sized NiO was spherical.
nickel oxide;nanoparticles;coordination homogeneous precipitation method;characterization
TQ138.13
:A
:1006-4990(2012)03-0060-03
2011-10-05
王红涛(1972—),男,本科,工程师,主要从事化工方面的工作,发表论文2篇。
