Zr9Ni11合金的吸氢性能测定
2012-03-21胡彦泽但贵萍
杜 良 胡彦泽 但贵萍 张 东
(中国工程物理研究院核物理与化学研究所 绵阳 621900)
氚在军事、能源、工业、农业、医疗等领域均有应用,需对涉氚工作现场气氛净化以确保职业安全[1]。常用除氚方法主要有氧化法和合金吸附法,后者不产生二次污染、处理工艺简单,受到高度关注[2–5]。
贮氢合金能在室温下快速吸收工作现场的氚,以净化现场空气。此类合金须有较高的贮氚容量、较快吸/放氢速率、较低的平衡压和较强的抗毒化性能。Ti、V、Pd、Zr、U等金属均可除氚,但U、Ti、V的氢化物易粉化、释热高、易着火[6],而 Pt性能稳定但价格昂贵。Zr基材料具有对空气杂质气体反应性较低、价廉、无放射性等优点,是较有发展空间的除氚材料,其中Zr-Ni系合金因其Ni组分的催化作用具有良好的吸氢动力学性能。
本文对Zr9Ni11合金,用定容变压法研究其常温和低氢压力下的吸氢性能,考察其吸氢前后结构变化特征,以探索其作为氚操作现场除氚合金的可能性,为研究常温低压除氚技术提供基础。
1 材料和方法
1.1 合金制备
Zr9Ni11合金由北京有色金属研究院制备,主要过程为:将Zr与Ni的纯金属粉末(纯度>99.9%)以9:11的原子比混合均匀,压块后放入真空感应炉内翻身熔炼3次,合金成形后在1050ºC左右退火。XRD分析表明合金组成均匀,主要为Zr9Ni11相。用稀盐酸洗净合金后人工破碎成1 mm左右的颗粒待用。
1.2 实验装置
该合金消氢装置为高真空金属系统,包括加热、真空、压力测量和反应室等部分,其示意图见图1。真空系统的真空极限可达2.0×10–5Pa;压力测量系统包括电容规(0–10,000 Pa,精度 0.5‰)、电阻规(0–100 kPa,精度±30%)和压力传感器(0–250 kPa,精度0.1 kPa);反应室为容积52 mL的钢瓶;加热电炉可升至1200ºC,有温度控制与机械升降系统。实验系统有效体积285 mL。
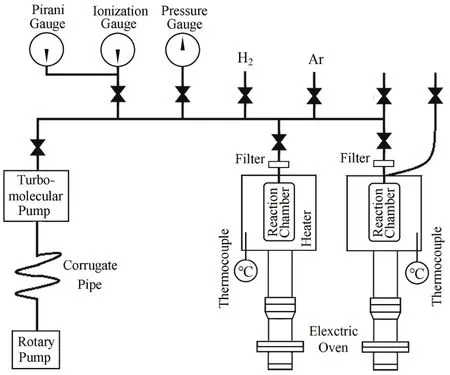
图1 合金消氢实验装置示意图Fig.1 Schematic diagram of hydrogen absorption system.
1.3 实验方法
采用定容变压法进行实验。用稀盐酸清洗合金颗粒表面以去除微量的金属氧化物后用蒸馏水清洗,再用丙酮除去合金表面残留的油污,最后用无水乙醇脱水。将处理好的合金颗粒放入消气系统反应室并充入纯度为 99.999%(v%)的氢气进行反应,实验步骤如下:
(1) 真空除气:将实验样品装入反应室后,开启涡旋片真空泵,压力达到5 Pa后,启动涡轮分子泵,继续抽真空至压力达到5×10–4Pa,并同时加热至850ºC,持续时间8 h。
(2) 合金活化:将氢气充入反应室,反复加热、冷却,直至合金在极短时间内将氢气吸尽且吸氢量稳定,表明合金已经活化。
(3) 在室温下采用定容变压法,即在室温、系统体积一定的情况下,充入一定量氢气,使反应系统压力为161 kPa,开展合金吸氢实验,而后加热至400ºC,同时抽真空(真空度高于1×10–1Pa)25 min完成合金除氢过程,如此循环作室温下吸氢性能测试。
用扫描电镜(SEM)观察合金在吸放氢循环前后的表面形貌变化,用能量色散能谱(EDS, energy dispersive spectrometry)分析合金表面化学组成。合金相结构分析在DX-1000型X射线衍射仪上进行,工作条件为:Cu靶Kα射线源,35 kV,25 mA,DSSS:10,RS:0.2 mm,扫描速度为0.06°/s。
2 结果与讨论
2.1 Zr9Ni11合金在室温下的吸氢量
图2(a)为Zr9Ni11合金在室温下六次循环的吸氢曲线,多次循环的吸氢速率无明显差别,但吸氢量随循环次数增大而略有下降(图2b)。可见该合金吸氢容量较大,平均吸氢容量为 0.0045 mol/g。随循环次数增加吸氢量略降的原因可能为:(1) 合金吸附氢后,部分氢在解吸过程中未释放出来,导致下一个吸氢循环中吸氢量的降低[6];(2) 本文实验气体中含有微量的杂质气体,可能会引起合金中毒[7],合金内出现不能吸附氢的颗粒;(3) 合金在多次循环过程中粉化,有些超细合金颗粒被真空泵抽走,导致反应床中合金样品有轻微的质量亏损,引起吸氢量下降。因此,解决吸氢量下降对于保证合金在工程中得到多次使用具有现实意义。
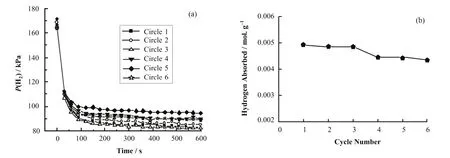
图2 Zr9Ni11合金吸氢曲线(a)和吸氢量随循环次数的变化(b)Fig.2 Absorption curves (a) of Zr9Ni11 and the hydrogen-absorbed as a function of the cycle number (b).
2.2 Zr9Ni11合金在不同初始压力下的吸氢性能
由图3(a),氢压力高于100 kPa时,受合金吸氢容量限制,不能除去反应室中所有的氢;而氢分压低于50 kPa时,Zr9Ni11合金基本可将氢气吸完,压力越低,氢气吸收越完全。在一般氚操作现场,氚的分压低于kPa量级,因此,在室温条件下Zr9Ni11合金可较彻底去除工作现场中的氚。
定义反应程度α为某时刻氢的反应量与反应达平衡时氢的总反应量之比[8],则氢压力、反应程度与时间的关系见图3(b)。合金初始吸氢速率(可用曲线的斜率表示)随氢气压力增大。在较低初始压力下,合金初始吸收速率仍可在300 s内完成总反应量的95%的吸附,表明Zr9Ni11合金在室温、低压条件下,仍有较快的吸附速率,其动力学性能满足现场除氚要求。
Zr9Ni11合金在不同吸氢阶段有不同的反应速率,这可能与吸氢反应的步骤相关。氢气与合金反应生成金属氢化物过程为[9]:(1) 氢分子在金属表面吸附;(2) 氢原子由表面扩散至合金基体内;(3) 氢原子与合金组分发生氢化反应。在合金吸氢初始阶段,氢分子在合金表面的吸附与氢压力密切相关。当初始压力较高时,表面吸附过程较强,单位时间内参与扩散过程的氢原子较多,反应速率较快;而当初始压力较低时,表面吸附过程较弱,导致单位时间内扩散至合金基体参与反应的氢原子减少,反应速率较慢。也即在合金吸氢过程中,不同的初始压力对应不同的平衡压力,实际压力与平衡压力的差值反映合金对平衡状态的偏离程度,表现为吸氢速度,故在较高初始压力下,Zr9Ni11合金的吸氢速率较快。

图3 Zr9Ni11在不同压力下的吸氢曲线(a)和动力学曲线(b)Fig.3 Absorption curves (a) and kinetic curves (b) under low pressure.
2.3 合金微观形貌与相结构分析
Zr9Ni11合金氢化反应前后表面形貌变化较显著(图4),吸氢前表面光滑,放大164倍并无明显裂纹;数次吸放氢循环后,合金表面出现大量裂痕,变得粗糙。同时,合金颗粒在吸放氢过程中被破碎,粒径减小。EDS分析表明,吸氢前表面锆镍原子比为45.56:56.44;吸放氢后,对合金表面三个随机微观区域统计的锆镍原子比分别为 53.04:46.94、18.66:81.34、53.18:46.82,表明合金在吸放氢循环中表面元素组成发生不均匀改变,这也是影响合金吸氢容量和动力学性能的因素。

图4 Zr9Ni11合金吸氢前(a)后(b)的SEM图像Fig.4 SEM image of Zr9Ni11 before (a) and after (b) hydrogen absorption.
图5为 Zr9Ni11合金吸氢前和吸放氢循环后的XRD衍射谱,合金吸氢前主要为Zr9Ni11相;多次吸放氢循环后,基线的隆起部分(图中方框所示)表明合金出现大量相组成复杂的非晶相。石正坤等[10]研究表明,Zr9Ni11合金在吸放氢循环后,出现了Zr2Ni和Zr0.17Ni0.83,也可能存在Zr2Ni7等新相。本文采取的实验条件与文献[10]不同,合金吸氢后的相结构也不同。新相的出现对于合金吸氢容量的影响,需开展进一步研究。
多次循环后合金表面锆镍比和相结构发生变化,组成趋于复杂,导致合金吸氢容量发生变化。

图5 Zr9Ni11合金吸氢前(a)后(b)的XRD衍射谱图Fig.5 XRD patterns of Zr9Ni11 before (a) and after (b) hydrogen absorption.
3 结语
室温下多次吸放氢循环实验表明,Zr9Ni11合金的吸氢量较高,其吸氢量随循环次数增大而略呈下降,但涉氚操作现场的氚浓度较低,因此,该合金多次循环后其吸氢量仍可满足使用要求。
实验结果表明,该合金吸氢初始速率随氢气压力减小,但在较低氢压力下仍可在几分钟内完成对氢的吸收,表明该合金具有良好的吸氢活性。
1 杨怀远. 氚的安全与防护[M]. 北京: 原子能出版社, 1997: 177–181 YANG Huaiyuan. Safety and prevention about tritium[M]. Beijing: Atomic Energy Press, 1997: 177–181
2 Gary Sandrock. A panoramic overview of hydrogen storage alloys from a gas reaction point of view[J]. J Alloys Compo, 1999, 293–295: 877–888
3 Chuang H J, Huang S S, Ma C Y, et al. Effect of annealing heat treatment on an atomized AB2hydrogen storage alloy[J]. J Alloys Compo, 1999, 285(1–2): 284–291
4 Masakazu Aoki, Nobuko Ohba, Tatsuo Noritake, et al. Hydriding and dehydriding properties of CaSi[J]. J Alloys Compo, 2005, 404–406: 402–404
5 Peng C H, Zhu M. Microstructure and hydrogen storage properties of a multi-phase Ml0.7Mg0.3Ni3.2hydrogen storage alloy[J]. J Alloys Compo, 2004, 375(1–2): 324–329
6 蒋国强, 罗德礼, 陆光达, 等. 氚和氚的工程技术[M].北京: 国防工业出版社, 2007: 410–413
JIANG Guoqiang, LUO Deli, LU Guangda, et al. Tritium and industry technology of tritum[M]. Beijing: National Defense Industry Press, 2007: 410–413
7 桑 革, 李全安, 闫康平, 等. CO对MlNi4.5Al0.5合金吸氢动力学特性的影响[J]. 稀有金属, 2005, 25(3): 178–180
SANG Ge, LI Quan’an, YAN Kangping, et al. Effect of impurity of Hydrogen absorption kinetics of MlNi4.5Al0.5[J]. Chinese J Rare Metal, 2005, 25(3): 178–180
8 万竟平, 彭述明, 龙兴贵, 等. TiV合金吸氢动力学研究[J]. 材料导报, 2009, 21(5): 247–249
WAN Jingping, PENG Shuming, LONG Xinggui, et al. Investigations on Hydrogen-absorption kinetics of Ti-V alloys[J]. Mater Rev, 2009, 21(5): 247–249
9 Diego Escobar, Sesha Srinivasan, Yogi Goswami, et al. Hydrogen storage hehavior of ZrNi 70/30 and ZrNi 30/70 composites[J]. J Alloys Compo,2008, 458(1–2): 223–230
10 石正坤, 曾 敏, 康厚军. Zr9Ni11合金吸氢性能研究[J].原子能科学技术, 2002, 36(4/5): 439–457
SHI Zhengkun, ZENG Min, KANG Houjun. Property of Zr9Ni11absorption Hydrogen[J]. At Energy Sci Technol, 2002, 36(4/5): 439–457
