煤气和工艺冷凝液中氯化氢的测定
2012-02-09卢乙试
卢乙试
(河南龙宇煤化工有限公司,河南永城 476600)
0 前言
煤气中的HCl、H2S会对煤气管线(304材质)造成较大的腐蚀,尤其Cl-对其腐蚀较为严重。所以检测煤气中的HCl、H2S成分将对管材的保护起检测作用,对选材起到指导作用。本文所述方法适用于煤气和工艺冷凝液中氯离子的测定。寻找一个简单易行的实验方法对日常的检测有很大的意义。经过笔者的摸索与实验,把方法锁定在莫尔法上,然而吸收下来的溶液或工艺冷凝液成分复杂,测定影响因素多,需要大量的处理工作,本文从原理到实验设计,实验步骤注意事项等做了详细的阐述。
1 实验原理
煤气主要成分有:CO、CO2、H2、N2、H2S、微量HCl、NH3、CH4和氧氩等。用稀碱液吸收粗煤气,气体中的 HCl、CO2、H2S、NH3一同被吸收。NH3与Ag+形成Ag(NH3)2+影响结果的准确度,可以加强碱然后加热使NH3溢出,消除其对测定的影响。由于Ag2S的溶度积为2×10-49,所以S2-对Cl-的测定有影响,可用30%的过氧化氢把S2-氧化成硫酸根(Ag2SO4的溶度积为1.4×10-5,AgCl的浓度积为1.8×10-10),从而消除了S2-对测定的影响。在中性或弱碱性条件下,以铬酸钾为指示剂,用硝酸银标准液进行滴定,以消耗的硝酸银的量计算HCl的含量。反应方程式如下:

2 试剂和仪器
试剂:0.05 mol/L氢氧化钠溶液;0.1 mol/L氢氧化钠溶液;200 g/L碳酸氢钠溶液;1+1硝酸溶液;1%酚酞指示剂(95%乙醇溶液),10%铬酸钾指示剂,30%过氧化氢(H2O2);0.05 mol/L硝酸银标准溶液。
仪器:自动滴定仪1台;500 mL容量瓶;湿式流量计1台;吸收瓶2个;乳胶管若干;弹簧夹1支;三通1支。
3 实验设计
在吸收瓶中加入0.05 mol/L氢氧化钠溶液至吸收瓶体积的1/2,如图1所示连接好。

图1 实验连接示意图
调节好流量(约5 L/min),根据具体情况吸收200~1 000 L气体。吸收液转移至500 mL容量瓶中,定容至刻度。用移液管准确吸取100 mL吸收液于250 mL锥形瓶中,加1 mL 30%过氧化氢溶液。如有NH3存在,可用此步骤消除影响。加200 g/L氢氧化钠溶液5.00 mL,然后在电炉上加热使NH3溢出,完毕时取下冷却至室温,加入适量蒸馏水。2~3滴酚酞指示剂,用1+1硝酸溶液中和至刚好无色。加入1 mL 10%铬酸钾指示剂,用硝酸银标准溶液滴至橙色,记下硝酸银标准溶液的消耗量V,同时做空白试验,记下硝酸银标准溶液消耗量V0。
4 结果计算
气体中HCl的含量X(mg/L)按下式计算:
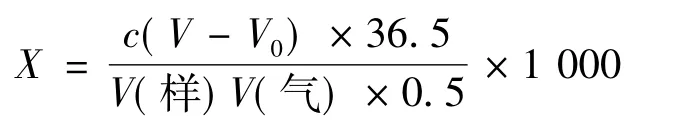
其中:c,硝酸银标准溶液浓度,mol/L;V,滴定水样时硝酸银标准溶液的消耗量,mL;V0,空白试验时硝酸银标准溶液的消耗量,mL;V(样),滴定中所取水样的体积,mL;V(气),所取粗煤气样体积,L;0.5,容量瓶体积,L;36.5,HCl相对分子质量。
5 注意事项
①取气样时流速不易太大。②取气样体积不易太小,太小了溶液中的Cl-含量过少,终点不易判断。③加入过氧化氢若出现浑浊,则适当加大过氧化氢的量或适当减少取样量。④NH3的存在对测定结果影响很大,务必使其溢出完全,可用pH试纸或红色石蕊试纸在煮沸的瓶口测试。⑤铬酸钾指示剂不可加多或少加,加多了终点将过早出现,加少了终点将过迟出现,影响滴定的准确度。⑥临近终点时要剧烈摇动,以减少AgCl对Cl-的吸附以免终点提前到达。
