萃取法制备工业级磷酸二氢铵-萃取剂的反萃取研究*
2012-02-07罗建洪马春磊
罗建洪,李 军,金 央,马春磊
(四川大学 化工学院,四川 成都 610065)
用湿法磷酸生产工业级MAP时,溶液一般中和到pH值为4~4.5左右。在此pH值下,绝大部份金属阳离子已被除去。但由于Mg2+水解pH值较高的缘故,中和液中仍含有一定量的Mg2+,会在后续的浓缩、冷却结晶过程中形成水不溶物,造成产品水不溶物超标。因此,在结晶之前需要采取其它方法把Mg2+脱除。
本课题以D2EHPA为萃取剂,采用溶剂萃取法来提取MAP溶液中的Mg2+杂质,从而实现生产工业级MAP的目的;但是实现其产业化的难点之一,就是反萃取剂的选择,而在选择反萃取剂时关键是实现络合物D2EHPA-Fe3+的有效分离,因为络合物D2EHPA-Fe3+是非常稳定的,而且Fe3+的富集能使萃取剂老化。因此,选择有效的反萃取剂来实现D2EHPA的循环回收利用是非常有必要的。
载Fe3+-D2EHPA一般是用浓度较高的HCl[1,2]、HNO3[3]或 H2SO4[4,5]对载 Fe3+有机相进行反萃,或是对有机相还原反萃[6]。这些研究表明高浓度的HCl为反萃取剂效果虽然良好,但是在工业化生产中对材质的要求很苛刻,因此,本课题提出以H2SO4+添加剂A为反萃取剂,来萃取金属有机载体D2EHPAFe3+溶液中的Fe3+进行研究,研究内容是系统地考察了各个影响因素,包括反萃取剂H2SO4浓度,相比(水相∶有机相),反应温度,反应时间,搅拌速度等对反萃取率的影响,以求得适宜反萃工艺条件,从而实现萃取剂D2EHPA的循环利用,对实现工业级的MAP的产业化目标具有重要意义。
1 实验部分
1.1 原料、试剂及仪器
萃取剂:D2EHPA(A.R.河南中达化工有限公司);
稀释剂:磺化煤油(成都科龙化工有限公司);
反萃取剂:H2SO4,(A.R.成都科龙化工有限公司);
MgSO4·7H2O,(A.R.天津科密欧化学试剂有限责任公司);Fe2(SO4)3(C.P.天津耀华化学试剂有限责任公司);H3PO4(A.R.成都科龙化工有限公司);NH3(工业级);实验采用二次蒸馏水。
HH-S型水浴锅(北京市中兴伟业仪器有限公司);JJ-2型搅拌器(江苏省金坛市医疗仪器厂)。
1.2 分析方法
铁的测定方法——邻菲啰啉比色法。
2 结果与讨论
反萃取过程的分离效果,用反萃取率(E)来表征,定义如下:
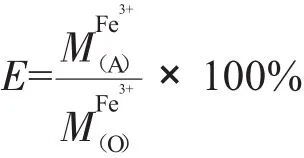
2.1 反萃取剂浓度的影响
研究发现,添加剂A不变的情况下,反萃取率随反萃取剂H2SO4浓度的增加而增加,这是因为,H2SO4的浓度增加,参加反萃取反应的活性溶剂的量提高。但是到一定的浓度后,萃取率变化不明显,这是由于反萃取反应已经达到平衡的缘故。同时考虑到H2SO4的浓度过高可能引起酸化,因此,H2SO4的浓度以4mol·L-1为较佳。实验结果见图1。
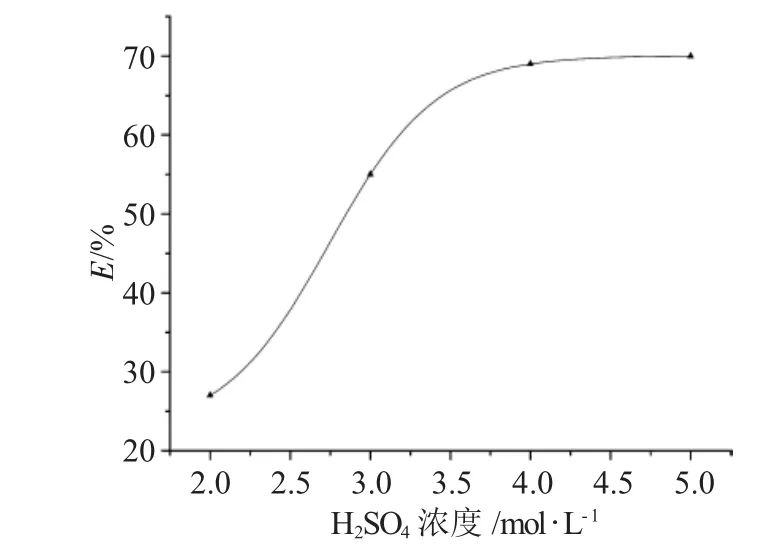
图1 反萃取剂浓度对反萃取率的影响Fig.1 Effect of the concentration of H2SO4onstripping efficiency(E)versus
2.2 反应时间的影响
实验条件为:相比为1∶1,搅拌速度550r·min-1,反应温度为 40℃,反萃取剂浓度为 4mol·L-1。
反应时间对反萃取过程的影响见图2。
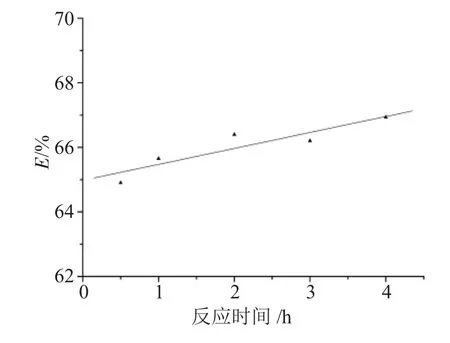
图2 反应时间对反萃取率的影响Fig.2 Effect of the reaction time on stripping efficiency(E)versus
由图2可见,Fe3+的反萃取率随搅拌时间的增加而增加。但当反应时间到0.5h时,Fe3+的反萃取率随时间变化并不明显。考虑到生产能耗等因素,反应时间以0.5h为较佳。
2.3 相比的影响
实验条件为:搅拌时间为0.5h,搅拌速度550r·min-1,反应温度 40℃,反萃取剂浓度为 4mol·L-。
相比(水相/有机相)的影响,实验结果见图3。
由图3可见,发现了随着相比(R)的增加,反萃取率(E)渐渐增加。这是因为,相比的增加,反萃取剂H2SO4中的反萃取剂的含量也增加,因此,萃取率也随着增加。
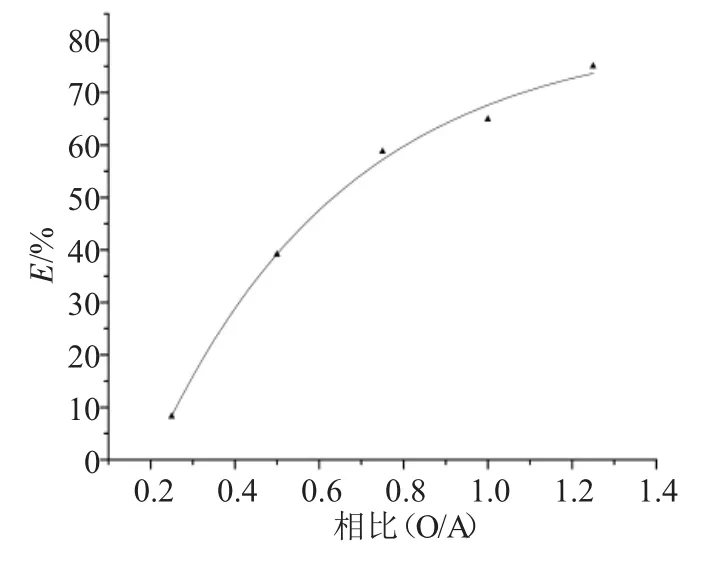
图3 相比对反萃取率的影响Fig.3 Effect of the phase ratio(R)on stripping efficiency(E)versus
2.4 反应温度的影响
实验条件为:相比 1∶1,搅拌速度 550r·min-1,反萃取剂浓度为4mol·L-1,搅拌时间为0.5h。
反应温度的影响,实验结果见图4。
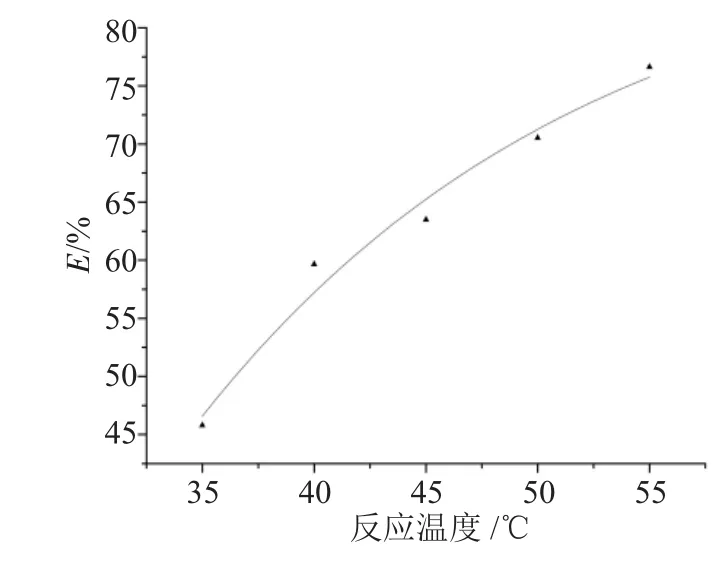
图4 反应温度对反萃取率的影响Fig.4 Effect of the reaction temperature on stripping efficiency(E)versus
由图4可见,随着温度的增加,Fe3+的反萃取率增加,说明该反应体系是吸热反应。但是温度若过高,增加能耗,同时也可能引起酸化。
2.5 搅拌速度的影响
实验条件为:相1∶1,反萃取剂浓度为4mol·L-1,搅拌时间为 0.5h。
搅拌速度对Fe3+的反萃取率的影响见图5。
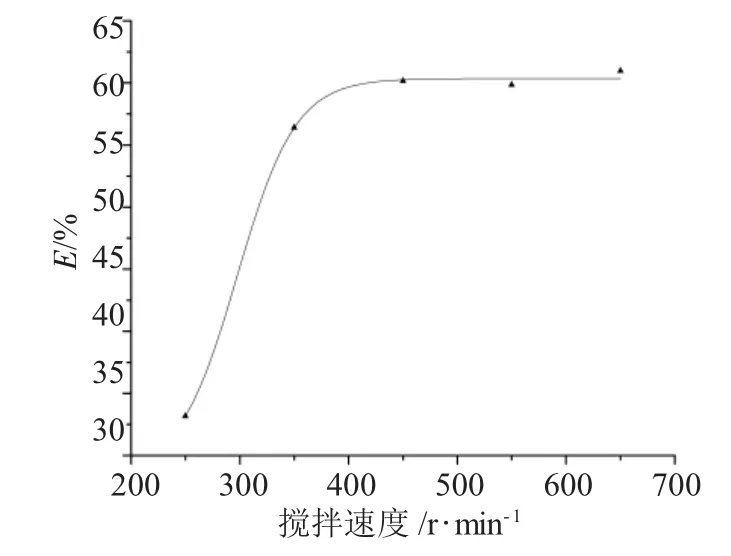
图5 搅拌速度对反萃取率的影响Fig.5 Effect of the stirring speed on eextraction ratio(E)versus
随着搅拌速度的增加,Fe3+的反萃取率增加,但是当搅拌速度增加到450r·min-1后,搅拌速度对Fe3+的萃取率影响并不明显,说明搅拌速度很大时,搅拌速度对反应体系的相接触面积增加并不明显,因此搅拌速度以550r·min-1为宜。
3 结论
基于用H2SO4+添加剂A的为反萃取剂来萃取金属有机载体D2EHPA-Fe3+溶液中的Fe3+进行研究,实验结果,可以得到以下结论:
(1)H2SO4+添加剂A可以作为有效的反萃取剂来脱除金属有机载体D2EHPA-Fe3+溶液中的Fe3+,实现萃取剂D2EHPA的循环利用。
(2)反萃取过程的适宜工艺参数为:H2SO4浓度4mol·L-1,反应温度 45℃,相比为 1∶1,搅拌速度550r·min-1,搅拌时间 0.5h。
[1]Hirato T.,Wu Z.,Yamada Y.et al.Improvement of the stripping characteristics of Fe-III utilizing a mixture of di(2-ethylhexyl)phosphonic acid and tri-n-butyl phosphate[J].Hydrometallurgy,1992,28:81-93.
[2]Sahu K.K.,Das R.P..Synergistic extraction of iron-III.At higher concentrations in D2EHPA-TBP mixed solvent systems [J].Metall.Mater.Trans.,1997,B28B:181-189.
[3]Jayachandran J.,Dhadke P.M..Liquid-liquid extraction separation of iron(III)with di(2-ethylhexyl)phosphonic acid mono 2-ethyl hexyl ester[J].Talanta,1997,(44):1285-1290.
[4]Weert G.V.,T.van Sandwijk,Hogeweg P..Solvent extraction of ferric iron from zinc sulfate solutions with DEHPA investigation of nitric acid as stripping agent,in:B.Mishra(Ed,Extraction and Processing Division Congress,TMS,Warrendale(PA),1998,245-266.
[5]Chen J.,Yu S.,Liu H.et al.New mixed solvent systems for the extraction and separation of ferric ion in sulphate solutions[J].Hydrometallurgy,1992,(30):401-416.
[6]Lupi C.,Pilone D..Reductive stripping in vacuum of Fe-III from D2EHPA[J].Hydrometallurgy,2000,57:201-207.
