磁性可回收钯催化剂催化Suzuki反应的研究进展*
2012-01-09万红亮白雪峰1
万红亮,白雪峰1,**
(1黑龙江省科学院石油化学研究院,黑龙江 哈尔滨150040;2.黑龙江大学 化学化工与材料学院,黑龙江 哈尔滨150080)
磁性可回收钯催化剂催化Suzuki反应的研究进展*
万红亮2,白雪峰1,2**
(1黑龙江省科学院石油化学研究院,黑龙江 哈尔滨150040;2.黑龙江大学 化学化工与材料学院,黑龙江 哈尔滨150080)
钯催化剂催化卤代芳烃和芳基硼酸生成碳-碳键的Suzuki偶联反应是合成联苯化合物的最重要的途径之一。相比于传统均相钯催化剂的利用率低,污染产品等缺点,磁性钯催化剂易回收,可重复利用,具有工业化应用前景,受到了广泛的关注。综述了近年来无配体磁性钯催化剂、无包裹磁性钯配体催化剂以及以碳、氧化硅、聚合物包裹的具有核壳结构的磁性钯配体催化剂的制备及其催化Szuki偶联反应的研究进展。
磁性;钯催化剂;Suzuki反应
前 言
钯催化卤代芳烃与有机苯硼酸及其衍生物的Suzuki反应开创了碳-碳偶联的新途经[1~2]。其反应条件温和,原料廉价易得,对底物要求宽松,被广泛地应用于功能高分子液晶材料合成、非线性光学材料以及药物合成等[3~6]。
均相钯催化剂在反应中分散效果好,具有很高的反应活性和选择性,已在Suzuki反应中广泛使用。但由于反应后催化剂与产物、溶剂分离困难,昂贵的钯不易回收,催化剂难以重复利用,而且残留的重金属也会污染产品,限制了它在工业上的应用。均相钯催化剂可以通过固载化的方式实现回收利用,具有较大比表面的硅基材料[7]、碳基材料[8]、聚合物[9]等,均可作为催化剂载体。
近年来,磁性材料负载催化剂引起了人们的关注[10]。相对于其他化学或物理分离方法,如萃取,色谱法,过滤和离心等,磁性材料负载催化剂只需一个外加磁场就能方便有效地实现同反应体系相分离,是一种更绿色环保的分离方法。本文综述了近年来各种磁性钯催化剂在Szuki反应中的研究进展。
1 无配体磁性钯催化剂
在磁性载体上直接负载钯,或载体经修饰后再与钯结合制得的磁性钯催化剂,无需配体,是一种简便有效的催化剂制备途径。
刘诗咏等[11]利用静电作用,将带负电的PdCl42-吸附到带正电的Fe3O4胶体粒子表面,再用抗坏血酸还原PdCl42-,得到了Pd(0)纳米团簇的磁性Fe3O4纳米粒子催化剂。该催化剂对溴代芳烃和碘代芳烃表现出较优异的催化活性,在0.5mol%Pd,K2CO3作碱,DMF-H2O体系下目标产物收率均能达到85%以上。催化剂重复利用4次后依然能够得到85%的收率,但催化反应6次后催化活性开始明显下降,这是由于出现了钯的流失和催化剂钝化的缘故。Cano等[12]在碱性条件下,将PdCl2固载到Fe3O4上制得了Pd(OH)2-Fe3O4催化剂,该催化剂对芳基碘化物的催化活性较好,对芳基溴化物也具有一定的催化效果,而对芳基氯化物和氟化物则没有催化活性。催化剂循环3次后产物的产率略有下降。Zhou等[13]将零价态钯负载到氧化铁包裹的铁的磁性纳米粒子上,制得了Fe@FexOy/Pd催化剂。以H2O/EtOH为溶剂,K2CO3为溶剂,0.5mol%催化剂用量时,对芳基碘化物和芳基溴化物与苯硼酸的Suzuki反应有很好的催化活性,但对芳基氯化物的催化活性较低。循环反应三次催化剂活性基本无降低。Plucinski[14]等通过一种简单的途径制备了三种无配体的超顺磁纳米Fe3O4负载钯催化剂(见图1),其直径为7~17nm。AAS测试得2a的钯负载量要大于2b和2c,分别1.0mmol/g,0.06~0.18mmol/g 和 0.06mmol/g。上述催化剂在Suzuki反应中均有较高的催化活性,其中2b的催化活性要高于2a和2c,催化各种溴代芳烃时,转化率可达97%~100%,反应完成后催化剂的回收率可达99%(wt)。重复实验表明,2a和2b重复反应几次后催化活性并无明显降低,但2c在第二次反应后活性明显下降。从TEM表征结果可知,反应时发生了催化剂的团聚从而导致催化活性位的下降。反应的动力学研究证明,影响反应速度的是溴代芳烃的化学性质,而不是扩散速率的限制。钯的浸出测试还表明,催化剂的不稳定性是因为溴代芳烃的存在,而动力学研究结果表明,每次重复实验后催化剂的活性都会有所降低。
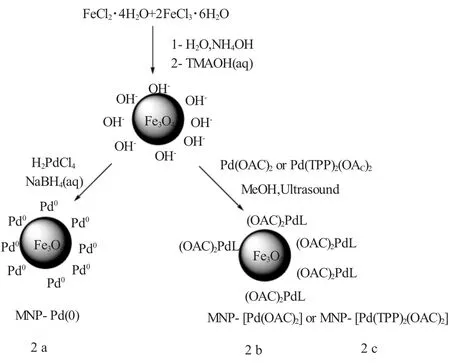
图1 磁性纳米粒子负载钯催化剂的制备Fig.1 The preparation of MNP-supported palladium catalysts
磁性载体修饰后可以增强催化剂的稳定性,减少钯的流失。Amali等[15]将钯固载到用聚乙烯(PEI)修饰过的Fe3O4上制得Pd@Fe3O4催化剂。Suzuki反应结果表明,催化剂对芳基碘化物和溴化物都有很好的催化效果,对芳基氯化物也有75%~95%的转化率。与之对比的Pd/C催化剂的催化效果要低于Pd@Fe3O4催化剂,原因可能是前者的为Pd(0)态存在且钯的尺径为纳米级因而具有更高的催化活性。因为载体表面有高度支链化的PEI,催化剂催化循环10次其催化活性仍未见下降。Yoon等[16]将纳米钯粒子分散在氮掺杂的磁性碳纳米粒子上制得Pd/N-MCNPs催化剂,其钯负载量达40%(wt)。催化剂中的钯未出现聚集,且即使超声5~10min也未流失,这要归因于其载体的形状、结构以及氮掺杂后载体与钯结合紧密。在催化苯硼酸与碘代噻吩的Suzuki反应时,1.2mol%的钯加入量,反应3h即可得到94%的产物收率。镍在Suzuki反应中也有一定的催化活性[17]。Wu等[18]制备了Pd-Ni合金催化剂。催化剂在催化苯硼酸与对溴苯甲醚和碘苯的Suzuki反应时选择性达到100%,催化碘苯与苯硼酸反应5次未见催化活性降低。
Kohsuke等[19]首次用手性2,2-二(二苯基膦基)-1,1-二萘(BINAP)修饰以氧化铁为核心,钯为外壳的FePd纳米粒子得到了两种催化剂FePd-(S)-BINAP和FePd-(R)-BINAP,并用来催化1-溴-2-甲氧基萘与1-萘硼酸的Suzuki反应。催化剂在反应完后能够在外加磁场下分离和再利用(见图2)。
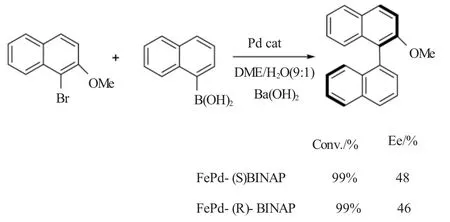
图2 FePd-(S)-BINAP和FePd-(R)-BINAP催化的Suzuki反应Fig.2 The Suzuki reactions catalyzed by FePd-(S)-BINAP and FePd-(R)-BINAP
Gao等[20]将钯固载到具有介孔结构的NiFe2O4载体上,制得了可磁性分离的Pd-NiFe2O4催化剂(Pd/NF300和Pd/NF700)。由于NF300具有一定的碱性且其介孔结构使钯能够很好的分散在载体表面,故催化剂在Suzuki反应中有很高的催化活性,0.08mol%的钯能够很好的催化芳基碘化物和溴化物与苯硼酸反应,对芳基氯化物也有一定的催化活性。催化剂循环反应5次活性没有降低。Babita等[21]以多巴胺修饰的NiFe2O4为载体,制备了NiFe2O4-DA-Pd催化剂。在较高温度(130℃)和较长反应时间(36h)下,通过加入相转移剂TBAB,可以较好地催化芳基氯化物的Suzuki反应。实验结果表明,当选择DMA作溶剂时,反应能得到很高的转化率,但催化剂不能回收,这是由于溶剂与催化剂形成了配合物。碱对反应也有重要影响,当用K2CO3或三乙胺代替K3PO4时产物收率只有10%~20%。
2 含配体磁性钯催化剂
配体能够与钯形成配合物,提高其催化活性,减少钯的流失。将钯配体固载到磁性材料上,制成的磁性钯催化剂有更好的催化效果,是磁性钯催化剂研究的重点。
2.1 无包裹磁性钯配体催化剂
2.1.1 磁性膦钯配体催化剂
膦配体钯催化剂作为Suzuki反应早期研究使用的催化剂,具有与钯配位好,催化活性高的优点。
Zhu等[22]用表面富含磷酸基团、直径为100nm的磁性纳米粒子作为载体制得了钯催化剂(见图3)。催化溴苯和苯硼酸的Suzuki反应结果表明,K2CO3为碱,水作溶剂,10mol%催化剂用量,80℃下反应5h,产物收率为83%,反应3次后未观察到明显的活性降低。
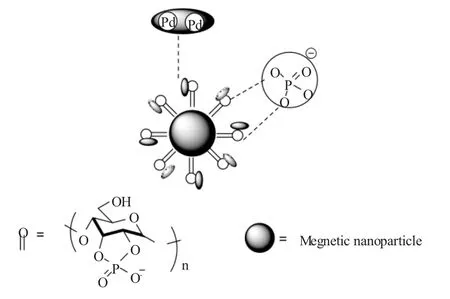
图3 磁性纳米粒子负载钯的纳米催化剂Fig.3 Magnetic nanoparticle-supported palladium nanoparticles catalyst
Duanmu等[23]将膦钯配体固载到Fe2O3上,制备了催化剂(见图4)。该催化剂的特点是可以通过添加不同数量的哌嗪和三聚氯腈来调整配体的级数,从而使催化剂有不同的溶解性,使其较好地分散在不同的溶剂中。催化碘苯与苯硼酸反应的产率为81%,循环使用2次,催化活性变化不大。该催化剂对芳基溴化物也有较好的催化活性。
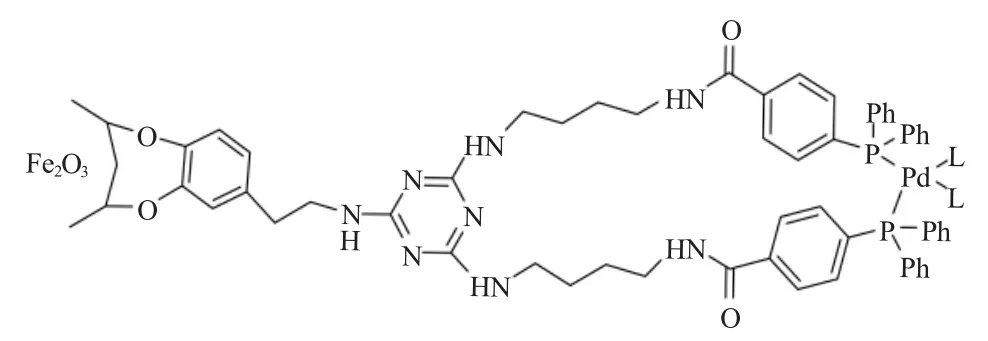
图4 氧化铁纳米粒子负载的钯催化剂Fig.4 Iron oxide nanoparticle-supported Pd catalyst
2.1.2 磁性氮钯配体催化剂
相对于膦配体,氮配体更加绿色环保,且对空气和水不敏感。Taher等[24]将钯-N-杂环卡宾离子液体固载到表面覆盖有离子液体的Fe3O4上,制备了Fe3O4-Pd-NHC催化剂(见图5)。该催化剂对带有不同基团的芳基溴化物与各种芳基硼酸的Suzuki反应均有很好的催化效果。这种高催化活性可能是由于均匀分散在离子液体相中的Pd-NHC易于与反应物接触。催化剂循环反应5次催化活性未明显降低。
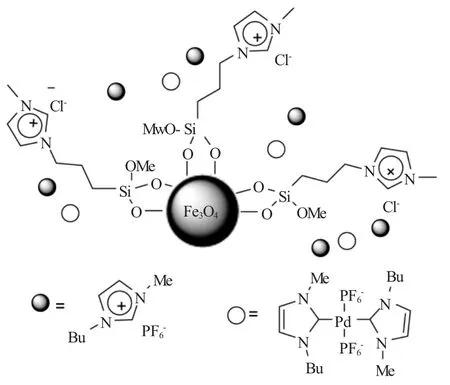
图5 纳米钯-氮杂环卡宾-Fe3O4离子液体催化剂Fig.5 Nano-Pd-NHC-Fe3O4-ionic liquid catalyst
Zhang等[25]制备了两种以上Fe3O4为载体的半均相催化剂Fe3O4-G4-PAMAM dendrimers-Pd(0)和Fe3O4-PEGs-Pd(0)(见图6)。两种催化剂催化活性均高于非均相催化剂Fe3O4-APTS-Pd(0)。在DMF中,以K3PO4为碱时,三种催化剂对芳基碘化物、芳基溴化物与苯硼酸的Suzuki反应均有很高的催化活性,对芳基氯化物也有较好的催化活性。催化活性Fe3O4-G4-PAMAM dendrimers-Pd(0)>Fe3O4-PEGs-Pd(0)>Fe3O4-APTS-Pd(0),这是由于前两者在有机溶剂中的溶解性更好,钯分散的更加均匀。催化剂循环反应4次后,钯含量分别从9.13%(wt),9.11%(wt) 和 9.12%(wt) 下降到 8.82,8.80 和8.79%(wt),催化剂活性基本没有下降。
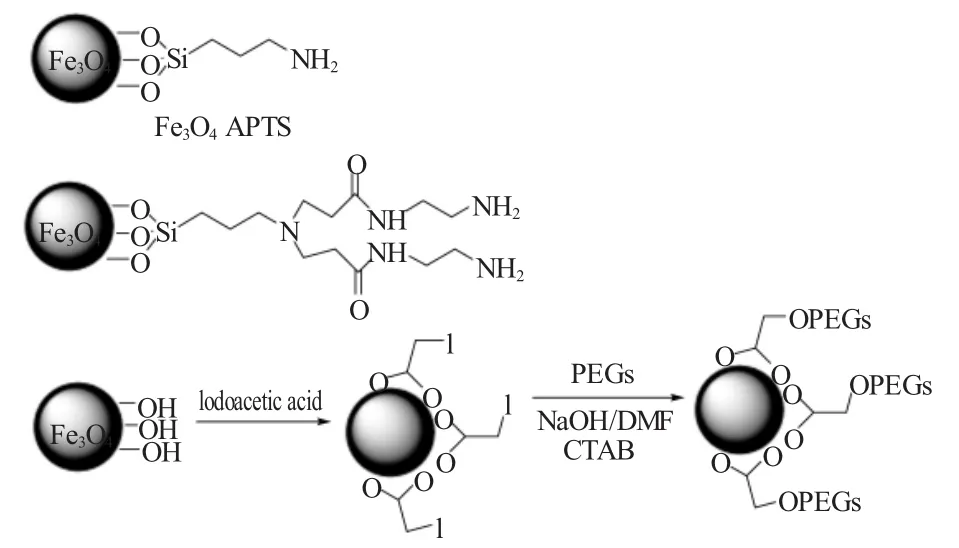
图6 Fe3O4微球作载体的催化剂Fig.6 Fe3O4microspheres-supported catalysts
Gao等[26]将N-杂环卡宾钯配体固载到经油酸改性的磁性γ-Fe2O3表面,制备了稳定、高活性的磁性催化剂(见图7),钯含量达1.5mmol/g。由于其直径很小(~11nm)且外层由有机物包裹,故而能部分溶解于多种有机介质中,其磁性γ-Fe2O3核使得催化剂能够在外加磁场下集中与再分散。催化Suzuki反应结果表明,在DMF溶液中,以Na2CO3为碱,7.3mol%的催化剂量,能有效的催化芳基碘化物和芳基溴化物。催化剂在反应完后经过洗涤和干燥后再参与反应,循环反应5次催化剂活性无明显降低。
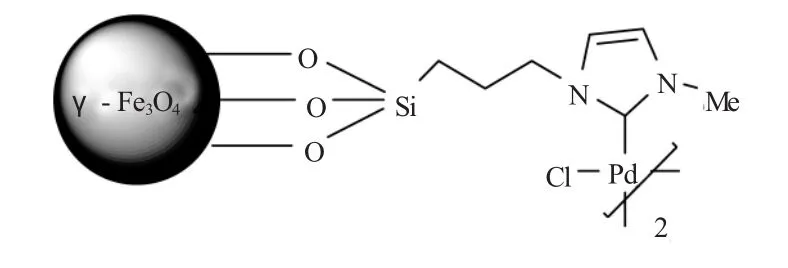
图7 γ-Fe2O3负载的氮杂环卡宾钯配合物Fig.7 Maghemite nanoparticle-supported NHC-Pd complexes
Zhang等[27]以纳米Fe3O4固载钯联吡啶配体催化剂Fe3O4-Bpy-Pd(OAc)2用来催化Suzuki反应(见图8)。催化芳基碘化物和芳基溴化物与芳基硼酸的反应时,产物收率能达到99%(对硝基溴苯为80.3%),对芳基氯化物也有一定的催化活性。未用Fe3O4负载的Pd(OAc)2(Bpya)来催化四溴苯甲醚与苯硼酸的Suzuki反应,只得到了51%的产率,而Fe3O4-Bpy-Pd(OAc)2的反应产率则大于99%,原因可能是后者在THF中有更好的分散度。
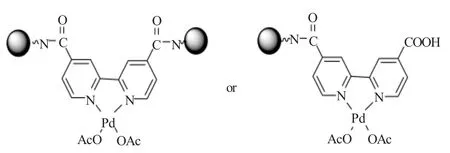
图8 Fe3O4负载钯联吡啶配体催化剂Fig.8 Fe3O4-Bpy-Pd(OAc)2complex catalyst
2.2 包裹磁性钯配体催化剂
磁性粒子在强酸或强碱环境下易受到破坏,如果外面包裹一层保护外壳,可以增强磁性材料的耐酸性和耐碱性,防止磁性材料聚集;外壳如果富含活泼基团时,还可以更好的与其他配体结合来制备催化剂。
2.2.1 碳包裹磁性钯配体催化剂
Schätz等[28]以碳包裹的钴为载体,固载上膦钯配体制备了可回收钯催化剂。该催化剂对芳基碘化物和溴化物与芳基硼酸能在较温和的条件下得到较高的产率,对氯化物也有一定的活性。
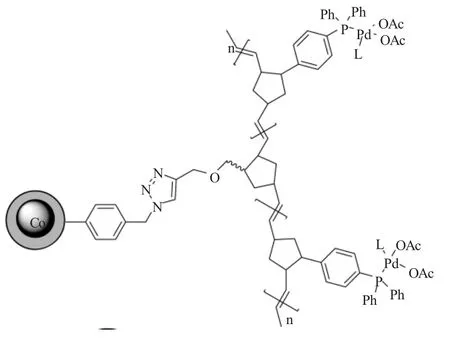
图9 磁性纳米Co/C负载钯催化剂Fig.9 Nano magnetic Co/C supported palladium catalyst
2.2.2 氧化硅包裹磁性钯配体催化剂
氧化硅由于其不易被破坏腐蚀,表面富有活泼的羟基等优点,包裹磁性粒子后能增强其稳定性和更易负载上其他配体。
Shylesh等[29]将 (L)2PdCl2(L=PPh3改性的 Si(OMe)3)负载到具有介孔结构的氧化硅包裹的γ-Fe2O3载体上制备了Pd@Mag-MSN催化剂。氮气吸附-脱附曲线表明,此催化剂载体具有很大的表面积,未负载钯配体前表面积为1140m2/g,负载后为758m2/g。催化剂在二氧六环溶剂中,对芳基碘化物和溴化物与苯硼酸的Suzuki反应有着较高的催化活性,在循环反应3次后活性几乎没有降低,原子吸收光谱分析表明只有不到0.5%的钯残留在反应溶液中。
Costa等[30]以3-氨丙基三乙氧基硅烷修饰的SiO2包裹的Fe3O4为载体,负载2-二苯基膦苯甲醛钯配体制备了Fe3O4@SiO2-iminophosphine-Pd催化剂(见图10)。对苯硼酸和对溴苯甲醚的Suzuki反应结果表明,当以KOH为碱,在THF中时,催化剂的催化效果最好,选择性为100%,产物收率大于99%。该催化剂对芳基溴化物的Suzuki反应有很好的催化效果,但对芳基氯化物没有催化活性。催化剂循环反应两次后催化活性从大于99%下降到69%,其原因是载体被腐蚀和钯出现了聚集。但如果在加入苯硼酸和碱后再加入催化剂,催化剂可循环反应10次,且反应7次催化活性基本不变。
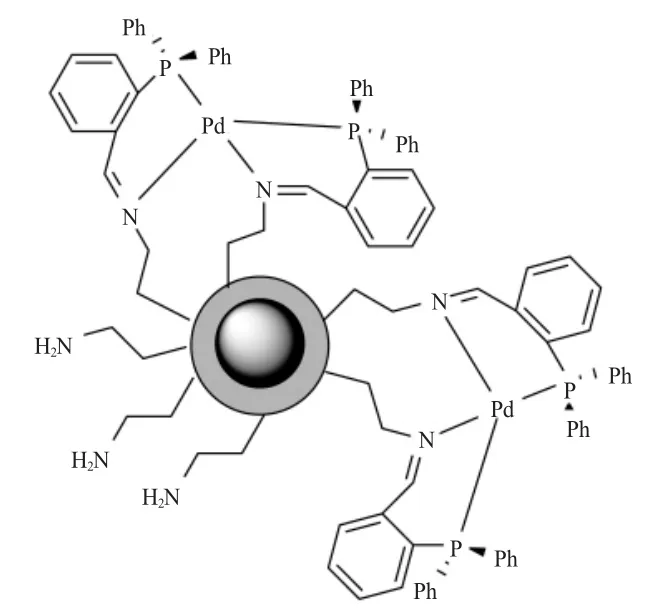
图10 Fe3O4·SiO2负载亚胺膦钯配体催化剂Fig.10 The Fe3O4·SiO2-iminophosphine-Pd catalyst
Jin等[31]将经三乙氧基硅烷修饰的钯配合物固载到稳定的SiO2/Fe3O4粒子表面,制得了磁性纳米粒子负载的(β-氧代亚氨基)膦基钯催化剂(见图11)。该催化剂在催化芳基硼酸和芳基氯代物的Suzuki反应时表现出很高的活性。在水相中,以TBAB作相转移剂,K2CO3为碱,60℃和0.5mol%催化剂用量时对各种活泼的芳基氯代物如对氯苯腈,对硝基氯苯,邻硝基氯苯有着很高的催化活性,对不活泼的芳基氯代物如对氯苯甲醚、对氯苯酚、对氯甲苯等也有不错的催化效果,并且对大位阻的芳基氯代物如2-氯-1,3-二甲基苯与邻或对甲基苯硼酸在延长反应时间时也能得到较高的收率。

图11 磁性纳米粒子负载的(β-氧代亚氨基)膦基钯催化剂的制备Fig.11 Synthesis of the MNP-supported(β-oxoiminato)(phosphanyl)palladium complex
Lv等[32]制备了磁性纳米颗粒固载的双(2-吡啶)二氯钯配体催化剂[6](见图12)。以0.2mol%催化剂,K2CO3为碱,DMF为溶剂,在100℃下对供电子芳基溴化物和吸电子芳基溴化物的Suzuki反应都有很好的催化效果,在循环反应5次后对对溴苯乙酮和苯硼酸的催化依然能达到95%以上的产物收率,且对空气和水不敏感,但即使在加大催化剂用量和延长反应时间下,对芳基氯代物和杂环溴化物的催化效果依然难以令人满意。
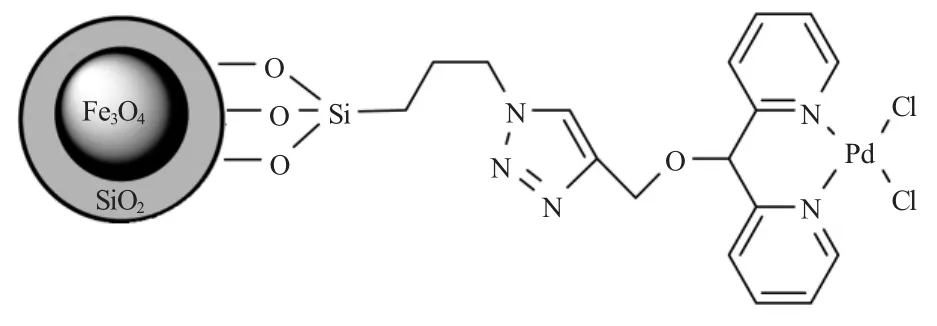
图12 磁性纳米颗粒固载的双(2-吡啶)二氯钯配体催化剂的制备Fig.12 Preparation of MNP-supported di(2-pyridyl)methanol-Pd complex
Shylesh等[33]将带有三甲氧基硅烷的二价钯膦配合物固载到磁性纳米颗粒上,用来催化溴苯和碘苯的Suzuki反应(见图13)。以Cs2CO3为碱,二氧六环为溶剂,1mol%催化剂用量,80℃下反应15h产物收率大于99%。在此条件下该非均相催化剂对芳基氯化物也能得到34%的产物收率,催化剂在循环反应7次后收率仍能达到92%。
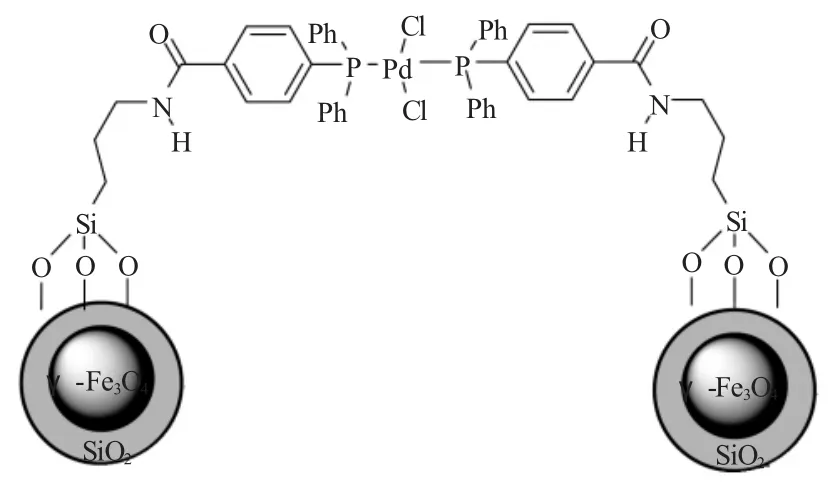
图13 磁性纳米粒子负载的二价钯膦配合物Fig.13 Pd(II)-phosphine complexes supported on magnetic nanoparticles
2.2.3 聚合物包裹磁性配体催化剂
聚合物有制备方便、价格低廉、来源广泛等优点,也被用来包裹磁性粒子以增强其稳定性。
Stevens等[34]用乳液聚合法将N-杂环卡宾钯配体固载到外包有聚合物壳的γ-Fe2O3超顺磁性纳米粒子上,制备了稳定的、可溶性的催化剂(见图14)。以DMF为溶剂,Na2CO3作碱,催化芳基碘代物和溴代物与苯硼酸的偶联反应具有非常高的催化活性。催化剂在反应完成后在外加磁场下与反应体系相分离,循环使用5次后发现,每次能回收到88%±3%的催化剂,且未观察到催化剂有明显的活性降低。
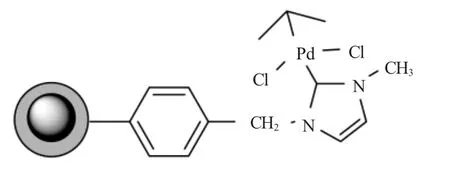
图14 氧化铁纳米粒子负载氮杂环卡宾钯配合物Fig.14 Iron oxide nanoparticle-supported Pd-NHC complex
Heuzé等[35]将双环己烷-双膦钯配体固载到具有核壳结构的磁性颗粒上(见图15),制得的催化剂对芳基碘化物和溴代物的Suzuki反应有非常好的催化效果,但对芳基氯化物与苯硼酸的反应需要更长的反应时间和更大的催化剂用量。反应在循环25次后活性未明显降低。
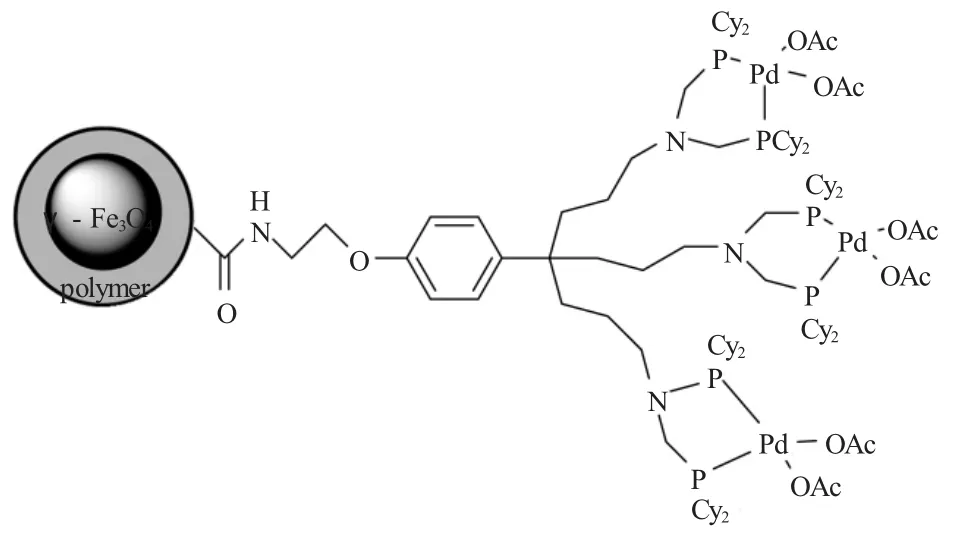
图15 树枝结构的核壳超顺磁纳米粒子的合成Fig.15 Synthesis of dendron-functionalized core-shell super paramagnetic nanoparticles
3 结 语
催化Suzuki反应的磁性钯催化剂,由于其具有分离容易、易回收利用、催化效果好等优点,近年来受到越来越多的关注。但还存在其表征方法较少,对芳基氯化物的催化活性不高,反应机理和失活机制不明确等不足,需要以后进一步的研究。
[1]MIYAURA N,YAMADA K,SUZUKI A.A new stereospecific cross-coupling by the palladium-catalyzed reaction of 1-alkenylboranes with 1-alkenyl or 1-alkynyl halides[J].Tetrahedron Letters,1979,36:3437~3440.
[2]MIYAUR N,YANAGI T,SUZUKI A.The palladium-catalyzed cross-coupling reaction of phenylboronic acid with haloarenes in the presence of bases[J].Synthetic Communications,1981,11(7):513~515.
[3]MIYAURA N,SUZUKI A.Palladium-catalyzed cross-coupling reactions of organoboron compounds [J].Chemical Reviews,1995,95(7):2457~2483.
[4]KOTHA S,LAHIRI K,KASHINATH D.Recent applications of the Suzuki-Miyaura cross-coupling reaction in organic synthesis[J].Tetrahe-Dron,2002,58:9633~9695.
[5]BAUDOIN O,CESARIO M,GUÉNARD D,et al.Application of the palladium-catalyzed Borylation/Suzuki coupling (BSC)reaction to the synthesis of biologically active biaryl lactams[J].The Journal of Organic Chemistry,2002,67:1199~1207.
[6]ROBERTO D A,ARSENIA R.Short synthesis of undecylprodigiosine.A new route to 2,2'-bipyrrolyl-pyrromethene systems[J].Synlett,1996,3:513~514.
[7]CORMA A,DAS D,GARCÍA H,et al.A periodicmesoporous organosilica containing a carbapalladacycle complex as heterogeneous catalyst for Suzuki cross-coupling[J].Journal of Catalysis,2005,229:322~331.
[8]SEKI M.Recent advances in Pd/C-catalyzed coupling reactions[J].Synthesis,2006:2975~2992.
[9]LUO F T,XUE C,KO S L,et al.Preparation of polystyrene-supported soluble palladacycle catalyst for Heck and Suzuki reactions[J].Tetrahedron,2005,61:6040~6045.
[10]POLSHETTIWAR V,LUQUE R,FIHRI A,et al.Magnetically recoverable nanocatalysts[J].Chemical Reviews,2011,111(5):3021~3666.
[11]刘诗咏,吴家守,蒋华江,等.正电性磁性氧化铁胶粒负载钯催化的 Suzuki偶联反应[J].有机化学,2009,29(10):1587~1592.
[12]CANO R,RAMÓN D J,YUS M.Impregnated palladium on magnetite,a new catalyst for the ligand-free cross-coupling Suzuki-Miyaura reaction[J].Tetrahedron,2011,67:5432~5436.
[13]ZHOU S,JOHNSON M,VEINOT J G C.Iron/iron oxide nanoparticles:a versatile support for catalyticmetals and their application in Suzuki-Miyaura cross-coupling reactions[J].Chemical Communications,2010,46:2411~2413.
[14]LASKA U,FROST C G,PRICE G J,et al.Easy-separable magnetic nanoparticle-supported Pd catalysts:Kinetics,stability and catalyst re-use [J].Journal of Catalysis,2009,268(2):318~328.
[15]AMALI A J,RANA R K.Stabilisation of Pd(0)on surface functionalised Fe3O4nanoparticles:magnetically recoverable and stable recyclable catalyst for hydrogenation and Suzuki-Miyaura reactions[J].Green Chemistry,2009,11:1781~1786.
[16]YOON H,KO S,JANG J.Nitrogen-doped magnetic carbon nanoparticles as catalyst supports for efficient recovery and recycling[J].Chemical Communications,2007:1468~1470.
[17]PARK J,KANG E,SON S U,et al.Monodisperse nanoparticles of Ni and NiO:synthesis,characterization,self-assembled superlattices,and catalytic applications in the Suzuki coupling reaction[J].Advanced Materials,2005,17:429~424.
[18]WU Y,WANG D,ZHAO P,et al.Monodispersed Pd-Ni nanoparticles:composition control synthesis and catalytic properties in the Miyaura-Suzuki reaction [J].Inorganic Chemistry,2011,50:2046~2048.
[19]MORI K,KONDO Y,YAMASHITA H.Synthesis and characterization of FePd magnetic nanoparticles modified with chiral BI-NAP ligand as a recoverable catalyst vehicle for the asymmetric coupling reaction[J].Physical Chemistry Chemical Physics,2009,11:8949~8954.
[20]GAO Z,FENG Y,CUI F,et al.Pd-loaded superparamagneticmesoporous NiFe2O4as a highly active and magnetically separable catalyst for Suzuki and Heck reactions [J].Journal of Molecular Catalysis A:Chemical,2011,336:51~57.
[21]BARUWATI B,GUIN D,MANORAMA S V.Pd on surfacemodified NiFe2O4nanoparticles:A magnetically recoverable catalyst for Suzuki and Heck reactions[J].Organic Letters,2007,9(26):5377~5380.
[22]ZHU Y,SHIP C P,EMI A,et al.Supported ultra small palladium on magnetic nanoparticles used as catalysts for Suzuki cross-coupling and Heck reactions[J].Advanced Synthesis &Catalysis,2007,349:1917~1922.
[23]DUANMU C,SAHA I,ZHENG Y.Dendron-functionalized superparamagnetic nanoparticles with switchable solubility in organic and aqueous media:matrices for homogeneous catalysis and potential mri contrast agents [J].Chemistry of Matarials,2006,18:5973~5981.
[24]TAHER A,KIM J,JUNG J B,et al.Highly active and magnetically recoverable Pd-NHC catalyst immobilized on Fe3O4nanoparticle-ionic liquid matrix for Suzuki reaction in water[J].Synlett,2009,15:2477~2482.
[25]ZHANG Y,WEI X,YAO Z.Synthesis of Fe3O4microspheressupported catalysts for Suzuki coupling reaction[J].Chinese Journal of Chemistry,2010,28:2274~2280.
[26]STEVENS P D,LI G,FAN J,et al.Recycling of homogeneous Pd catalysts using superparamagnetic nanoparticles as novel soluble supports for Suzuki,Heck,and Sonogashira cross-coupling reactions[J].Chemical Communications,2005,35:4435~4437.
[27]ZHANG Y Q,WEI X W,YU R.Fe3O4nanoparticles-supported palladium-bipyridine complex:Effective catalyst for Suzuki coupling reaction[J].Catalysis Letters,2010,135:256~262.
[28]SCHÄTZ B A,LONG T R,GRASS R N.Immobilization on a nanomagnetic Co/C surface using ROM polymerization:Generation of a hybrid material as support for a recyclable palladium catalyst[J].Advanced Functional Materials,2010,20:4323~4328.
[29]SHYLESH S,LEI W,DEMESHKO S,et al.Facile synthesis of mesoporous magnetic nanocomposites and their catalytic application in carbon-carbon coupling reactions[J].ChemCatChem,2010,2:1543~1547.
[30]COSTA N J S,KIYOHARA P K,MONTEIRO A L.A singlestep procedure for the preparation of palladium nanoparticles and a phosphine-functionalized support as catalyst for Suzuki cross-coupling reactions[J].Journal of Catalysis,2010,276:382~389.
[31]JIN M J,LEE D H.A practical heterogeneous catalyst for the Suzuki,Sonogashira,and Stille coupling reactions of unreactive aryl chlorides [J].Angewandte Chemie International Edition,2010,49:1119~1122.
[32]LV G,MAIL W,JIN R,et al.Immobilization of dipyridyl complex to magnetic nanoparticle via click chemistry as a recyclable catalyst for Suzuki cross-coupling reactions [J].Synlett,2008(9):1418~1422.
[33]SHYLESH S,WANG L,THIEL W R.Palladium(II)-phosphine complexes supported on magnetic nanoparticles:filtration-free,recyclable catalysts for Suzuki-Miyaura cross-coupling reactions[J].Advanced Synthesis & Catalysis,2010,352:425~432.
[34]STEVENS P D,FAN J,GARDIMALLA H M R,et al.Superparamagnetic nanoparticle-supported catalysis of Suzuki cross-coupling reactions[J].Organic Letters,2005,7:2085~2088.
[35]ROSARIO-AMORIN D,WANG X,GABOYARD M,et al.Dendron-functionalized core-shell superparamagnetic nanoparticles:magnetically recoverable and reusable catalysts for Suzuki C-C cross-coupling reactions[J].Chemistry-A European Journal,2009,15:12636~12643.
Progress in Research on Suzuki Reaction over Magnetical Recoverable Palladium(Pd)-Based Catalysts
WAN Hong-Liang2and BAI Xue-Feng1,2
(1.Institute of Petrochemistry,Heilongjiang Academy of Sciences,Harbin 150040,China;2.College of Chemistry and Material Science,Heilongjiang University,Harbin 150080,China)
The Suzuki cross-coupling reactions catalyzed by palladium catalysts to form the carbon-carbon bonds between aryl halides and aryl boronic acids is one of the most important way of synthesizing biphenyl compound.Compared with the traditional homogeneous catalysts whose disadvantages are low catalyst recycling rate and polluting products,magnetic palladium-based catalysts are easy separable and recycled,which is suitable for industrial application and attracts much greater attention.This paper introduces some latest development process in the preparation of no-ligand magnetic palladium catalysts,palladium-based catalysts supported on no-coated magnetic particles and shell-core structure palladium-based catalysts support on magnetic particles coated by the materials,such as carbons,silica,polymers and their application in Suzuki reactions.
Magnetic;palladium catalysts;Suzuki reaction
TQ 426.94
A
1001-0017(2012)01-0048-06
2011-05-27 *
黑龙江省科学院科研基金项目
万红亮(1986-),男, 人,在读硕士研究生。
**通讯联系人:白雪峰(1964-),男,汉族,博士,研究员,主要从事工业催化方面研究。
