5-氟尿嘧啶在pH敏感型分子筛控释载体中的缓释行为
2012-01-08吴都督龙烁杭施志海吴锐彬
吴都督,陈 稚,龙烁杭,施志海,吴锐彬
(1.广东医学院 药学院,广东 东莞523808; 2.广东医学院 分析中心,广东 东莞523808)
5-氟尿嘧啶在pH敏感型分子筛控释载体中的缓释行为
吴都督1*,陈 稚2,龙烁杭1,施志海1,吴锐彬1
(1.广东医学院 药学院,广东 东莞523808; 2.广东医学院 分析中心,广东 东莞523808)
以肠溶性的羟丙基甲基纤维素邻苯二甲酸酯(HPMCP)作为包覆材料,制备了HPMCP包覆的SBA-15介孔分子筛药物控释载体(HPMCP/SBA-15),并考察了抗癌药物5-氟尿嘧啶(5-Fu)负载于控释载体后,在不同pH释放环境中的释放行为.结果表明,在模拟胃液中(pH=1.2),HPMCP能明显地延缓5-Fu的释放速度;药物释放4h后,其释放率仅为15%.而在模拟肠液中(pH=7.5)HPMCP迅速溶解,对5-Fu释放速度的影响甚微;药物释放4h后,释放率可达到80%.与此同时,包覆膜的干燥温度影响5-Fu的释放行为,干燥温度越高,药物在模拟胃液中的释放速度越慢.
5-氟尿嘧啶;羟丙基甲基纤维素;邻苯二甲酸酯;pH敏感型介孔分子筛;药物缓释行为
5-氟尿嘧啶(5-Fu)是常用的治疗癌症(如肠癌)的药物[1].但在传统口服给药方式中,药物分子在到达肠道以前大部分被胃吸收或者被胃中的酶所破坏,这样不仅降低了药物到达肠道后的有效浓度,而且5-Fu的毒副反应容易对胃、肝等正常器官造成伤害[2].因此开发一些新型的肠道靶向药物控释系统具有重要的实用价值和广阔的应用潜力.最近,纳米技术的发展激发了广大研究者使用新开发的纳米材料作为医药载体的兴趣.而硅基介孔分子筛因具有分布均匀且连续可调的纳米孔径、高比表面积、大孔容、表面可官能团化和良好的生物相容性等优点,已成为一种很有应用潜力的新型药物载体[3].2001年,VALLET-REGÍ首次报道了介孔分子筛的药物输送性能,将硅基介孔分子筛的应用拓展到药物制剂领域[4].随后,相继有几个研究小组分别报道了以介孔分子筛作药物载体的安全性和生物相容性等方面的研究成果,并对调控药物释放速度的影响因素,如介孔孔径、分子筛表面官能团、药物释放环境等进行了探索性的研究,这些研究结果表明在以硅基介孔分子筛为载体的药物体系中,药物分子能够以分子级别分布在介孔孔道中,从而可更加精确地调控药物释放速度,实现对药物的定时定量释放[5-7].
与此同时,人体环境是一个很复杂的生理环境,比如整个相连通的消化系统中,胃液的pH是1.2左右,十二指肠中的pH是5.4左右,而小肠部位的pH又是7.4左右,所以复杂的人体环境为介孔分子筛这种新型载体的发展也提出了复杂的要求,“靶向释放”这种更高级的药物释放模式被人们提了出来.鉴于胃和肠道各自环境中pH的差异,设计一种pH控制的药物释放载体应用于药物控释应该是一个切合实际的研究方向.如果设计出的pH控制药物释放系统,不仅能够很明显地延缓药物(如5-Fu)在胃液中的释放速度,而且又不限制药物在其他器官(如肠道)中的释放,那么所得到的应该是一个好的pH敏感的药物释放系统.该控释系统不仅可阻止毒副反应对胃、肝等器官的损害,还可提高药效,因而在癌症(如肠癌)治疗中应具有良好的应用前景.然而,到目前为止,基于介孔分子筛这种新型载体的pH敏感药物控释研究却只有很少的报道.YANG等人利用羧基官能团化SBA-15表面的-COOH和聚电解质PDDA之间的静电相互作用,开发了一种pH敏感药物释放载体.该系统在碱性条件下,利用聚合物将药物束缚在介孔孔道内,使之不能很快释放出来.而在酸性条件下,聚合物与分子筛表面的作用力消失,药物则能够快速的被释放.遗憾的是,该控释系统对酸过于敏感,应用价值不大[8].
羟丙基甲基纤维素邻苯二甲酸酯(HPMCP)是一种良好的pH敏感包覆材料,自从1971年上市以来,常作为纤维素的衍生物用于包衣,并在药学行业中广泛应用[9].它具有非常好的成膜能力,所以在制备过程中无须任何其他处理,就能与负载药物的载体紧密结合.操作过程非常简单,而且对制备过程无特别要求,因此是一种理想的介孔分子筛的包覆材料.因此,作者以pH敏感的HPMCP作为包覆材料,通过提拉的方法,制备HPMCP包覆的SBA-15介孔分子筛药物控释载体(HPMCP/SBA-15),同时利用5-Fu与分子筛的表面硅羟基的耦合将5-Fu负载于载体中,并考察其在模拟胃液(SGF)和模拟肠液(SIF)中的药物控释行为,以验证HPMCP/SBA-15载体的pH敏感性能.
1 实验部分
1.1 试剂
5-氟尿嘧啶,分析纯,Sigma公司;羟丙基甲基纤维素邻苯二甲酸酯,分析纯,广州市鼎泰树脂有限公司;P123(H(CH2CH2O)20(CH2CH2CH2O)70(CH2CH2O)20H),分析纯,Aldrich公司;正硅酸乙酯(TEOS),分析纯,天津市化学试剂一厂;磷酸二氢钾,磷酸氢二钾,分析纯,天津科密欧化学试剂公司;无水乙醇,盐酸,分析纯,广东番禺化学试剂厂.
1.2 介孔分子筛SBA-15的合成
在磁力搅拌下,将4.0g表面活性剂P123加入到80mL 2.0mol·L-1的HCl溶液中,温度恒定在40℃,搅拌至P123完全溶解后,加入5.0mL的TEOS.反应混合物在40℃下恒温搅拌24h后转移至100 mL的晶化釜中,于100℃下晶化36h.所得产物过滤后,用去离子水和无水乙醇反复冲洗直至滤液的pH为7.0左右,然后样品在80℃下干燥,最后将样品在索氏抽提器中用无水乙醇萃取48h,80℃下烘干即得纯硅基介孔SBA-15.
1.3 药物吸附
分别取1.0g SBA-15粉末和1.5g 5-氟尿嘧啶,加入到250mL的去离子水和甲醇的等体积混合溶剂中.室温搅拌12h后过滤,所得固体在80℃烘箱中干燥.取2.0mL滤液稀释到25.0mL,用WFZ-26A型紫外可见分光光谱仪(天津拓普仪器有限公司)测定溶液中的5-氟尿嘧啶的浓度,按公式(1)确定载药量.

1.4 HMPCP/SBA-15的制备和药物缓释行为的测定
取0.20g负载了药物的SBA-15粉末,在5.0MPa的轴向压力下制得13mm×3mm的药片.然后将2.0g的HPMCP加入到总体积为50mL的甲醇和去离子水的混合溶剂中(甲醇和水的体积比为1∶1),搅拌至HPMCP全部溶解.接着以提拉的方式在SBA-15药片上包覆HPMCP聚合物,提拉的速度控制在20 cm/min.每个药片的HPMCP包覆过程重复3次.将包覆有HPMCP聚合物膜的药片置于烘箱中干燥30 min,然后20℃下真空干燥12h备用.
在100r/min的搅速下,将以上所得药片分别在模拟胃液(pH=1.2,HCl水溶液)和模拟肠液(pH=7.4,磷酸氢二钾和磷酸二氢钾的缓冲溶液)中研究药物的缓释行为,实验温度控制在37℃.用WFZ-26A型紫外可见分光光谱仪测定溶液中释放出来的5-氟尿嘧啶的浓度,并按公式 (2)确定药物释放率.
药物释放率 = (释放过程中游离的药物质量/负载的药物质量)×100% (2)
1.5 材料表征
透射电镜(TEM)测试在日立H 600透射电镜仪上进行,具体操作为:首先把少量样品放入称量瓶内,乙醇作分散剂,超声振荡20min后,用洁净的滴管取一滴于铜网上,干燥后进行观察,操作电压为200kV.
红外光谱在FTS175C-UMA500型傅立叶红外光谱仪(美国Bio-Rad公司)上测得,扫描累加128次.采用KBr压片法进行测定.
X射线衍射(XRD)测试于日本理学(Rigaku)D/max-γA型X射线衍射仪上进行,使用Cu Kα辐射(λ=0.154 2nm),金属Ni滤波,石墨单色器,电压40kV,电流30mA,闪烁记数器记录强度.
N2吸附-脱附和孔分布在美国Tristar 3000自动物理吸附仪上进行.样品在80℃和1.33×10-4Pa下脱气12h后,在-196℃下进行测定,并由Brunauer-Emmett-Teller(BET)方程计算样品的比表面积,用Barrett-Joyner-Halenda(BJH)方法和N2吸附-脱附曲线中的脱附分支计算材料的孔分布.
2 结果与讨论
2.1 材料的表征分析
2.1.1 SBA-15介孔分子筛的透射电镜分析
SBA-15介孔分子筛的透射电镜图如图1所示.由图1可见,所合成的SBA-15长度约为10~20μm,并具有很好的直径均一的棒状结构.
2.1.2 SBA-15介孔分子筛的红外光谱分析
表1列出了SBA-15介孔分子筛吸附5-Fu前后的主要红外特征吸收峰.由表1可见,纯SBA-15介孔分子筛在3 465cm-1、1 644cm-1、1 090cm-1、971.6cm-1和 802.5cm-1出现特征吸收峰.其中,3 465cm-1属于分子筛表面吸附的水的O-H伸缩振动,1 644cm-1属于吸附的水的O-H弯曲振动,1 090 cm-1属于Si-O的不对称伸缩振动,971.6cm-1和802.5cm-1属于SiO-H 的弯曲振动[10].当SBA-15介孔分子筛吸附5-Fu后,其表面除了依然有上述硅骨架的特征峰外,还在1 730cm-1、882.6cm-1和753.3 cm-1出现了新的特征峰.其中,1 730cm-1属于5-Fu的CO伸缩振动,882.6cm-1属于-CFCH-中C-H的面外弯曲振动,753.3cm-1属于-CFCH-中C-H的面外变形振动[11].这些属于5-Fu的特征峰的出现,意味着5-Fu已成功地负载到介孔SBA-15的表面.
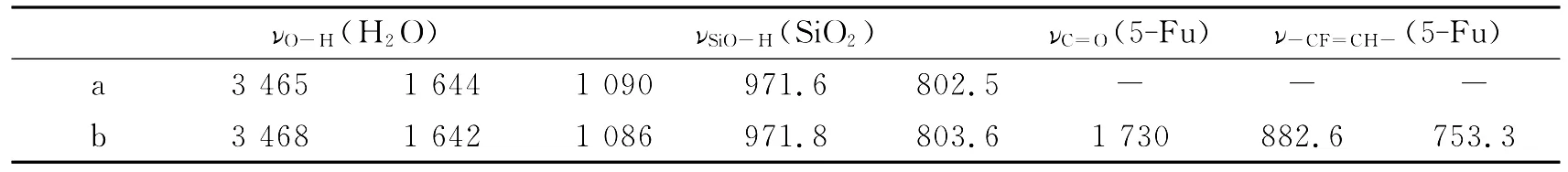
表1 SBA-15介孔分子筛的主要红外吸收峰Table 1 Principal IR band frequencies of SBA-15mesoporous molecular sieves cm-1
2.1.3 SBA-15介孔分子筛的X射线衍射分析
图2是负载5-Fu前后的SBA-15介孔分子筛的XRD图.由图可见,SBA-15在负载5-Fu前后均在2θ=1.0°左右存在一个六方晶系d100衍射主峰,与文献报道一致[12].该衍射峰是典型的SBA-15介孔材料的特征峰,表明样品长程有序的六方孔道结构已经形成.另外,SBA-15在负载5-Fu后,其XRD图基本不变,仅峰强度略有降低,这表明5-Fu在SBA-15上负载并不会改变分子筛的有序结构,但是会使其介孔结构的有序性降低.
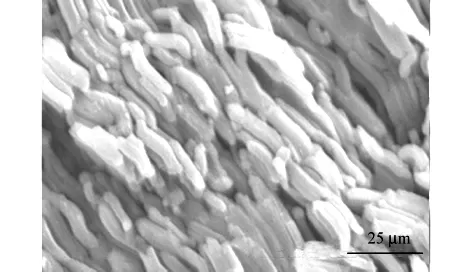
图1 SBA-15介孔分子筛的透射电镜图Fig.1 Typical TEM image of SBA-15 mesoporous molecular sieves
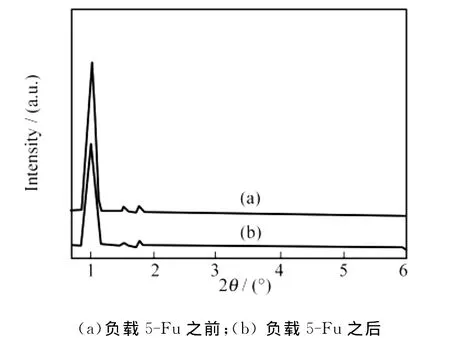
图2 SBA-15介孔分子筛的XRD图Fig.2 Typical XRD image of SBA-15 mesoporous molecular sieves
2.1.4 SBA-15介孔分子筛的N2吸附-脱附和孔分布图
图3是羧基官能团化SBA-15吸附5-Fu前后的N2吸附脱附和孔分布图.如图3所示,两样品在吸附5-Fu前后吸附脱附等温线都呈现了典型的Ⅳ型曲线并保留着完整的H1滞后环,这说明所合成的SBA-15具有有序的介孔结构.同时,发现当分子筛在吸附药物后,其比表面积由543.7m2/g降至509.5m2/g,孔容由1.023cm3/g降至0.962cm3/g,孔径由5.9nm降为5.6nm.分子筛吸附药物后,其比表面积、孔径和孔容的降低,再次证实了5-Fu分子被成功地负载到介孔SBA-15的孔道内.另外,根据UV-Vis所测得的浓度,计算出5-Fu在SBA-15介孔分子筛上的药物负载量为10.3%.

图3 SBA-15介孔分子筛的N2吸附-脱附图和孔分布曲线(插图)Fig.3 BET isotherms and pore size distributions(inserts)patterns of SBA-15mesoporous molecular sieves
2.2 药物缓释行为
采用体外模拟释放实验来评价药物载体对5-Fu的缓释行为.图4是SBA-15载药粒和HPMCP/SBA-15载药粒在模拟胃液(a)和模拟肠液(b)中的缓释行为.从图4(a)中可以看到,没有包覆HPMCP的SBA-15载药粒在模拟胃液中释放5-Fu的速度很快,2h后药物基本释放完全.而有HPMCP包覆的SBA-15载药粒在模拟胃液中释放5-Fu的速度较慢(见图4(a)),2h之前药物的释放不超过10%,而到达4h时,被释放出来的5-Fu也仅有15%,即使24h后,药物的释放也仅达到50%,这表示HPMCP/SBA-15可以很好地延缓5-Fu在模拟胃液中的释放速度.由于食物在胃中的停留时间一般为4h,因此我们认为HPMCP/SBA-15可以很好的在胃环境中保护吸附于介孔孔道中的药物分子.另外,我们发现,在模拟肠液中,药物缓释过程基本不受所包覆的HPMCP膜层的影响,包覆前后的药物缓释曲线变化不大,5-Fu在模拟肠液中均可快速释放,这一点,恰恰可以满足5-Fu对于肠道疾病治疗(如肠癌)的需要.因为该药物缓释系统,不仅可以明显延缓5-Fu在胃液中的释放速度,而且又不影响5-Fu在肠液中的释放,可减少胃液对药物的影响,因而是一种理想的pH敏感载体.
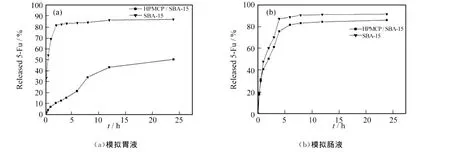
图4 5-Fu在纯SBA-15和 HPMCP/SBA-15中的释放曲线Fig.4 5-Fu released profiles of SBA-15and HPMCP/SBA-15in different solutions
另外,HPMCP(pKa值约为4.5~5.5)是一种生物兼容和pH敏感的聚合物,其表面存在一个pH控制的疏水作用和静电斥力之间的敏感平衡.在模拟胃液中,HPMCP会因为表面羧基被质子化,疏水作用占主导地位,从而包覆在SBA-15药片上不溶解,使药物难以释放.因此,膜的厚度对载体的缓释效果有着重要的影响,而干燥温度无疑是影响膜厚度的一个重要因素[10].因此,我们考察了膜的干燥温度对药物释放行为的影响.从图5(a)可见,提高干燥温度对药物在模拟胃液中的释放速度减缓效果非常明显,样品干燥温度越高,5-Fu的释放速度越慢,这说明提高干燥温度可以使HPMCP的膜层变得更加致密,使药物的缓释效果增强.而在模拟肠液中,我们发现提高制样时的干燥温度对5-Fu的释放速度基本没有影响,5-Fu在短时间内均可快速释放(见图5(b)),这主要是因为HPMCP在模拟肠液中,其表面的静电斥力起主导作用,可使其快速溶解的缘故[13].
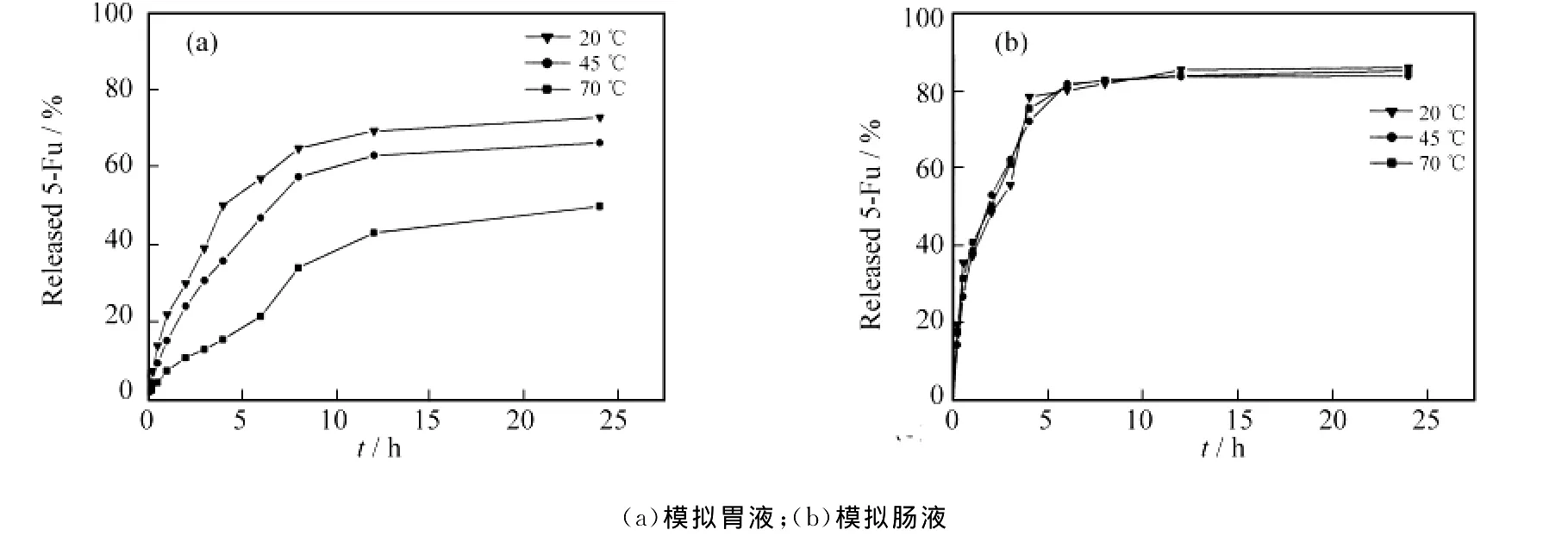
图5 膜的不同干燥温度对5-Fu在HPMCP/SBA-15中的释放的影响Fig.5The effect of drying temperature of HPMCP on the release of 5-Fu from HPMCP/SBA-15
结论:通过简单的提拉方法,将HPMCP聚合物膜成功包覆于负载有5-Fu的SBA-15药片的表面,制备了pH敏感型药物缓释材料HPMCP/SBA-15,并且考察了其在模拟胃液和模拟肠液中的缓释行为.研究发现,在包覆HPMCP后,载体HPMCP/SBA-15能够有效地减缓抗癌药物5-Fu在模拟胃液中的释放速度.同时,又不影响药物在模拟肠液中的释放速度,是一种较好的pH敏感型药物缓释材料.而且,膜的干燥温度越高,载体的缓释性能越强.HPMCP/SBA-15良好的pH敏感性能,有望使其实现对肿瘤组织的主动靶向和控制释药.
[1]陈志和,黄灵珍.奥沙利铂联合5-氟尿嘧啶、亚叶酸钙治疗晚期大肠癌的临床观察 [J].医学理论与实践,2011,24(5):543-544.
[2]季风存,程若川,康俊升.5-氟尿嘧啶诱导直肠癌HR8348细胞凋亡作用的研究 [J].中国普外基础与临床杂志,2003,10(6):564-567.
[3]ANGELOS S,JOHANSSON E,STODDART J F,et al.Mesostructured silica supports for functional materials and molecular machines[J].Adv Funct Mater,2007,17(14):2261-2271.
[4]VALLET-REGI M,RAMILA A,DEL REAL R P,et al.A new property of MCM-41:Drug delivery system[J].Chem Mater,2001,13(2):308-311.
[5]RADU D R,LAI Cheng Yu,JEFTINIJA K,et al.A polyamidoamine dendrimer-capped mesoporous silica nanospherebased gene transfection reagent[J].J Am Chem Soc,2004,126(41):13216-13217.
[6]SONG S W,HIDAJAT K,KAWI S.Functionalized SBA-15materials as carriers for controlled drug delivery:influence of surface properties on matrix-drug interactions[J].Langmuir,2005,21(21):9568-9575.
[7]HORCAJADA P,RAMILA A,GERARD F.Influence of superficial organic modification of MCM-41matrices on drug delivery rate[J].Solid State Sci,2006,8(10):1243-1249.
[8]YANG Qing,WANG Shi Chao,FAN Pei Wei,et al.pH-responsive carrier system based on carboxylic acid modified mesoporous silica and polyelectrolyte for drug delivery[J].Chem Mater,2005,17(24):5999-6003.
[9]张宪康,沈健平.肠溶性药用辅料HPMCP的合成研究 [J].中国医药工业杂志,1993,24(3):104-107.
[10]徐武军,高 强,徐 耀,等.基于HPMCP包覆介孔SBA-15的pH敏感药物缓释系统[J].化学学报,2008,66(14):1658-1662.
[11]梁丽芸,郭 俊,谭必恩.5-氟尿嘧啶明胶微球的制备、表征及释药性能 [J].广东化工,2009,36(5):117-119.
[12]ZHAO Dong Yuan,FENG Jiang Lin,HUO Qi Sheng,et al.Triblock copolymer syntheses of mesoporous silica with heriodic 50to 300angstrom pores[J].Science,1998,279:548-552.
[13]QIU Yong,PARK K.Environment-sensitive hydrogels for drug delivery[J].Adv Drug Deliver Rev,2001,53(3):321-339.
Release behavior of 5-fluorouracil in pH-sensitive molecular sieve drug release carrier
WU Du-du1*,CHEN Zhi2,LONG Shuo-hang1,SHI Zhi-hai1,WU Rui-bin1
(1.SchoolofPharmacy,GuangdongMedicalCollege,Dongguan523808,Guangdong,China;2.CenterofAnalysis,GuangdongMedicalCollege,Dongguan523808,Guangdong,China)
A pH-sensitive mesoporous molecular sieve as drug release carrier was synthesized by coating SBA-15tablet with hydroxypropyl methylcellulose phthalate(HMPCP)so as to improve the cancer targeting ability and selectivity of antineoplastic agent 5-fluorouracil(5-Fu).Into the drug release carrier(HPMCP/SBA-15)was loaded 5-Fu by adsorption in the mixed solution of water and methanol(volume ratio 1:1).The releasing behavior of loaded 5-Fu in two kinds of release fluids with different pH environment,simulated intestinal fluid(SIF,pH=7.4)and simulated gastric fluid(SGF,pH =1.2),was examined.Results indicate that in SGF the coating carrier can effectively delay the release rate of 5-Fu,with release rate being only 15%after 4hof drug release.However,in SIF it has no obvious effect on the drug delivery rate,possibly due to the dissolution of HPMCP in SIF;and in this case the release rate reaches 80%after 4hof drug release.Moreover,the release behavior of 5-Fu is also dependent on the temperature for drying HPMCP,and higher drying temperature corresponds to better drug release performance of loaded 5-Fu in SGF.
5-fluorouracil;hydroxypropyl methylcellulose;phthalate;pH-sensitive mesoporous molecular sieves;drug release behavior
O 629.9
A
1008-1011(2012)01-0024-05
2011-08-07.
广东省卫生厅项目(B2009190),东莞市高等院校科研机构项目(200910815254),2010年广东省教育厅育苗工程,2010年广东省大学生创新项目(KY1031).
吴都督 (1981-),男,讲师,博士.从事材料化学和药剂学方面的研究.*
,E-mail:wududucz@126.com.
