氧气对茶多酚化学氧化合成茶黄素的影响*
2011-11-28张建勇江和源崔宏春江用文
张建勇,江和源,崔宏春,江用文
1(中国农业科学院茶叶研究所,农业部茶及饮料植物产品加工与质量控制重点开放实验室,浙江杭州,310008)2(杭州市农业科学研究院茶叶研究所,浙江 杭州,310024)
氧气对茶多酚化学氧化合成茶黄素的影响*
张建勇1,江和源1,崔宏春2,江用文1
1(中国农业科学院茶叶研究所,农业部茶及饮料植物产品加工与质量控制重点开放实验室,浙江杭州,310008)2(杭州市农业科学研究院茶叶研究所,浙江 杭州,310024)
研究了O2对茶多酚化学氧化(碱性氧化和酸性氧化)形成茶黄素类物质的影响。结果表明:在接近真空、露置空气和通氧等3种不同O2含量的条件下,茶多酚碱性氧化和酸性氧化均可得到茶黄素类物质,其含量随着2种反应体系中O2含量的增加而增加,且化学氧化中儿茶素消耗的主体是EGCG、EGC、C、EC,说明O2是茶多酚化学氧化形成茶黄素的一个重要影响因素,而相关研究报道却极少涉及到关于O2在茶多酚化学氧化合成茶黄素过程所发挥的作用;另外,比较茶多酚碱性氧化法和酸性氧化法形成茶黄素的情况,前者比后者得到更多茶黄素类物质。文中还考察了O2对茶黄素化学氧化形成的影响。
O2,茶多酚,化学氧化,茶黄素,儿茶素,碱性氧化,酸性氧化
茶黄素是红茶中的主要成分,是多酚类物质氧化聚合形成的一类能溶于乙酸乙酯、具有苯骈卓酚酮结构的化合物的总称[1],具有抗肿瘤、抗氧化、抗衰老、抗炎、抗病毒、抗突变及抗心脑血管疾病等[2-9,30]多种药理功效。由于红茶中茶黄素类含量较低(一般为0.3% ~1.5%[10]),因此茶黄素类物质主要通过儿茶素体外氧化途径获得。茶黄素体外氧化制备方法按催化剂的不同可分为酶促氧化法和化学氧化法2种。化学氧化法是指利用化学氧化剂催化多酚类物质氧化聚合形成茶黄素的方法,根据化学氧化剂种类的不同,又可分为碱性氧化和酸性氧化。与酶促氧化法相比,化学氧化法可消除酶提取纯化困难、酶性质不稳定、反应时间较长等因素的影响,大大简化反应体系,缩短反应时间,因而成为研究茶黄素形成机理的一种简便而有效的方法。Roberts 等[11-24,26-27]对茶多酚化学氧化形成茶黄素进行了广泛的研究,认为“在酶促氧化中,儿茶素与氧是反应底物,酶是催化剂,酶促反应时提高氧气浓度,有利于茶黄素的形成和积累,但是却极少涉及到关于O2在茶多酚化学氧化合成茶黄素过程所发挥的作用。在茶多酚酶促氧化体系中,O2是反应底物,是茶黄素形成的重要影响因素,但是化学氧化中O2对茶黄素形成的影响报道甚少。本文通过研究接近真空、露置空气、通氧3种不同氧气含量的条件下,茶多酚碱性氧化和酸性氧化2种反应体系中氧化产物中茶黄素的形成量,发现在化学氧化中,O2仍是影响茶多酚化学氧化形成茶黄素的一个重要因素,O2浓度的增加有利于茶黄素的形成和富集,这与很多学者的论断不同。
1 材料与方法
1.1 实验材料
98%茶多酚(海南群力药业有限公司);茶黄素(TF)、茶黄素-3-没食子酸酯(TF-3-G)、茶黄素-3'-没食子酸酯(TF-3'-G)、茶黄素-3,3'-没食子酸酯(TF-3,3'-G)标准单体,均为本实验室自制,HPLC纯度分别为980.0、960.0、960.0、980.0 mg/g;乙腈(MECRO 色谱纯),乙酸、乙酸乙酯、柠檬酸、铁氰化钾、碳酸氢钠、硝酸铁,均为国产分析纯试剂。
1.2 仪器设备
Agilent 1100型高效液相色谱仪(美国Agilent公司),MR3001型磁力搅拌器(德国 Heidoph公司),KQ100E型医用超声波脱气机(江苏昆山医用超声仪器有限公司),SHZ-D型循环水式真空泵(河南巩义市英峪豫华仪器厂),R-124型旋转蒸发仪(德国BUCHI公司),5510R型高速冷冻离心机(德国Eppendorff公司),FA-210型电子天平(上海舜宇恒平科学仪器有限公司),818型pH计(美国奥立龙公司),DHG-9123A型电热恒温鼓风干燥箱(上海精密实验设备有限公司)。
1.3 实验方法
1.3.1 茶多酚化学氧化
碱性氧化法:配制10 mL碱性氧化剂溶液(K3Fe(CN)6 75 mg/mL和 NaHCO325 mg/mL),以及50 mL茶多酚溶液(50 mg/mL),将碱性氧化剂溶液加入茶多酚溶液中,磁力搅拌(转速100 r/min),分别在露置空气(广口容器自然敞开)、接近真空(0.09 MPa)、通氧(通入普通O25.0L/min)3种条件下分别反应15 min,温度25℃(磁力搅拌器控温±1℃),反应结束后,200 μL柠檬酸水溶液(pH值1.79)终止反应,加入等体积冰乙酸乙酯(-10℃)萃取1次,静止分层,酯层经等体积Tris-HCl洗涤1次,合并酯层,放入4℃冰箱中待测。
酸性氧化法:配制10 mL酸性氧化剂溶液[Fe(NO3)3100 mg/mL],以及50 mL茶多酚溶液(50 mg/mL),将酸性氧化剂溶液加入茶多酚溶液中,磁力搅拌(转速100 r/min),分别在露置空气(广口容器自然敞开)、接近真空(0.09 MPa)、通氧(通入普通O25.0L/min)3种条件下分别反应15 min,温度25℃(磁力搅拌器控温±1℃),反应结束后,立即加入等体积冰乙酸乙酯(-10℃),萃取1次,静止分层,,酯层经等体积Tris-HCl洗涤1次,合并酯层,放入4℃冰箱中待测。
1.3.2 茶黄素HPLC分析
色谱柱为 Hypersil BDS C18(4.6 mmi.d×150 mm,5 μm),流动相A为2%乙酸,流动相B为100%乙腈,流速1.5 mL/min,柱温40℃,检测波长380nm,进样量5μL,梯度洗脱,流动相B在35 min内由8%线性梯度变化到26%,40 min回到初始状态,平衡5 min。
1.3.3 儿茶素HPLC分析
色谱柱为 Hypersil BDS C18(4.6 mmi.d×150 mm,5 μm),流动相A为2%乙酸,流动相B为100%乙腈,流速1.0 mL/min,柱温30℃,检测波长280nm,进样量5μL,梯度洗脱,流动相 B在 12 min内由6.5%线性梯度变化到8%,16 min变化到15%,20 min变化到25%,26 min回到初始状态,平衡5 min。
2 结果与分析
2.1 茶多酚碱性氧化和酸性氧化
本实验选择了接近真空、露置空气、通氧3种不同O2含量的条件,对茶多酚进行化学氧化,考察O2的含量对茶多酚化学氧化的影响。以茶多酚碱性氧化反应液经乙酸乙酯和Tris-HCl处理后的酯相HPLC图谱(图1)为例,可以看出,茶多酚化学氧化体系在露置空气、接近真空、通氧3种环境条件均可以得到茶黄素(TF)、茶黄素-3-没食子酸酯(TF-3-G)、茶黄素-3'-没食子酸酯(TF-3'-G)、茶黄素-3,3'-没食子酸酯(TF-3,3'-G)4种主要茶黄素类物质,且这4种茶黄素的形成呈逐渐递增的趋势,说明O2含量的高低影响茶黄素类的物质形成,而 Takeo等[11-23]学者的研究却极少提到茶多酚化学氧化中O2的参与作用。
另外,从实验现象来看,在接近真空、露置空气、通氧3种不同O2含量的条件下,茶多酚化学氧化反应液颜色逐渐加深变红,说明随着O2含量的增加,反应液中有色物质含量也在增加。其次,从图1中HPLC的出峰情况来看,接近真空、露置空气、通氧3种条件下茶多酚化学氧化产物的组分类似,说明本实验条件下O2只对茶黄素类物质的形成量有较大影响,而对所形成的色素类物质的组成影响较小。

图1 三种条件下茶多酚碱性氧化反应液HPLC图谱(380nm)
2.2 茶黄素形成和儿茶素消耗的分析
为了深入探讨O2对茶多酚化学氧化的影响,分析了接近真空、露置空气、通氧3种不同O2含量条件下,茶多酚碱性氧化反应液和酸性氧化反应液中茶黄素形成和儿茶素消耗情况,以进一步分析O2在茶黄素形成的重要作用,详见表1~表3。
由表1可知,在茶多酚碱性氧化和酸性氧化2种反应体系中,接近真空、露置空气、通氧3种不同O2含量条件下的化学氧化反应产物中均含有茶黄素类物质,且其含量分别随着2种反应体系中O2含量的增加而增加,以通氧条件下茶多酚碱性氧化反应液中4种主要茶黄素总量最高,进一步说明了O2是茶多酚化学氧化反应体系中的一个重要影响因素,可促进反应产物中茶黄素的形成。
比较通氧时茶黄素形成量分别与接近真空和露置空气时茶黄素形成量的比值,可以发现,通氧条件下的4种主要茶黄素总量比接近真空条件下的均可提高4.1倍,比露置空气中可分别提高3.5倍和2.4倍,而对于不同茶黄素组分而言,茶多酚碱性氧化反应液中TF-3,3'-G的“通氧/接近真空”和“通氧/露置空气”2种比值最高,分别达到6.7和4.7,说明O2对4种主要茶黄素中的TF-3,3'-G形成影响最大。有关研究表明[29-32],4 种主要茶黄素中双酯型茶黄素(TF-3,3'-G)的生物活性最高,其对于保证茶黄素类产品的高生物活性极为必要。本实验研究发现,在茶多酚碱性氧化反应液中通入O2,可显著提高反应体系TF-3,3’-G,因此可为获得高活性茶黄素类产品提供借鉴。
同时,比较茶多酚碱性氧化和酸性氧化反应产物中茶黄素的形成量,发现前者比后者均可得到更多的茶黄素,且露置空气、接近真空、通氧3种不同O2含量条件下,前者4种主要茶黄素总量分别是后者的2.9倍、2.0倍、2.9倍,说明茶多酚碱性氧化法比酸性氧化法更有利于茶黄素类物质的形成,因此,与碱性氧化法相比,尽管酸性氧化法是一种比较特别的茶黄素制备途径,但是就目前而言,茶多酚碱性氧化仍是化学氧化制备茶黄素的主要方法。
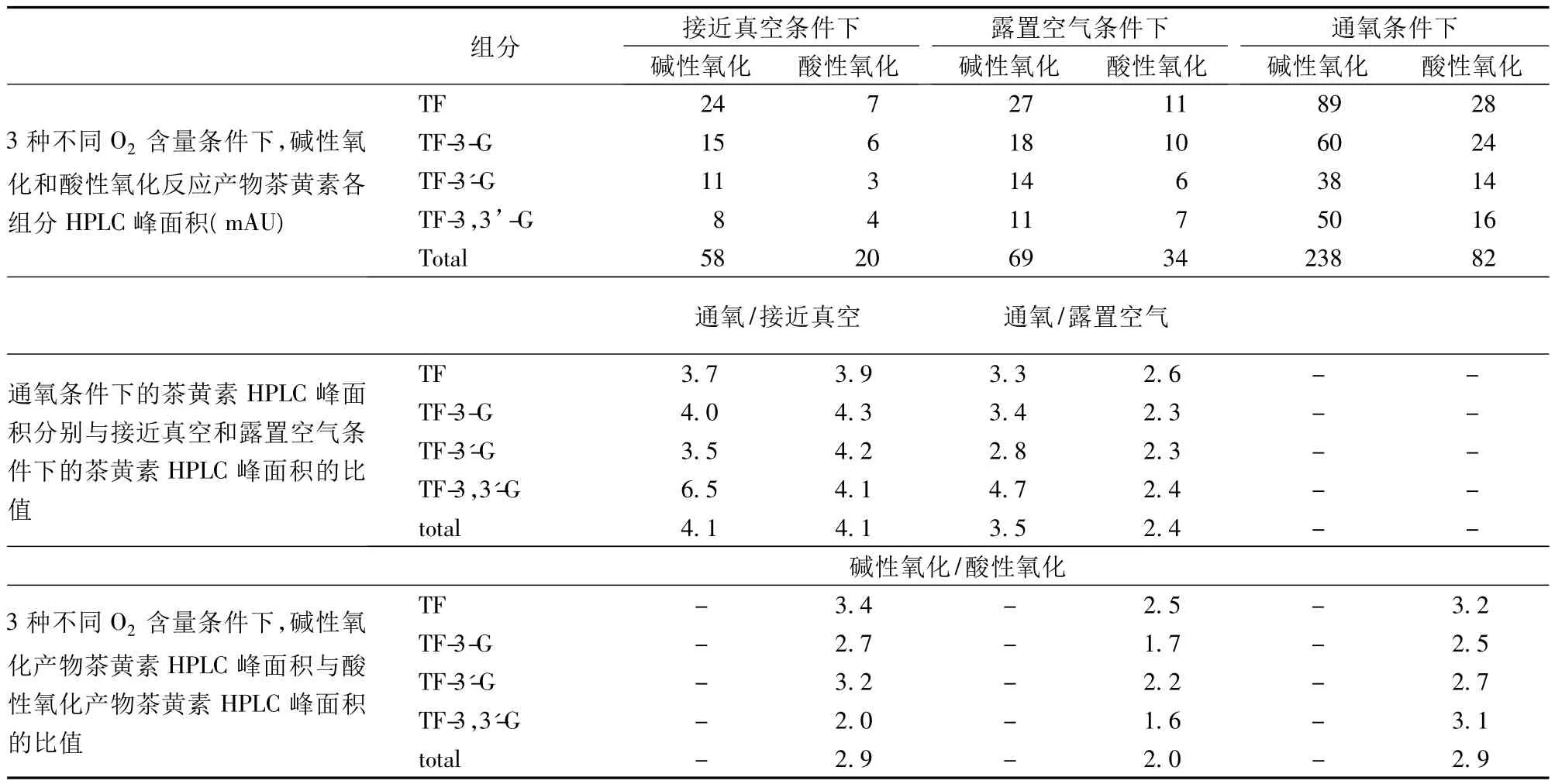
表1 不同O2含量对茶黄素形成的影响
由表2和表3中各儿茶素组分消耗率可知[儿茶素消耗率=(原液中儿茶素-反应后溶液儿茶素)/原液中儿茶
素)],在接近真空、露置空气、通氧3种不同O2含量条件下,无论是碱性氧化,还是酸性氧化,8种儿茶素总量的消耗率均随O2含量的增加而增加,且碱性氧化的儿茶素总量消耗率大于酸性氧化的儿茶素总量消耗率,这与前述的茶黄素形成量变化规律相对应,即氧化产物中茶黄素形成量较高时,儿茶素残留量相对则较低,反之亦然。
另外,比较各个儿茶素组分的消耗率,可以发现,茶多酚碱性氧化和酸性氧化的主体均是 EGCG、EGC、C、EC,以 EGCG的消耗率最高,其他4种儿茶素也有不同程度的消耗。不论是酶促氧化还是化学氧化,氧化的主体是EGCG和EGC,大部分EC也被氧化,且在酶促氧化中,大部分ECG被氧化[26],但在本实验的茶多酚碱性氧化和酸性氧化反应体系中,ECG消耗的并不多。

表2 不同O2含量对茶多酚碱性氧化反应液中儿茶素的影响

表3 不同O2含量对茶多酚酸性氧化反应液中儿茶素的影响
3 讨论
Bokuchava等[25]于1951年提出茶色素的形成机理假设:儿茶素+O2→邻醌+H2O,邻醌→有色产物。由于在O2的存在下,PPO对儿茶素的氧化,导致醌类的形成,从而生成茶黄素、茶色素及茶褐素等茶色素类物质。这一理论被后来的体外氧化实验所证实。因此,儿茶素的酶促氧化是一个需氧过程,且O2是酶促反应底物,是茶黄素形成的重要影响因素。自Roberts[11]首次以 K3Fe(CN)6和 NaHCO3为化学氧化剂进行儿茶素体外模拟化学氧化实验以来,Collier[12-23]等发现,儿茶素化学氧化同样可形成具有苯骈卓酚酮结构的茶黄素类物质,由于化学氧化剂同样可以氧化多酚的邻位二羟基而形成邻醌,而邻醌以后的缩聚反应系非酶促作用,并且经邻醌形成联苯酚醌后所发生的歧化作用均系非酶促反应,因此可发生氧化缩聚而形成苯骈卓酚酮类物质。这一点对研究儿茶素的氧化机理以及茶黄素的生产具有十分重要的理论价值。然而,这些理论仅仅考虑化学氧化剂的催化作用,却极少考虑 O2可能起到的作用。在Bokuchava提出的经典茶色素形成理论中,儿茶素是在氧气的参与下形成邻醌,再形成色素类物质的,本研究以此为切入点,通过比较分析O2对茶多酚化学氧化反应的影响发现,在其它条件相同的条件下,增加O2的量,反应液颜色逐渐加深,且HPLC检测显示茶黄素类物质形成量显著增加,说明O2在儿茶素化学氧化时也发挥着重要的作用,推测其影响机理,O2可能通过促进化学氧化剂氧化多酚的邻位二羟基形成邻醌而促进茶黄素类物质的形成,但是否作为反应物直接参与茶黄素的形成有待于进一步研究。
另外,本研究中茶多酚化学氧化HPLC图谱显示,除茶黄素(TF)、茶黄素-3-没食子酸酯(TF-3-G)、茶黄素-3'-没食子酸酯(TF-3'-G)、茶黄素-3,3'-没食子酸酯(TF-3,3'-G)4种主要茶黄素类物质色谱峰以外,还有较多峰面积较大的未知色谱峰,这就预示着对应的是一些复杂的未知茶多酚化学氧化产物,可能是一些未知的茶黄素、茶红素或者茶褐素等色素类物质,可以利用柱层析法、高速逆流色谱法等分离纯化技术和质谱、红外光谱及核磁共振波谱技术相结合,明确这些未知氧化产物的特性和结构,并有利于深入分析O2对复杂的茶多酚化学氧化产物形成的影响。
[1] 宛晓春主编.茶叶生物化学(第三版)[M].北京:中国农业出版社,2003:192.
[2] Arghya A,Suchismita M,Lakshmishri L,et al.Theaflavins retard human breast cancer cell migration by inhibiting NF-κB via p53-ROS cross-talk[J].FEBS Letters,2010,584(1):7-14.
[3] Cheng Peng,Ho Yin Edwin Chan,Yuk Man Li,et al.Black tea theaflavins extend the lifespan of fruit flies[J].Experimental Gerontology.2009,44(12):773-783.
[4] Kapil S,Shamsher S Bari,Harsh P Singh,et al.Biotransformation of tea catechins into theaflavins with immobilized polyphenol oxidase[J].Journal of Molecular Catalysis B:Enzymatic.2009,56(4):253-258.
[5] Yang Ziyin,Jie Guoliang,Fang Dong,et al.Radical-scavenging abilities and antioxidant properties of theaflavins and their gallate esters in H2O2-mediated oxidative damage system in the HPF-1 cells[J].Toxicology in Vitro.2008,22(5):1 250-1 256.
[6] Wang Kunbo,Liu Zhonghua,Huang Jian-an,et al.Preparative isolation and purification of theaflavins and catechins by high-speed countercurrent chromatography[J].Journal of Chromatography B.2008,867(2):282-286.
[7] Neetu K,Kavita S,Sahdeo P,et al.Theaflavins induced apoptosis of LNCaP cells is mediated through induction of p53,down-regulation of NF-kappa B and mitogen-activated protein kinases pathways[J].Life Sciences.2007,80(23):2 137-2 146.
[8] Prasad S,Kaur J,Roy P,et al.Theaflavins induce G2/M arrest by modulating expression of p21waf1/cip1,cdc25C and cyclin B in human prostate carcinoma PC-3 cells[J].Life Sciences.2007,81(17/18):1 323- 1 331.
[9] Babli H,Swapan P,Sibabrata M,et al.Anticlastogenic effects of black tea polyphenols theaflavins and thearubigins in human lymphocytes in vitro[J].Toxicology in Vitro.2006,20(5):608-613.
[10] 杨贤强,王岳飞,陈留记.茶多酚化学[M].上海:上海科学技术出版社,2003:33-38.
[11] Roberts E A H.The phenolic substances of f manufactured tea(I)[J].J Sci Food Agric,1957,8:72 -80.
[12] Collier P D,Mallows R,Korver O et al.The theaflavins of black tea[J].Tetrahedon,1973,29:125 -142.
[13] Takeo T.Studies on the mechanism of the oxidation of tea catechins[J].Photoehemistry,1981,20(9):2 145 -2 147.
[14] Wan Xiaochun,Harry E Nursten,Cai Ya,et al.A new type of tea pigments-from the chemical oxidation of epicatechin gallate and isolated from tea[J].J Sci Food Agric,1997(74):401-408.
[15] Davies M J,Judd J T,Baer D J,et al.Black tea consumption reduces total and LDL cholesterol in mildly hypercholesterolemia adults[J].J Nutr,2003,133(10):3 298-3 302.
[16] Nonaka G J.Tannins and related compounds XXXVI,isolation and structures of theaflagallins,New red pigments from black tea [J].Chen Pharm bull,1986,34(1):61-65.
[17] Sang S,Tian S.New dibenzotropolone derivatives characterized from black tea using LC/MS/MS[J].Bioorg Med Chem,2004,12:3 009-3 017.
[18] 萧伟祥,宛晓春,胡耀武.茶儿茶素体外氧化产物分析[J].茶叶科学,1999,19(2):145 -149.
[19] 李大祥.茶儿茶素化学氧化的研究[D].合肥:安徽农业大学,2000.
[20] 李大祥,宛晓春,萧伟祥.儿茶素化学氧化条件的研究简报[J].茶业通报,2000,22(2):17-18.
[21] 李大祥,宛晓春.论儿茶素的化学氧化[J].茶业通报,2000,22(3):22-23.
[22] 李立祥.茶多酚氧化实验研究[J].南京农业大学学报,2002,25(2):101 -104.
[23] 李立祥.酸性条件对茶多酚酸性氧化的影响[J].中国茶叶加工,2003(2):28-30.
[24] 黄海涛,屠幼英.儿茶素体外氧化制取茶黄素的研究进展[J].中国茶叶,2003(6):15-16
[25] Bokuchava M著,阮宇成译.制茶工艺学与生物化学[M].杭州:中国农业科学院茶科所情报资料室,1982.
[26] 张建勇,江和源,江用文.咖啡碱和蛋白质对酯型儿茶素氧化形成TFDG的影响[J].茶叶科学,2007,27(3):185-191.
[27] 张建勇.酯型茶黄素化学氧化形成的影响因素及其机理研究[D].北京:中国农业科学院,2007.
[28] 江和源,Hang Xiao,袁新跃,等.茶黄素双没食子酸酯的抗癌活性及其作用机理研究[J].茶叶科学,2007,27(1):33-38.
[29] Sang Shengmin,Tian Shiying,Jhoo Jinwoo,et al.Chemical studies of the antioxidant mechanism of theaflavins:radical reaction products of theaflavin 3,3'-digallate with hydrogen peroxide[J].Tetrahedron Letters.2003,44(30:5 583-5 587.
[30] Babich H,Pinsky S M,Muskin E T,et al.In vitro cytotoxicity of a theaflavin mixture from black tea to malignant,immortalized,and normal cells from the human oral cavity[J].Toxicology in vitro.2006,20(5):677 -688.
[31] Schuck A G,Ausubel M B,Zuckerbaun H L,et al.Theaflavin-3,3'-digallate,a component of black tea:An inducer of oxidative stress and apoptosis[J].Toxicology in Vitro,2008,22(3):598-609.
[32] Lu Jiebo,Alexander G Alice,Liu Yeechang,et al.PCR differential display-based identification of regulator of G protein signaling 10 as the target gene in human colon cancer cells induced by black tea polyphenol theaflavin monogallate[J].European Journal of Pharmacology,2008,601(1-3):66-72.
The Impact of Oxygen on Theaflavins Synthesis by Chemical Oxidation of Tea Polyphenol
Zhang Jian-yong1,Jiang He-yuan1,Cui Hong-chun2,Jiang Yong-wen1
1(Tea Research Institute of CAAS,Key Laboratory of Tea and Beverage Plant Products Processing and Quality Control of Agriculture Ministry,Hangzhou 310008,China)2(Tea Research Institute of Hangzhou Academy of Agriculture,Hangzhou 310024,China)
This study is focused on the impact of oxygen on chemical oxidation(alkalinity oxidation,acidity oxidation)of tea polyphenol.The results showed that the theaflavin could be obtained by alkali oxidation or acid oxidation of tea polyphenol in three conditions:vacuum,air exposing and oxygen infusion.The more oxygen in the reaction,the more theaflavins were produced.Furthermore,the principal part of chemical oxidation were EGCG、EGC、C、EC.Therefore,oxygen was the important factor in the reaction of chemical oxidation of tea polyphenol.But this was rarely reported.In addition,the yield of alkali oxidation was more than the acid oxidation.This paper reviews the impact of oxygen on chemical oxidation in the preparation of theaflavins for the first time.It lays the foundation for indepth study of mechanism and preparation of theaflavins formation.
oxygen,tea polyphenol,chemical oxidation,theaflavins,catechins,alkalinity oxidation,acidity oxidation
硕士,助理研究员(江和源为通讯作者)。
*现代农业茶叶产业技术体系红茶加工岗位;基本科研业务费专项(0032010033);国家863项目(2007AA10Z303)。
2010-10-15,改回日期:2011-02-24
