壳聚糖溶液的流变学性质及应用研究
2011-11-14李星科姜启兴夏文水
李星科,姜启兴,夏文水,*
(1.江南大学食品科学与技术国家重点实验室,江苏无锡214122;2.江南大学食品学院,江苏无锡214122)
壳聚糖溶液的流变学性质及应用研究
李星科1,2,姜启兴1,2,夏文水1,2,*
(1.江南大学食品科学与技术国家重点实验室,江苏无锡214122;2.江南大学食品学院,江苏无锡214122)
对壳聚糖稀溶液的流变学性质进行了研究,探讨了分子量和脱乙酰度结构参数以及温度、浓度、剪切速率、pH、离子强度等环境因素对壳聚糖稀溶液流变性质的影响。结果表明:壳聚糖溶液的黏度随分子量的增大而增大;随着脱乙酰度的增大和pH的增大,壳聚糖溶液的黏度先减小后增大,分别在脱乙酰度70.8%和pH4.9时黏度达到最小;离子强度的增大导致壳聚糖溶液的黏度降低。壳聚糖溶液是剪切变稀的假塑性流体,其黏度随浓度的增加逐渐增加,随温度的升高而减小,在0~80℃范围内,温度对壳聚糖溶液的黏度的影响符合Arrhenius模型,活化能为32.60kJ/mol。因此当作为食品增稠剂时,应该选用高分子量、高脱乙酰度的壳聚糖,添加到酸性低盐食品体系中。
壳聚糖溶液,黏度,流变性质,应用
食品增稠剂对保持食品(流态食品、冻胶食品)的色、香、味、结构和食品的稳定性起非常重要的作用,这种作用的大小取决于增稠剂分子本身的结构和它的流变性[1]。壳聚糖作为一种多功能性天然水溶性多糖,在食品工业中的应用越来越广泛[2-4]。日本、韩国早已把壳聚糖批准为食品添加剂使用[5-6]。中国也已经批准壳聚糖作为食品增稠剂使用[7]。当一种增稠剂应用于食品体系时,必须先研究其流变性质。本文主要研究结构参数(分子量和脱乙酰度)和环境因素(如浓度、剪切速率、温度、pH、离子强度等)对壳聚糖溶液流变性质的影响,为壳聚糖在食品工业中的应用提供一定的理论指导。
1 材料与方法
1.1 材料与设备
壳聚糖 不同分子量壳聚糖的制备采用超声波降解方法[8-9],不同脱乙酰度壳聚糖的制备采用加乙酰基的方法[10-11],分子量的测定采用凝胶渗透色谱法[4],脱乙酰度的测定采用电位滴定法[12];表中为实验室制备的壳聚糖样品,其中表1为脱乙酰度相同、分子量不同的样品,表2为分子量相同、脱乙酰度不同的样品;冰醋酸、氯化钠、氢氧化钠等 均为分析纯。
DELTA-320-S pH计 梅特勒-托利多仪器(上海)有限公司;AR1000流变仪 英国TA公司;DVII+Pro黏度计 美国Brookfield公司;DDS-11A型电导率仪、DJS-1C型电导电极 上海雷磁仪器厂。

表1 相同脱乙酰度、不同分子量的壳聚糖

表2 相同分子量、不同脱乙酰度的壳聚糖
1.2 实验方法
1.2.1 壳聚糖溶液的制备 称取1g壳聚糖,置于洁净的烧杯中,分别加入100mL 1%的醋酸溶液,搅拌溶解,冰箱中冷却过夜,测定溶液的pH为3.9。另取四份壳聚糖溶液,分别用氢氧化钠溶液调节pH为4.4、4.9、5.4、5.9。壳聚糖溶液的离子强度(0~0.68mol/L)根据添加不同浓度的氯化钠来调节。以相同的方法制备不同浓度(0.2%、0.4%、0.6%、0.8%、1.2%和1.4%)的壳聚糖溶液。
1.2.2 壳聚糖溶液流变性质的测定 在研究分子量、脱乙酰度、pH和离子强度等对壳聚糖溶液流变性质影响的实验中,采用Brookfield DV-II+Pro黏度计测量,选择超低粘度适配器和配套的转子,所有样品均在室温25℃下测定。
在研究剪切速率、浓度、温度等对壳聚糖溶液的流变性质的影响实验中,采用AR1000流变仪,选择40mm平板,平板间距为1mm。
1.2.3 数据处理 所有的实验均重复三次,求其平均值。
2 结果与讨论
2.1 分子量对壳聚糖溶液流变性质的影响
从图1可以看出,随着分子量的增大,壳聚糖的黏度也在增大,这与王伟等的研究结果一致[13]。分子量是决定壳聚糖黏度的一个重要的因素,壳聚糖为高聚物,分子量大,说明聚合度高,在溶液中分子链也相对比较长,可以相互缠结或聚集,产生较强的氢键和疏水相互作用,溶液黏度较大;而低分子量壳聚糖的分子链相对较短,因此溶液黏度较小。因此当作为食品增稠剂使用时,应该选用高分子量的壳聚糖。
2.2 脱乙酰度对壳聚糖溶液流变性质的影响
壳聚糖分子链由氨基葡萄糖结构单元和乙酰氨基葡萄糖结构单元构成,壳聚糖的物化性质、生物活性和溶液流变性质与两种结构单元的比例即脱乙酰度密切相关[14]。图2显示的是五种相同分子量、不同脱乙酰度的壳聚糖(60.5%,65.4%,70.8%,77.3%,86.1%)溶液的黏度,由图可知,随着脱乙酰度的增大,壳聚糖的黏度先减小而后增大,脱乙酰度70.8%的壳聚糖黏度最小。脱乙酰度的大小导致壳聚糖分子构象转变的主要原因是:a.改变了壳聚糖分子链上的电荷密度;b.乙酰基团具有较大的空间位阻效应和疏水性[10]。高脱乙酰度的壳聚糖分子带电荷多,由于静电斥力作用,高脱乙酰度壳聚糖的分子链比较舒展。低脱乙酰度的壳聚糖含有较多的乙酰基团,乙酰基团的增加引发的空间位阻也会增加分子链的刚性,并且倾向于形成氢键和疏水相互作用,分子链也比较舒展[8]。Schatz和Lamarque等的研究认为,当脱乙酰度大于75%,壳聚糖显示聚电介质行为,分子链具有较高的柔顺性;而脱乙酰度介于50%和75%之间,是亲水和疏水作用平衡的过渡区域,壳聚糖分子链的刚性逐渐增强[15-16]。因此脱乙酰度60.5%、65.4%、70.8%的壳聚糖溶液黏度随着脱乙酰度增加而降低,而77.3%、86.1%的壳聚糖溶液黏度随着脱乙酰度增加而升高。因此当选择壳聚糖作为食品增稠剂时,应该选择高脱乙酰度的壳聚糖。

图1 分子量对壳聚糖溶液流变性质的影响

图2 脱乙酰度对壳聚糖溶液流变性质的影响
2.3 温度对壳聚糖溶液流变性质的影响
温度是影响高分子聚合物流变性质的重要因素之一。如图3所示,随着温度的升高,壳聚糖溶液的黏度逐渐降低。这是由于温度升高,壳聚糖分子的运动加剧,分子间相互作用减弱,分子流动阻力降低,因而黏度下降。
流体的流动活化能反映了高聚物流动所需克服的能量,一般来说,分子间相互作用力愈大,或分子链刚性愈强,则流动所需的活化能愈高,这类高聚物的黏度对温度有较大的敏感性。在不太宽的温度范围内,流体的黏度与温度之间的关系符合阿伦尼乌斯方程:η=A·eE/RT或lnη=lnA+E/RT。其中:η为溶液的黏度;A为常数;R为气体常数;T为绝对温度;E为粘流活化能。活化能是黏度对温度敏感程度的一种量度;活化能越大,温度对黏度的影响也越大,因而从活化能的大小可以了解用温度改变流体黏度的可行性。在一定的条件下,当活化能较大时,用升温来降低黏度是可行的,但如果活化能很小,升温的方法就不是很有效[17]。

表3 壳聚糖溶液的流动指数和稠度指数
本实验研究了浓度为1%的壳聚糖溶液在0~80℃的温度范围内黏度的变化情况,以lnη对1/T作图,如图4所示,并由此求得E=32.60kJ/mol,与吴国华等研究的结果(E=33.482kJ/mol)比较接近,说明壳聚糖溶液对温度变化比较敏感[18]。
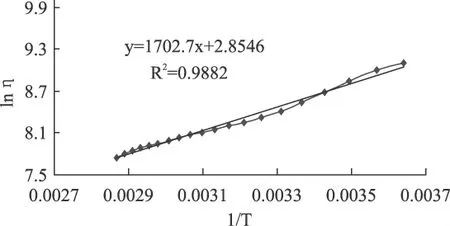
图4 壳聚糖溶液的黏度与温度的关系
2.4 浓度和剪切速率对壳聚糖溶液流变性质的影响
绝大多数高分子材料在加工过程中的流动都不服从牛顿定律,至今还没有一个确切的能反映聚合物材料本质的流变方程,到目前为止大多数还采用1925年 Ostwald和 Dewaele提出的经验方程:τ= K·γn。式中:τ-剪切应力;K-稠度系数;γ-剪切速率;n-流动指数,表示该流体与牛顿流体的偏差程度。当n=1时,流体为牛顿流体,其黏度不随γ的变化而变化;当n<1时,流体为非牛顿假塑性流体,其黏度随γ的增大而下降;当n>1时,流体为非牛顿胀塑性流体,其黏度随γ的增大而增大[17-18]。
壳聚糖的黏度和浓度密不可分。剪切速率和剪切力也是影响壳聚糖流变特性的重要因素。如图5所示,用1%的醋酸分别配制不同浓度的壳聚糖溶液,在剪切速率为20~90(1/s)的范围内测其黏度,同时根据lgτ=nlgγ+lgk计算流动指数n和稠度系数K,见表3。表3结果表明,壳聚糖溶液的流动指数均小于1,为非牛顿假塑性流体,其黏度随着剪切速率的增加而减少。而且随着壳聚糖浓度的增大,溶液的稠度指数在增大,流动指数在减小,说明壳聚糖溶液浓度越高,其粘稠性越大,假塑性流体的特征越来越明显。瓜尔豆胶是食品工业上常用的胶之一,为了比较壳聚糖的增稠性质,与1%的瓜尔豆胶溶液比较发现,1.4%的壳聚糖溶液稠度系数小于其稠度系数,而流动指数大于其流动指数,说明相同浓度下,壳聚糖的粘稠度不如瓜尔豆胶,但假塑性程度比瓜尔豆胶高。

图5 浓度和剪切速率对壳聚糖溶液流变性质的影响
2.5 pH对壳聚糖溶液流变性质的影响
壳聚糖溶液的表观黏度随pH的变化情况如图6所示。结果表明,随着溶液pH的升高,其表观黏度先减小后升高,这与王伟等的研究结果不一致[19],可能他们研究的是壳聚糖浓溶液的性质,而且pH的范围也不一致,但是与Il’ina和Varlamov报道的结果一致[20]。壳聚糖分子在溶液中存在着4种相互作用力:范德华力、氢键、疏水作用和静电作用。在酸性溶液中,壳聚糖上的NH2质子化为NH+3,因此分子内和分子间存在着较强的静电相互作用;由于壳聚糖分子上含有大量的羟基和乙酰氨基,因此会形成较强的分子内氢键作用[14]。随着pH的增加,壳聚糖分子带电越来越少,而离子强度逐渐增加,降低了正电荷间的静电作用,从而使壳聚糖分子链趋于弯曲,分子链的有效体积减少,降低了体系的黏度,在pH4.9左右时降到最低。而后随着pH的进一步升高,壳聚糖分子链上的-NH+3基团在碱的中和作用下变成-NH2,质子化程度降低,带电越来越少,相应的分子内和分子间的静电相互作用变弱,而壳聚糖分子上含有大量的羟基和乙酰氨基,会形成较强的氢键作用,促使壳聚糖分子间相互缠绕,体系黏度变大。因此壳聚糖可以作为增稠剂添加到弱酸性食品体系中。
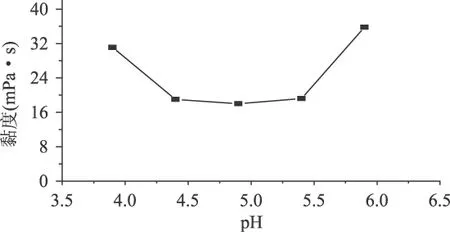
图6 pH对壳聚糖溶液流变性质的影响
2.6 离子强度对壳聚糖溶液流变性质的影响
如图7~图9所示,壳聚糖溶液的黏度随着离子强度的增加而降低,这与王伟等报道的结果一致[13]。在酸性溶液中,壳聚糖上的-NH2质子化为NH+3,因此分子内和分子间存在着较强的静电相互作用,离子强度对这种相互作用有重要影响。当加入强电解质氯化钠时,反离子将屏蔽质子化氨基,使分子构象收缩卷曲,分子链的有效体积减少,降低了体系的黏度。

图7 离子强度对不同分子量壳聚糖溶液流变性质的影响

图8 离子强度对不同脱乙酰度壳聚糖溶液流变性质的影响

图9 离子强度对不同pH壳聚糖溶液流变性质的影响
在相同脱乙酰度、不同分子量的壳聚糖溶液中加入不同浓度的氯化钠后,发现高分子量的壳聚糖黏度降低的幅度比较大,而低分子量的壳聚糖变化较小。如图7所示,当离子强度升高至0.68mol/L时,分子量为880、708、600、410、299的壳聚糖黏度分别降低了65.5%、60%、50%、49.4%和48.2%。这是因为分子量比较大的壳聚糖分子中含有较多的氨基基团,带电比较多,容易受离子强度的影响。
在相同分子量不同脱乙酰度的壳聚糖溶液中加入不同浓度的氯化钠后,如图8所示,当离子强度升高至 0.68mol/L时,脱乙酰度为 60.5%、65.4%、70.8%、77.3%和86.1%的壳聚糖黏度分别降低了43.9%、47.1%、47.6%、47.6%和49.8%,这主要是因为脱乙酰度升高,壳聚糖分子带电增多,溶液的黏度受离子强度的影响变大。
在相同浓度不同pH的壳聚糖溶液中加入不同浓度的氯化钠后,如图9所示,随着离子强度的增加,pH3.9、4.4、4.9、5.4的壳聚糖溶液的黏度一直在降低,当离子强度升高至0.68mol/L时,黏度分别降低了60.7%、35.8%、25.5%和10.9%,这主要是因为随着pH的升高,壳聚糖分子带电越来越少,因此受离子强度的影响越来越弱。而pH5.9的壳聚糖溶液随着离子强度的增加,黏度越来越大,这可能是壳聚糖分子间较强的氢键作用的结果。
2.7 存放时间对壳聚糖流变性质的影响
将浓度1%、不同pH的壳聚糖溶液在25℃下放置一段时间,测定溶液的黏度的变化情况。如图10所示,所有的壳聚糖溶液黏度随着放置时间的延长呈降低趋势,pH3.9的壳聚糖溶液变化最快,15d后降到原来的51.8%,而其他pH的壳聚糖溶液降低比较缓慢,这主要是因为壳聚糖分子在酸性溶液中会缓慢降解,分子量降低,溶液的粘度也降低。因此壳聚糖可以作为增稠剂添加到弱酸性食品体系中。
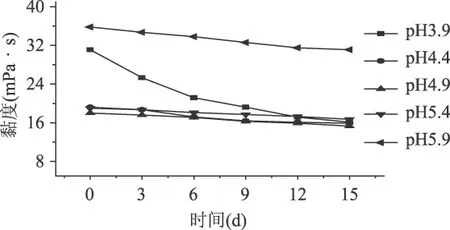
图10 时间对不同pH壳聚糖溶液流变性质的影响
3 结论
壳聚糖的结构对其流变学性质有重要影响,壳聚糖溶液的表观黏度随分子量的增大而增大;随着脱乙酰度的增大,壳聚糖的黏度先减小而后增大,脱乙酰度70%的壳聚糖黏度最小;随着pH的增大,壳聚糖溶液的表观粘度先减小而后增大;离子强度的增大导致高脱乙酰度和高分子量的壳聚糖溶液的粘度急剧降低。壳聚糖溶液是剪切变稀的假塑性流体,其表观粘度随质量分数的增加逐渐增加;温度对壳聚糖溶液的表观粘度的影响符合Arrhenius模型,活化能为32.60kJ/mol;壳聚糖可以作为增稠剂添加到酸性食品体系中,当选择壳聚糖作为增稠剂时,应该选用分子量比较大、脱乙酰度比较高的壳聚糖。壳聚糖可以作为良好的增稠剂添加到酸性低盐食品体系中。
[1]黄来发.食品增稠剂[M].第二版.北京:中国轻工业出版社,2009:5.
[2]夏文水.壳聚糖的生理活性及其在保健食品中的应用[J].中国食品学报,2003,3(1):77-81.
[3]Xia WS,Liu P,Zhang JL,et al.Biological activities of chitosan and chitooligosaccharides[J].Food Hydrocolloids,2011,25:170-179.
[4]Li XK,Xia WS.Effects of chitosan on gel properties of saltsoluble meat proteins from silver carp[J].Carbohydrate Polymers,2010,82:958-964.
[5]KFDA.Korea Food and Drug Administration[M].Food Additives Code,Seoul,1995.
[6]Weiner ML.An overview of the regulatory status and of the safety ofchitin and chitosan asfood and pharmaceutical ingredients//Brine CJ,Sandford PA,Zikakis JP(Eds.).Advances in chitin and chitosan[M].London:Elsevier,1992:663-670.
[7]GB2760-2007食品添加剂使用卫生标准[M].
[8]Gao Q,Wan AJ.Effects of molecular weight,degree of acetylation and ionic strength on surface tension of chitosan in dilute solution[J].Carbohydrate Polymers,2006,64:29-36.
[9]Tsaih ML,Tseng LZ,Chen RH.Effects of removing small fragments with ultrafiltration treatment and ultrasonic conditions on the degradation kinetics of chitosan[J].Polymer Degradation and Stability,2004,86:25-32.
[10]Berth G,Dautzenberg H.The degree of acetylation of chitosans and its effect on the chain conformation in aqueous solution[J].Carbohydrate Polymers,2002,47:39-51.
[11]VachoudL,ZydowiczN,DomardA.Formation and characterization of a physical chitin gel[J].Carbohydrate Research,1997,302:169-177.
[12]Lin RX,Jiang SH,Zhang MS.The determination of degree of deacetylation[J].Chemistry Bulletin,1992,3:39-42.
[13]王伟,徐德时.壳聚糖浓溶液流变性质研究-分子量的依赖性[J].高分子学报,1995(5):596-600.
[14]高群,王国建,李文涛.壳聚糖在稀溶液中的分子构象及其影响因素[J].化学通报,2009,72(4):1-6.
[15]Schatz C,Viton C,Delair T,et al.Typical Physicochemical Behaviors of Chitosan in Aqueous Solution[ J] . Biomacromolecules,2003(4):641-648.
[16]Lamarque G,Lucas JM,Viton C,et al.Physicochemical Behavior of Homogeneous Series of Acetylated Chitosans in Aqueous Solution:Role of Various Structural Parameters[J]. Biomacromolecules,2005,6:131-142.
[17]符若文,李谷,冯开才.高分子物理[M].北京:化学工业出版社,2005.
[18]吴国杰,姚汝华.壳聚糖溶液流变学性质的研究[J].华南理工大学学报,1997,25(10):62-66.
[19]王伟,徐德时,李素清,等.聚电解质-壳聚糖浓溶液流变学性质研究:浓度、温度、溶pH和外加盐对粘度及流动性的影响[J].高分子学报,1994(3):328-334.
[20]Il’inaAV,VarlamovVP.EffectofPhysicochemical Parameters on the Formation of Chitosan-Based Gels[J].Applied Biochemistry and Microbiology,2004,40:599-602.
Study on rheological properties and application of chitosan solution
LI Xing-ke1,2,JIANG Qi-xing1,2,XIA Wen-shui1,2,*
(1.State Key Laboratory of Food Science and Technology,Wuxi 214122,China;2.School of Food Science and Technology,Jiangnan University,Wuxi 214122,China)
Rheological properties and application of chitosan solutions,in which the effects of internal factors(molecular weight and degree of deacetylation)and external factors(concentration,shear rate,temperature,pH and ionic strength)on viscosities of chitosan solution were studied.Results showed that viscosity increased with the increase of molecular weight and initially decreased and then increased with the increase of degree of deacetylation and pH,reached the minimum at 70.8%within the range 60.5%to 86.1%and at pH 4.9 between 3.9 and 5.9 respectively.Viscosities of chitosan solution decreased with the increase of ionic strength excessively. Furthermore,chitosan solution exhibited shear thinning behavior following the power law model.Viscosity increased with the increase of concentration,and decreased with the increase of temperature.The decrease in viscosity(within 0~80℃)followed an Arrhenius temperature dependence,and the activation energy was 32.60kJ/mol.As food thickener,it is suitable to choose chitosan with higher molecular weight and higher degree of deacetylation and add into the acidic food systems containing low salt.
chitosan solution;viscosity;rheological property;application
TS201.7
A
1002-0306(2011)02-0065-05
2010-11-19 *通讯联系人
李星科(1981-),男,博士研究生,研究方向:食品化学及大分子结构与功能。
国家863计划项目(2007AA100401);食品科学与技术国家重点实验室目标导向项目(SKLF-MB-200805);江苏省科技成果转化项目(BA2009082)。
