微波作用下反应结晶制备碱式碳酸镁*
2011-11-09杨小波祁敏佳宋兴福于建国
杨 晨,杨小波,郑 东,祁敏佳,汪 瑾,宋兴福,于建国
(1.华东理工大学国家盐湖资源综合利用工程技术研究中心,上海 200237; 2.青海盐湖工业集团股份有限公司)
微波作用下反应结晶制备碱式碳酸镁*
杨 晨1,杨小波2,郑 东2,祁敏佳1,汪 瑾1,宋兴福1,于建国1
(1.华东理工大学国家盐湖资源综合利用工程技术研究中心,上海 200237; 2.青海盐湖工业集团股份有限公司)
采用等初末温度比较法和等温法分别在微波及水浴加热下反应结晶合成了碱式碳酸镁颗粒。用扫描电镜(SEM)、X射线衍射(XRD)以及粒度分析表征不同阶段样品的晶体结构、表面形貌和粒度分布,用化学分析(滴定法)跟踪反应结晶过程中镁离子浓度的变化。实验结果表明:所得晶体由纳米片自组装而成,微波场对碳酸镁结晶具有促进作用,即微波对碳酸镁结晶中初级纳米颗粒的组装具有促进作用,可提高碱式碳酸镁的生长速率,增大颗粒粒度,但没有改变产物晶习;不同温度下碱式碳酸镁转变路径不同,较高温度时无定形颗粒直接组装成碱式碳酸镁,较低温度时将出现正碳酸镁中间态,经由不同相转变历程的碱式碳酸镁纳米片微观形貌和组装方式并不相同。
碱式碳酸镁;反应结晶;微波
新技术的兴起给可控合成具有复杂形貌和等级结构、多尺度延展的功能化材料带来用武之地,结晶过程与外场耦合已成为研究热点。与传统的加热过程不同,微波(分子水平)加热使得反应结晶中温度分布更加均匀,可消除因温度梯度引起的局部过饱和。微波合成(Microwave Synthesis)技术以其高效、均匀、节能、环保等诸多优点备受关注,在无机合成上的应用日臻繁荣[1-3]。碱式碳酸镁[4MgCO3· Mg(OH)2·4H2O]为单斜晶体,由于其自组装特性,片状微晶将聚集形成一定的层状结构,目前报道的碱式碳酸镁按形貌分有管状[4]、棒状[5]、玫瑰花状[6]、巢状[7]、球状[8]等。碱式碳酸镁可用作绝热、耐高温的防火保温材料,还可应用于食品、药物、油墨颜料,以及用于制造日用品添加剂、作为载体等[9-10]。将微波应用于碳酸镁的制备研究尚处于起步阶段,有必要将微波与碳酸镁反应结晶耦合,开拓功能性碳酸镁制备的新思路。
1 实验材料和方法
1.1 实验仪器与试剂
仪器:MAS-Ⅱ型常压微波合成/萃取反应工作站(上海新仪微波化学科技有限公司);DC-2006型低温恒温槽(上海衡平仪器仪表厂)。
试剂:氯化镁、碳酸钠,均为分析纯(上海凌峰化学试剂有限公司)。
1.2 分析测试仪器
扫描电镜(SEM),JSM-6360LV型,日本JEOL公司;转靶X射线多晶衍射仪(XRD),D/MAX 2550 VB/PC型,日本RIGAKU公司;马尔文激光粒度分析仪,Mastersizer 2000型,英国马尔文公司。
1.3 实验方法
分别采用等初末温度比较法和等温法研究碱式碳酸镁的制备。
等初末温度法具体控制步骤:将同体积的0.20 mol/L的 MgCl2和 Na2CO3溶液各自恒温于293.15 K,并一次性快速混合(3~4 s),持续搅拌,按设定的程序升温至353.15 K,达到设定温度后保温30 min,将所得产物抽滤并洗涤,烘干后待分析测试。同时采用等初末温度法对比常规加热效果,即将混合后的料浆加入到已经升温到353.15 K的结晶反应器(采用水浴加热,并与微波反应器规格相同)中,其余操作步骤相同。
等温法具体控制步骤:将同体积的0.20 mol/L的MgCl2和Na2CO3溶液各自恒温于323.15 K,并一次性快速混合(3~4 s),在微波或者水浴条件下持续搅拌并保持在323.15 K,2 h后出料,将所得产物抽滤并洗涤,烘干后待分析测试。
2 实验结果与讨论
2.1 不同加热过程所得碱式碳酸镁的分析
图1为等初末温度法合成产物的XRD谱图。由图1可以看出,所有峰值位置指示此物相为单斜晶体4MgCO3·Mg(OH)2·4H2O,与文献值(JCPDS 25-0513)吻合良好。
图2为等初末温度法合成碱式碳酸镁的SEM照片。从图2可以看出,碱式碳酸镁呈片层状结构而非典型的“House of cards”结构。碱式碳酸镁由30~40 nm厚的碱式碳酸镁纳米晶组装堆积成多层结构,层状晶体交叉拼接成三维结构。

图1 353.15 K条件下制得产物XRD谱图

图2 353.15 K条件下制得碱式碳酸镁SEM照片
等温法所得产物经XRD表征均为碱式碳酸镁,图3为等温法所得碱式碳酸镁SEM照片。由图3a、b可以看出,采用等温法所得碱式碳酸镁呈多孔的玫瑰花状结构,构成聚集体的纳米片状晶体呈弯曲状,明显区别于等初末温度法所得产物。由图3还可以看出,微波场对晶体结构并没有本质的改变,与常规水浴加热方式相同,仍保持原有晶习。

图3 323.15 K条件下不同阶段制得碱式碳酸镁SEM照片
图4为等初末温度法(微波300 W)所得产物粒度分布图,产物平均粒径由体积等效粒径d[3-4]表示。变异系数是用来表征颗粒粒度分布范围的参数,其值愈大表明颗粒的粒度分布愈宽广。定义变异系数:
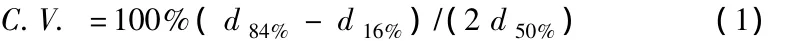
式中:d16%、d50%、d84%分别表示累计体积在16%、50%和84%时对应的颗粒粒度。

图4 微波300 W条件下所得产物粒度分布图
等初末温度法不同条件所得产物平均粒径d及变异系数C.V.值列于表1。从表1可以看出,微波条件下生成的晶体粒度及变异系数普遍比水浴条件下的大。
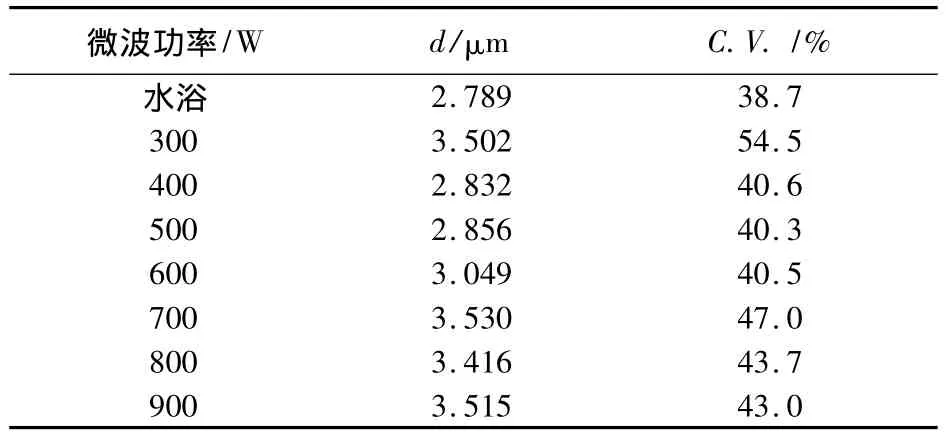
表1 等初末温度法不同条件所得碱式碳酸镁平均粒径及变异系数
2.2 碱式碳酸镁反应结晶过程分析
为深入研究不同条件下反应结晶过程的差异,对反应过程中镁离子浓度进行跟踪分析。实验采用间歇取样,并采用 EDTA滴定法分析。图 5为353.15 K条件下,在水浴及微波300 W和600 W条件下反应溶液中Mg2+浓度随时间的变化。由图5可以看出,采用等初末温度法时,无论是微波条件还是水浴条件,镁离子浓度变化均呈现先快速下降,再缓慢下降,最终趋于平衡状态。快速下降阶段微波加热比水浴加热突跃点提前,即碱式碳酸镁自组装加快,这与微波加热迅速有关,说明其可以促进结晶。在后期消除过饱和阶段,微波加热比水浴加热消除过饱和的程度大,即微波强化了反应进程。
图6为323.15 K条件下等温法反应过程的镁离子浓度随时间的变化。由图6看出该过程可分为3个阶段:第一阶段,溶液中的镁离子快速减少,碳酸钠和氯化镁混合后的絮状碳酸镁快速组装形成棒状的正碳酸镁(此时的产物如图3c),最低点趋近正碳酸镁在溶液中的溶解度;在第二阶段,镁离子浓度重新上升,是因为正碳酸镁转变成碱式碳酸镁的过程中(此时的产物如图3d),重新溶解造成局部过饱和生成了无定形物,无定形物有较高溶解度,从而使镁离子浓度上升,故从浓度变化可以推测出这个转变是正碳酸镁溶解、碱式碳酸镁组装的过程;第三阶段为消除过饱和的过程,此时溶液中没有足够的无定形物维持过饱和,镁离子浓度逐渐趋于平衡。
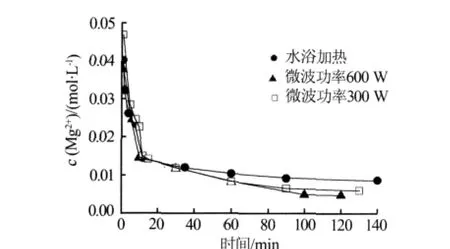
图5 353.15 K条件水浴及微波条件下反应溶液中Mg2+浓度随时间的变化
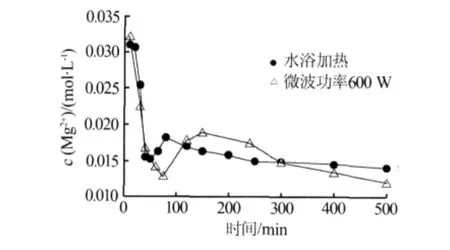
图6 微波及水浴条件在323.15 K条件下反应溶液中Mg2+浓度随时间的变化
与常规加热方式相比,在微波作用下镁离子浓度变化呈现如下特点:第一阶段镁离子浓度下降最低点更低,即反应进行得更彻底,这可用微波促进初始纳米颗粒的组装来解释;第二阶段镁离子浓度上升持续了更长时间,看似微波延缓了结晶过程,但结合本体系特点可以发现这一有趣现象同样反映了微波场对纳米碳酸镁构筑结晶相的强化促进作用。此时,因为正碳酸镁溶解再次生成无定形纳米碳酸镁颗粒,在323.15 K下这些纳米颗粒既可以向正碳酸镁转变(如第一阶段),也可以向碱式碳酸镁转变(如第二阶段),这是一个动力学控制过程。正因为微波对无定形的组装或者碳酸镁的结晶有促进作用,使得这两个转变过程相互制约,从而延长了动力学转变的时间窗口。综合以上分析,可以得知无论何种合成温度和方法(等温/变温),微波对碳酸镁的结晶均起到促进作用。
2.3 微波对碱式碳酸镁结晶影响机理初步探讨
基于实验结果与分析,碱式碳酸镁晶体是由一个生长中心向外辐射式生长,与水浴相比,微波促进了片状晶体的外延生长,增大了其生长速率,使得其粒度增大。在微波场作用下,反应物和产物分子在吸收微波后,分子运动速度加快,致使分子“搅拌”加剧,同时发生摩擦而使体系温度升高;其次,微波作用又使溶剂的氢键得到破坏,电离程度加大,溶剂结构发生变化,待结晶的溶质向晶体相界面的扩散能力提高,到达晶体表面的溶质与晶体的碰撞几率也增大,这些作用都促使结晶速率加快。本体系中,碱式碳酸镁是通过无定形碳酸镁按照一定规律自组装或自组织而形成,微波场的存在促进了无定形颗粒从主体溶液中向晶体表面迁移附着,形成结晶相。本文研究中未发现微波作用的非热效应和其他特殊效应,但随着对其深入研究,将更多揭示出微波场在本体系中的种种效应。
3 结论
利用微波加热合成了纳米片层状结构碱式碳酸镁,实验结果表明微波场可以促进初始纳米碳酸镁颗粒的组装结晶,从而增大颗粒粒度,但微波没有改变产物晶习;不同温度下碱式碳酸镁转变路径不同,较高温度时无定形颗粒直接组装成碱式碳酸镁,较低温度反应时将出现正碳酸镁中间态,这种不同相转移历程使得碱式碳酸镁纳米片微观形貌产生差异。不同温度作用下反应历程可由镁离子浓度变化间接反应出来,微波对碳酸镁结晶具有强化促进作用,具体作用机理还应做深入研究。
[1]Siddharthan A,Seshadri S K,Sampath Kumar T S.Influence of microwave power on nanosized hydroxyapatite particles[J].Scripta Materialia,2006,55(2):175-178.
[2]Jhung S H,Jin T H,Hwang Y K,et al.Microwave effect in the fast synthesis of microporous materials:which stage between nucleation and crystal growth is accelerated by microwave irradiation[J].Chemistry-A European Journal,2007,13(16):4410-4417.
[3]Mariusz Pietrowski,Maria Wojciechowska.Microwave-assisted synthesis of spherical monodispersed magnesium fluoride[J].Journal of Fluorine Chemistry,2007,128(3):219-223.
[4]Mitsuhashi K,Tagami N,Tanabe K,et al.Synthesis of microtubes with a surface of"house of cards"structure via needlelike particles and control of their pore size[J].Langmuir,2005,21(8):3659-3663.
[5]Hao Zhihua,Pan Jie,Du Fanglin.Synthesis of basic magnesium carbonate microrods with a surface of"house of cards"structure[J].Materials Letters,2009,63(12):985-988.
[6]华东理工大学.一种多孔玫瑰花状碱式碳酸镁的制备方法:中国,101830489[P],2010-09-15.
[7]Liu Fei,Sun Congting,Yan Chenglin,et al.Solution-based chemical strategies to purposely control the microstructure of functional materials[J].Journal of Materials Science and Technology,2008,24(4):641-648.
[8]Zhang Zhiping,Zheng Yajun,Zhang Jixiu,et al.Synthesis and shape evolution of monodisperse basic magnesium carbonate microspheres[J].Crystal Growth&Design,2007,7(2):337-342.
[9]胡庆福.镁化合物生产与应用[M].北京:化学工业出版社,2004.
[10]日铁矿业株式会社.碱式碳酸镁及其制备方法和用途:中国,1646430[P].2005-07-27.
Preparation of hydromagnesite via reactive crystallization under microwave irritation
Yang Chen1,Yang Xiaobo2,Zheng Dong2,Qi Minjia1,Wang Jin1,Song Xingfu1,Yu Jianguo1
(1.National Engineering Research Center for Integrated Utilization of Salt Lake Resource,East China University of Science and Technology,Shanghai200237,China;2.Qinghai Salt Lake Industry Group Co.,Ltd.)
Same initial and final temperature comparative method and isothermal method were chosen to synthesize hydromagnesite particles under microwave irritation and water bath heating.SEM,XRD,and CSD were used to characterize crystal structure,surface morphology,and particle size distribution of the samples at different stages.Chemical titration analysis was used to track the change of magnesium ion concentration in crystallization process.Experimental results showed that hydromagnesite crystals were constructed of lots of self-assembled nano-sheets.Microwave accelerated the crystallization of magnesium carbonate,that is to say microwave could accelerate the assembly of primary nano-particles in magnesium carbonate crystallization,thus enhanced the growth rate of hydromagnesite and then increased the crystal size,but did not change the crystal habit;transition paths of hydromagnesite at different temperatures were different,the amorphous substance assembled into hydromagnesite at higher temperature and nesquehonite intermediate would appear at lower temperature,and the micro-morphology and assemble manner of hydromagnesite nano-sheets by different phase-transfer processes were not the same.
hydromagnesite;reactive crystallization;microwave
TQ132.2
A
1006-4990(2011)06-0020-04
上海自然科学基金项目(09ZR147900);中央高校基本科研业务费专项基金项目;新世纪优秀人才基金项目(NCET-08-0776);上海市重点学科建设基金项目(No.B506)。
2010-12-27
杨晨(1984— ),男,博士研究生,从事工业结晶研究。
联系人:宋兴福
联系方式:xfsong@ecust.edu.cn
