N-乙基-2,3-双氧哌嗪紫外分光光度法建立
2011-11-07张中华
张中华
(山西电力职业技术学院,山西 太原 030021)
N-乙基-2,3-双氧哌嗪紫外分光光度法建立
张中华
(山西电力职业技术学院,山西 太原 030021)
对用紫外分光光度法分析N-乙基-2,3-双氧哌嗪进行了探索并建立其定性定量分析方法。
N(4)-乙基-2,3-双氧哌嗪;紫外分光光度法;分析方法
N(4)-乙基-2,3-双氧哌嗪,别名:N-乙基双氧哌嗪,双酮乙哌,N(4)-乙基-2,3-二酮哌嗪,英文名 称 :4-ethyl-2,3-dioxypiperazine,CAS:59702-31-7。 分子式:C6H10N2O2, 分子量:142.16。 本品为白色或淡黄色粒状结晶,密度 0.64;熔点 121~126℃[1],溶于水及各类醇,其结构式[2]为:
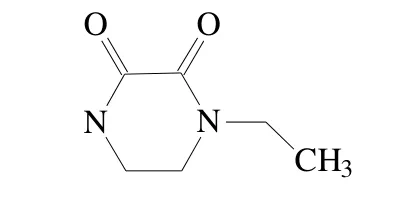
N(4)-乙基-2,3-双氧哌嗪是重要的有机合成原料和医药中间体[3~6],是哌拉西林、头孢拉腙、头孢哌酮等基本合成原料之一。经文献检索,未见使用紫外分光光度法对N-乙基-2,3-双氧哌嗪进行定性和定量分析的方法,而紫外分光光度法使用起来简便快捷,能大大提高工厂效率,故对其分析方法进行了研究探索。
1 实验试剂及仪器
环己烷(AR),正己烷(AR),甲醇(色谱纯),无水乙醇 (AR),二次蒸馏水 (自制),溴化钾(AR),乙腈(AR)。
电热鼓风干燥箱101-1A型,电子天平BS-210s型,熔点测定仪TX-4型,可见-紫外光谱仪TU-1901型,红外光谱仪FTIR-8400s型。
2 实验内容
2.1 传统测定方法
2.1.1 熔点测定
通过TX-4型熔点仪测定N-乙基-2,3双氧哌嗪的熔点,与文献值进行比较。
2.1.2 红外光谱测定
采用岛津FTIR-8400S型红外光谱仪[7]测定N-乙基-2,3双氧哌嗪的红外谱图,溴化钾压片法,将样品图与标准品图谱进行比较。
2.2 紫外分光光度法探索[8~10]
2.2.1 溶剂及波长的选择
选择甲醇、乙醇、乙腈、1,2-二氯乙烷为溶剂,溶解适量样品,在200~400 nm处进行紫外扫描,以选择最佳溶剂。在1,2-二氯乙烷中出峰位置为229 nm,但其末端吸收为235 nm,故排除这种物质。样品易溶于乙腈中,吸收峰为222 nm;在甲醇、乙醇中吸收峰为222 nm。甲醇、乙醇、乙腈3种物质的末端吸收均为210 nm,对测定没有影响。故在甲醇、乙醇、乙腈3种溶剂中选择一种溶剂,因乙醇无毒无害,且价格较为便宜,故采用乙醇作为溶剂。
图1为N-乙基-2,3双氧哌嗪的乙醇溶液的紫外扫描图。
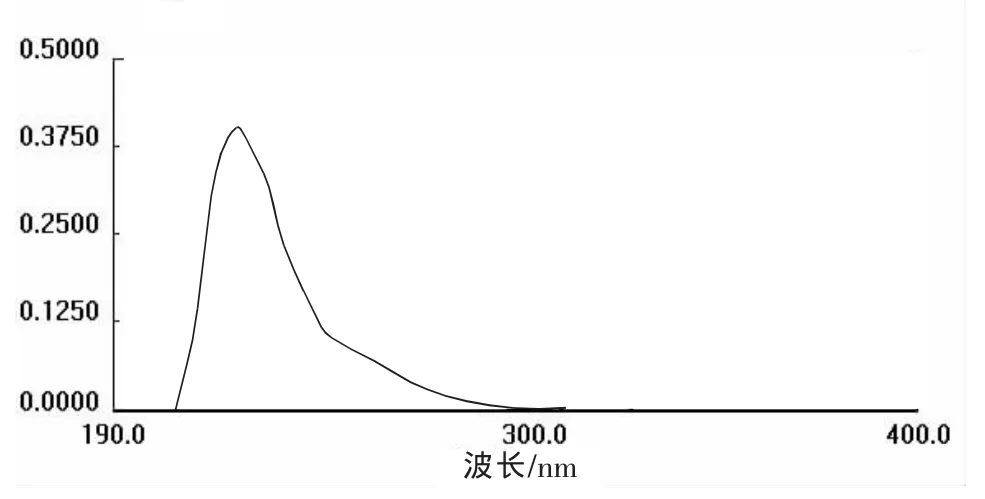
图1 N-乙基-2,3双氧哌嗪的乙醇溶液的紫外扫描图Fig1 UV-Spectrophotometric of N-ethyl-2,3-dioxypiperazine in alcohol
2.2.2 标准曲线的绘制
精密称定双氧哌嗪0.5018 g用少量乙醇溶解,移到50 mL容量瓶中定容作为一级贮备液,在其中移取1 mL至100 mL容量瓶中用乙醇定容,作为二级贮备液,此时贮备液浓度为 0.1mg·mL-1。在二级贮备液中分别移取 1.5 mL、2 mL、2.5 mL、3mL、3.5mL、4mL、4.5mL、5mL、5.5mL、6mL、6.5mL、7mL至12个容量瓶中用乙醇定容至50mL,使各个容量瓶中所含双氧哌嗪的浓度分别为3、4、5、6、7、8、9、10、11、12、13、14 μg·mL-1。 以乙醇作为空白溶剂,在222nm处测量其吸光度,得工作曲线(图2)。
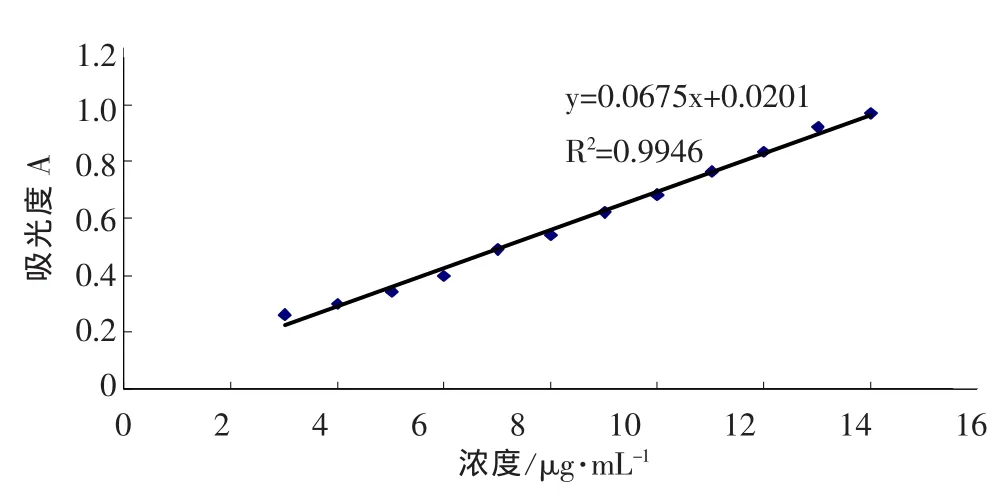
图2 N-乙基-2,3-双氧哌嗪紫外工作曲线Fig2 UV-Spectrophotometric calibration curve of N-ethyl-2,3-dioxypiperazine
由工作曲线可得回归方程为 y=0.0675x+0.0201,相关系数 R=0.9973。由图 2 可知,在 3~14 μg范围内,该工作曲线有较好的线性关系。
2.2.3 精密度试验
取 7 μg·mL-1、8 μg·mL-1、9 μg·mL-1等 3 种不同浓度的溶液进行精密度测量,结果见表1。
以上数据说明此仪器的精密度良好,适宜于做定量测定。
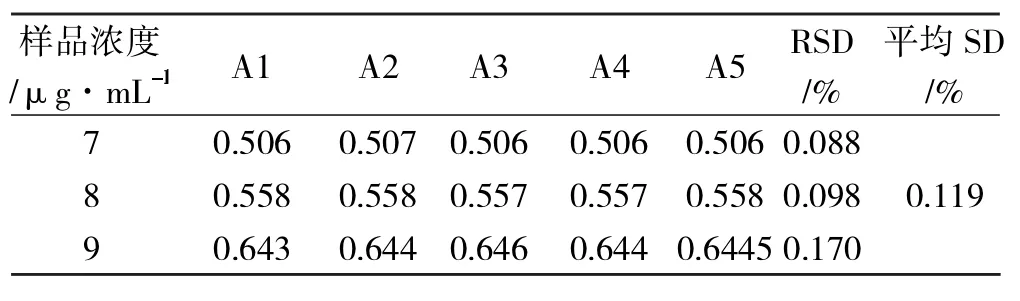
表1 精密度的测量Tab1 Measurement of precision
2.2.4 稳定性试验
将同一批样品,每隔2h测量一次,吸光度值分 别 为 0.3990、0.4013、0.4022、0.4035、0.4052、0.4067,RSD=0.687%。
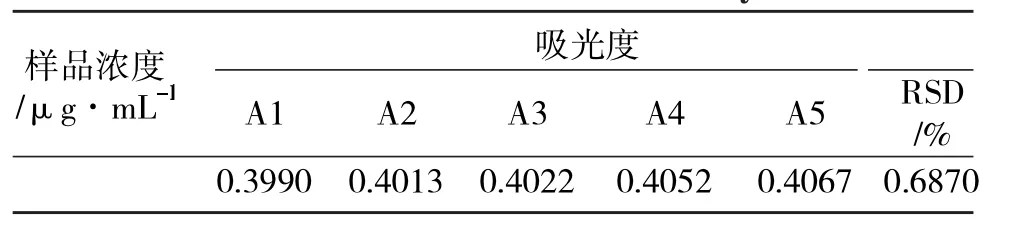
表2 稳定性试验Tab2 Measurement of stability
说明此方法在12 h内稳定,但随着时间增加,吸光度不断增加,有可能为乙醇的缓慢挥发导致溶液浓度的增大,故应及时测量,使测量结果有较好的准确度。
2.2.5 回收率试验
精密称取样品 0.0826 g、0.1333 g、0.1689 g,将3份样品用无水乙醇溶解、稀释于50mL容量瓶中定容; 并分别于容量瓶中移取 0.2 mL、0.1 mL、0.2 mL再于50 mL容量瓶中用无水乙醇定容(为使待测溶液落入标准工作曲线线性范围内,相当于分别将样品稀释12500倍、12500倍、25000倍)。取二次定容液分别进行测量得以下数据(表3)。

表3 回收率试验(n=5)Tab3 Recovery test(n=5)
由以上工作曲线的绘制,精密度试验、稳定性试验、回收率试验所得数据可知,用此方法测定N-乙基-2,3-双氧哌嗪的含量比较可靠。
3 实验结论
3.1 定性检测
在甲醇、乙醇、乙腈3种溶剂中选择一种溶剂(因乙醇无毒无害,且价格较为便宜,故采用乙醇作为溶剂),N-乙基-2,3-双氧哌嗪在 222 nm 处有最大吸收峰,故可使用紫外分光光度法对其进行定性检测,并可与熔点测定及红外检测结果进行比较测定。
3.2 定量检测
由图2的工作曲线有良好的线性关系(回归方程为 y=0.0675x+0.0201 相关系数 R=0.9973)及精密度试验、稳定性试验、回收率试验所得数据可知,用此方法测定N-乙基-2,3-双氧哌嗪的含量比较可靠。实际工作中可用图2的工作曲线对其进行定量检测,并可与红外检测结果进行比较测定。
[1] 陈芬儿.有机药物物合成法(第 1卷)[M].北京:中国医药科技出版社,1998.467-470.
[2] 许建帼,谢建伟,吴敏,等.N-乙基-2,3-二氧代哌嗪的合成[J].精细化工中间体,2005,35(4):18-19.
[3] 包锦芝.国外抗生素发展动态[J].新药与治疗,1986(2):1-6.
[4] 严朝贵.我国头孢菌素的现状及发展前景[J].中国药房,1999,10(3):102-103.
[5] 李双军,张业华.国内头孢菌素类抗生素状况[J].山东医药工业,1994,13(2):28-29.
[6] 余健民.抗生素研究进展[J].九江医学,2001,16(2):113-117.
[7] 李润卿.有机结构波谱分析[M].天津:天津大学出版社,2002.7-10.
[8] 张玉梅,孙学斌,高旭年,等.紫外分光光度法测定大豆异黄酮的含量[J].中国食品卫生杂志,2000,12(4):7-9.
[9] 王严国,许勇,凌娟.紫外分光光度法测定复方银杏叶胶囊总黄酮含量 [J]. 东南国防医药,2005,(3):206-207.
[10] 李浩春.分析化学手册(第 5册)[M].北京:化学工业出版社,1999.
Determination of N-ethyl-2,3-dioxypiperazine by Ultraviolet Spectrophotometry
ZHANG Zhong-hua
(Shanxi Vocational and Technical College of Power, Taiyuan 030021,China)
A UV-spectrophotometric method of N-ethyl-2,3-dioxypiperazine was build up.N-ethyl-2,3-dioxypiperazine was analyzed by UV-spectrophotometric to assure its structure and purity.
N-ethyl-2,3-dioxypiperazine; ultraviolet spectrophotometry; analysis method
0657.32
A
1671-9905(2011)04-0038-03
张中华(1978-),女,山东莱阳人,助教,2007年毕业于太原理工大学,硕士,主要从事水处理及有机合成研究,Tel:13934215667,Email: mmjjzzh@163.com
2011-01-17
